鐵及含鐵化合物活化過硫酸鹽的研究進展
張洛紅,熊鑫,柴易達,翟迎博,李芮瑩
(西安工程大學 環境與化學工程學院,陜西 西安 710600)
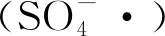
鐵屬于過渡金屬元素,在地殼中分布較廣,相對于銅、錳等金屬元素毒性較低,Fe0、Fe2+在活化過硫酸鹽方面已經有比較廣泛的研究,并且近些年來鐵的一系列化合物如鐵礦石、鋼渣等由于其較為經濟的成本也越來越受到業界的關注和研究。本文對鐵及含鐵化合物活化過硫酸鹽產生活性自由基的技術進行綜述,介紹其反應機理以及目前仍面臨的問題,以促進相關研究工作的進一步發展。
1 Fe2+活化過硫酸鹽



(1)

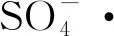
傳統的金屬離子活化過硫酸鹽,不僅可能會造成重金屬離子污染,而且需要高昂的運營成本投入。相比之下,固體金屬與金屬氧化物非均相催化具有不需要大量能量、環保、成本低等優點,同時也帶來了耐久性差、難以回收二次利用等問題[8]。因此需要開發具有更好的穩定性和可再現性的新型非均相催化劑。
Lu等[9]制備Fe2(MoO4)3催化劑,以活化過硫酸鹽降解羅丹B(RhB)。在Fe2(MoO4)3/過硫酸鹽體系中,添加4 mmol/L過硫酸鹽和0.4 g/L Fe2(MoO4)3在240 min內可以使10 mg/L RhB達到59.88%的去除效率,并且RhB降解的中間產物,如羥基苯、醌化合物,可以充當電子轉移劑,將Fe3+還原為Fe2+,構成鐵的氧化還原循環。這種催化劑還可重復利用多達6次,且每次Fe浸出量低于2.9%,在具有高效性的前提下,也顯示出優異的穩定性。
Shi等[10]采用幾種不同方法制備了鐵固定樹脂炭,并以此活化過硫酸鹽降解偶氮類染料OG。降解實驗結果表明,通過摻雜法(CSa)制備的樹脂炭在較寬泛的pH和溫度范圍內表現出優異的過硫酸鹽活化性能,對OG具有明顯的降解能力。在pH=6,溫度35 ℃的條件下,30 min內OG的降解率幾乎達到了100%。
2 Fe0活化過硫酸鹽
由于Fe2+活化過硫酸鹽在堿性條件下效果較差,以及Fe2+的初始添加量不能過多等問題,目前常使用Fe0作為Fe2+的替代品。
Kang等[11]研究了零價鐵-過硫酸鹽工藝對土壤中對氯硝基苯(p-CNB)的降解作用。隨著Fe0劑量從0.1 mmol/g增加到1.0 mmol/g,p-CNB去除率從10.8%顯著增加到90.1%。同時,p-CNB的去除隨著初始pH值的降低而增加,酸性條件比中性和堿性條件更有利于p-CNB的降解。在零價鐵-過硫酸鹽體系中,Fe0不但可以用于生成Fe2+活化過硫酸鹽,還能夠循環Fe3+生成新的Fe2+,回收Fe3+[12-13],反應見式(2)、式(3)所示:
Fe0→Fe2++2e-
(2)
2Fe3++Fe0→3Fe2+
(3)
Fe0根據粒徑大小可以分為顆粒Fe0和納米Fe0,不同形態的Fe0對過硫酸鹽的活化效果不同[14]。Pardo等比較了Fe2+、顆粒Fe0和納米Fe0活化過硫酸鹽降解生物柴油的能力,發現在酸性pH下并通過添加相同量的鐵,使用Fe0可獲得最高的降解率(約60%),而加入Fe2+只能降解約40%。同時,使用納米Fe0可以在更短的時間內獲得最大的降解率。
與Fe2+類似,Fe0也常通過添加螯合劑和制備催化劑的方法來提高降解效果。
Rahmani等[15]研究發現,在過硫酸鹽/納米Fe0/EDTA體系降解苯酚的過程中,Fe0可以與EDTA形成絡合物,控制反應速率,反應見式(4)所示:
在實驗中,苯酚降解率隨螯合劑濃度的增加而增加。當采用1∶1的Fe/EDTA比時,得到了最高的降解率。
黃捷等[16]通過液相還原法制備多壁碳納米管負載零價鐵(MWCNTs-nFe0)催化劑活化過一硫酸鹽降解雙酚A(BPA)。表征結果表明,碳納米管可以較好地分散nFe0的顆粒,避免nFe0聚集,進而增加nFe0的比表面積和分散性,提高催化效果,同時,碳納米管可以充當快速電子轉移通道,增加了催化劑活性使其能應用于更廣的pH范圍。重復利用3次后,BPA降解率由98.6%略微下降至91.3%,具有較好的重復利用性能。
3 含鐵礦物活化過硫酸鹽
自然界中存在多種鐵礦石,如赤鐵礦(Fe2O3)、磁鐵礦(Fe3O4)、黃鐵礦(FeS2)、褐鐵礦(FeO(OH)·nH2O)等,這些礦石價格低廉且易獲得,因而也被用作過硫酸鹽的活化劑。這些天然礦物不僅可以避免大量的能源和化學物質投入,同時也是一種儲量充足的環境友好型活化劑,因此具有以高效率和成本效益的方式活化過硫酸鹽的潛力。
赤鐵礦是地表儲量最大的礦石之一,由于赤鐵礦中含有的是三價鐵,而不是二價鐵,單獨的三價鐵鹽無法直接活化過硫酸鹽。Lu等[17]通過研究Fe3+/過硫酸鹽降解羅丹明B的反應過程,認為反應過程中產生了中間產物,即三價鐵還原成二價鐵,進而二價鐵活化過硫酸鹽產生自由基降解有機污染物。
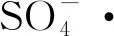

(5)

(6)
(7)
(8)
Liu等[19]采用水熱法、煅燒法將TiO2、Fe2O3負載到沸石上制備(n)TiFeZ催化劑,并在可見光照射下活化過硫酸鹽降解環丙沙星(CIP)。在可見光下,(n)TiFeZ表面的TiO2和Fe2O3納米粒子可以被激發產生電子空穴對,進而Fe3+得到電子被還原為Fe2+,活化過硫酸鹽。在中性條件下(pH=7),投加1 g/L (n)TiFeZ和5 mmol/L過硫酸鹽可以在2 h內完全降解500 mg/L的CIP。
磁鐵礦(Fe3O4)屬于一種多價態混合物,組成成分為FeO·Fe2O3,在水中可以產生大量Fe2+,由于其天然具有磁性,便于在反應后從溶液中分離。
Liu等[20]研究了在超聲波輔助條件下Fe3O4活化過硫酸鹽降解四環素類抗生素(TC),當磁性納米Fe3O4的投加量為0.3 g/L,過硫酸鹽濃度為 4 mmol/L,抗生素濃度為10 mg/L時,TC和COD去除效率分別達到了92.99%和79.85%。

4 鋼渣活化過硫酸鹽
我國是產鋼大國,鋼產量已經連續多年居于世界前列,而鋼渣是產鋼過程中必然出現的副產物,其產量巨大,占我國產鋼總量的15%~20%[23]。但與之相反的是,我國目前對鋼渣的總利用率僅達到了10%[24],大量未被回收利用的鋼渣不僅需要擴建渣廠進行存放,而且一旦處置不當,會造成對土地、水質的污染,破壞生態環境。
鋼渣本身含有Fe2O3、SiO2、FeO和CaO[25]等物質,其中的二價鐵等直接活化過硫酸鹽,CaO和 CaCO3等堿性氧化物也可以通過在溶液中水解釋放出OH-,通過堿活化的方式間接活化過硫酸鹽。
郭婧怡等[26]研究發現,切割鋼渣可以活化過硫酸鹽以染料酸性紅73,鋼渣中含有的石墨碳和FeO可以活化過硫酸鹽。隨著過硫酸鹽和鋼渣投入量的增加,AR73的降解速率也逐漸增加;在pH為3~9范圍內,AR73均可被有效去除。當該污染物濃度為25 mg/L時,15 min內的降解率可達99.9%;同時該技術對某實際印染廢水(CODCr=5 625 mg/L)的有機物去除率達到了49.9%。
黃凱[27]取粒徑為0.850 mm的鋼渣,在過硫酸鹽體系內降解X3B,實驗表明在一定范圍內,X3B的去除率隨著pH值、初始X3B濃度的升高而降低,隨著溫度和鋼渣、過硫酸鹽的投加量的增大而升高,在反應5 min后,X3B的降解率最高可達100%,幾乎被完全降解。
Vasiliki等[28]研究了在轉爐鋼渣在酸性介質中通過氧化消化而制得催化劑,以活化過硫酸鹽,生成用于氧化對羥基苯甲酸丙酯(PP)的活性自由基。研究發現,在90 min內,當加入濃度為1 g/L的過硫酸鈉和50 mg/L的催化劑時,PP的去除率約為90%(初始濃度為0.4 mg/L)。同時催化劑在整個降解過程中顯示出很高的穩定性。

(9)
(11)
同時,過硫酸鹽也會被鋼渣表面存在的少量FeO活化,并且在堿性條件下被轉化成OH·。

5 展望
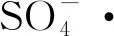
(1)反應結束后,不可避免地會產生鐵泥,后續處理不易,如果一旦處理不當,極易造成重金屬污染;同時,也存在Fe2+容易被氧化成Fe3+,反應過程中副反應較多,氧化劑利用效率低等問題。
(2)從目前現有的研究可以看出,鐵活化過硫酸鹽大部分需要創造酸性甚至是強酸性的pH環境,小部分也需要強堿性環境,能在中性條件下仍有較好的處理效果的反應較少,一旦反應結束后,酸或堿性的廢液需要后續調節pH。
(3)催化劑雖然可以提高處理效果,降低損耗,但催化劑制備不易,需要開發更簡單易得、高效、可重復利用的催化劑,降低該技術的使用門檻及使用成本。
(4)使用鋼渣或者鐵礦石等化合物可以降低成本,但單獨使用鐵化合物,在反應過程中容易在表面形成鐵氧化膜,阻止內部的Fe2+釋放,影響處理效果。
(5)大部分研究都是使用模擬單一廢水或者模擬混合廢水進行處理,實際廢水的使用比較少,需要多進行實際廢水的研究,并開發相關配套的處理工藝,推進過硫酸鹽氧化的工業化。

