通道下后方經椎間孔入路行病灶清除聯合椎間植骨內固定術治療腰椎結核的效果分析
薛海濱 羅小波 孫飛 簡偉 李金龍
腰椎結核的治療方法一直存在較大爭議[1-3]。雖然相當一部分患者可以通過保守治療的方法治愈,但對于局部持續疼痛難以控制、出現神經損傷癥狀,或者腰椎畸形及保守治療無效的患者,手術仍然能夠顯示出其優勢。腰椎結核的具體手術方式包括前路、前后路或后路病灶清除植骨內固定術等[4-6]。單純后路手術治療腰椎結核一直爭議較大,但近年來,通過后路手術治療腰椎結核的報道逐漸增加[5, 7],后路手術又有多種術式。筆者嘗試采用通道下后方經椎間孔入路行病灶清除聯合椎間植骨內固定的方式治療腰椎結核患者,對其適應證和療效進行初步探討。
資料和方法
一、研究對象
2013年1月至2019年3月,解放軍總醫院第八醫學中心骨科采用通道下后方經椎間孔入路行病灶清除聯合椎間植骨內固定治療的腰椎結核患者共84例,選取其中資料完整的56例患者進行分析。
二、納入和排除標準
1.納入標準:(1)經病史、臨床癥狀、實驗室檢驗、影像學檢查、穿刺活檢病理學及病原學檢測,以及試驗性抗結核治療等方式診斷為腰椎結核的患者;(2)劇烈腰痛經抗結核、止痛及臥床治療2~4周后效果不佳;(3)存在神經受累表現;(4)椎體破壞造成局部不穩或畸形;(5)對應椎體破壞缺損不超過50%;(6)隨訪時間至少18個月且資料完整。
2.排除標準:(1)疼痛不嚴重、不伴畸形或神經損傷表現,保守治療效果良好者;(2)靜止或陳舊性病灶伴畸形,需要行截骨矯形者;(3)對應椎體破壞缺損超過50%,或超過2個節段受累;(4)隨訪時間不足18個月或病歷資料不完整者。
三、患者資料
56例患者中,男30例,女26例;年齡18~74歲,平均(49.6±10.5)歲。病程2~6個月,平均(3.4±1.1)個月。患者皆為1個椎間隙和對應椎體受累,病變累及腰1~2椎體者5例,腰2~3椎體者8例,腰3~4椎體者10例,腰4~5椎體者17例,腰5椎體~骶1椎體者16例。
患者以腰痛為主要表現,術前疼痛視覺模擬評分(visual analog scale,VAS)為(7.46±1.45)分,Oswestry功能指數(Oswestry disability index,ODI)為(75.84±9.61)%。按照美國脊柱損傷協會(American Spinal Injury Association,ASIA)脊髓損傷神經功能分級標準,出現D級截癱者4例。
實驗室檢查包括血常規、肝腎功能、血紅細胞沉降率(erythrocyte sedimentation rate,ESR)、C反應蛋白(C-reactive protein,CRP)和γ-干擾素釋放試驗等。56例患者入院時首次檢查ESR為30~125 mm/1 h,平均(57.6±10.4)mm/1 h;CRP為208~1347 mg/L,平均(525.6±102.5)mg/L。
56例患者術前均行X線、CT和MRI檢查,42例伴不同程度椎旁膿腫。腰椎X線側位片測量近端感染椎體上終板和遠端感染椎體的下終板連線夾角為病變部位前凸角度,術前病變部位前凸角度為-12°~5°,平均(2.8±0.6)°。至少合并一種其他疾病者28例,其中糖尿病18例,高血壓12例,尿毒癥4例,肝硬化2例,長期應用糖皮質激素者2例。
四、治療方案
1.術前準備和手術時機:32例患者入院前在外院曾給予不同時間的抗結核治療,采用異煙肼、利福平、吡嗪酰胺、鹽酸乙胺丁醇聯合規律用藥者25例,間斷用藥者7例。所有患者入院后經檢查明確診斷后,均足量聯合應用抗結核藥物進行治療。化療方案:異煙肼(5 mg/kg)、利福平(10 mg/kg)、乙胺丁醇(15~25 mg/kg)、吡嗪酰胺(15~50 mg/kg)。合并巨大(直徑>5 cm)腰大肌或髂腰肌膿腫者,術前給予超聲引導下穿刺置管引流。按CT及MRI檢查結果判斷病椎破壞情況及擬固定椎體的椎弓根情況,以確定病灶清除范圍、植骨方案及置釘方法。
術前抗結核治療1~2周,期間加強全身營養支持治療,糾正貧血,常規評估患者對手術的耐受情況,并請相關科室會診,處置并發癥。符合麻醉手術的要求后,即可進行手術。
2.手術方法:氣管插管全麻,取俯臥位,以責任間隙為中心,中線旁旁開2~3 cm,雙側縱向切口長約4 cm。先自病變重的一側沿標記線切開皮膚、皮下深筋膜,找到最長肌與多裂肌間隙,自間隙進入鈍性分離,自椎弓根連線位置中點處插入導針,沿導針依次放置擴張套管,置入可擴張通道,縱向撐開通道,并使用扳手進一步擴張通道底部,安裝自由臂和冷光源,側方擋板葉片按照“內短外長”的方法撐開肌肉,充分顯露手術野,選擇椎弓根釘進釘點,開口、擴孔后置入定位針,通過C型臂透視定位針,待位置滿意后撥出定位針,以骨蠟封口備用。將下位腰椎的上關節突鑿除,去除上位腰椎的椎板外側部分及部分下關節突,咬除椎間孔內的黃韌帶,保護好上位神經根,自“安全三角”到達病變椎間盤后外側,切開纖維環進入病變椎間,用髓核鉗及長柄大勺刮匙深入病灶內清理壞死物、死骨和破壞的椎間盤,刮除病變椎體硬化骨質,向外側打開外側纖維環,刮除椎旁膿腫或肉芽組織,反復沖洗。取咬除的附件骨質、同種異體骨或適宜的填充自體松質骨的椎間融合器植入椎間隙。依定位針上下各置入1枚椎弓根釘,根據腰椎曲度預彎安裝連接棒。在通道下置入對側椎弓根螺釘,安裝連接棒。逐層縫合兩側腰背筋膜切口及皮膚。
3.術后處理:術后進行常規脊椎手術外科護理和對癥支持治療。術中清除病變組織做結核分枝桿菌培養和藥物敏感性試驗,未癱瘓者術后第1~2天佩戴腰圍開始下床活動,癱瘓者根據肌力恢復情況積極進行康復鍛煉。戴支具時間持續3~6個月。定期復查血常規、肝腎功能、ESR和CRP等指標,術后依術前方案繼續行抗結核藥物治療,根據ESR、CRP變化情況調整用藥,總療程12~18個月。于術后1、3、6、12個月復查X線片,此后每年攝片1次,必要時進行CT或MRI檢查,觀察結核病灶的愈合、腰椎曲度和骨融合情況。
五、臨床觀察指標和影像學評估
臨床觀察指標包括手術時間、術中出血量、并發癥、疼痛緩解和功能恢復情況,ESR和CRP變化情況,以及神經功能改善情況。影像學觀察指標包括術前、術后與最終隨訪時病灶愈合情況、病變部位前凸角度及植骨融合率等。
六、統計學處理
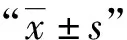
結 果
56例患者采用門診復查和在線醫療等方式進行隨訪,隨訪時間為18~48個月,平均(21.5±5.8)個月。
56例患者手術時間90~180 min,平均(124.5±26.2)min;術中出血量150~400 ml,平均(248.4±46.7)ml。所有患者術后切口均一期愈合,2例術后1~2個月切口處形成竇道,經換藥后愈合;無進入手術室行清創治療的患者。最終隨訪時,所有患者病灶均治愈,無結核感染復發或慢性不愈合需再次進行手術治療的患者。
56例患者術后腰部疼痛均明顯緩解,有2例存在術側根性神經痛,經服用鎮痛及神經營養藥物,3個月后得到改善。56例患者術后1~2周后ESR及CRP均逐漸下降,至抗結核治療結束時ESR及CRP均恢復至正常水平。4例ASIA為D級的截癱者改善至E級。術后1周及最終隨訪時,56例患者VAS評分、ODI值及病變部位前凸角度均較術前明顯改善,差異均有統計學意義(表1)。所有患者術后6~10個月[平均(7.5±1.2)個月]植骨均獲得骨性融合。隨訪期間未出現內固定物松動、斷裂及移位等并發癥。典型患者影像資料見圖1~13。
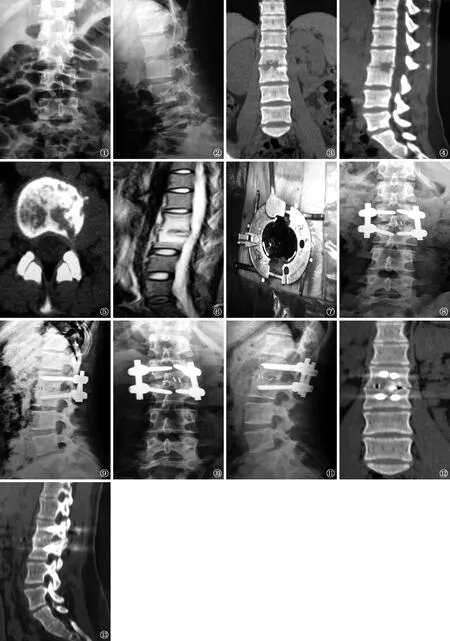
圖1~13 患者,女,39歲,腰2~3椎體結核。圖1、2分別為術前腰椎正側位X線片,顯示腰2、3椎體椎間隙變窄,腰椎曲度變直,局部前凸角度為-8°。圖3~5為術前CT片,顯示腰2、3椎體破壞、椎旁膿腫形成。圖6為術前MRI,顯示腰2、3椎體炎性浸潤、椎間隙破壞、膿腫形成。圖7顯示在可擴張通道下直視完成病灶清除植骨及置釘固定。圖8、9分別為術后1周腰椎正側位X線片,顯示內固定位置良好,前凸角度為6°,達到正常生理曲度。圖10、11分別為術后2年腰椎正側位X線片,顯示內固定位置良好,前凸角度為6°,矯形無丟失。圖12、13為術后2年腰椎CT片,顯示腰2~3椎體間骨融合
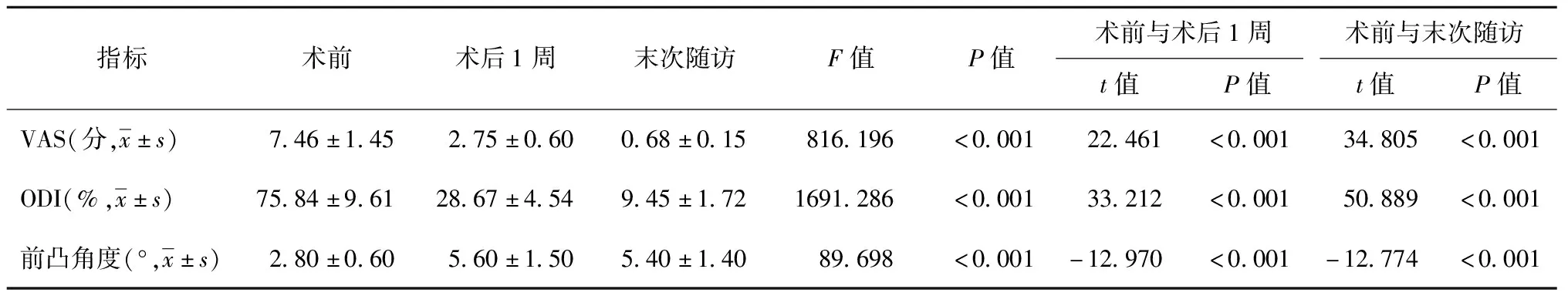
表1 56例患者術前、術后1周及末次隨訪時VAS、ODI及前凸角度變化情況
討 論
一、腰椎結核的手術方式
傳統治療腰椎結核的手術方式是前路病灶清除植骨融合術。由于單純病灶清除植骨術術后仍需臥床,且易出現植骨塌陷移位、難以改善矢狀面畸形或維持正常生理曲度等問題。因此,內固定逐漸應用于腰椎,包括脊柱其他部位結核病的治療,可即刻穩定脊柱,促進康復以植骨融合[7]。但前路內固定手術入路復雜,創傷大,存在損傷血管及內臟器官等風險,同時,內固定器械固定及矯形力相對不足。而采取前路病灶清除植骨后路內固定也存在需要2個切口、創傷大和手術時間長等缺點。也有術者采取單純后路病灶清除植骨內固定的方式治療腰椎結核,取得良好的效果[4, 8-9]。
隨著微創技術在脊柱外科的廣泛應用,有術者采取微創技術治療腰椎結核,包括CT引導下經皮穿刺置管引流沖洗結合局部置藥[10-11]、脊柱內鏡下病灶清除灌洗引流[12-13]等,此類微創技術主要針對結核病灶,起到促進病灶愈合的目的,但不能進行脊柱功能的修復重建,包括矯形、避免病灶愈合過程中繼發后凸畸形及植骨融合等。同時,相當一部分患者術后仍需臥床,不利于早期康復。也有術者采取通道下斜外側前方入路(OLIF)結合后路微創內固定的方式治療腰椎結核[14],此技術是傳統前后路手術的微創化,避免了后路手術肌肉廣泛剝離置釘固定及前路長切口暴露的不足,是一種值得推崇的技術,但也存在前后路手術需要變換體位的不足。同時,通道下前路手術也增加了血管、輸尿管或神經損傷的風險,對術者技術要求高,學習曲線長。此種手術方式更適合前方病灶破壞廣泛,病灶清除后椎間缺損大需要椎間支撐植骨的患者。
二、通道下后方經椎間孔入路治療腰椎結核的優勢
傳統腰椎后路手術出血量大,術中需要將椎旁肌肉廣泛剝離和牽拉,易引起肌肉壞死,造成術后慢性腰背痛。多裂肌與最長肌之間無血管神經分布,是較為理想的手術界面,微創經多裂肌與最長肌間隙椎間孔入路完成腰椎管減壓椎間融合手術由于具有出血量少、手術時間短、減少術后腰背疼痛等優勢,在腰椎退行性病變的手術中逐漸開展[15-16]。
通道下經椎間孔入路病灶清除植骨內固定術治療腰椎間隙感染或椎間盤炎已有報道[17-18]。筆者自2013年開始嘗試對于一部分腰椎結核患者通過通道下經椎間孔入路的方式進行手術治療,本入路采用棘突兩側作小切口,自多裂肌和最長肌間隙通過通道顯露,完成病灶清除、神經減壓、椎間植骨及經椎弓根內固定,可在通道下方直視情況下進行手術,無需手眼分離訓練要求,學習曲線較短,降低了廣泛開展的門檻。在通道下方置釘可避免反復透視經皮置釘對患者和術者射線暴露的缺陷。僅作單側關節突切除及有限椎板切除可最大限度避免破壞脊柱結構。本研究56例患者在最終隨訪時,病灶皆治愈,植骨均獲得骨性融合,腰椎曲度獲得改善,無內固定失敗患者,基本可達到病前生活和工作的狀態。
三、本術式的缺點和注意事項
本術式也存在一定的缺點和不足。首先,由于暴露視野局限,若病灶破壞廣泛,骨缺損大,病灶清除相對困難,不便于鑿出植骨床。同時,植骨塊放置困難,難以達到理想的椎間支撐植骨。其次,對于椎旁流注性膿腫的處理相對前路手術而言欠佳,但此問題可通過術前超聲引導下置管引流解決[19]。由于此術式通過椎管行病灶清除,硬膜及神經根損傷的概率相對增加,增加了術后硬膜和神經根粘連的機會。因此,需嚴格掌握手術的適應證,筆者認為手術適應證包括:(1)劇烈腰痛經抗結核及止痛治療效果不佳;(2)存在神經受累表現;(3)椎體破壞造成局部不穩或畸形;(4)對應椎體破壞缺損不超過50%。
手術中進行病灶清除、神經減壓時要特別保護好硬脊膜和出口及行走神經根,在安全三角自椎間盤后外側緣進入病灶,進入病灶后可應用長柄的大刮匙、髓核鉗及其他器械進行病灶清除,可以越過中線清除對側病灶,打開外側纖維環清除椎旁病灶,但需注意控制深度,避免損傷到前方重要結構。本組患者手術減壓時無一例出現硬脊膜或神經根撕裂。后路椎弓根系統固定時,近端椎體一般可作為固定椎,遠端病椎若近端骨破壞難以作為固定椎,則需擴大固定節段。
總之,通道下后方經椎間孔入路行病灶清除聯合椎間植骨內固定術治療腰椎結核創傷小、出血量少,如果適應證選擇得當,則臨床療效良好。但該技術作為一種脊柱微創技術也存在一定的局限和不足,對于病變破壞廣泛或重度畸形需要進行矯正的患者不宜選擇。

