高血壓患者中基線體質量指數對癌癥發病的時變影響
朱晶晶 余勇夫 許慧琳 秦國友,4
1 復旦大學公共衛生學院生物統計學教研室,200032 上海; 2 上海市閔行區疾病預防控制中心,201100 上海;3 復旦大學公共衛生學院閔行分院, 201101 上海; 4 復旦大學公共衛生安全教育部重點實驗室,200032 上海
高血壓作為心血管疾病和死亡的主要風險因素,造成了嚴重的疾病負擔,全球每年有760萬人死于高血壓[1-2]。同時,癌癥的發病率和死亡率也已成為一個世界性的公共衛生問題,在2017年有2 450萬新病例和960萬人死亡[3]。隨著人口老齡化的發展,腫瘤合并高血壓的患者大幅增加,越來越多的研究關注高血壓和腫瘤的內在關系,引出了“腫瘤-高血壓”這一概念。研究顯示,血壓升高會增加癌癥的發病風險和死亡風險[4-6]。此外,肥胖作為高血壓和腫瘤共同的危險因素,影響高血壓和腫瘤的發生發展[7]。大量流行病學數據表明,體質量指數(BMI)升高與常見和較少見的惡性腫瘤風險增加相關[8]。國際上推薦將控制肥胖和降低體質量作為預防和控制高血壓和癌癥的手段。然而,關于高血壓人群中BMI和癌癥之間關系的研究相對有限。1項包含363 992名瑞典男性的隊列研究發現,隨著舒張壓和BMI的增加,患腎細胞癌的風險持續上升[9]。 此外,先前的研究都使用Cox比例風險模型來評估BMI對癌癥發病影響,基于BMI的效應不會隨時間改變這一等比例風險假設。如果將違反PH假設的時變因素作為與時間無關的變量納入模型,將會獲得有偏估計,而傳統Cox模型也有可能忽略感興趣的變量僅在特定隨訪時間內對結局的影響。因此,檢測和考慮時變效應在建模過程中至關重要,有助于提供更有價值的隨時間變化的效應信息。但是,目前還沒有研究探索在高血壓患者中BMI對癌癥發生的時變效應。在中國,高血壓患者數量正在逐年增加。因此,本研究進行了1項大樣本量的回顧性隊列研究,收集了上海市閔行區電子健康信息系統(EHR)的數據,采用變系數Cox 回歸模型研究高血壓人群中的基線BMI與癌癥發病風險之間的關聯,為高血壓患者的體質量管理提供建議,以期降低癌癥發病風險、提高生存質量。
1 資料與方法
1.1 研究對象
從上海市閔行區EHR中選取2007—2015年記錄的成年高血壓患者作為研究對象。排除標準:①人口統計數據缺失;②非上海永久登記居民;③基線年齡<20歲或≥85歲;④隨訪時間少于3個月;⑤身高/體質量數據缺失或BMI極端的數據(≥40.0 kg/m2);⑥其他風險因素數據缺失。
1.2 研究方法
采用回顧性隊列研究,開始隨訪時間為首次記錄患者的時間,觀察截止時間為2018年12月31日。觀察結局為癌癥發生,截尾刪失情況包括失訪、癌癥發病前死亡及觀察結束時未發生癌癥的患者。EHR記錄了患者的基線信息和隨訪狀態,包括性別、年齡、自我報告的身高和體質量、主要慢性病家族史、糖尿病綜合征以及吸煙、飲酒和體育鍛煉情況。
1.3 相關指標定義及診斷標準
根據世界衛生組織(WHO)指南,高血壓定義為收縮壓≥18.67 kPa(140 mmHg)和/或舒張壓≥12.00 kPa(90 mmHg)。糖尿病綜合征定義為空腹血糖≥7.0 mmol/L (126 mg/dL)或2 h血糖≥11.1 mmol/L (200 mg/dL)。BMI的計算使用登記之日記錄的自報身高和體質量。根據世界衛生組織對亞洲人口的BMI的分類建議,將患者分為低體質量(<18.5 kg/m2),正常體質量(18.5~22.9 kg/m2),超體質量(23~24.9 kg/m2),一級肥胖(25~29.9 kg/m2),二級肥胖(≥30 kg/m2)5組[10]。癌癥發病參照國際疾病分類ICD-10(編碼C00-D49)標準。所有疾病均由醫生進行確診。吸煙定義為每天吸煙至少持續1年,包括戒煙。規律飲酒定義為每周至少2次飲酒持續1年。規律鍛煉定義為每周至少進行150 min的中等強度運動或75 min的高強度運動。
1.4 統計學方法
使用SAS 9.4軟件進行統計分析。雙側檢驗,檢驗水準α=0.05。偏態分布的定量資料采用中位數(M)和四分位數(P25,P75)進行描述,定性資料采用例數(n)和構成比(%)進行描述。Pearson卡方檢驗和Kruskal-Wallis檢驗用于評估不同BMI組患者的基線特征及不同患者的癌癥發病率。使用有向無環圖描述變量之間的關系以識別潛在的混雜因素,二分類變量直接納入模型,多分類變量設置為啞變量納入模型。使用Cox比例風險模型評估高血壓患者中基線BMI對癌癥發病的風險比(HR)及95%置信區間(CI)。
1.4.1 變系數Cox回歸模型
基線BMI以正常體質量為參照組,通過擬合BMI與時間的限制性立方樣條(restricted cubic splines,RCS)函數來評估其是否滿足等比例風險(proportional hazards,PH)假設[11]。公式如下:
h(t)=h0(t)exp{β1BMI+β2BMIt+β3BMIS(t)+βX},
式中,h(t)是在危險因素X的影響下,t時刻的風險函數;h0(t)是所有自變量為0時;t時刻的基準風險函數;X表示混雜因素;t表示隨訪時間;S(t)表示立方樣條時間函數的非線性部分;ti(i=1,2,3) 表示3個節點所在的時間,節點放置在第10、50和90百分位數。在此過程中進行了3次統計檢驗,分別對應于3個零假設和P值。1)H0:β1=β2=β3=0,P<0.05代表BMI與癌癥發生存在相關性。2)H0:β2=β3=0,P<0.05代表BMI違反了PH假設,需要與時間進行交互作用。3)H0:β3=0,P<0.05代表BMI的效應隨時間呈非線性變化;反之,效應呈線性變化,公式為:
h(t)=h0(t)exp{β1BMI+β2BMIt+βX}。
1.4.2 敏感性分析
根據性別和年齡進行分層分析。在敏感性分析中,為了防止新發和長期高血壓患者對死亡結局的不同影響,本研究將分析限制在隨訪超過2年的患者中。其次,排除隨訪2年內發生癌癥的患者進一步分析以減少可能存在的因果倒置影響。此外,將研究限制在未患有糖尿病綜合征的患者中,因為高血壓在許多方面與糖尿病共享病理生理機制[12]。最后,由于高血壓的患病率在不同年齡階段顯著不同,研究排除年齡小于40歲的患者以控制年齡的不均衡分布[13]。
2 結果
2.1 患者基線特征
該研究納入212 394名高血壓患者,其中男性99 038名和女性113 356名,平均年齡62.6(P25,P75:55.3,72.1)歲,小于60歲占40.7%(86 407/212 394),大于等于60歲占59.3%(125 987/212 394)。患者中正常體質量、超體質量和肥胖者,分別占33.0%、28.5%和32.3%,低體質量患者占2.4%,二級肥胖患者占3.8%。與體質量正常,超體質量或肥胖的患者相比,低體質量的高血壓患者有較低的糖尿病合并癥、慢性病家族史、吸煙和飲酒者比例。值得注意的是,體質量過輕的高血壓患者平均年齡更大。見表1。

表1 高血壓患者中基線BMI水平的特征描述
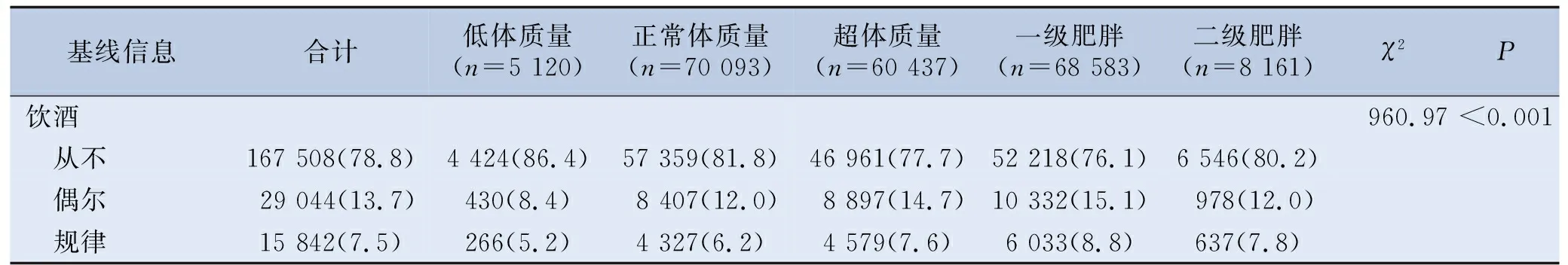
表1 (續)
2.2 癌癥發病率
在9.5(P25,P75:6.2,10.6)年的隨訪時間中,患者癌癥發病率為10.4%(22 141/212 394)。相比于正常體質量、超體質量、一級肥胖和二級肥胖,低體質量患者具有相對較高的癌癥發病率,為13.9%。男性相比于女性也有更高的癌癥發病率,分別為11.1%和9.8%。老年人(≥60歲)的癌癥發病率為13.0%,要明顯高于中青年患者(6.7%)。見表2。

表2 不同基線信息高血壓患者的癌癥發病情況
2.3 BMI類別對癌癥發病的影響
2.3.1 單因素分析
相比于正常體質量,超體質量、一級肥胖和二級肥胖都對高血壓患者的癌癥發病風險具有時變的保護效應,一級肥胖的HR在10年隨訪中相對穩定,而超體質量和二級肥胖的HR隨著時間逐漸增加。反之,低體質量患者與較高的癌癥發病風險相關,HR在隨訪期間逐漸降低,在第10年時危險效應不具有統計學意義。見表3。
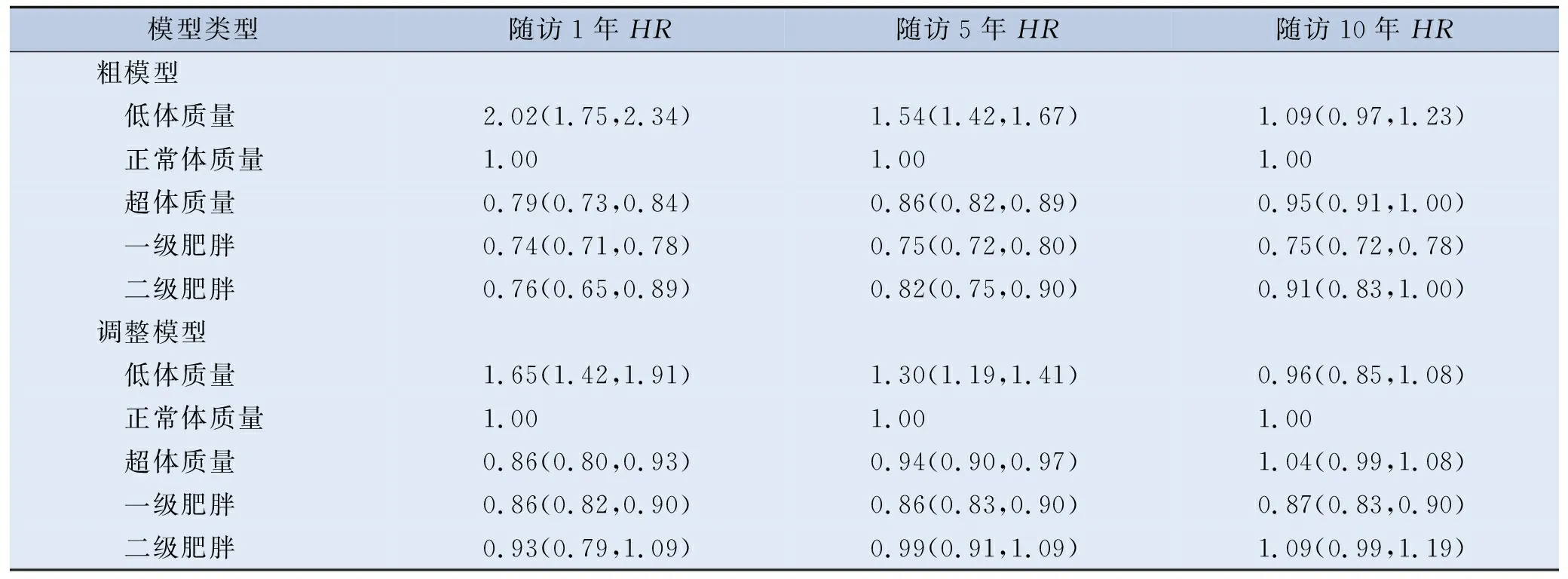
表3 高血壓患者中基線BMI對癌癥發生的時變效應(n=212 394)
2.3.2 多因素Cox回歸分析
(1)基線BMI對癌癥發病的時變效應
通過有向無環圖識別潛在的混雜因素,最終納入模型的混雜變量包括性別、年齡、心血管家族史、糖尿病家族史、卒中家族史、高血壓家族史、吸煙、鍛煉和飲酒。多因素回歸分析發現不同BMI類別對癌癥發病的影響會隨著隨訪時間發生變化。低體質量與隨訪期間較高的癌癥發病風險相關,HR從隨訪1年的1.65(95%CI:1.42~1.91)降至隨訪5年的1.30(95%CI:1.19~1.41),在隨訪10年時其危險效應不具有統計學意義。相比之下,超體質量和一級肥胖的癌癥發病風險相比于正常體質量更低,超體質量的保護作用在隨訪期間逐漸減弱,隨訪1年和10年的HR為0.86(0.80~0.93),1.04(0.99~1.08);而一級肥胖具有較為穩定的保護效應,隨訪1年和10年的HR為0.86(0.82~0.90),0.87(0.83~0.90)。此外,二級肥胖對癌癥發病的影響與正常體質量區別沒有統計學意義。見表3。
(2)不同性別和年齡層中基線BMI對癌癥發病的時變效應
在按性別和年齡組(<60歲或≥60歲)進行的分層分析中,不同BMI類別的這些時變模式與全人群相似。無論是男性還是女性、中青年還是老年患者,都可以在隨訪前5年觀察到低體質量對癌癥發病的危險效應。一級肥胖隨時間相對穩定的保護效應也可以在各亞組觀察到。見表4。
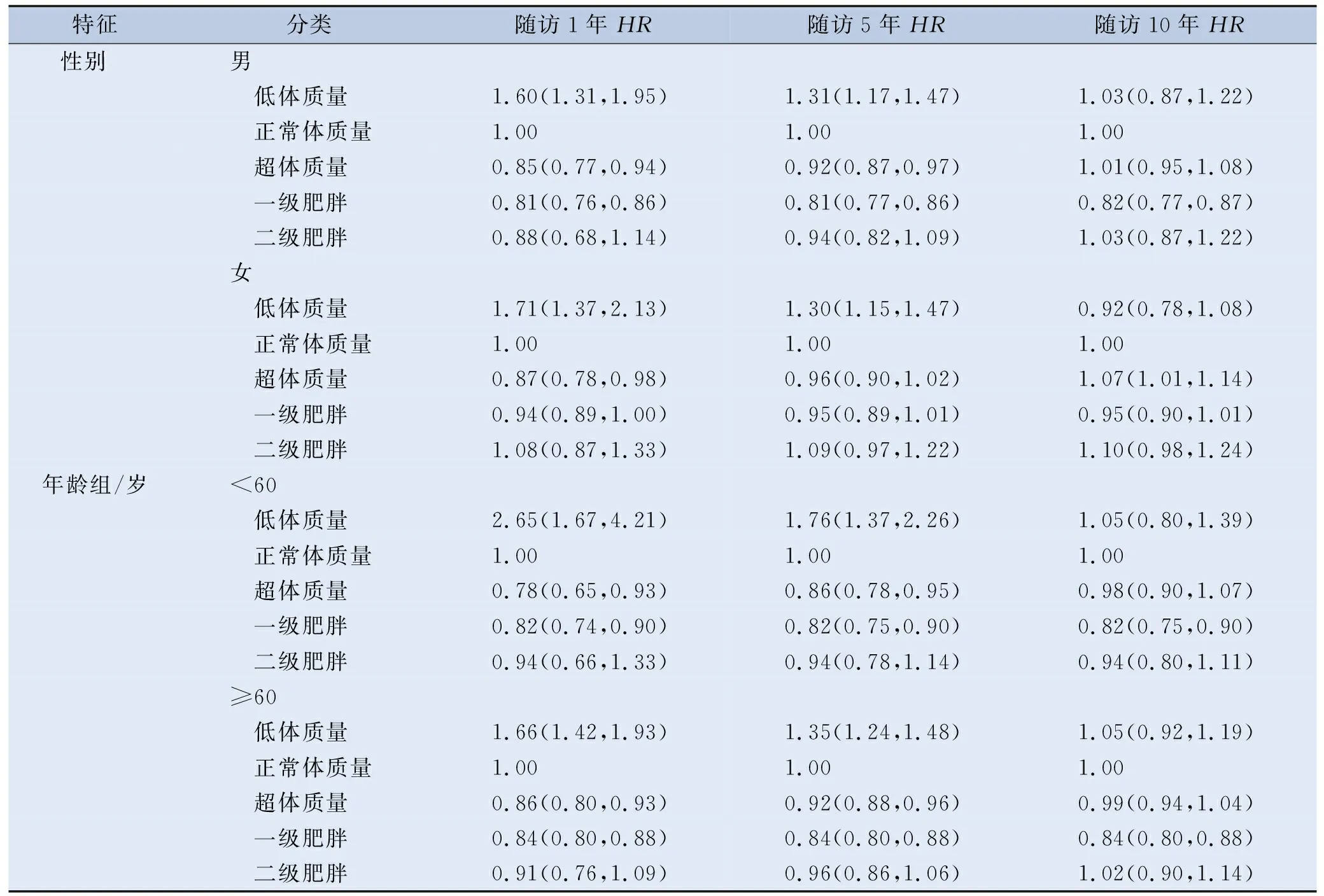
表4 不同性別和年齡層中基線BMI對癌癥發生的時變效應
2.3.3 敏感性分析
高血壓患者的基線BMI對癌癥發病的時變影響的敏感性分析結果見圖1。在敏感性分析中剔除登記后2年內發生癌癥的患者,排除隨訪時間小于2年的患者,控制年齡大于等于40歲及未患有糖尿病綜合征的患者,體質量指數和癌癥發病之間關系的變化呈現相似的結果,即低體質量高血壓患者有更高的癌癥發病風險,但其風險呈下降趨勢;同時也可以觀察到超體質量和一級肥胖的HR隨著時間緩慢上升。
3 討論
隨著高血壓患病率在我國逐漸增加,高血壓疾病的健康管理越來越引起重視。本研究利用上海市閔行區EHR數據,采用變系數Cox模型研究在高血壓患者中基線BMI和癌癥發病風險之間的關聯,為高血壓患者的體質量管理提供建議,降低癌癥發病率。
本研究發現在高血壓患者中低體質量與較高的癌癥發病風險相關,這與以往的研究結果一致[14-15]。1項包含137 366名參與者的隊列研究顯示,與正常體質量相比,男性低體質量者胃癌(HR=3.82,95%CI:1.97~7.38)和肝癌(HR=3.00,95%CI:1.36~6.65)的發病風險增加[14]。體質量過輕的患者更有可能出現低脂肪組織和瘦肉率,導致機體免疫力降低,出現不良結局[16]。同時,也有研究表明,已存在的嚴重慢性疾病(糖尿病、慢性心力衰竭等)或癌前病變(胃癌的癌前病變)以及伴隨的不健康生活方式(過度吸煙和飲酒)可能會導致體質量降低,影響BMI和癌癥發病的關聯[17]。因此,我們在進一步分析中調整了吸煙、飲酒、運動,分別排除患有糖尿病合并癥和2年內死亡的患者,觀察到的相似結果表明存在反向因果效應的可能性較小。值得注意的是,低體質量的不良影響僅在隨訪5年中觀察到,后續隨訪期間內體質量的改變可能會影響其與癌癥發生的關系。上述隊列研究也表明,在某些特定的癌癥類型中,低體質量與高癌癥發病風險之間沒有顯著的關聯。因此,我們需要進行更深入的研究,納入動態BMI的變化來探索低體質量和不同類型癌癥之間的關聯。
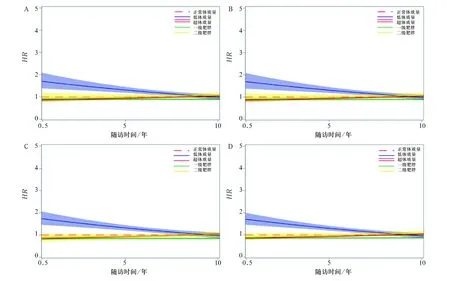
A:排除2年內發生癌癥的高血壓患者;B:排除隨訪時間<2年的高血壓患者;C:沒有糖尿病合并癥的高血壓患者;D:排除年齡<40歲的高血壓患者
本研究還觀察到相比于正常體質量,超體質量和一級肥胖有更低的癌癥發病風險。而二級肥胖對癌癥發病的影響與正常體質量沒有顯著區別。1項包含31項研究的meta分析表示,對于肺癌、鱗狀細胞癌和腺癌,BMI≥25 kg/m2與它們的發病風險呈負相關[18]。有研究表明,體脂和肥胖相關基因的等位基因可降低癌癥發病風險,而其與BMI增加存在相關性,這似乎可以為解釋超體質量或肥胖降低男性肺癌發病風險提供依據[19]。此外,較高體質量的高血壓患者伴隨著更高的代謝儲備和更好的心肺健康水平,可能導致較低的相關癌癥發病率[20]。
目前有關肥胖與惡性腫瘤相關的生物學機制仍存在爭議。但是,在高血壓患者中,越來越多的研究表明較高的BMI與患者更好的預后相關,即存在“肥胖悖論”[21]。本研究提示高血壓患者中BMI與癌癥之間存在一定的關聯,超體質量和一級肥胖的患者有更低的癌癥發病風險。在高血壓患者中進行進一步的隨訪、內暴露指標的測量及病因學的探索將有助于更加精準地探討 BMI與惡性腫瘤發病風險的相關性及其機制的研究。
本研究基于全面高質量的數據收集系統,擁有大樣本量人群和長期隨訪時間(中位隨訪時間9.5年)。此外,由于亞洲人和西方人群在體脂比和慢病發病率上存在差異,研究選擇了更加適合亞洲人口的BMI分類標準。當然,本研究也存在一定的局限性。首先,由于本研究為回顧性研究,可能存在選擇偏倚,肥胖患者更有可能自覺地尋求治療并在EHR系統中注冊。其次,BMI是身體成分的粗略指標。體質量指數相似的個體可能具有不同程度的脂肪或代謝狀況,從而導致不同的健康結局。本次研究僅收集了BMI的基線信息,隨訪期間BMI的變化可能會影響與癌癥發病風險之間的關聯。第三,不同腫瘤間BMI與其發病風險的相關性存在差異,而本研究沒有對癌癥進行分類。第四,高血壓患者的低BMI可能由癌癥前期導致或是健康狀況較差的指標,因此與高癌癥發病風險相關。但是,敏感性分析排除入組2年內發生癌癥的患者后顯示出與原人群相似的結果,表明觀察到的低BMI與癌癥發病的關聯受到反向因果關系的影響較小。
總之,根據目前變系數Cox模型的結果顯示,低體質量的高血壓患者與更高的癌癥發病風險相關,而超體質量和一級肥胖則與較低的癌癥發生風險相關。對于高血壓患者的體質量管理,應盡量控制體質量在合理范圍內,且更加關注低體質量患者。但在未來尚需進一步的研究以探索在高血壓患者中BMI與不同類型癌癥的關聯和潛在的生理機制。

