超聲引導下微波消融治療甲狀腺良性結節效果及其影響因素
付倩倩,吳翠萍,王詩雨,劉瀅瀅,康 松,田家瑋,姜雙全*
(1.哈爾濱醫科大學附屬第二醫院超聲醫學科,黑龍江 哈爾濱 150086;2.大慶市人民醫院超聲室,黑龍江 大慶 163316)
隨著影像學技術的發展,甲狀腺結節檢出率逐年提高,其中80%~95%為良性。甲狀腺良性結節導致局部壓迫或考慮惡變時,需積極治療[1]。外科手術存在創傷大、可致醫源性甲狀腺功能減退(甲減)等不足。近年來,超聲引導下熱消融治療甲狀腺良性結節已被多部指南所推薦[2-3],其中微波消融(microwave ablation, MWA)具有加熱速度快、凝固能力強,原位滅活壞死組織可被機體逐漸吸收等優勢,但臨床實踐顯示良性甲狀腺結節經MWA后病灶吸收程度及速度存在較大個體差異。本研究觀察MWA治療甲狀腺良性結節的效果,并分析其影響因素。
1 資料與方法
1.1 一般資料 回顧性分析2018年12月—2020年2月115例(115枚結節)接受MWA治療的甲狀腺良性結節患者,男17例,女98例,年齡19~74歲,平均(43.7±11.1)歲。納入標準(同時滿足標準①及②或③):①超聲未見惡性征象,穿刺活檢病理診斷為良性甲狀腺結節;②存在頸部壓迫、異物感等癥狀;③患者因焦慮而主動要求手術。排除標準:①既往接受甲狀腺手術或消融治療;②伴嚴重心、肺疾病或凝血功能障礙;③降鈣素異常增高;④多發結節及病理資料不完整。
1.2 儀器與方法 采用 Esaote MyLab ClassC超聲診斷儀,LA523探頭(頻率4~13 MHz)及LA332探頭(頻率3~11 MHz)。南京康友KY2000 MWA儀,配備16G一次性無菌消融針。造影劑為聲諾維(Bracco),單次用量1.5 ml。
術前完善血常規、凝血功能、甲狀腺功能檢查。囑患者仰臥,頸部輕度過伸。實時監測生命體征。首先依次以二維超聲、CDFI(并采用文獻[4]方法評價血流分布)、彈性成像及超聲造影(contrast enhanced ultrasound, CEUS)評估結節的特征;測量結節大小,根據公式V=(上下徑×左右徑×前后徑)×π/6計算結節體積(V)。之后常規消毒、鋪巾,以2%利多卡因對穿刺點行局部浸潤麻醉。向甲狀腺被膜與頸總動脈、氣管、食管等結構之間的間隙內推注0.9%生理鹽水20~40 ml,形成“隔離帶”。對囊性為主結節先吸出囊液。設定MWA儀輸出功率為30 W,對靶結節行移動式消融,待結節完全被強回聲氣化區覆蓋、CDFI顯示結節內無血流信號后行CEUS檢查,如發現存在殘留增強區則行補充消融。術畢對消融區域加壓冷敷1 h。由1名具有5年MWA經驗的主任醫師完成所有治療。
1.3 術后隨訪 于術后1、3、6、12個月復查超聲,觀察結節內血流灌注情況,計算結節體積縮小率(volume reduction ratio, VRR),VRR=(V術前-V隨訪時)/V術前×100%[5]。以術后12個月為隨訪終點評價療效,以VRR>90%為治愈,VRR≤90%為未治愈。
1.4 統計學分析 采用SPSS 22.0統計分析軟件。以±s表示符合正態分布的計量資料,采用方差分析比較各時間點結節體積及VRR,兩兩比較采用LSD-t檢驗;行單因素分析時,組間比較采用獨立樣本t檢驗。計數資料以頻數表示,采用χ2檢驗進行比較。以結節治愈與未治愈作為因變量,術前臨床資料、實驗室檢查結果及超聲特征作為自變量,對每一自變量與因變量行單因素分析,之后對差異有統計學意義的自變量行多因素逐步Logistic回歸分析,采用BackwardLR檢驗,根據結果建立Logistic回歸模型,以回歸模型預測診斷概率logit(P),以logit(P)=0.5為分隔值,將logit(P)≥0.5判定為VRR≤90%,logit(P)<0.5判定為VRR>90%。以回歸模型繪制VRR為90%的受試者工作特征(receiver operating characteristic, ROC)曲線。P<0.05為差異有統計學意義。
2 結果
對115例患者均順利完成治療。術后11例(11/115,9.57%)訴明顯頸部脹痛并放射至面部、耳根、牙齒或肩部,于術后5天內完全消失;4例(4/115,3.48%)皮下或肌肉間血腫,于術后2~7天吸收;2例(2/115,1.74%)發熱,于術后3天退熱;3例(3/115,2.61%)出現一過性聲音嘶啞,于術后1天恢復;2例(2/115,1.74%)聲音嘶啞,于術后3個月恢復。
2.1 療效 術前及術后1、3、6、12個月結節體積呈持續減小趨勢(F=20.23,P<0.01),各時間點兩兩比較差異均有統計學意義(P均<0.05);術后12個月共29枚(29/115,25.22%)結節完全消失。術后1、3、6、12個月VRR呈逐漸增加趨勢(F=193.33,P<0.01),各時間點兩兩比較差異均有統計學意義(P均<0.05)。見表1、圖1。
表1 超聲引導下MWA治療良性甲狀腺結節前后各時間點結節體積、VRR比較(±s)
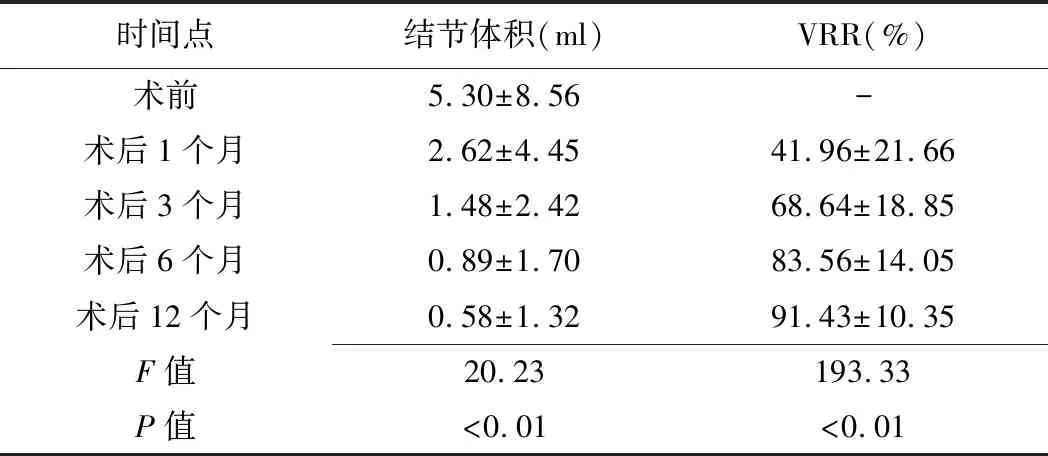
表1 超聲引導下MWA治療良性甲狀腺結節前后各時間點結節體積、VRR比較(±s)
時間點結節體積(ml)VRR(%)術前5.30±8.56-術后1個月2.62±4.4541.96±21.66術后3個月1.48±2.4268.64±18.85術后6個月0.89±1.7083.56±14.05術后12個月0.58±1.3291.43±10.35F值20.23193.33P值<0.01<0.01
注:結節體積、VRR各時間點兩兩比較,P均<0.05
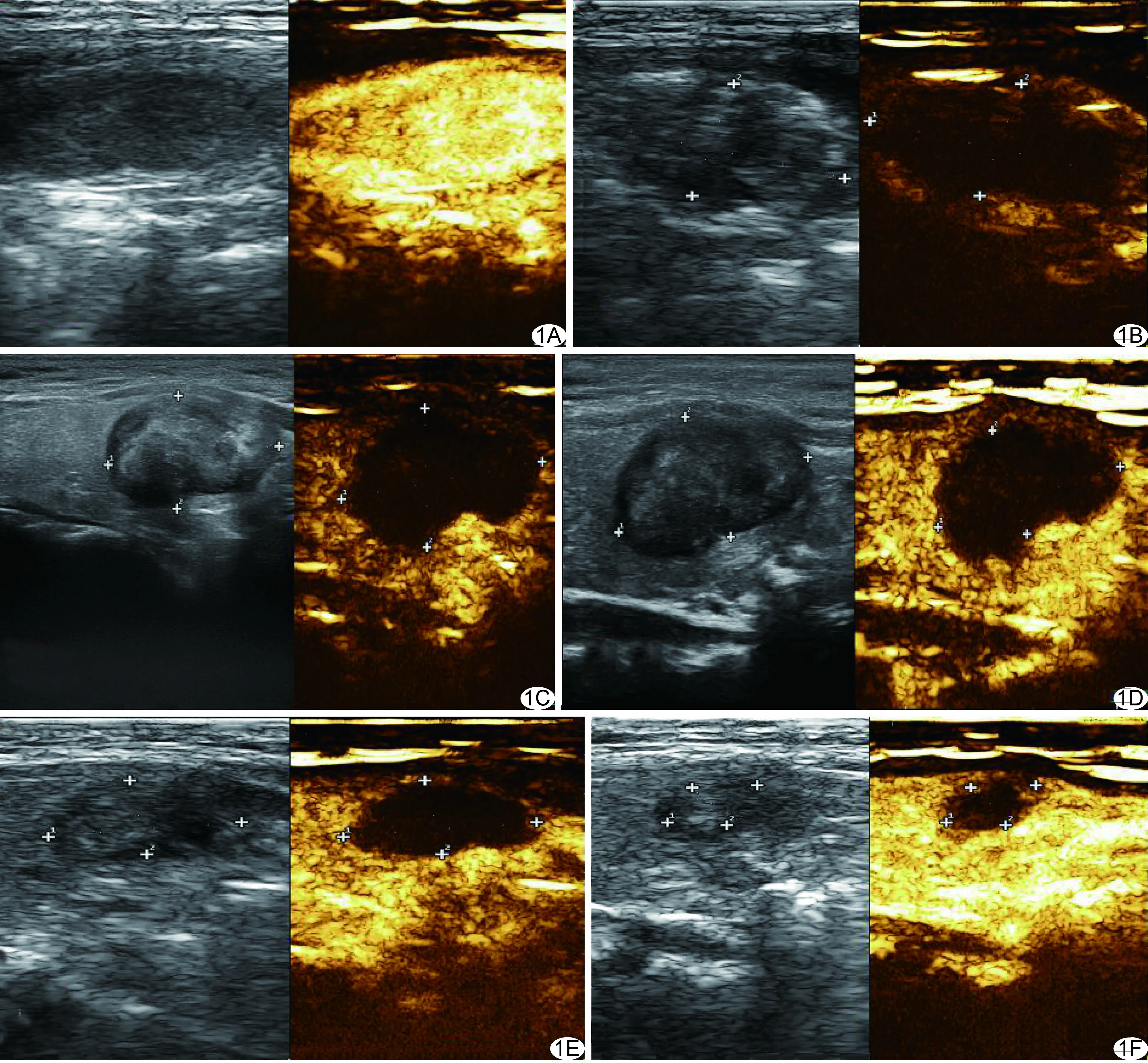
圖1 患者女,54歲,甲狀腺右葉良性結節,接受MVA治療 A.術前二維超聲聲像圖(左)示病灶呈橢圓形低回聲,邊界清晰,CEUS(右)呈均勻高增強; B.術后即刻結節被氣化區覆蓋(左),CEUS呈無增強(右); C~F.分別為術后1(C)、3(D)、6(E)、12(F)個月二維超聲聲像圖(左)及CEUS圖(右),病灶體積逐漸縮小
2.2 影響MWA療效的因素 至術后12個月,115例中,治愈75例,未治愈40例。單因素分析結果顯示,治愈與未治愈患者年齡、性別、術前甲狀腺功能、結節硬度及結節內鈣化差異均無統計學意義(P均>0.05),結節最大徑、術前體積、回聲、內部成分、血流分布、增強模式及術后即刻體積組間差異均有統計學意義(P均<0.05)。針對差異有統計學意義的變量行多因素Logistic回歸分析,結果顯示結節內部成分、增強模式及術后即刻體積是MWA療效的獨立影響因素(P均<0.05)。見表2、3。
2.3 預測效能 將篩選出的3個變量,即結節內部成分(X1)、增強模式(X2)及消融術后即刻體積(X3)帶入Logistic回歸方程,得出公式logit(P)=-1.242+1.997X1(囊性為主)-1.9X1(實性為主)-0.386X2(等增強)+1.171X2(高增強)+0.077X3。根據回歸模型繪制預測MWA療效的ROC曲線,結果顯示曲線下面積(area under the curve, AUC)為0.82,敏感度67.50%,特異度88.00%,準確率79.13%。
3 討論
MWA利用組織中水分子在消融過程中振蕩所產熱能使腫瘤細胞凋亡并發生凝固性壞死,壞死組織最終被機體免疫系統降解[6]。本研究結果顯示,MWA術后,隨時間延長,甲狀腺結節體積逐漸縮小、VRR逐漸增大,與既往研究[7-8]結果相符。
本研究單因素及多因素回歸分析結果顯示,結節內部成分、增強模式及消融術后即刻體積為影響MVA效果的獨立因素。術后12個月囊性為主結節的VRR明顯大于實性及實性為主結節,而實性結節與實性為主結節之間VRR無明顯差異;分析原因,可能在于本組對囊性為主結節首先抽吸囊液,再對實質部分進行MWA,術后即刻結節體積已較術前明顯縮小,而VRR計算結節體積所用為抽液前數據。
囊液抽吸過程中,少數結節囊腔內可能存在新鮮出血,當出血速度較快又無法確定出血點時,處理較為棘手,故抽吸囊液時應避免針尖劃傷實質部分或囊壁,抽吸速度不宜過快,以免囊腔內壓力驟降增加出血風險。如結節實性部分血流較豐富,可先消融實性部分,再于抽液后消融囊壁,以減少囊內出血。
本研究治愈與未治愈結節間最大徑、術前體積及消融術后即刻體積差異均有統計學意義。盡管不同研究[5]所采用的直徑或體積分組標準有所差異,但對于治療后小結節的VRR較大結節更顯著的認識基本一致。消融術后壞死組織被巨噬細胞、淋巴細胞等包裹、吞噬,最終被機體清除[9]。結節體積越大,病灶區壞死組織越多,吞噬、清除所需時間越長。多因素回歸分析顯示消融術后即刻結節體積是療效的獨立影響因素,提示術者應在保證結節消融完全的基礎上盡量縮小消融區范圍,以利于結節吸收。
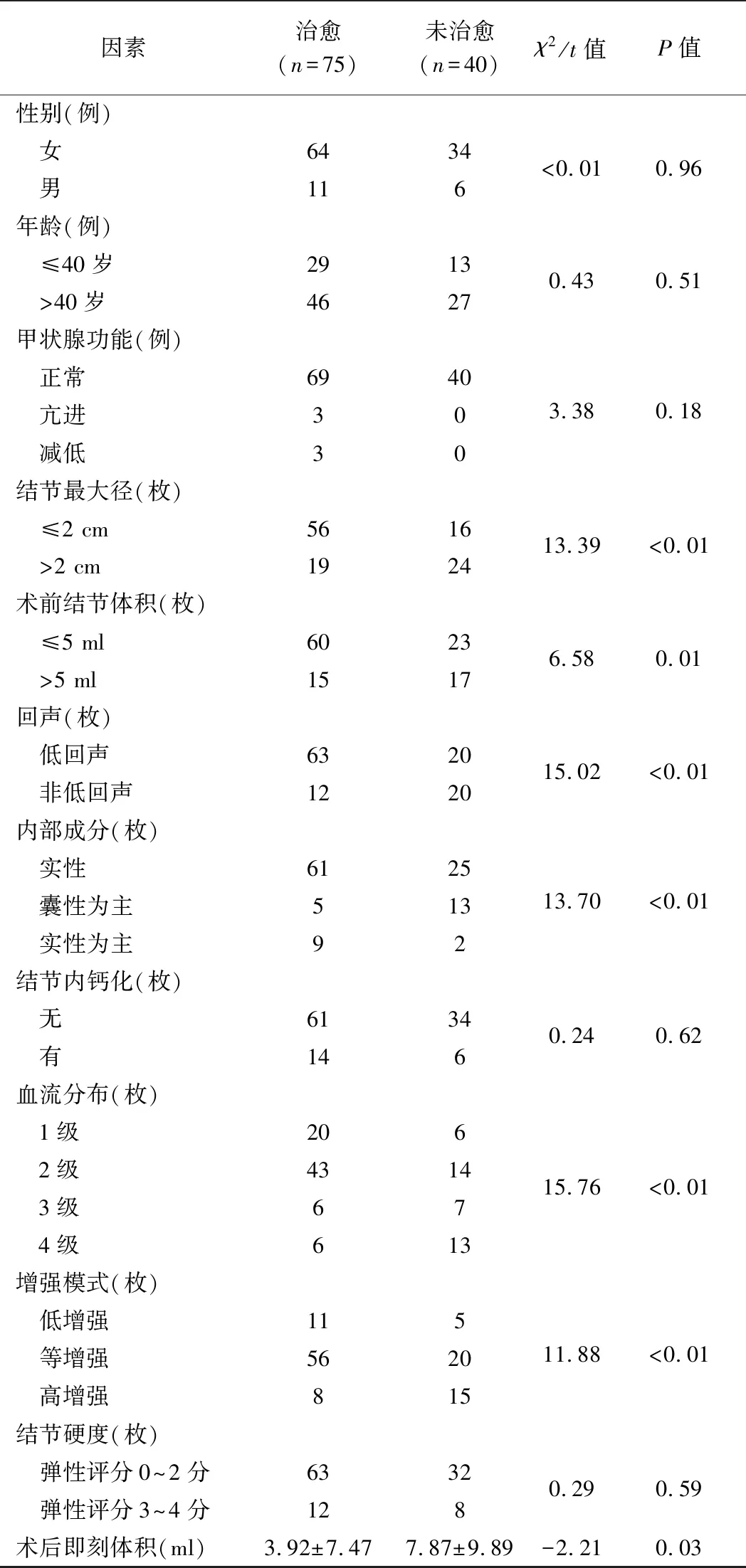
表2 超聲引導下MWA后治愈與未治愈甲狀腺良性結節相關因素比較
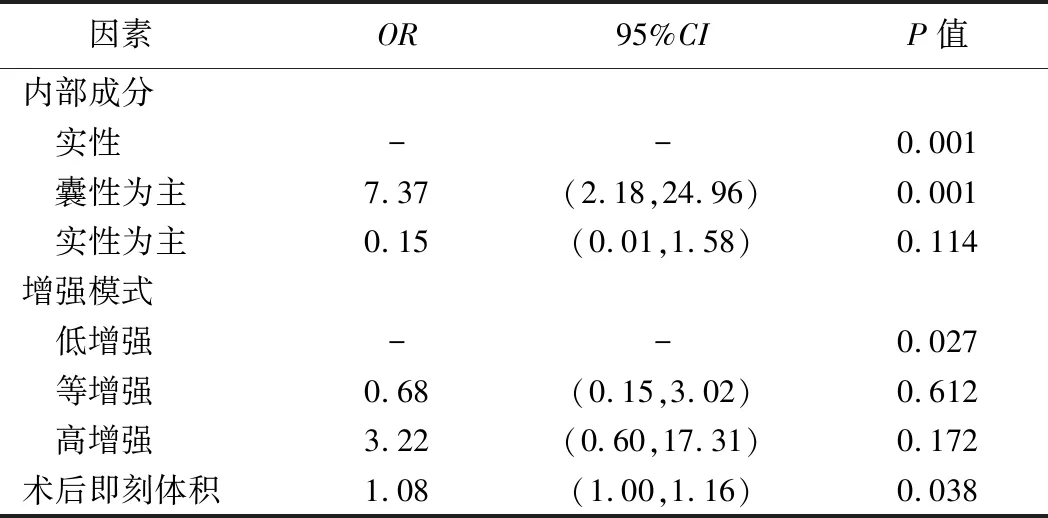
表3 影響超聲引導下MWA治療甲狀腺良性結節效果的多因素Logistic回歸分析
DEANDREA等[10]關于射頻消融治療甲狀腺良性結節的多中心研究顯示,血流豐富的結節對消融治療反應更佳。本研究中,MWA治療高增強結節較其他增強模式治療結節療效更優,可能原因為CEUS反映結節內微循環灌注情況,高增強結節內部纖維組織及間質占比較低,而血液占比較高,其內水分子更多,MWA短時間內振蕩可產生更多熱能,熱凝固效果更強。此外,消融時間較短有利于減少碳化帶和結節吸收。
總之,超聲引導下MWA是治療甲狀腺良性結節的有效且安全的方法;結節內部成分、增強模式及術后即刻體積是MWA療效的獨立影響因素。但本研究納入樣本量相對少,且缺少長期隨訪數據,尚需完善。