LncRNA44372在卵巢癌中的差異表達(dá)及生物信息學(xué)分析
丁璟, 楊鑫鑫, 鄒雪琴, 高淑君, 劉雪, 潘玲麗,張?chǎng)q丹, 趙楊靜, 梁秀婷,王薈, 朱彥玲, 邵啟祥
(1. 江蘇大學(xué)醫(yī)學(xué)院, 江蘇 鎮(zhèn)江 212013; 2. 江蘇大學(xué)附屬徐州醫(yī)院婦產(chǎn)科, 江蘇 徐州 221005)
長(zhǎng)鏈非編碼RNA(long non-coding RNA,lncRNA)是長(zhǎng)度大于200 nt的RNA轉(zhuǎn)錄物,具有很少的蛋白編碼功能[1]。研究表明,lncRNA與多種生理和病理過(guò)程有關(guān),尤其是癌癥的發(fā)生發(fā)展,其異常表達(dá)可致癌細(xì)胞不受細(xì)胞周期調(diào)控,無(wú)限增殖[2]。lncRNA可從基因的轉(zhuǎn)錄前、轉(zhuǎn)錄和轉(zhuǎn)錄后水平進(jìn)行調(diào)控,還調(diào)控DNA甲基化,重構(gòu)染色質(zhì)和組蛋白甲基化、乙酰化等表觀遺傳[3]。lncRNA常見的作用機(jī)制是通過(guò)海綿體吸附某些miRNA從而影響下游靶mRNA,構(gòu)成競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò),從而調(diào)控基因的表達(dá)和功能的發(fā)揮[4]。但是,lncRNA在卵巢癌中發(fā)揮的生物學(xué)作用尚不清楚。本研究通過(guò)GEO數(shù)據(jù)庫(kù)篩選獲得在卵巢癌中具有顯著差異表達(dá)的lncRNA44372,其位于chr6:165773201-165773271。進(jìn)一步采用生物信息學(xué)技術(shù)對(duì)其生物學(xué)作用進(jìn)行預(yù)測(cè)分析,并運(yùn)用定量PCR驗(yàn)證其在卵巢癌細(xì)胞中的表達(dá)水平。
1 材料與方法
1.1 細(xì)胞株、主要試劑與儀器
人卵巢癌細(xì)胞系HO8910,3AO,A2780,OVCR3以及卵巢上皮HOSEpiC細(xì)胞由江蘇大學(xué)醫(yī)學(xué)院周小明教授惠贈(zèng);人卵巢癌SKOV3細(xì)胞由江蘇大學(xué)醫(yī)學(xué)院盧小東教授惠贈(zèng)。
DMEM,RPMI 1640,胎牛血清購(gòu)于美國(guó)Gibco公司;Trizol 試劑購(gòu)于寶日醫(yī)生物技術(shù)(北京)有限公司;異丙醇、氯仿、無(wú)水乙醇購(gòu)自上海國(guó)藥集團(tuán)化學(xué)試劑有限公司;逆轉(zhuǎn)錄試劑盒、PCR ExTaqDNA聚合酶和SYBR?Premix ExTaqTMⅡ購(gòu)自寶日醫(yī)生物技術(shù)(北京)有限公司;焦炭酸二乙酯(DEPC)水購(gòu)于上海生工生物工程有限公司;實(shí)時(shí)熒光定量PCR儀(美國(guó)Bio-Rad公司);NanoDrop1000測(cè)定儀(美國(guó)Thermo Scientific公司)。
1.2 研究方法
1.2.1 下載數(shù)據(jù)庫(kù) 從NCBI GEO(https:∥www.ncbi.nlm.nih.gov/geo/)數(shù)據(jù)庫(kù)中下載基因芯片數(shù)據(jù)集。進(jìn)入NCBI網(wǎng)站,找到“GEO DataSets”搜索關(guān)鍵詞“ovarian tissue samples”,“normal”,“tumor”,點(diǎn)擊“search”,下載基因表達(dá)譜芯片數(shù)據(jù)GSE119054。它的基因芯片平臺(tái)是GPL19615 Agilent-067406 CBC lncRNA + mRNA microarray V4.0。
1.2.2 篩選在卵巢癌中差異表達(dá)的lncRNA 在腫瘤轉(zhuǎn)錄組數(shù)據(jù)庫(kù)CRN(http:∥syslab4.nchu.edu.tw/index.jsp)中對(duì)來(lái)自NCBI GEO數(shù)據(jù)庫(kù)中卵巢癌及正常組織樣本數(shù)據(jù)分析,以P<0.05,差異倍數(shù)1.2倍以上為條件,篩選出在卵巢癌中表達(dá)上調(diào)和下調(diào)的lncRNA。
1.2.3 篩選與lncRNA44372作用的相關(guān)基因 通過(guò)在線工具Annolnc(http:∥annolnc.cbi.pku.edu.cn/)[5]篩選出可能與lncRNA44372表達(dá)水平相關(guān)的基因,并用互作分?jǐn)?shù)來(lái)表示共表達(dá)的強(qiáng)度。
1.2.4 lncRNA44372的GO分析和信號(hào)通路分析 利用在線工具David[6-7](https:∥david.ncifcrf.gov)對(duì)篩選出的共表達(dá)基因進(jìn)行基因本體論分析(gene ontology,GO)及信號(hào)通路分析。
1.2.5 lncRNA44372的競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)構(gòu)建 通過(guò)在線工具starbase(http:∥starbase.sysu.edu.cn/)研究lncRNA44372可靶向的miRNA分子和下游靶mRNA分子。利用在線數(shù)據(jù)庫(kù)GEPIA(http:∥gepia.cancer-pku.cn)研究靶mRNA分子在卵巢癌中的表達(dá)量。
1.2.6 細(xì)胞培養(yǎng) 將卵巢癌SKOV3,HO8910,OVCR3和3AO細(xì)胞用含10%胎牛血清的DMEM培養(yǎng),卵巢上皮細(xì)胞癌A2780細(xì)胞和卵巢上皮HOSEpiC細(xì)胞用含10%胎牛血清的RPMI 1640培養(yǎng)基培養(yǎng)。
1.2.7 RNA提取 取對(duì)數(shù)生長(zhǎng)期的“1.2.6”細(xì)胞,以1×105密度接種于6孔板中,待細(xì)胞長(zhǎng)至匯合度80%時(shí)取出;棄去培養(yǎng)基,用預(yù)冷PBS洗滌2次;每孔加入1 mL Trizol 試劑,在冰上靜置5 min;用微量移液器小心吹打細(xì)胞使其脫落并轉(zhuǎn)移至1.5 mL EP管中,加入200 μL氯仿,上下顛倒混勻5次,靜置5 min;于4 ℃ 12 000×g離心15 min;取上清液,加入500 μL異丙醇,上下顛倒混勻5次后靜置5 min;于4 ℃ 12 000×g離心10 min;棄上清液,每管加入75%乙醇1 mL漂洗沉淀;于4 ℃ 7 500×g離心5 min;棄去上清液后室溫干燥,每管加入適量DEPC水溶解RNA,用NanoDrop ND-1000測(cè)定RNA濃度和純度。
1.2.8 逆轉(zhuǎn)錄反應(yīng) 根據(jù)逆轉(zhuǎn)錄試劑盒說(shuō)明書將提取的總RNA逆轉(zhuǎn)錄成cDNA。反應(yīng)條件:37 ℃反應(yīng)15 min, 85 ℃反應(yīng)5 min,4 ℃得到cDNA,保存于-20 ℃?zhèn)溆谩?/p>
1.2.9 實(shí)時(shí)熒光定量PCR檢測(cè)lncRNA44372表達(dá) 引物設(shè)計(jì)采用Primer 5.0軟件,β-肌動(dòng)蛋白上游引物序列為5′-CACGAAACTACCTTCAACTCC-3′,下游引物序列為5′-ATACTCCTGCTTGCTGATC-3′;lncRNA44372上游引物序列為5′-TATTGCACTTGGACGGAGCA-3′,下游引物序列為5′-AAGGCAAGCAACTTGACACG-3′,引物由上海生工生物工程有限公司合成。以cDNA 0.5 μL為模板,上下游引物各0.2 μL,SYBR Premix ExTaqTMⅡ5.0 μL,滅菌水4.1 μL,配制10 μL反應(yīng)體系。反應(yīng)條件:95 ℃預(yù)變性30 s,95 ℃ 變性5 s,60 ℃退火30 s,72 ℃延伸30 s,共40個(gè)循環(huán)。每個(gè)樣本設(shè)置3個(gè)復(fù)孔,根據(jù)熔解曲線形態(tài)判斷反應(yīng)的特異性,通過(guò)2-ΔΔCt法計(jì)算目的基因相對(duì)表達(dá)量。
1.3 統(tǒng)計(jì)學(xué)分析
2 結(jié)果
2.1 卵巢癌中差異表達(dá)的lncRNA
在腫瘤轉(zhuǎn)錄組數(shù)據(jù)網(wǎng)站CRN中對(duì)來(lái)自NCBI GEO數(shù)據(jù)庫(kù)中有關(guān)的卵巢癌樣本結(jié)果分析,其中根據(jù)表達(dá)量差異及P值發(fā)現(xiàn),與卵巢正常組織相比,卵巢癌組織中表達(dá)上調(diào)的lncRNA有CROCCP2,lncRNA 00883,lncRNA00704,MCM3AP-AS1,DLEU2,NBLA00301;表達(dá)下調(diào)的lncRNA有l(wèi)ncRNA44372,lncRNA00657,RP11-890B15.3,TP73-AS1,差異具有統(tǒng)計(jì)學(xué)意義(P<0.05)。本實(shí)驗(yàn)室前期芯片檢測(cè)結(jié)果[7]發(fā)現(xiàn),在卵巢癌細(xì)胞系中有227個(gè)lncRNA表達(dá)上調(diào),有483個(gè)lncRNA表達(dá)下調(diào);結(jié)合基因表達(dá)譜芯片數(shù)據(jù)GSE119054選擇lncRNA44372作為研究對(duì)象。
2.2 與lncRNA44372作用相關(guān)的共表達(dá)基因的篩選結(jié)果
根據(jù)相關(guān)作用分?jǐn)?shù)及P值<0.05,篩選出與lncRNA44372存在相互作用關(guān)系的基因有579個(gè)。根據(jù)相關(guān)作用分?jǐn)?shù)對(duì)579個(gè)基因進(jìn)行排序,篩選出最具有相關(guān)性的10個(gè)基因(表1)。這些基因的功能主要涉及蛋白激酶活性、細(xì)胞凋亡、細(xì)胞周期等。
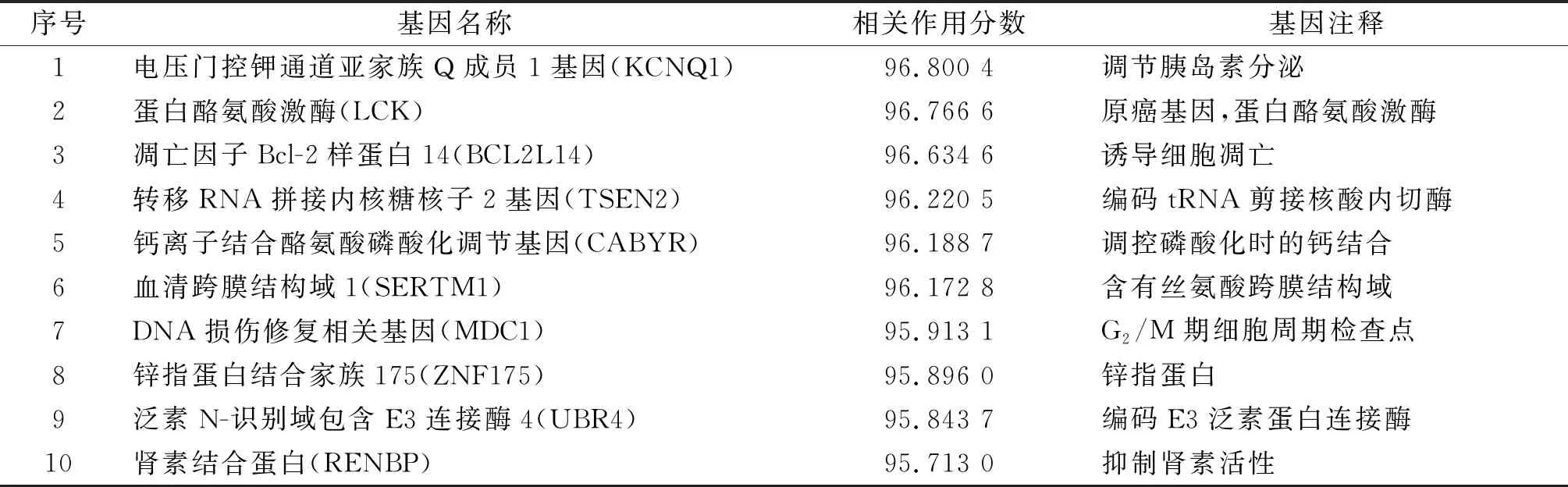
表1 相關(guān)性顯著的10個(gè)基因
2.3 與lncRNA44372共表達(dá)基因的GO分析
對(duì)579個(gè)相關(guān)基因和lncRNA44372進(jìn)行GO分析(表2)。結(jié)果顯示,共表達(dá)基因在生物過(guò)程中富集在細(xì)胞周期調(diào)控、細(xì)胞轉(zhuǎn)運(yùn)、細(xì)胞骨架調(diào)控、細(xì)胞遷移、蛋白肽調(diào)節(jié)等方面;分子功能主要富集在信號(hào)傳感器活性的調(diào)節(jié)、MHCⅡ類受體分子的活性、GTP酶激活劑活性、蛋白蘇氨酸/酪氨酸激酶活性、蛋白結(jié)合能力等方面。見圖1。
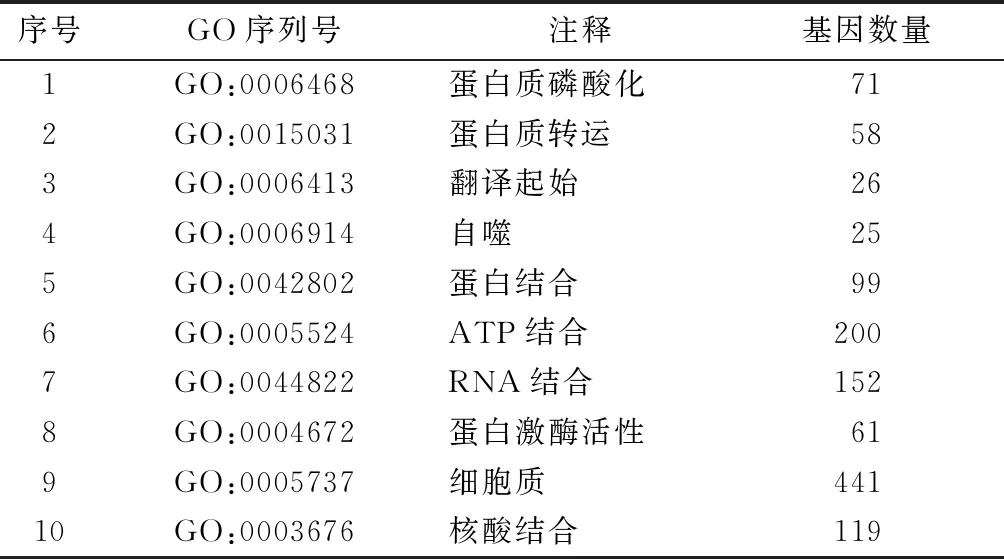
表2 相關(guān)基因的GO分析
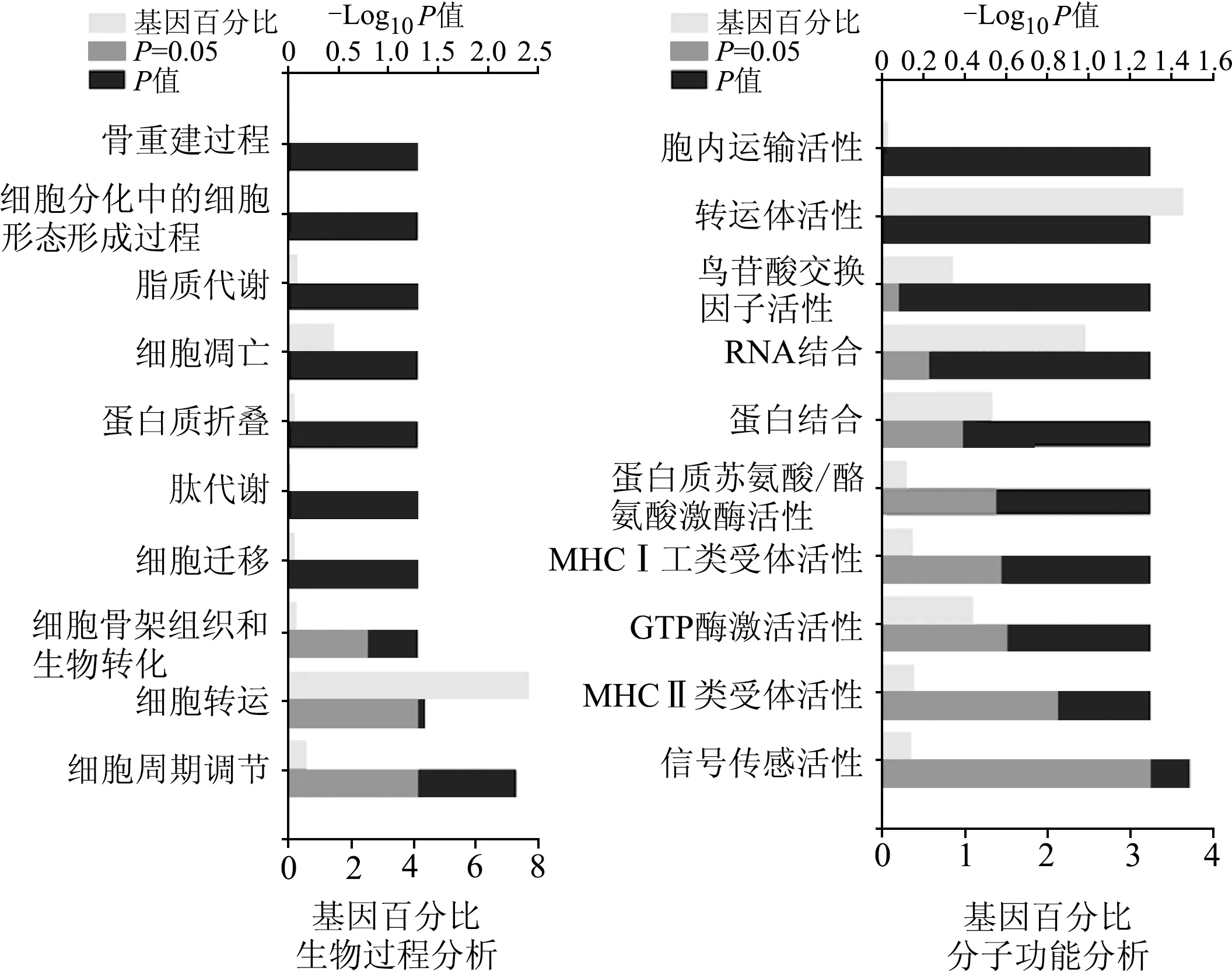
圖1 相關(guān)基因的GO分析
2.4 與lncRNA44372共表達(dá)基因的信號(hào)通路分析
信號(hào)通路富集分析表明,lncRNA44372可以在腫瘤壞死因子受體及其介導(dǎo)的細(xì)胞凋亡途徑、p75神經(jīng)營(yíng)養(yǎng)因子受體介導(dǎo)的細(xì)胞凋亡通路,神經(jīng)生長(zhǎng)因子及其受體酪氨酸激酶A介導(dǎo)的腫瘤發(fā)生、增殖、血管生成和轉(zhuǎn)移等相關(guān)途徑發(fā)揮作用。
2.5 lncRNA44372的競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)構(gòu)建
生物信息學(xué)在線工具starbase分析發(fā)現(xiàn)lncRNA44372可靶向的miRNA分子有miR-190和miR-193,相關(guān)的下游靶mRNA分子有UBLCP1、PHF20L1、ULK2、MED15、DPY19L1、PYROXD1和LONP2等(圖2 A)。通過(guò)GEPIA數(shù)據(jù)庫(kù)預(yù)測(cè)靶mRNA分子在卵巢癌中的表達(dá),結(jié)果顯示與正常樣本相比,ULK2分子(t=2.43,P<0.05)和LONP2分子(t=2.49,P<0.05)在卵巢癌中表達(dá)明顯降低(圖2B)。
2.6 lncRNA44372在卵巢癌細(xì)胞的表達(dá)
qRT-PCR檢測(cè)結(jié)果顯示,與卵巢正常HOSEpiC細(xì)胞相比,lncRNA44372在卵巢癌細(xì)胞A2780(t=13.18,P<0.01),SKOV3(t=12.82,P<0.01),HO8910(t=5.36,P<0.05),OVCR3(t=5.19,P<0.05),3AO(t=4.73,P<0.05)中表達(dá)明顯下調(diào),且與生物信息學(xué)結(jié)果一致。見圖3。
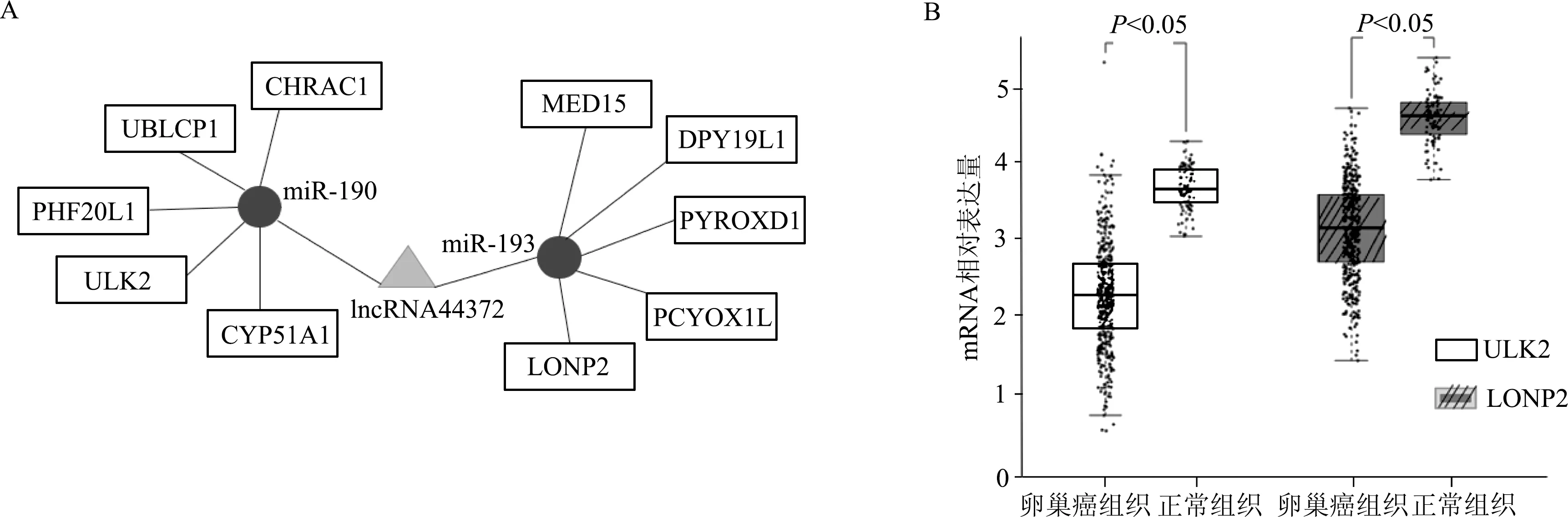
A:競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)構(gòu)建; B: ULK2和LONP2在卵巢癌組織及正常組織中的表達(dá)圖2 競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)及靶mRNA在卵巢癌組織和正常組織中的表達(dá)
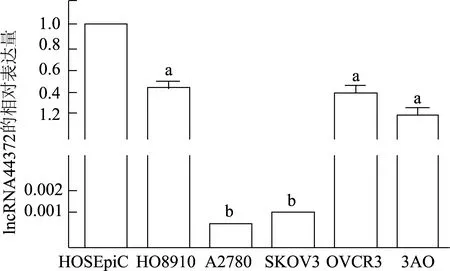
a:P<0.05,b: P<0.01,與HOSEpiC細(xì)胞比較圖3 lncRNA44372在卵巢癌細(xì)胞系和卵巢正常細(xì)胞中的表達(dá)
3 討論
本研究首先通過(guò)NCBI GEO數(shù)據(jù)庫(kù)篩選出在卵巢癌中表達(dá)具有差異意義的lncRNA44372,并進(jìn)一步分析與其相關(guān)的基因。GO分析和信號(hào)通路分析結(jié)果顯示,lncRNA44372可能與調(diào)控細(xì)胞遷移、侵襲變化,細(xì)胞周期改變,細(xì)胞骨架蛋白調(diào)控,蛋白蘇氨酸/酪氨酸激酶活性的調(diào)節(jié)等有關(guān)。
研究表明,細(xì)胞遷移和侵襲變化可促進(jìn)腫瘤細(xì)胞的上皮間質(zhì)轉(zhuǎn)化過(guò)程[8],促進(jìn)腫瘤轉(zhuǎn)移;細(xì)胞周期失控可以使得腫瘤細(xì)胞不接受抑制信號(hào),持續(xù)增殖[9];細(xì)胞骨架蛋白R(shí)ho經(jīng)GDP激活后,可以與下游分子結(jié)合使得細(xì)胞骨架重排。有文獻(xiàn)指出,lncRNA PCGEM1可以通過(guò)上調(diào)RhoA表達(dá)促進(jìn)卵巢癌的發(fā)展[10]。此外,蘇氨酸/酪氨酸蛋白激酶活性對(duì)腫瘤細(xì)胞的遷移具有調(diào)控作用。例如,lncRNA-BANCRY通過(guò)激活蘇氨酸/酪氨酸蛋白激酶,從而通過(guò)調(diào)節(jié)細(xì)胞自噬來(lái)抑制甲狀腺癌細(xì)胞增殖[11]。但是,lncRNA44372在上述生物學(xué)過(guò)程中發(fā)揮的作用尚需進(jìn)一步研究。
通過(guò)生物信息學(xué)預(yù)測(cè),lncRNA44372可能與miR-190,miR-193及下游UBLCP1、PHF20L1、ULK2、MED15、DPY19L1、PYROXD1和LONP2的靶mRNA分子構(gòu)成競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)。在該網(wǎng)絡(luò)中,與正常組織相比,lncRNA44372呈低表達(dá)且像海綿體一樣吸附靶miRNA分子,而被吸附的miRNA分子可負(fù)向調(diào)控靶mRNA分子。因此,只有在卵巢癌中下調(diào)表達(dá)的mRNA分子才可能發(fā)揮作用。
研究發(fā)現(xiàn),ULK2分子在卵巢癌中呈低表達(dá),其主要作用是編碼絲氨酸/蘇氨酸激酶,并且可以調(diào)節(jié)細(xì)胞代謝和自噬途徑[12],該發(fā)現(xiàn)與本研究中GO分析結(jié)果相一致。此外,LONP2分子同樣在卵巢癌中呈低表達(dá)。有研究發(fā)現(xiàn),LONP2 在宮頸癌中通過(guò)氧化應(yīng)激促進(jìn)子宮頸癌細(xì)胞增殖、遷移和侵襲[13]。因此推斷,lncRNA44372可能與miR-190,miR-193及ULK2和LONP2構(gòu)成競(jìng)爭(zhēng)性內(nèi)源RNA網(wǎng)絡(luò)。此外,在細(xì)胞水平證實(shí)lncRNA44372在卵巢癌中呈低表達(dá),與生物信息學(xué)預(yù)測(cè)結(jié)果一致。
綜上所述,lncRNA44372在卵巢癌組織中呈低表達(dá),可能通過(guò)影響卵巢癌細(xì)胞凋亡、細(xì)胞周期和細(xì)胞蛋白激酶活性等促進(jìn)卵巢癌發(fā)展。

