注射用丹參多酚酸鹽對動脈粥樣硬化大鼠的作用和機制探討*
陳 麗,蔡惠鈴,李影雄,孟泳錚,李敏霞
(1.佛山市中醫院,廣東 佛山 528000;2.廣州中醫藥大學第二附屬醫院,廣東 廣州 510102)
動脈粥樣硬化(atherosclerosis,AS)是一種全身性慢性疾病,是冠心病、缺血性腦卒中等多種心腦血管疾病最重要的病理基礎,最終致死率和致殘率非常高[1]。流行病學調查顯示,冠心病、腦卒中等動脈粥樣硬化性疾病是我國居民致死的首要原因,嚴重威脅我國居民的健康,降低生活質量[2]。而且隨著生活方式的改變和老齡人口的劇增,AS的發病率明顯上升并且趨于年輕化。脂質代謝紊亂、炎癥反應、氧化損傷、細胞外基質降解等均是導致AS發生發展的核心機制[3]。AS屬于中醫學“胸痹”“脈痹”“中風”等范疇,其核心病機為瘀血痹阻。注射用丹參多酚酸鹽由丹參提取而成,具有活血、化瘀、通脈等功效,本課題組臨床研究發現注射用丹參多酚酸鹽可以降低冠心病、腦卒中患者頸動脈斑塊厚度,縮小斑塊面積,但其機制仍未闡明。因此,本實驗復制了AS大鼠模型,并給予注射用丹參多酚酸鹽干預,觀察其對AS大鼠斑塊、血脂、炎癥、氧化損傷、細胞外基質等的影響,初步探討其防治AS的作用和可能機制。
1 材料與方法
1.1 實驗動物6周齡SPF級雄性SD大鼠43只,體質量(200±10)g,購自廣東省醫學實驗動物中心,生產許可證號:SCXK(粵)2019-0035;飼養環境為溫度(22±2)℃,濕度50%~60%,12 h明暗交替。實驗過程中采用過量麻醉法處死。高脂飼料配方:基礎飼料81.3%、豬油10%、蔗糖5%、丙基硫氧嘧啶0.2%、膽酸鈉0.5%、膽固醇3%;基礎飼料和高脂飼料委托廣東省醫學實驗動物中心進行加工。本實驗通過佛山市中醫院醫學實驗動物倫理委員會的批準。
1.2 藥物與試劑 注射用丹參多酚酸鹽(上海綠谷制藥有限公司,批號:20190113,規格:100 mg/瓶);阿托伐他汀鈣片(輝瑞制藥有限公司,批號:20181215,規格:10 mg/片);血脂試劑盒[總膽固醇(total cholesterol,TC)試劑盒(貨號:HL20142)、甘油三酯(triglyceride,TG)試劑盒(貨號:HL20195)、低密度脂蛋白膽固醇(low density lipoprotein cholesterol,LDL-C)試劑盒(貨號:HL20197)、高密度脂蛋白膽固醇(high density lipoprotein cholesterol,HDL-C)試劑盒(貨號:HL20196)、氧化型低密度脂蛋白(oxidized low density lipoprotein,ox-LDL)試劑盒(貨號:HL10046)](上海哈靈生物科技有限公司);腫瘤壞死因子-α(TNF-α)試劑盒(貨號:ER1393)、白介素-1β(IL-1β)試劑盒(貨號:ER1094)、白介素-6(IL-6)試劑盒(貨號:ER1105)、白介素-10(IL-10)試劑盒(貨號:ER0033)(武漢菲恩生物科技有限公司);超氧化物歧化酶(SOD)試劑盒(貨號:GD-AW1922)、谷胱甘肽過氧化物酶(glutathione peroxidase,GSH-Px)試劑盒(貨號:GD-JG0454-E)、丙二醛(malondialdehyde,MDA)試劑盒(貨號:GD-S1921-A)、單核細胞趨化蛋白-1(Monocyte chemoattractant protein-1,MCP-1)試劑盒(貨號:GD-DS1710)、血管細胞黏附分子-1(Vascular Cell Adhesion Molecule-1,VCAM-1)試劑盒(貨號:GD-DX1591)、基質金屬蛋白酶-9(matrix metalloproteinases-9,MMP-9)試劑盒(上海古朵生物科技有限公司)。
1.3 主要儀器TGL-15M臺式微量高速冷凍離心機(湖南平凡科技有限公司);AU5800全自動生化分析儀(貝克曼庫爾特商貿中國有限公司);HBS-1096C酶標分析儀(南京德鐵實驗設備有限公司);Tissuelyser-24冷凍液氮低溫研磨儀(上海凈信實業發展有限公司)。
1.4 造模與分組43只大鼠進行適應性喂養7 d,隨機取10只作為對照組。其余33只大鼠參照文獻[4]建立AS大鼠模型,造模第1天一次性腹腔注射維生素D3 60萬U/kg,并且給予高脂飼料喂養(20 g/d);對照組大鼠一次性腹腔注射等體積的生理鹽水,并且給予基礎飼料喂養(20 g/d),造模時間為8周。AS模型成功的標準[5]:主動脈見斑塊形成。8周后,27只大鼠造模成功,造模成功率為81.82%(27/33)。隨后將成模27只大鼠隨機分為模型組、丹參多酚酸鹽組和阿托伐他汀組,每組9只。
1.5 實驗給藥 按照“人和動物體表面積折算的等效劑量比率表”,丹參多酚酸鹽組大鼠予以注射用丹參多酚酸鹽腹腔注射,20 mg/(kg·d);阿托伐他汀組大鼠灌胃給予阿托伐他汀鈣片溶液,2 mg/(kg·d),對照組和模型組大鼠予以等體積的生理鹽水腹腔注射,連續給藥4周。4周后處死大鼠,取材并進行相關指標檢測。
1.6 觀察指標
1.6.1 血清指標 腹腔注射10%水合氯醛麻醉后,剖開腹腔,腹主動脈取血,離心后取血清,采用全自動生化檢測儀檢測大鼠血清TC、TG、LDL-C、HDL-C,ELISA法檢測血清ox-LDL、TNF-α、IL-1β、IL-6含量,光度法測定血清SOD、GSH-Px、MDA含量。
1.6.2 主動脈病理變化 處死大鼠,取主動脈,生理鹽水沖洗后4%多聚甲醛固定,石蠟包埋,切片,HE染色。光鏡下觀察主動脈病理變化。
1.6.3 主動脈MCP-1、VCAM-1、MMP-9含量 取適量大鼠主動脈組織,PBS反復清洗去除血液,稱重,將主動脈和PBS加入勻漿器后充分研磨,再利用超聲破碎。勻漿液經5 000 g離心5 min后取上清液,采用ELISA法檢測MCP-1、VCAM-1、MMP-9含量。
1.7 統計學方法 采用SPSS 25.0軟件進行統計處理,計量資料用“均數±標準差”(±s)表示,多組間比較采用單因素方差分析,兩兩比較采用LSD-t法檢驗,以P<0.05為差異有統計意義。
2 結 果
2.1 各組大鼠主動脈病理變化 對照組大鼠主動脈內膜、中膜、外膜均未見增生、肥厚;模型組大鼠主動脈中膜平滑肌細胞明顯增生,血管壁明顯增厚,大量泡沫細胞聚集,形成一動脈粥樣硬化斑塊;丹參多酚酸鹽組和阿托伐他汀組大鼠主動脈中膜輕微增生,無動脈粥樣硬化斑塊形成。(見圖1)

圖1 各組大鼠主動脈病理變化(HE,×200,標尺=100μm)
2.2 各組大鼠血清TC、TG、LDL-C、HDL-C、ox-LDL含量比較 與對照組比較,模型組大鼠血清TC、TG、LDL-C、ox-LDL含量明顯升高(P<0.05),HDL-C含量明顯降低(P<0.05);與模型組比較,丹參多酚酸鹽組和阿托伐他汀組大鼠血清TC、TG、LDL-C、ox-LDL含量明顯降低(P<0.05),HDL-C含量明顯升高(P<0.05)。(見圖2)

圖2 各組大鼠血清TC、TG、LDL-C、HDL-C、ox-LDL含量比較(±s,n=9)
2.3 各組大鼠血清TNF-α、IL-1β、IL-6、IL-10含量比較 與對照組比較,模型組大鼠血清TNF-α、IL-1β、IL-6含量明顯升高(P<0.05),IL-10含量明顯降低(P<0.05);與模型組比較,丹參多酚酸鹽組和阿托伐他汀組大鼠血清TNF-α、IL-1β、IL-6含量明顯降低(P<0.05),IL-10含量明顯升高(P<0.05)。(見圖3)
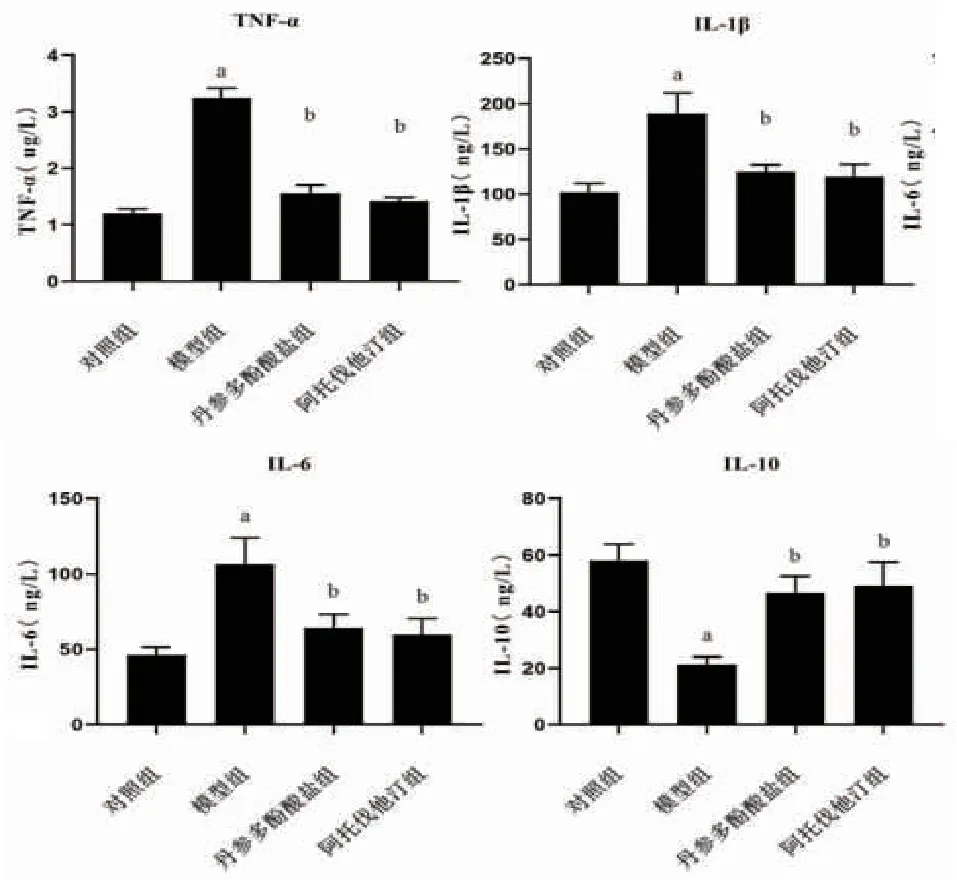
注:與對照組比較,aP<0.05;與模型組比較,bP<0.05
圖3各組大鼠血清TNF-α、IL-1β、IL-6、IL-10含量比較(±s,n=9)
2.4 各組大鼠血清SOD、GSH-Px、MDA含量比較 與對照組比較,模型組大鼠血清MDA含量明顯升高(P<0.05),SOD、GSH-Px含量明顯降低(P<0.05);與模型組比較,丹參多酚酸鹽組和阿托伐他汀組大鼠血清MDA含量明顯降低(P<0.05),SOD、GSH-Px含量明顯升高(P<0.05)。(見圖4)
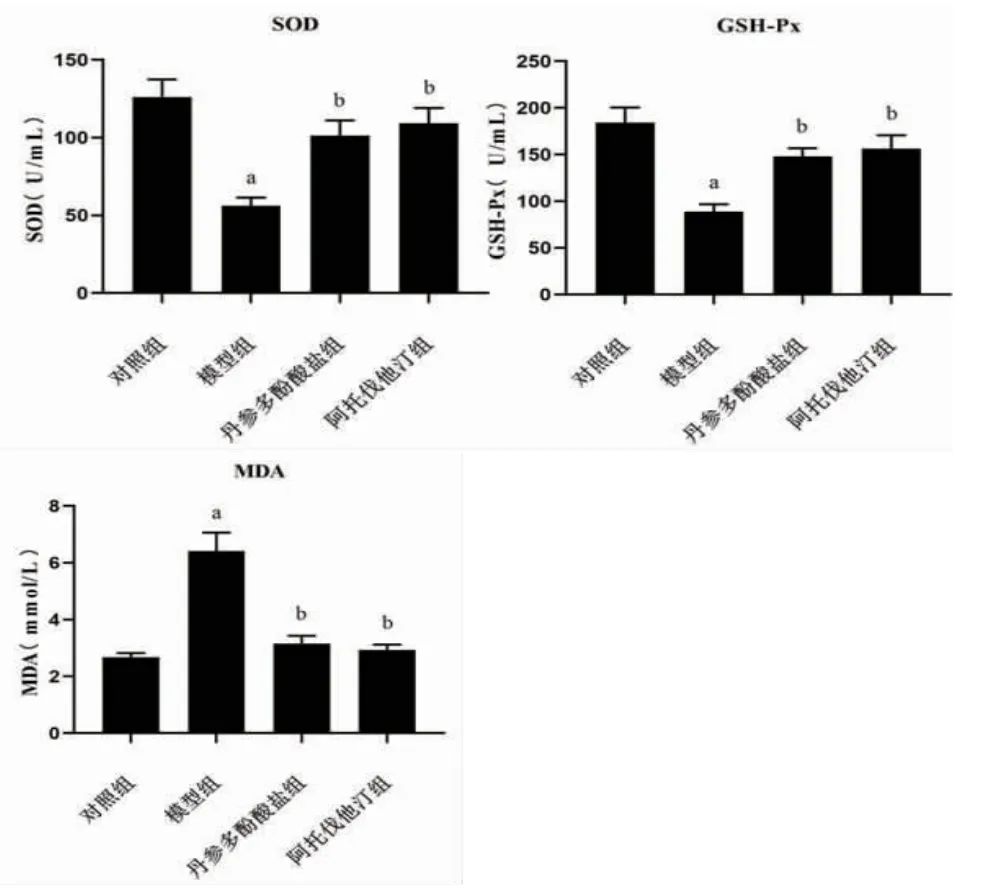
圖4 各組大鼠SOD、GSH-Px、MDA含量比較(±s,n=9)
2.5 各組大鼠主動脈MCP-1、VCAM-1、MMP-9含量比較 與對照組比較,模型組大鼠主動脈MCP-1、VCAM-1、MMP-9含量明顯升高(P<0.05);與模型組比較,丹參多酚酸鹽組和阿托伐他汀組大鼠主動脈MCP-1、VCAM-1、MMP-9含量明顯降低(P<0.05)。(見圖5)
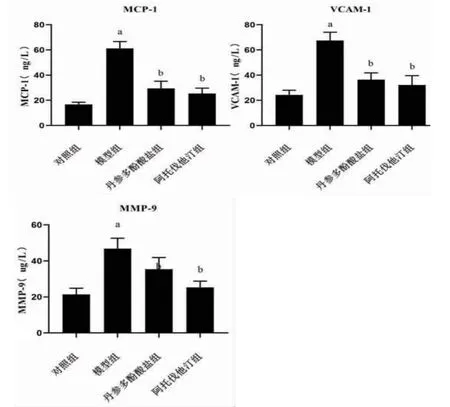
圖5 各組大鼠主動脈MCP-1、VCAM-1、MMP-9含量比較(±s,n=9)
3 討 論
中醫學無AS之病名,根據其臨床表現,可歸屬于中醫學“胸痹”“脈痹”“中風”等范疇,中醫學認為其核心病機為瘀血痹阻,氣為血之帥,血為氣之母,氣血失和,或氣虛而滯,或氣郁而滯,均可引起血流不暢,瘀血內生,痹阻血脈,化生斑塊[6-8]。痰濁、寒凝、水濕等均可以導致血運不暢,滯而成瘀,痹阻血脈,化生斑塊。因此,治療上應以活血化瘀為大法。注射用丹參多酚酸鹽是由丹參經提取的多酚酸鹽化合物組成,丹參味苦,性微寒,歸心、肝經,具有活血化瘀、通絡止痛等功效。注射用丹參多酚酸鹽具有活血、祛瘀、通絡功效。現代藥理研究表明,注射用丹參多酚酸鹽具有抗氧化損傷、抑制炎癥等作用[9]。
動脈粥樣硬化機制尚未完全闡明,脂質代謝紊亂、炎癥反應、氧化損傷、細胞外基質降解等在動脈粥樣硬化的發生發展中均起到重要的作用。脂質代謝紊亂是導致AS的最重要病理基礎,血液中TG、TC、LDL-C含量升高可以導致血管內皮損傷,引發血管內皮功能障礙,單核細胞通過破損的血管內皮進入內膜間隙,并吞噬ox-LDL形成泡沫細胞。泡沫細胞可以刺激生長因子釋放,進而促進血管平滑肌增殖,血管壁肥厚,形成脂質條紋并進展為動脈粥樣硬化斑塊[10-11]。HDL-C可以通過促進膽固醇運載至外周組織細胞,從而減少脂質沉積于血管內膜[12]。因此,調節脂質代謝是防治AS的關鍵。本研究結果發現,AS模型組大鼠主動脈斑塊形成,血清TC、TG、LDL-C、ox-LDL含量明顯升高,HDL-C含量明顯降低;而丹參多酚酸鹽組大鼠主動脈無斑塊形成,血清TC、TG、LDL-C、ox-LDL含量明顯降低,HDL-C含量明顯升高。因此,注射用丹參多酚酸鹽具有抑制和減緩動脈粥樣硬化斑塊形成的作用,可能是通過調節脂質代謝途徑實現。
有學者提出動脈粥樣硬化屬于一種慢性低度炎癥性反應。在AS形成過程中,平滑肌細胞、巨噬細胞釋放TNF-α、IL-1β、IL-6等炎性因子,導致機體處于一種慢性低度炎癥反應狀態。TNF-α可以增加血管內皮的通透性,從而促使LDL-C進入血管內皮細胞進而形成泡沫細胞[13-14]。而且TNF-α還可以刺激IL-1β、IL-6釋放,加重血管炎癥反應[15]。IL-1β可以通過促進黏附因子表達和內皮細胞增殖介導AS形成[16]。IL-6可以加強局部炎癥反應,促進黏附因子的表達,促進單核細胞和巨噬細胞遷移,促進血管內皮平滑肌細胞增殖,從而導致斑塊形成,并可以導致斑塊不穩定[17]。IL-10是一種強效抑炎因子,可以抑制炎癥因子的生成和釋放,抑制平滑肌細胞增殖,減緩動脈粥樣硬化。因此,抑制TNF-α、IL-1β、IL-6等促炎因子的表達和促進IL-10的表達可以改善動脈粥樣硬化。氧自由基可以損傷血管內皮細胞,促進脂質和單核細胞進入血管內膜下,導致斑塊形成[18-19]。而機體內的抗氧化酶可以清除氧自由基,減輕氧化損傷。SOD、GSH-Px是機體內的主要抗氧化酶,可以清除氧自由基。MDA是機體內的氧化代謝產物,反映機體氧化損傷的嚴重程度。SOD、GSH-Px、MDA是反映機體氧化損傷的重要標志物。本研究結果發現,AS模型組大鼠血清TNF-α、IL-1β、IL-6、MDA含量明顯升高,IL-10、SOD、GSH-Px含量明顯降低;而丹參多酚酸鹽組大鼠血清TNF-α、IL-1β、IL-6、MDA含量明顯降低,IL-10、SOD、GSH-Px含量明顯升高。說明注射用丹參多酚酸鹽可以通過下調TNF-α、IL-1β、IL-6、MDA的表達,上調IL-10、SOD、GSH-Px的表達,抑制炎癥反應和抗氧化損傷從而抑制和減緩AS的形成。
VCAM-1是一種由內皮細胞表達的糖蛋白,可以促進單核巨噬細胞、中性粒細胞等黏附在破損血管內壁,遷移至血管內膜后形成泡沫細胞,介導AS進展[20]。MCP-1可以趨化單核細胞和淋巴細胞遷移至血管內膜下,趨化炎性細胞聚集,介導斑塊形成。細胞外基質是血管壁的重要組成部分,其降解和重塑參與了AS的發生發展[21]。MMP-9可以降解細胞外基質,導致斑塊不穩定和斑塊形成。本研究結果發現,AS模型組大鼠主動脈MCP-1、VCAM-1、MMP-9含量明顯升高;而丹參多酚酸鹽組大鼠主動脈MCP-1、VCAM-1、MMP-9含量明顯降低。說明注射用丹參多酚酸鹽可以通過抑制MCP-1、VCAM-1、MMP-9的表達而抑制AS的形成。
綜上所述,注射用丹參多酚酸鹽可以通過調節脂代謝,抑制炎癥和抗氧化損傷改善動脈粥樣硬化。

