三鄰甲苯磷酸酯對(duì)人誘導(dǎo)多能干細(xì)胞來(lái)源的人腦類(lèi)器官的毒性
陳學(xué)軍,崔雅嵐,王 陳,石 童,張瑞華,徐建富,李麗琴
(國(guó)民核生化災(zāi)害防護(hù)國(guó)家重點(diǎn)實(shí)驗(yàn)室,北京 102205)
三鄰甲苯磷酸酯(tri-ortho-cresyl phosphate,TOCP)具有化學(xué)和熱穩(wěn)定性,可用作增塑劑、阻燃劑、軟化劑使用,在工業(yè)上和日常生活中被廣泛應(yīng)用。TOCP作為有機(jī)磷酸酯類(lèi)化合物的代表,具有嚴(yán)重的神經(jīng)毒性,包括抑制膽堿酯酶產(chǎn)生急性神經(jīng)毒性,一次或多次接觸后的神經(jīng)退行性綜合征及遲發(fā)性神經(jīng)毒性[1]。TOCP還是有機(jī)磷誘導(dǎo)的遲發(fā)性神經(jīng)病(organophosphorus ester-induced delayed neuropathy,OPIDN)最常用的造模劑。研究表明,OPIDN大鼠大腦的多個(gè)部位氧化應(yīng)激產(chǎn)物增加,抗氧化酶活性降低[2]。體外研究發(fā)現(xiàn),TOCP可導(dǎo)致人神經(jīng)母細(xì)胞瘤細(xì)胞SH-SY5Y和大鼠星形膠質(zhì)細(xì)胞C6氧化應(yīng)激產(chǎn)物增加,抗氧化能力減弱[3-4]。目前對(duì)TOCP的神經(jīng)毒性研究大多基于動(dòng)物實(shí)驗(yàn)或體外單一細(xì)胞培養(yǎng),相對(duì)于人體復(fù)雜的神經(jīng)系統(tǒng),存在跨種屬差異、生理相關(guān)度低等問(wèn)題。因此,開(kāi)發(fā)人源化、生理相關(guān)度高的模型進(jìn)行TOCP的神經(jīng)毒性研究,對(duì)于評(píng)估其人體神經(jīng)毒性及機(jī)制具有重要意義。
類(lèi)器官是利用干細(xì)胞的誘導(dǎo)分化和聚集特性在體外培養(yǎng)的三維“迷你”器官,與對(duì)應(yīng)的器官擁有類(lèi)似的空間組織構(gòu)成并能重現(xiàn)器官的部分功能,從而提供一個(gè)高度生理相關(guān)系統(tǒng)。類(lèi)器官技術(shù)的出現(xiàn)及應(yīng)用表明,中樞神經(jīng)系統(tǒng)細(xì)胞多樣性的可再生發(fā)育不需要胚胎環(huán)境,體外培養(yǎng)構(gòu)建的人腦類(lèi)器官具有與人大腦皮質(zhì)類(lèi)似的結(jié)構(gòu)和細(xì)胞組成。單細(xì)胞測(cè)序分析表明,人腦類(lèi)器官中表達(dá)有多種類(lèi)型的神經(jīng)元和膠質(zhì)細(xì)胞,細(xì)胞發(fā)生順序與體內(nèi)腦發(fā)育過(guò)程類(lèi)似[5-6]。神經(jīng)類(lèi)器官還可表現(xiàn)出相關(guān)的生理功能,形成功能性的神經(jīng)環(huán)路,培養(yǎng)260 d的人腦類(lèi)器官,可產(chǎn)生與早產(chǎn)兒腦電波信號(hào)相似的電信號(hào)[7]。Pellegrini等[8]構(gòu)建的中樞脈絡(luò)叢類(lèi)器官,可分泌腦脊液。此外,相較于實(shí)驗(yàn)動(dòng)物,人腦類(lèi)器官由人源干細(xì)胞通過(guò)誘導(dǎo)分化而來(lái),更能體現(xiàn)人體神經(jīng)組織微環(huán)境與功能,可有效解決跨種屬毒性效應(yīng)差異及實(shí)驗(yàn)動(dòng)物倫理學(xué)限制等問(wèn)題。因此,人腦類(lèi)器官相較于單獨(dú)的神經(jīng)元或膠質(zhì)細(xì)胞更適用于化合物的神經(jīng)毒性評(píng)估。人腦類(lèi)器官已用于乙醇、納米材料、新型冠狀病毒等的神經(jīng)毒性研究[9-13]。本研究擬應(yīng)用人腦類(lèi)器官進(jìn)行TOCP的神經(jīng)毒性評(píng)估,為闡明其人體神經(jīng)毒性提供參考。
1 材料與方法
1.1 人腦類(lèi)器官、試劑和主要儀器
人腦類(lèi)器官(培養(yǎng)60 d左右)和人腦類(lèi)器官維持培養(yǎng)基,浙江霍德生物工程有限公司。慢病毒包被的GCaMP6載體,武漢樞密腦科學(xué)技術(shù)有限公司;TOCP(純度99%),上海阿拉丁生化科技股份有限公司;CellTiter-Glo?3D Reagent(CTG試劑),美國(guó)Promega公司;二甲基亞砜(純度99%),美國(guó)Sigma-Aldrich公司。4%多聚甲醛,索萊寶生物科技有限公司;TUNEL細(xì)胞凋亡檢測(cè)試劑盒,上海碧云天生物技術(shù)有限公司;人丙二醛(malondialdehyde,MDA)和谷胱甘肽(glutathione,GSH)檢測(cè)試劑盒及BCA蛋白定量試劑盒,上海信裕生物科技有限公司;總抗氧化能力(total antioxidant capacity,T-AOC)、一氧化氮(nitric oxide,NO)和過(guò)氧化氫(hydrogen peroxide,H2O2)檢測(cè)試劑盒,南京建成生物工程研究所。
6孔超低黏附細(xì)胞培養(yǎng)板和96孔超低黏附細(xì)胞培養(yǎng)板,美國(guó)Corning公司;細(xì)胞培養(yǎng)箱(3111),美國(guó)Thermo公司;倒置熒光顯微鏡(Ti2-U),日本Nikon公司;多功能酶標(biāo)儀(Spark),瑞士Tecan公司;超聲細(xì)胞破碎儀(VCX760),美國(guó)Sonics公司;臺(tái)式高速冷凍離心機(jī)(5424R),德國(guó)Eppendorf公司。
1.2 人腦類(lèi)器官培養(yǎng)和分組處理
人腦類(lèi)器官培養(yǎng)于96孔超低黏附細(xì)胞培養(yǎng)板中,每孔1個(gè),置于37℃,5% CO2細(xì)胞培養(yǎng)箱內(nèi)的搖床上培養(yǎng),轉(zhuǎn)速70 r·min-1,每日換液。經(jīng)1 d適應(yīng)性培養(yǎng)后,分組給藥,每組3個(gè)重復(fù)樣本,分別為正常對(duì)照組、TOCP 1,5和10 mmol·L-1(終濃度)染毒組,染毒時(shí)間24 h。
1.3 CTG法檢測(cè)人腦類(lèi)器官細(xì)胞活力
取1.2分組處理的人腦類(lèi)器官,吸去培養(yǎng)基,加入PBS清洗3次,加入100 μL培養(yǎng)基,室溫平衡30 min,然后加入100 μL的CTG試劑,渦旋振蕩使細(xì)胞完全裂解,室溫繼續(xù)孵育30 min。應(yīng)用酶標(biāo)儀進(jìn)行化學(xué)發(fā)光檢測(cè),通過(guò)對(duì)ATP的定量來(lái)測(cè)定人腦類(lèi)器官的細(xì)胞存活率,設(shè)定積分時(shí)間為每孔1 s,讀取各孔發(fā)光值,計(jì)算各組細(xì)胞存活率。細(xì)胞存活率(%)=TOCP組發(fā)光值/正常對(duì)照組發(fā)光值×100%。
1.4 TUNEL法檢測(cè)人腦類(lèi)器官細(xì)胞凋亡
人腦類(lèi)器官分為正常對(duì)照組和TOCP 5 mmol·L-1組,每組3個(gè),正常對(duì)照組加入含0.1% DMSO置于細(xì)胞培養(yǎng)箱內(nèi)搖床孵育24 h,收集人腦類(lèi)器官,4%多聚甲醛固定,經(jīng)抗凍保護(hù)、包埋、速凍、冷凍切片、TUNEL染色,進(jìn)行熒光成像,觀(guān)察人腦類(lèi)器官細(xì)胞凋亡,以NIS-Elements AR軟件分析各組TUNEL和DAPI熒光強(qiáng)度,兩者比值表示細(xì)胞凋亡率。
1.5 倒置熒光顯微鏡檢測(cè)人腦類(lèi)器官鈣震蕩
rLV-EF1a-GCaMP6s-WPRE以培養(yǎng)液稀釋至0.1 kU·L-1,與人腦類(lèi)器官在培養(yǎng)箱中共孵育,8 h后換液,繼續(xù)培養(yǎng)3 d。將轉(zhuǎn)染了GCaMP6的人腦類(lèi)器官轉(zhuǎn)移至6孔超低黏附細(xì)胞培養(yǎng)板中,調(diào)節(jié)熒光倒置顯微鏡至4×物鏡、FITC模式,觀(guān)察人腦類(lèi)器官鈣成像效果。應(yīng)用NIS-Elements AR軟件,設(shè)置ND Acquisition模式記錄熒光-時(shí)間變化,時(shí)長(zhǎng)1 min,間隔無(wú)延遲,并通過(guò)時(shí)間測(cè)量功能分析1 min內(nèi)鈣熒光強(qiáng)度變化,選取鈣震蕩節(jié)律為3~9s的人腦類(lèi)器官模型進(jìn)行TOCP染毒分析。TOCP染毒時(shí),設(shè)置記錄時(shí)長(zhǎng)為3 min,記錄正常鈣信號(hào)約40 s,加入TOCP(終濃度5 mmol·L-1)或者0.1% DMSO溶液,測(cè)試完成后,通過(guò)時(shí)間測(cè)量功能導(dǎo)出各時(shí)間點(diǎn)熒光值(Ft),設(shè)起始熒光值F0為1,計(jì)算各時(shí)間點(diǎn)相對(duì)熒光值(Ft/F0)并作圖,根據(jù)相對(duì)熒光值變化曲線(xiàn)判斷細(xì)胞內(nèi)鈣濃度變化。
1.6 比色法檢測(cè)人腦類(lèi)器官H2O2,MDA,NO,T-AOC和GSH含量以及SOD和GSH-PX活性
取1.2分組處理的人腦類(lèi)器官,以預(yù)冷PBS輕輕沖洗3次,每孔加入200 μL PBS重懸,用寬口移液吸頭轉(zhuǎn)移至無(wú)菌離心管內(nèi),冰浴下超聲破碎20 s,使細(xì)胞完全裂解。4℃下13 000×g離心15 min,取上清液,參照試劑盒說(shuō)明書(shū)檢測(cè)氧化應(yīng)激產(chǎn)物H2O2,MDA和NO含量,T-AOC,GSH含量,以及抗氧化酶SOD和GSH-PX活性,各指標(biāo)含量均以各自樣本的總蛋白含量進(jìn)行校正。
1.7 統(tǒng)計(jì)學(xué)分析
實(shí)驗(yàn)結(jié)果數(shù)據(jù)用±s表示,采用SPSS19.0軟件進(jìn)行數(shù)據(jù)分析,多組間比較采用單因素方差分析析(One-way ANOVA)結(jié)合 Dunnettt檢驗(yàn)。P<0.05為差異具有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 TOCP對(duì)人腦類(lèi)器官細(xì)胞存活率的影響
圖1結(jié)果顯示,與正常對(duì)照組相比,TOCP 1 mmol·L-1組人腦類(lèi)器官細(xì)胞存活率無(wú)顯著差異,5和10 mmol·L-1組分別為正常對(duì)照組的(83±6)%和(79±10)%,均顯著下降(P<0.05),表明TOCP 5和10 mmol·L-1對(duì)人腦類(lèi)器官具有毒性作用。
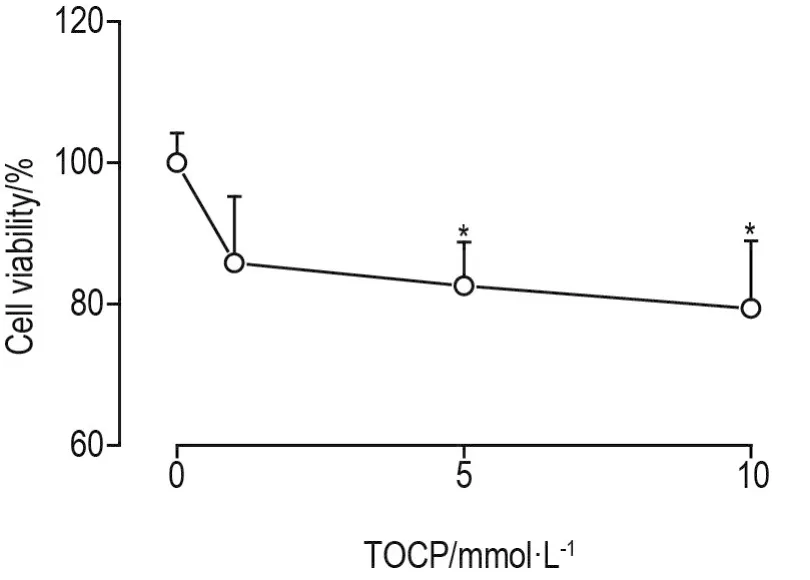
Fig.1 Effect of tri-ortho-cresyl phosphate(TOCP)on cell viability of human brain organoids.Brain organoids were treated with TOCP for 24 h and cell viability was determined with CellTiter-Glo? 3D Reagent.±s,n=3.*P<0.05,compared with normal control(0 mmol·L-1)group.
2.2 TOCP對(duì)人腦類(lèi)器官細(xì)胞凋亡的影響
TUNEL染色顯示(圖2),正常對(duì)照組人腦類(lèi)器官內(nèi)部細(xì)胞凋亡較少,TOCP 5 mmol·L-1組人腦類(lèi)器官內(nèi)部出現(xiàn)大量細(xì)胞凋亡(綠色熒光),熒光強(qiáng)度顯著高于正常對(duì)照組(P<0.01)表明TOCP可誘導(dǎo)人腦類(lèi)器官細(xì)胞凋亡,具有顯著的神經(jīng)毒性。
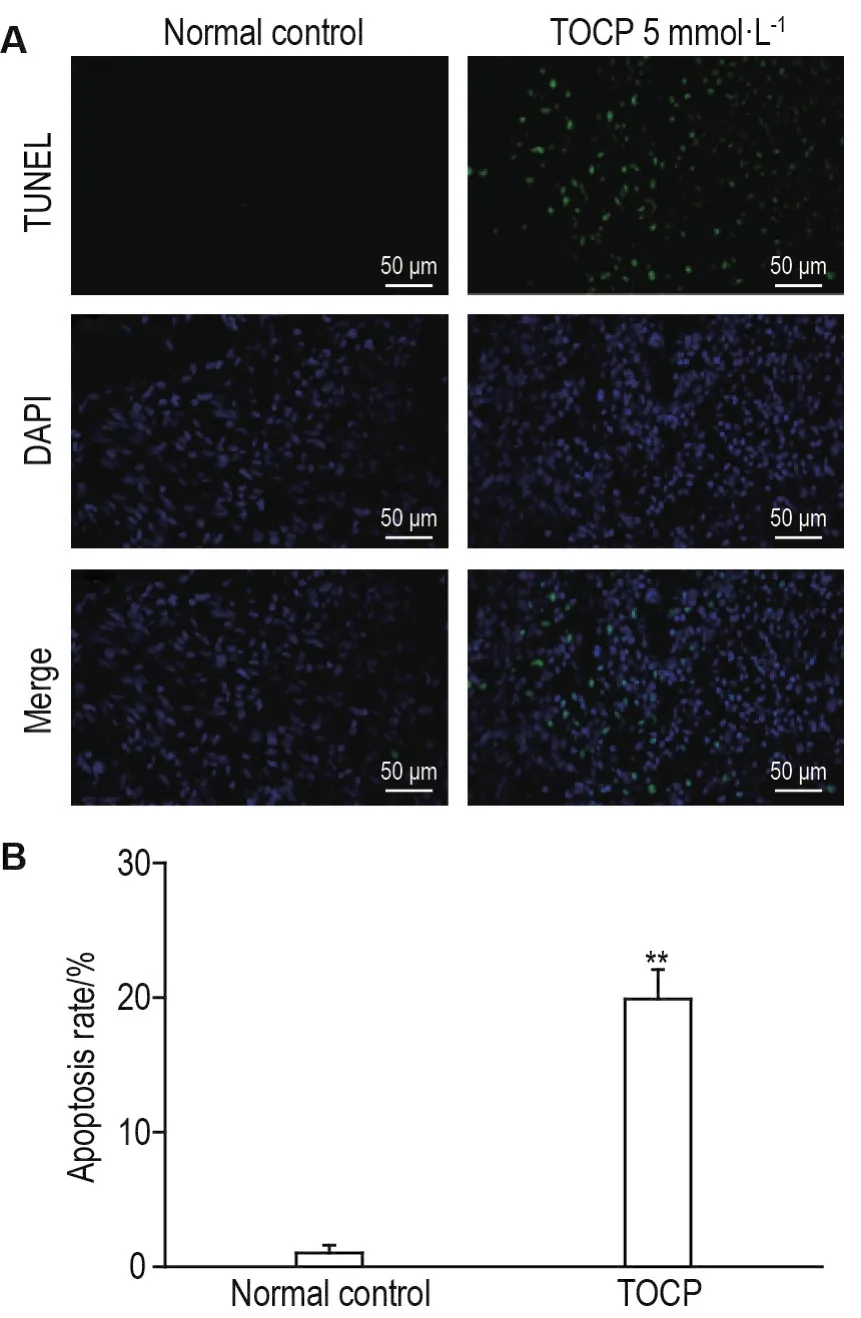
Fig.2 Effect of TOCP on cell apoptosis of human brain organoids by TUNEL staining.See Fig.1 for the treatment.Green fluorescence indicates apoptotic cells.B was the quantitative result of A.Apoptosis rate(%)=TUNEL intensity/DAPI intensity×100%.±s,n=3.**P<0.01,compared with normal control group.
2.3 TOCP對(duì)人腦類(lèi)器官細(xì)胞鈣震蕩的影響
倒置熒光顯微鏡下可見(jiàn),正常對(duì)照組人腦類(lèi)器官鈣震蕩出現(xiàn)擾動(dòng),但很快恢復(fù),且熒光強(qiáng)度和節(jié)律未受明顯影響(圖3A);TOCP 5 mmol·L-1組人腦類(lèi)器官鈣震蕩信號(hào)紊亂(圖3B),表現(xiàn)為鈣震蕩幅度和熒光強(qiáng)度的持續(xù)增強(qiáng),表明TOCP可使細(xì)胞內(nèi)鈣離子濃度升高,導(dǎo)致鈣穩(wěn)態(tài)失衡。
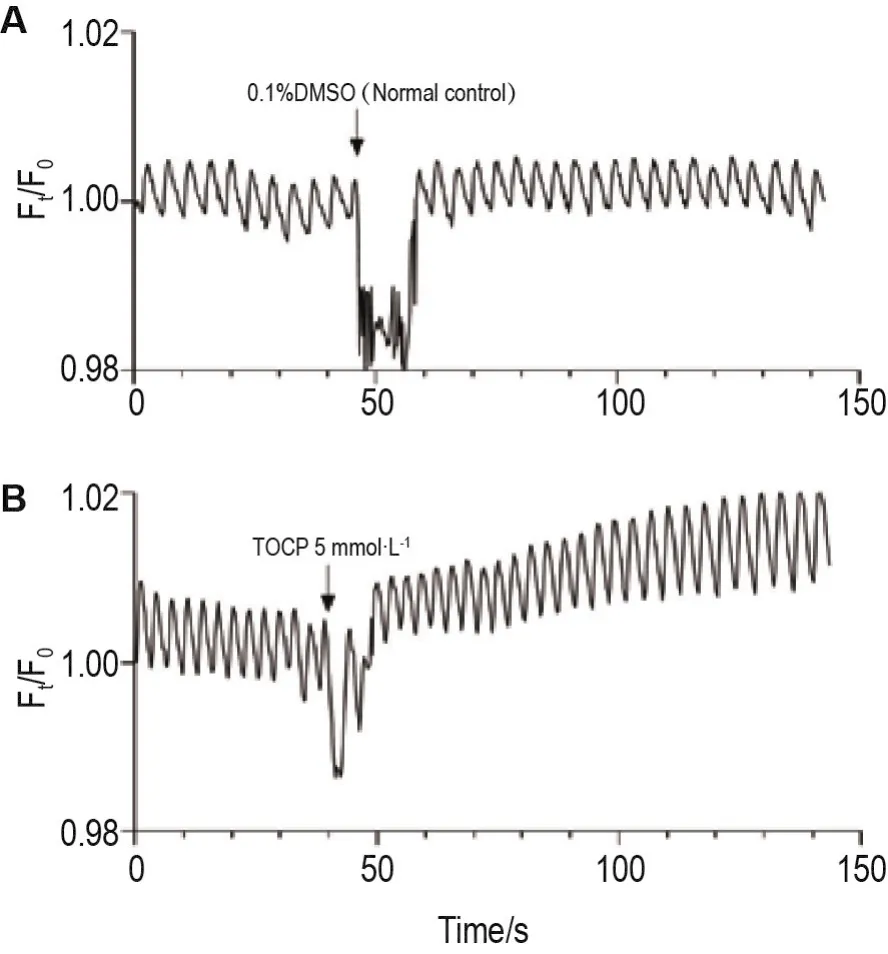
Fig.3 Effect of TOCP on calcium oscillations of human brain organoids.See Fig.1 for the treatment.Ft:real time fluorescence intensity;F0:initial fluorescence intensity.
2.4 TOCP對(duì)人腦類(lèi)器官H2O2,MDA,NO,T-AOC,GSH含量及SOD和GSH-PX活性的影響
如表1所示,與正常對(duì)照組比較,TOCP各組人腦類(lèi)器官H2O2水平均顯著增加(P<0.01),其含量分別為正常對(duì)照組的1.30,2.55和2.37倍;其中TOCP 10 mmol·L-1組 MDA 含量升高(P<0.01)。提示TOCP可引起脂質(zhì)過(guò)氧化產(chǎn)物增加(P<0.01)。各組NO水平與正常對(duì)照組比較無(wú)明顯變化。與正常對(duì)照比較,TOCP 5和10 mmol·L-1組T-AOC顯著降低(P<0.05,P<0.01);TOCP 1,5和10 mmol·L-1顯著GSH含量(P<0.05,P<0.01)。與正常對(duì)照比較,TOCP 5和10 mmol·L-1組人腦類(lèi)器官SOD活性顯著降低(P<0.01);TOCP 1,5和 10 mmol·L-1組GSH-Px活性顯著降低(P<0.05,P<0.01)。提示TOCP可破壞人腦類(lèi)器官的抗氧化能力,導(dǎo)致氧化應(yīng)激損傷。
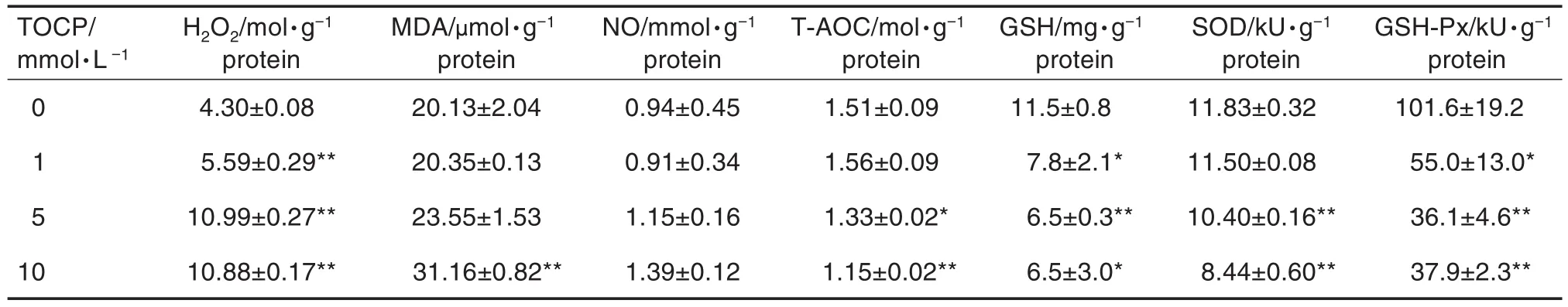
Tab.1 Effect of TOCP on levels of hydrogen peroxide(H2O2),malondialdehyde(MDA),nitric oxide(NO),total antioxidant capacity(T-AOC),glutathione(GSH),and activity of superoxide dismutase(SOD),glutathione peroxidase(GSH-Px)in human brain organoids
3 討論
本研究結(jié)果表明,TOCP可誘導(dǎo)人腦類(lèi)器官細(xì)胞凋亡,降低細(xì)胞存活率,具有顯著的神經(jīng)毒性。TOCP的神經(jīng)毒性機(jī)制可能與其誘導(dǎo)人腦類(lèi)器官的鈣震蕩節(jié)律紊亂相關(guān)。本研究結(jié)果表明,TOCP可引起人腦類(lèi)器官鈣離子震蕩幅度增大、強(qiáng)度持續(xù)增強(qiáng),表明細(xì)胞內(nèi)的鈣離子濃度提升,鈣穩(wěn)態(tài)失衡。鈣穩(wěn)態(tài)失衡參與有機(jī)磷類(lèi)化合物誘導(dǎo)的神經(jīng)組織損傷[14]。Fernandes等[15-16]研究報(bào)道,神經(jīng)元L型鈣離子通道和T型鈣離子通道參與了丙胺氟磷誘導(dǎo)的OPIDN過(guò)程。Ding等[16]報(bào)道,TRPV1通道阻斷劑HC030031能夠改善馬拉硫磷或TOCP導(dǎo)致的神經(jīng)損傷和共濟(jì)失調(diào)等OPIDN表現(xiàn)。敵敵畏長(zhǎng)期暴露可導(dǎo)致大鼠腦突觸內(nèi)鈣離子濃度升高,主要鈣外排酶(如Ca2+-ATP酶)活性降低,去極化引起電壓依賴(lài)的鈣離子通道開(kāi)放,鈣攝取增加、輔酶活性增強(qiáng),表明細(xì)胞內(nèi)鈣穩(wěn)態(tài)失衡介導(dǎo)了敵敵畏的慢性神經(jīng)毒性,導(dǎo)致神經(jīng)功能損傷[17]。
胞漿內(nèi)鈣離子的持續(xù)高濃度增加,尤其是線(xiàn)粒體中的鈣離子增加會(huì)導(dǎo)致自由基和氧化應(yīng)激產(chǎn)物的增加[18]。有機(jī)磷化合物暴露會(huì)導(dǎo)致氧化應(yīng)激反應(yīng)[19]。如引起腦中內(nèi)源性抗氧化酶和非酶抗氧化劑活性改變、線(xiàn)粒體功能損傷以及自由基介導(dǎo)的損傷(如脂質(zhì)過(guò)氧化)增加[20-21]。Zhang等[22]報(bào)道,母雞單次灌胃給予750 mg·kg-1TOCP使雞大腦、脊髓和坐骨神經(jīng)等組織MDA含量升高,SOD和GSH-PX等抗氧化酶的活性降低,GSH含量下降。龍鼎新等[4]研究發(fā)現(xiàn),TOCP孵育的SH-SY5Y細(xì)胞,MDA水平增加且H2O2酶含量降低,提示TOCP導(dǎo)致神經(jīng)細(xì)胞抗氧化能力減弱,脂質(zhì)氧化物水平增加。劉曉暉等[3]報(bào)道,TOCP處理的大鼠C6星形膠質(zhì)細(xì)胞,LDH釋放增加,細(xì)胞存活率減弱,抗氧化物GSH含量降低,GSH-PX活性下降,表明TOCP引起星形膠質(zhì)細(xì)胞的氧化應(yīng)激損傷。因此,TOCP的神經(jīng)毒性效應(yīng)是神經(jīng)元和膠質(zhì)細(xì)胞等共同作用的結(jié)果。本研究結(jié)果表明,TOCP處理的人腦類(lèi)器官,抗氧化物質(zhì)GSH含量降低,抗氧化酶SOD和GSH-PX活性減弱,T-AOC下降,氧化應(yīng)激產(chǎn)物MDA和H2O2增加。本研究結(jié)果表明,TOCP誘導(dǎo)人腦類(lèi)器官的氧化應(yīng)激反應(yīng),而氧化應(yīng)激是細(xì)胞凋亡的保守信號(hào)。因此,鈣穩(wěn)態(tài)失衡可能通過(guò)氧化應(yīng)激反應(yīng)介導(dǎo)了細(xì)胞的凋亡。
綜上所述,本研究結(jié)果表明,TOCP對(duì)人腦類(lèi)器官具有顯著毒性,其機(jī)制可能是通過(guò)破壞人腦類(lèi)器官的鈣穩(wěn)態(tài)失衡,增加細(xì)胞內(nèi)鈣離子濃度,引起氧化應(yīng)激紊亂,從而介導(dǎo)了細(xì)胞凋亡等發(fā)生。但人腦類(lèi)器官中的神經(jīng)元和膠質(zhì)細(xì)胞等各類(lèi)型細(xì)胞在TOCP所誘導(dǎo)損傷中的程度、作用及機(jī)制等還有待深入研究。
 中國(guó)藥理學(xué)與毒理學(xué)雜志2021年11期
中國(guó)藥理學(xué)與毒理學(xué)雜志2021年11期
- 中國(guó)藥理學(xué)與毒理學(xué)雜志的其它文章
- 藥物眼毒性反應(yīng)及作用機(jī)制分析
- 藥物性肝損傷有害結(jié)局路徑研究進(jìn)展
- 糖代謝重編程與“炎-癌轉(zhuǎn)化”及抗炎中藥靶向腫瘤糖代謝抗腫瘤作用機(jī)制研究進(jìn)展
- 肌萎縮側(cè)索硬化癥和額顳葉癡呆疾病相關(guān)9號(hào)染色體開(kāi)放閱讀框72基因(C9orf72)突變產(chǎn)物二肽重復(fù)蛋白對(duì)HeLa細(xì)胞線(xiàn)粒體生物學(xué)功能的影響
- 2種鹽酸二甲雙胍緩釋片在中國(guó)健康受試者空腹單次口服給藥條件下的生物等效性和安全性
- miR-148a-3p通過(guò)抑制lL-12/lL-12R β1/lL-12R β2/lFN- γ通路抑制Th1細(xì)胞極化
