HPLC-QAMS法同時(shí)測(cè)定榆槐片中11種有效成分的含量
遲靜 畢夏 劉志民 劉德軍

中圖分類號(hào) R944.2+7;R927.2 文獻(xiàn)標(biāo)志碼 A 文章編號(hào) 1001-0408(2021)22-2713-07
DOI 10.6039/j.issn.1001-0408.2021.22.05
摘 要 目的:建立同時(shí)測(cè)定榆槐片中梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷等11種有效成分含量的方法。方法:采用高效液相色譜-一測(cè)多評(píng)(HPLC-QAMS)法。以Agilent TC-C18為色譜柱,以乙腈-0.1%磷酸溶液為流動(dòng)相進(jìn)行梯度洗脫,流速為1.0 mL/min,柱溫為30 ℃,檢測(cè)波長(zhǎng)為238 nm(梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷和梔子苷)、203 nm(地榆皂苷Ⅰ和地榆皂苷Ⅱ)、283 nm(蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷)。以梔子苷為內(nèi)參物,計(jì)算其余10種成分相對(duì)于該成分的相對(duì)校正因子,從而計(jì)算10批樣品中各成分的含量,并與外標(biāo)法所得結(jié)果進(jìn)行比較。結(jié)果:梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷檢測(cè)質(zhì)量濃度的線性范圍分別為0.87~43.50、1.99~99.50、4.06~203.00、7.35~367.50、12.97~648.50、28.98~1 449.00、3.79~189.50、1.57~78.50、18.05~902.50、0.66~33.00和14.38~719.00 μg/mL(r均大于0.999 0),精密度、重復(fù)性、穩(wěn)定性(24 h)試驗(yàn)的RSD均小于2%(n=6),平均加樣回收率為96.90%~100.10%,RSD為0.67%~1.74%(n=9)。HPLC-QAMS法與外標(biāo)法所測(cè)得的10批榆槐片中梔子新苷等10種有效成分的含量比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)論:本研究所建立的HPLC-QMAS法操作簡(jiǎn)便、結(jié)果準(zhǔn)確,可用于榆槐片中梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷含量的同時(shí)測(cè)定。
關(guān)鍵詞 榆槐片;高效液相色譜-一測(cè)多評(píng)法;多指標(biāo)成分;相對(duì)校正因子;含量
Simultaneous Determination of 11 Active Components in Yuhuai Tablets by HPLC-QAMS
CHI Jing1,BI Xia2,LIU Zhimin3,LIU Dejun1(1. Preparation Center, the Third Affiliated Hospital of Liaoning University of TCM, Shenyang 110003, China; 2. Dept. of Clinical Pharmacy, the Third Affiliated Hospital of Liaoning University of TCM, Shenyang 110003, China; 3. Northeast Pharmaceutical Group Co., Ltd., Shenyang 110026, China)
ABSTRACT? ?OBJECTIVE:To establish the method for simultaneous determination of 11 active components in Yuhuai tablets,such as gardoside,shanzhiside,gardenoside,genipin 1-gentiobioside,geniposide,ziyuglycoside Ⅰ,ziyuglycoside Ⅱ,narirutin,naringin,hesperidin and neohesperidin. METHODS:HPLC-QAMS method was adopted. The determination was performed on Agilent TC-C18 column (250 mm×4.6 mm,5 μm) with mobile phase consisted of acetonitrile(A)-0.1% phosphoric acid solution(B) (gradient elution) at the flow rate of 1.0 mL/min. The column temperature was set at 30 ℃. The detection wavelengths were set at 238 nm for gardoside,shanzhiside,gardenoside,genipin 1-gentiobioside and geniposide,203 nm for ziyuglycoside Ⅰ and ziyuglycoside Ⅱ,and 283 nm for narirutin,naringin,hesperidin and neohesperidin. Using geniposide as an internal reference,the relative correction factors of other 10 components relative to this component were calculated,and the contents of each component in 10 batches of samples were calculated. The results obtained by HPLC-QAMS method were compared with those obtained by external standard method. RESULTS: The linear ranges of gardoside,shanzhiside,gardenoside,genipin 1-gentiobioside,geniposide,ziyuglycoside Ⅰ,ziyuglycoside Ⅱ,narirutin,naringin,hesperidin and neohesperidin were 0.87-43.50,1.99-99.50,4.06-203.00,7.35-367.50,12.97-648.50,28.98-1 449.00,3.79-189.50,1.57-78.50,18.05-902.50,0.66-33.00 and 14.38-719.00 μg/mL(all r>0.999 0). RSDs of precision,repeatability and stability (24 h) tests were all less than 2%(n=6). The average recoveries were 96.90%-100.10%, and RSDs were 0.67%-1.74%(n=9). There was no significant difference in the contents of 10 active components as gardoside between HPLC-QAMS method and external standard method in 10 batches of Yuhuai tablets(P>0.05). CONCLUSIONS: The HPLC-QMAS method established in this study is convenient and accurate. It can be used for the simultaneous determination of gardoside,shanzhiside,gardenoside,genipin 1-gentiobioside,geniposide,ziyuglycoside Ⅰ,ziyuglycoside Ⅱ,narirutin,naringin,hesperidin and neohesperidin in Yuhuai tablets.
KEYWORDS? ?Yuhuai tablets; HPLC-QAMS; Multi-index component; Relative correction factor; Content
榆槐片由地榆、槐花、黃芩、牡丹皮、梔子、枳殼和甘草加工而成,具有清熱燥濕、涼血止血的功效,主要用于治療具有肛門腫痛、出血、脫垂等癥狀的內(nèi)外痔[1]。榆槐片方中地榆可涼血止血、解毒斂瘡,槐花可涼血止血、清肝瀉火,黃芩可清熱燥濕、瀉火解毒,三者合為君藥;牡丹皮能清熱涼血、活血化瘀,梔子能瀉火利濕、涼血解毒,二者共為臣藥;枳殼能理氣寬中、行滯消脹,是為佐藥;甘草可清熱解毒、緩急止痛,是為使藥[2]。該藥成分眾多,但目前相關(guān)國(guó)家藥品標(biāo)準(zhǔn)僅以牡丹皮中的芍藥苷含量作為其質(zhì)控指標(biāo)[3],難以體現(xiàn)該藥的內(nèi)在整體質(zhì)量。
傳統(tǒng)的多指標(biāo)定量控制方法可能會(huì)因?yàn)槟承?duì)照品不易獲取或成本太高而無法得以廣泛應(yīng)用,而高效液相色譜-一測(cè)多評(píng)(HPLC-QAMS)法選取易得、價(jià)廉的單一對(duì)照品作為內(nèi)參物,通過相對(duì)校正因子計(jì)算其他成分的含量,可實(shí)現(xiàn)對(duì)多種成分的同步定量檢測(cè),大大降低了檢驗(yàn)成本。鑒于此,本研究以榆槐片方中君藥之一地榆所含的代表性成分地榆皂苷Ⅰ、地榆皂苷Ⅱ,臣藥之一梔子的主要活性成分梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷,以及佐藥枳殼的主要活性成分蕓香柚皮苷、柚皮苷、橙皮苷、新橙皮苷作為指標(biāo)[4-6],選取質(zhì)量穩(wěn)定、價(jià)廉易得的梔子苷作為內(nèi)參物,采用HPLC-QAMS法同時(shí)測(cè)定該藥中上述11種成分的含量,并與外標(biāo)法檢測(cè)結(jié)果進(jìn)行比較,以期為該藥質(zhì)量標(biāo)準(zhǔn)的提升提供參考。
1 材料
1.1 主要儀器
本研究所用的主要儀器包括1200型高效液相色譜(HPLC)儀及配備的可變波長(zhǎng)紫外檢測(cè)器、四元泵、真空脫氣機(jī)、柱溫箱、自動(dòng)進(jìn)樣器和ChemStation工作站(美國(guó)Agilent公司),2695型HPLC儀及配備的紫外-可見光檢測(cè)器、四元泵、在線脫氣機(jī)、自動(dòng)進(jìn)樣器、柱溫箱和Empower 3工作站(美國(guó)Waters公司),CPA225D型電子分析天平(精度為0.01 mg,德國(guó)Sartorius公司),CH-250型超聲波清洗器(北京創(chuàng)新德超聲電子研究所)等。
1.2 主要藥品與試劑
本研究所用的主要藥品與試劑包括榆槐片(太極集團(tuán)重慶桐君閣藥廠有限公司,規(guī)格為每片0.45 g,批號(hào)分別為19080016、19120026、20060014、20080011、20090010、20090015、20100008、20110012、20110016、20120003,依次編號(hào)為S1~S10),梔子苷、柚皮苷、橙皮苷、新橙皮苷對(duì)照品(中國(guó)食品藥品檢定研究院,批號(hào)分別為110749- 201919、110722-201815、110721-202019、111857-201804,純度依次為97.1%、91.7%、95.3%、99.4%),梔子新苷對(duì)照品(武漢天植生物技術(shù)有限公司,批號(hào)CFS201901,純度98.0%),山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷對(duì)照品(成都普瑞法科技開發(fā)有限公司,批號(hào)分別為PRF9071641、PRF9040843、PRF9051521、PRF8060821、PRF8060201、PRF9062802,純度依次為97.7%、99.3%、98.9%、98.7%、98.0%、99.8%);乙腈為色譜純,其余試劑均為分析純,水為純凈水。
2 方法與結(jié)果
2.1 溶液的制備
2.1.1 混合對(duì)照品溶液 精密稱取梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷對(duì)照品各適量,用甲醇溶解、稀釋,制得每1 mL含梔子新苷0.174 mg、山梔子苷0.398 mg、羥異梔子苷0.812 mg、京尼平龍膽雙糖苷1.470 mg、梔子苷2.594 mg、地榆皂苷Ⅰ5.796 mg、地榆皂苷Ⅱ0.758 mg、蕓香柚皮苷0.314 mg、柚皮苷3.610 mg、橙皮苷0.132 mg和新橙皮苷2.876 mg的混合對(duì)照品貯備液。精密吸取該混合對(duì)照品貯備液1.0 mL,置于20 mL量瓶中,用甲醇定容,搖勻,制得上述成分質(zhì)量濃度依次為0.008 7、0.019 9、0.040 6、0.073 5、0.129 7、0.289 8、0.037 9、0.015 7、0.180 5、0.006 6和0.143 8 mg/mL的混合對(duì)照品溶液。
2.1.2 供試品溶液 取榆槐片適量,研成細(xì)粉,精密稱定1.0 g,置于25 mL量瓶中,加入甲醇20 mL,超聲(功率250 W,頻率40 kHz)處理30 min,放冷,用甲醇定容,搖勻,經(jīng)0.45 μm微孔濾膜濾過,取續(xù)濾液,即得。
2.1.3 陰性供試品溶液和空白溶劑 按照榆槐片質(zhì)量標(biāo)準(zhǔn)中的處方和制備方法分別制得缺少梔子、地榆、枳殼的陰性樣品[3],再按“2.1.2”項(xiàng)下方法制得相應(yīng)的陰性供試品溶液。另取甲醇,作為空白溶劑。
2.1.4 加樣回收混合對(duì)照品溶液 精密稱取梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷對(duì)照品各適量,用甲醇溶解、稀釋,制得上述成分質(zhì)量濃度依次為0.115、0.269、0.451、0.845、1.431、3.472、0.398、0.185、2.023、0.091和1.587 mg/mL的加樣回收混合對(duì)照品溶液。
2.2 色譜條件
以Agilent TC-C18(250 mm×4.6 mm,5 μm)為色譜柱,以乙腈(A)-0.1%磷酸溶液(B)為流動(dòng)相進(jìn)行梯度洗脫(0~9 min,18.0%A;9~23 min,18.0%A→32.0%A;23~32 min,32.0%A→65.0%A;32~52 min,65.0%A→80.0%A;52~60 min,80.0%A→18.0%A);流速為1.0 mL/min;柱溫為30 ℃;檢測(cè)波長(zhǎng)為238 nm(0~23 min,測(cè)定梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷)[7-8]、203 nm(23~32 min,測(cè)定地榆皂苷Ⅰ、地榆皂苷Ⅱ)[9]、283 nm(32~60 min,測(cè)定蕓香柚皮苷、柚皮苷、橙皮苷、新橙皮苷)[10-11];進(jìn)樣量為10 ?L。
2.3 系統(tǒng)適用性試驗(yàn)
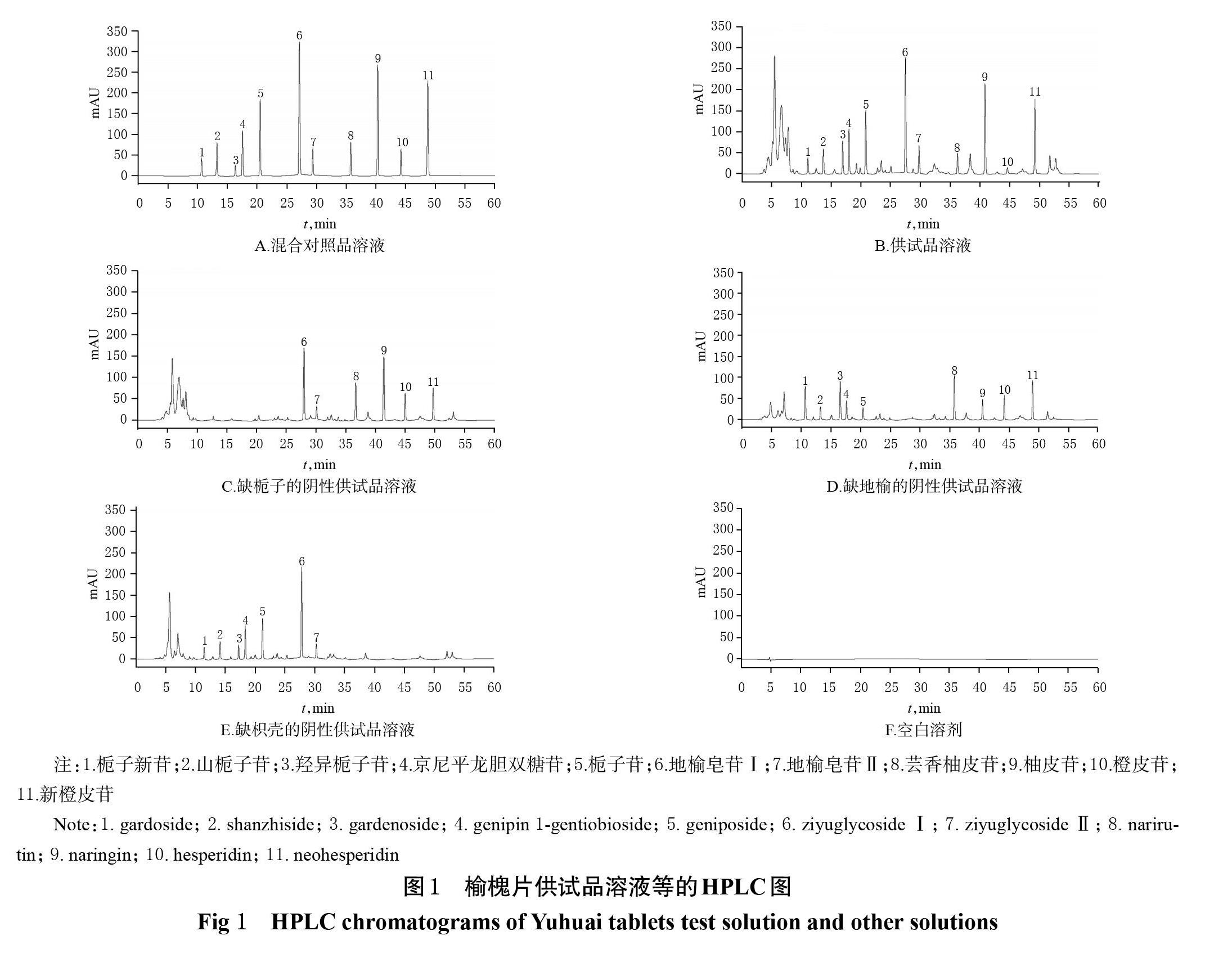
精密吸取“2.1”項(xiàng)下混合對(duì)照品溶液、供試品溶液、陰性供試品溶液和空白溶劑各適量,按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,記錄色譜圖(圖1)。結(jié)果顯示,供試品溶液中梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷、新橙皮苷與相鄰色譜峰間的分離度均大于1.5,理論板數(shù)均大于5 000,陰性供試品溶液和空白溶劑均不干擾待測(cè)成分的檢測(cè)。
2.4 線性關(guān)系考察
精密吸取混合對(duì)照品貯備液0.1、0.2、0.5、1.0、2.0、5.0 mL,分別用甲醇釋釋并定容至20 mL,搖勻,制得不同質(zhì)量濃度的系列混合對(duì)照品溶液Ⅰ~Ⅵ,按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,記錄峰面積。以梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷、新橙皮苷的峰面積(Y)為縱坐標(biāo)、其質(zhì)量濃度(X)為橫坐標(biāo)進(jìn)行線性關(guān)系考察,結(jié)果如表1所示。
2.5 精密度試驗(yàn)
精密吸取“2.1.1”項(xiàng)下混合對(duì)照品溶液適量,按“2.2”項(xiàng)下色譜條件連續(xù)進(jìn)樣測(cè)定6次,記錄峰面積。結(jié)果顯示,梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷峰面積的RSD分別為1.27%、1.06%、0.99%、0.71%、0.60%、0.53%、1.02%、1.13%、0.66%、1.31%和0.59%(n=6),表明儀器精密度良好。
2.6 重復(fù)性試驗(yàn)
取榆槐片(批號(hào)19080016)適量,共6份,分別按“2.1.2”項(xiàng)下方法制備供試品溶液,再按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,記錄峰面積并按外標(biāo)法計(jì)算各待測(cè)成分的含量。結(jié)果顯示,梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷含量的RSD分別為1.82%、1.76%、1.29%、1.33%、0.90%、0.83%、1.12%、1.66%、1.01%、1.87%和1.05%(n=6),表明本方法重復(fù)性良好。
2.7 穩(wěn)定性試驗(yàn)
取榆槐片(批號(hào)19080016)供試品溶液適量,分別于室溫條件下放置0、2、5、9、16、24 h時(shí)按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,記錄峰面積。結(jié)果顯示,梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷峰面積的RSD分別為1.33%、1.15%、1.07%、0.83%、0.68%、0.59%、1.14%、1.20%、0.72%、1.35%和0.71%(n=6),表明榆槐片供試品溶液在室溫條件下放置24 h內(nèi)穩(wěn)定性良好。
2.8 加樣回收率試驗(yàn)
取已知梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷含量的榆槐片(批號(hào)19080016)共9份,研細(xì),精密稱取細(xì)粉0.5 g,平行3組,每組精密加入“2.1.4”項(xiàng)下加樣回收混合對(duì)照品溶液0.8、1.0、1.2 mL,按“2.1.2”項(xiàng)下方法制備加樣回收供試品溶液,再按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,計(jì)算加樣回收率。結(jié)果顯示,上述11種待測(cè)成分的平均加樣回收率分別為99.05%、97.50%、98.85%、100.10%、99.76%、99.83%、96.90%、98.60%、100.04%、96.96%、99.09%,RSD分別為0.87%、1.74%、1.18%、0.73%、0.67%、0.76%、1.27%、0.93%、0.82%、1.24%、1.46%(n=9),表明本方法準(zhǔn)確度良好。
2.9 相對(duì)校正因子計(jì)算及耐用性考察
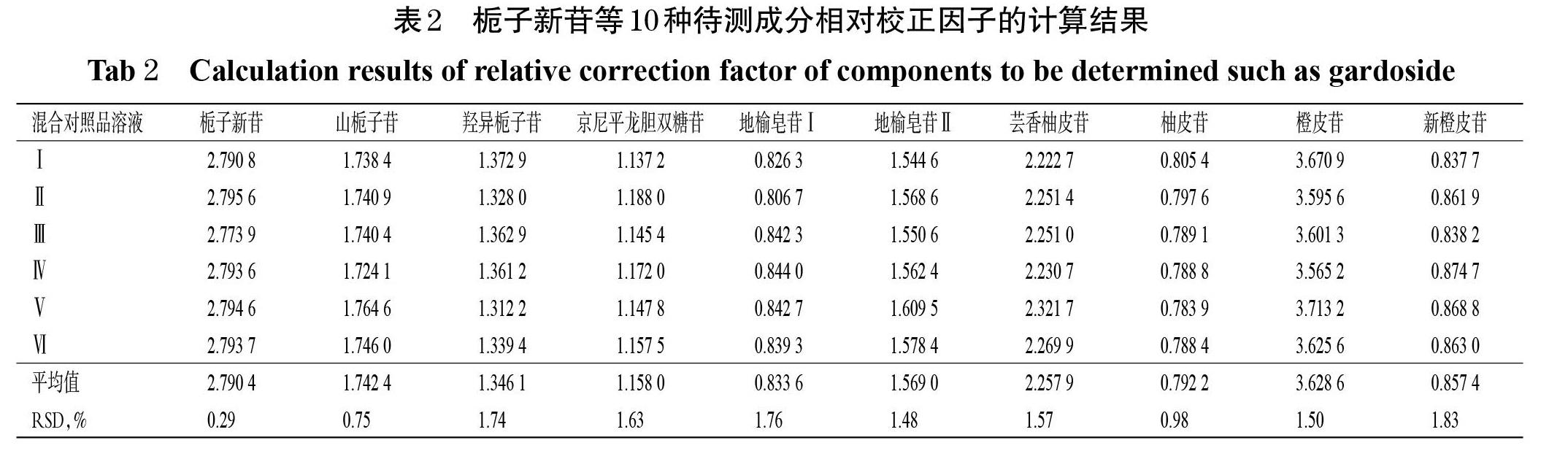
2.9.1 相對(duì)校正因子計(jì)算 精密吸取“2.4”項(xiàng)下系列混合對(duì)照品溶液Ⅰ~Ⅵ各適量,分別按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,記錄峰面積。以梔子苷為內(nèi)參物,計(jì)算梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷、新橙皮苷相對(duì)于梔子苷的相對(duì)校正因子(fk/s):fk/s=fk/fs=(ck×As)/(cs×Ak)。式中,f、c和A分別代表相對(duì)校正因子、成分質(zhì)量濃度和峰面積,下標(biāo)k和s分別代表待測(cè)成分和內(nèi)參物。相對(duì)校正因子的計(jì)算結(jié)果如表2所示。
2.9.2 不同儀器、色譜柱對(duì)相對(duì)校正因子的影響 選用不同HPLC儀(Agilent 1200型、Waters 2695型HPLC儀)和不同色譜柱(Agilent TC-C18、Capcell C18、Kromasil C18,規(guī)格均為250 mm×4.6 mm,5 μm),其余條件同“2.2”項(xiàng),精密吸取“2.1.1”項(xiàng)下混合對(duì)照品溶液適量,進(jìn)樣測(cè)定并記錄梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷的峰面積,按“2.9.1”項(xiàng)下方法計(jì)算上述各待測(cè)成分(梔子苷除外)的相對(duì)校正因子,結(jié)果如表3所示。由表3可知,梔子新苷等10種待測(cè)成分相對(duì)校正因子的RSD為0.53%~1.89%(n=6),表明不同儀器及色譜柱對(duì)相對(duì)校正因子的計(jì)算結(jié)果無顯著影響。
2.9.3 不同流速對(duì)相對(duì)校正因子的影響 選用不同流速(0.8、0.9、1.0、1.1、1.2 mL/min),其余條件同“2.2”項(xiàng),精密吸取“2.1.1”項(xiàng)下混合對(duì)照品溶液適量,進(jìn)樣測(cè)定并記錄梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷的峰面積,按“2.9.1”項(xiàng)下方法計(jì)算上述各待測(cè)成分(梔子苷除外)的相對(duì)校正因子,結(jié)果如表4所示。由表4可知,梔子新苷等10種待測(cè)成分相對(duì)校正因子的RSD為0.80%~1.88%(n=5),表明不同流速對(duì)相對(duì)校正因子的計(jì)算結(jié)果無顯著影響。
2.9.4 不同柱溫對(duì)相對(duì)校正因子的影響 選用不同柱溫(28、29、30、31、32 ℃),其余條件同“2.2”項(xiàng),精密吸取“2.1.1”項(xiàng)下混合對(duì)照品溶液適量,進(jìn)樣測(cè)定并記錄梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷的峰面積,按“2.9.1”項(xiàng)下方法計(jì)算上述各待測(cè)成分(梔子苷除外)的相對(duì)校正因子,結(jié)果如表5所示。由表5可知,梔子新苷等10種待測(cè)成分相對(duì)校正因子的RSD為0.52%~1.84%(n=5),表明不同柱溫對(duì)相對(duì)校正因子的計(jì)算結(jié)果無顯著影響。
2.10 目標(biāo)色譜峰的定位
選用不同HPLC儀(Agilent 1200型、Waters 2695型HPLC儀)和不同色譜柱(Agilent TC-C18、Capcell C18、Kromasil C18,規(guī)格均為250 mm×4.6 mm,5 μm),其余條件同“2.2”項(xiàng),精密吸取“2.1.1”項(xiàng)下混合對(duì)照品溶液適量,進(jìn)樣測(cè)定并記錄梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷的色譜峰保留時(shí)間,采用相對(duì)保留時(shí)間法對(duì)目標(biāo)色譜峰(梔子苷除外)進(jìn)行定位,結(jié)果如表6所示。由表6可知,梔子新苷等10種待測(cè)成分相對(duì)保留時(shí)間的RSD為0.65%~1.59%(n=6),表明采用相對(duì)保留時(shí)間法能夠?qū)δ繕?biāo)色譜峰進(jìn)行準(zhǔn)確定位。
2.11 樣品含量測(cè)定及結(jié)果比較
取10批榆槐片,每批平行3份,分別按“2.1.2”項(xiàng)下方法制備供試品溶液,再按“2.2”項(xiàng)下色譜條件進(jìn)樣測(cè)定,采用外標(biāo)法計(jì)算樣品中上述11種有效成分的含量;同時(shí),以梔子苷為內(nèi)參物,按“2.9.1”項(xiàng)下方法計(jì)算其余10種成分的相對(duì)校正因子并采用QAMS法計(jì)算成分含量。采用SPSS 26.0統(tǒng)計(jì)軟件對(duì)兩種方法所得結(jié)果進(jìn)行t檢驗(yàn)(檢驗(yàn)水準(zhǔn)α=0.05),結(jié)果如表7所示。由表7可知,采用HPLC-QAMS法所得梔子新苷等10種有效成分的平均含量與外標(biāo)法所得平均含量比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。
3 討論
3.1 供試品溶液制備方法的選擇
本研究在制備榆槐片供試品溶液時(shí),以梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷含量之和較高且單個(gè)成分含量要高于其平均值的綜合提取效果為指標(biāo),同時(shí)考慮雜質(zhì)干擾等影響因素,分別考察了以不同體積分?jǐn)?shù)(50%、60%、100%)的甲醇和不同體積分?jǐn)?shù)(70%、100%)的乙醇為溶媒[5-11],以及超聲提取和加熱回流提取兩種提取方式的效果,發(fā)現(xiàn)以甲醇為溶媒進(jìn)行超聲提取的效果較好。隨后,本研究對(duì)提取時(shí)間20、30、45、60 min進(jìn)行優(yōu)化,最終篩選出以甲醇超聲提取30 min為供試品溶液的制備方法。
3.2 色譜條件的優(yōu)化
在篩選流動(dòng)相時(shí),本研究考察了乙腈-水、乙腈-磷酸溶液、乙腈-甲酸溶液和乙腈-冰醋酸溶液等4個(gè)流動(dòng)相體系[4-5,7,11-13],綜合基線噪音、分離度、目標(biāo)成分靈敏度、檢測(cè)用時(shí)等情況,發(fā)現(xiàn)以乙腈-水、乙腈-甲酸溶液和乙腈-冰醋酸溶液為流動(dòng)相時(shí),所得色譜峰均出現(xiàn)不同程度的拖尾和變形現(xiàn)象,僅乙腈-磷酸溶液能滿足檢測(cè)要求;再經(jīng)過對(duì)磷酸溶液有機(jī)相、水相比例的摸索,最終確定以乙腈-0.1%磷酸溶液為流動(dòng)相,按“2.2”項(xiàng)下色譜條件進(jìn)行梯度洗脫。同時(shí),本研究參考文獻(xiàn)[6-14]對(duì)色譜柱類型(C18柱和C8柱)進(jìn)行了篩選,結(jié)果發(fā)現(xiàn)C18色譜柱的分離效果較佳;隨后對(duì)色譜柱(Agilent TC-C18、Capcell C18和Kromasil C18)、柱溫(28、29、30、31、32 ℃)、流速(0.8、0.9、1.0、1.1、1.2 mL/min)進(jìn)行了考察,發(fā)現(xiàn)上述3種色譜柱均能滿足檢測(cè)要求,且柱溫和流速對(duì)檢測(cè)結(jié)果的影響不大。綜合色譜峰峰形、理論板數(shù)、分離度、色譜響應(yīng)值等因素分析,最終選擇色譜柱為Agilent TC-C18(250 mm×4.6 mm,5 μm)、柱溫為30 ℃、流速為1.0 mL/min。
3.3 兩種檢測(cè)方法的比較
由表7可知,經(jīng)t檢驗(yàn)分析,采用HPLC-QAMS法和外標(biāo)法所測(cè)得的榆槐片中梔子新苷等10種有效成分的含量比較,差異均無統(tǒng)計(jì)學(xué)意義(P>0.05);但HPLC- QAMS法的操作更簡(jiǎn)便、成本更低廉,更具有優(yōu)勢(shì)。
綜上所述,本研究所建立的HPLC-QMAS法操作簡(jiǎn)便、結(jié)果準(zhǔn)確,有效地降低了檢驗(yàn)成本,可用于榆槐片中梔子新苷、山梔子苷、羥異梔子苷、京尼平龍膽雙糖苷、梔子苷、地榆皂苷Ⅰ、地榆皂苷Ⅱ、蕓香柚皮苷、柚皮苷、橙皮苷和新橙皮苷含量的同時(shí)測(cè)定,可為該藥的多指標(biāo)質(zhì)量評(píng)價(jià)提供實(shí)驗(yàn)依據(jù)。
參考文獻(xiàn)
[ 1 ] 陳輝.榆槐片配合熏洗法治療痔瘡50例[J].中國(guó)中醫(yī)藥現(xiàn)代遠(yuǎn)程教育,2009,7(11):101.
[ 2 ] 國(guó)家藥典委員會(huì).中華人民共和國(guó)藥典:一部[S]. 2020年版.北京:中國(guó)醫(yī)藥科技出版社,2020:88-89,130-131,179-180,257-260,314-315,370.
[ 3 ] 國(guó)家藥品監(jiān)督管理局.國(guó)家藥品標(biāo)準(zhǔn):WS-10932(ZD-0932)-
2002-2012Z[S/OL]. [2012-09-27]. https://www.dayi.org. cn/
drug/1019137.
[ 4 ] 王雪,戴衍朋,徐波,等.不同產(chǎn)地地榆飲片中地榆皂苷Ⅰ和地榆皂苷Ⅱ的含量測(cè)定及比較分析[J].中南藥學(xué),2018,16(3):400-404.
[ 5 ] 吳亞超,楊文靜,張磊,等.梔子中梔子苷等7個(gè)化學(xué)成分測(cè)定及質(zhì)量評(píng)價(jià)[J].中國(guó)藥學(xué)雜志,2016,51(10):841- 847.
[ 6 ] 田芳,何小芳,譚梓君,等.枳殼HPLC特征圖譜及6個(gè)黃酮苷類成分含量測(cè)定[J].中草藥,2020,40(6):1090- 1096.
[ 7 ] 黃躍前,程學(xué)仁,吳文平,等.基于指紋圖譜與多元統(tǒng)計(jì)分析的梔子不同炮制品評(píng)價(jià)[J].廣東藥科大學(xué)學(xué)報(bào),2020,36(6):765-770.
[ 8 ] 付小梅,楊超,吳志瑰,等.不同采收期梔子中8個(gè)有效成分含量動(dòng)態(tài)變化與顏色的相關(guān)性研究[J].中國(guó)中藥雜志,2020,45(13):3191-3202.
[ 9 ] 范奎,代良敏,熊永愛,等. HPLC-ELSD法測(cè)定地榆總皂苷中地榆皂苷-Ⅰ和地榆皂苷-Ⅱ的含量[J].中華中醫(yī)藥雜志,2017,32(6):2639-2642.
[10] 劉姍姍,蔣波,石雨荷,等. HPLC法同時(shí)測(cè)定湘產(chǎn)枳殼中5種成分含量的研究[J].湖南中醫(yī)雜志,2019,35(5):143-146.
[11] 田芳,譚梓君,何小芳,等.枳殼飲片標(biāo)準(zhǔn)湯劑質(zhì)量評(píng)價(jià)研究[J].中國(guó)現(xiàn)代應(yīng)用藥學(xué),2021,38(1):42-48.
[12] 馮敬騫,胡衛(wèi)南,徐禮萍,等. HPLC法同時(shí)測(cè)定不同采集地衢枳殼中12種黃酮類成分的含量[J].中國(guó)藥房,2020,31(5):571-575.
[13] 靳貝貝,裴香萍,梁惠珍.青皮藥材的HPLC指紋圖譜建立及聚類分析和主成分分析[J].中國(guó)藥房,2018,29(24):3336-3339.
[14] 唐俊,張杰,孫偉,等. LC-MS/MS法同時(shí)測(cè)定大鼠血漿中地榆皂苷Ⅰ和地榆皂苷Ⅱ的血藥濃度及其藥代動(dòng)力學(xué)[J].生物加工過程,2019,17(5):536-541.
(收稿日期:2021-05-08 修回日期:2021-10-07)
(編輯:胡曉霖)

