有氧運動治療對單純性肥胖兒童糖脂代謝、胰島素抵抗和血管內皮功能的影響
宋笑笑,何春風
近年來兒童肥胖的發病率越來越高,不僅會影響兒童的身心健康,而且也是成年后心腦血管疾病發病的高危因素[1]。兒童肥胖的發病機制較復雜,有研究發現胰島素抵抗及血管內皮功能紊亂在兒童肥胖發病中起重要作用[2-3]。運動治療是目前治療兒童肥胖常用的非藥物手段,但是否具有減輕胰島素抵抗和糾正血管內皮功能紊亂的作用國內報道較少[4-5]。本研究觀察了有氧運動對單純性肥胖兒童糖脂代謝、胰島素抵抗和血管內皮功能的影響,現報道如下。
1 資料與方法
1.1 一般資料 收集2020 年1—12 月在浙江省麗水市人民醫院兒科門診治療的單純性肥胖兒童患者84 例。納入標準:(1)符合兒童單純性肥胖癥的診斷標準[6],且體質量指數(BMI)≥28 kg/m2;(2)患兒父母或監護人均知情同意。排除標準:(1)繼發性肥胖;(2)并發內分泌或代謝性疾病者。按隨機數字表法分為觀察組和對照組,各42 例。觀察組男26例,女16 例;平均年齡(10.0±1.7)歲;平均BMI(30.78±2.17)kg/m2。對照組男24例,女18 例;平均年齡(9.9±1.7)歲;平均BMI(30.61±2.23)kg/m2。兩組一般資料差異無統計學意義(P>0.05)。
1.2 方法 對照組患兒予健康教育、行為矯正和飲食控制。觀察組患兒在對照組基礎上加有氧運動治療,根據患兒身體素質和運動愛好,選擇游泳、慢跑、跳繩、羽毛球、跑步或爬樓梯等運動方式,30~60 min/次,1 次/d,逐漸增加運動頻率和時間,強度以患兒感到輕度疲勞為宜。兩組連續干預12 周。
1.3 觀察指標 比較兩組治療前后糖脂代謝、胰島素抵抗及血管內皮功能指標變化。(1)糖代謝指標和胰島素抵抗指數:包括空腹血糖(FPG)、C 肽(C-P)和空腹胰島素(FINS),計算穩態模型胰島素抵抗指數(HOMA-IR)=(FINS×FPG)/22.5。(2)脂代謝指標:包括膽固醇(TC)、高密度脂蛋白(HDL-C)和低密度脂蛋白(LDL-C)。(3)血管內皮功能指標:包括一氧化氮(NO)和內皮素-1(ET-1),分別采用硝酸鹽還原酶法和酶聯免疫法測定。
1.4 統計方法 采用SPSS18.0 統計軟件進行分析,計量資料以均數±標準差表示,采用t 檢驗;計數資料采用檢驗。P<0.05 為差異有統計學意義。
2 結果
2.1 兩組血清 FPG、C-P、FINS 和HOMA-IR 水平比較 兩組干預前血清FPG、C-P、FINS 和HOMA-IR 水平差異均無統計學意義(均P>0.05),干預12周后,觀察組FPG、C-P、FINS和HOMAIR水平均低于對照組(均P<0.05)。見表1。

表1 兩組血清FPG、C-P、FINS 和HOMA-IR 水平比較
2.2 兩組血清TC、HDL-C 和LDL-C 水平比較 兩組干預前血清TC、HDL-C和LDL-C水平差異均無統計學意義(均P>0.05),干預12 周后,觀察組血清TC和LDL-C水平均低于對照組,HDL-C水平高于對照組(均P<0.05)。見表2。

表2 兩組血清TC、HDL-C 和LDL-C 水平比較 mmol/L
2.3 兩組血清NO 和ET-1 水平比較兩組干預前血清NO 和ET-1 水平差異均無統計學意義(均P>0.05),干預12 周后,觀察組血清NO高于對照組,血清ET-1水平低于對照組(均P<0.05)。見表3。
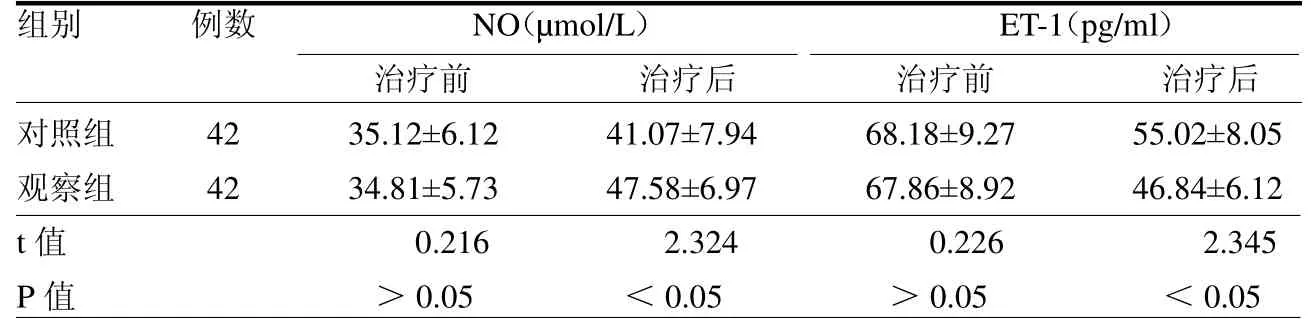
表3 兩組血清NO 和ET-1 水平比較
3 討論
近年來研究發現肥胖患者體內存在胰島素抵抗和血管內皮細胞異常[7-8],研究認為由于肥胖患者體內脂肪的數目增多及體積增大,引起血流供應不足,脂肪組織缺血缺氧,影響正常的新陳代謝,從而引起糖脂代謝紊亂和胰島素抵抗[7];同時肥胖患者血脂異常會引起乳糜微粒積累,進入血液循環刺激內皮細胞會產生活性氧,引起氧化應激反應,進而促進ET-1 合成,加速NO降解,引起血管內皮功能紊亂[8]。因此,減輕胰島素抵抗和保護血管內皮功能是目前治療兒童肥胖的新方向。
控制能量攝入及增加能量消耗是治療肥胖的關鍵,而單純飲食控制只能減少能量攝入,無法增加能量消耗,效果欠理想[9]。有氧運動被認為是最有效的減肥方式之一,主要通過促使體內脂肪變為游離脂肪酸進入血液,在運動中消耗能源,促進脂肪的燃燒,使能量攝入少于消耗而達到減肥的目的[10]。本研究結果顯示干預12 周后,觀察組血清FPG、C-P、FINS、TC、LDL-C 和HOMA-IR 下降及HDL-C 水平上升幅度均較對照組更明顯。這提示有氧運動用于單純性肥胖兒童可調節糖脂代謝,減輕胰島素抵抗。同時研究還發現觀察組血清NO上升幅度,血清ET-1 水平下降幅度較對照組更明顯,這提示有氧運動用于單純性肥胖兒童可改善血管內皮細胞功能。
綜上所述,有氧運動用于單純性肥胖兒童不僅可調節糖脂代謝,減輕胰島素抵抗,而且可改善血管內皮細胞功能。

