基于DNA分子標記的類煙產品鑒別檢驗抽樣方法研究
張 軻,王春瓊,張曉偉,孫浩巍,龍 杰,張冀武,童治軍,蓋小雷,蔡潔云,李海燕,陳 丹*
(1.云南省煙草質量監督檢測站,云南昆明 650106;2.云南省煙草農業科學院,云南昆明 650218;3.云南省煙草煙葉公司,云南昆明 650011)
近年來,除了電子霧化煙和加熱不燃燒煙草制品的流行,所謂的“花煙”“茶煙”“藥煙”等外形與卷煙相差無幾的類煙產品也頻繁出現在消費者的視線中,并且已經有未成年人吸食“茶煙”[1]和“藥煙”中檢出煙堿成分[2]的報道。盡管煙草專賣局、食品藥品監督局和市場管理局等部門已加強了對有一定市場空間和回購率且仍處于初期的類煙產品的監管力度,但對于仿冒程度較高的類煙產品,采用現有的方法進行鑒別及判定存在一定的誤判風險。因此,探索高效、簡便、準確、專屬性強的鑒別類煙產品抽樣方案和檢驗方法,對保障真品卷煙的合理流通、煙草專賣和市場監管具有重要意義。
目前,卷煙真偽鑒別檢驗以感官鑒別法和評吸鑒別法較為常用[3],而借助電子鼻技術[4]、近紅外光譜技術[5]和頂空-氣相色譜-質譜[6]等儀器鑒別的方法也正發展成為煙草分析的重要手段,但仍存在一定局限性,如抽樣量大、檢驗費用高,準確、及時鑒別仿冒程度較高的卷煙產品難度大。同時,在現行鑒別檢驗類煙產品的方法中,主要通過測定樣品中煙堿和N-亞硝胺含量,來判定此類產品是否為煙草專賣品。但煙堿并非煙草所獨有,很多茄科植物也含有,并且煙草特有N-亞硝胺的含量極低,常出現卷煙樣品中檢不出煙草特有N-亞硝胺的情況,因此,利用該方法鑒別檢驗類煙產品存在較大司法風險[7]。DNA標記是指用直接或間接的手段反映研究對象在DNA序列上的差異,即DNA多態性,具有操作簡便、樣品預處理簡單、基本干擾小、樣本量少、結果準確、及時等優點,已在司法鑒定[7]、海關檢疫[8]、農產品鑒別檢驗[9]等領域廣泛應用。此外,DNA測序技術[10]和環介導等溫擴增技術(LAMP)[11]的迅速發展,為利用煙草DNA分子特異標記鑒定檢驗卷煙產品奠定堅實的理論和技術基礎。在抽樣方法上,與隨機抽樣、分層抽樣等方法相比,序貫抽樣法具有明顯優勢,即任何一次抽樣都可作為終結檢驗,可大大降低平均樣本量、檢驗成本和時間,此法較為適合取樣量少的DNA標記技術[12]。以往鑒別檢驗卷煙真偽的研究大多集中在感官鑒別法、評吸鑒別法和儀器鑒別法,而關于序貫抽樣與DNA標記結合鑒別類煙產品研究鮮有報道。筆者以市場上獲得的400支茶煙為材料,研究構建適合類煙產品最小和最大抽樣量的序貫抽樣檢驗方案以及DNA檢測方法,為科學、準確、高效地鑒別類煙產品提供技術支撐。
1 材料與方法
1.1 材料該研究的材料來源于市場銷售的某品牌規格相同的類煙產品(茶煙)400支;煙支規格為長84 mm,直徑7.7 mm。
1.2 方法
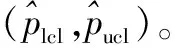

抽樣特性曲線(OC曲線)是基于抽樣方案(ncum,c)繪制的,即從整體為N的產品中抽取樣本數量為ncum的樣本進行檢驗,若符合判定標準c,則判定該批產品總體合格,否則判定不合格,通過OC曲線與抽樣方案變化的關系可以進一步驗證抽樣方案的合理性。
1.2.2DNA分子標記鑒別檢驗類煙產品。為驗證抽樣方法在檢測中的實際效果,將材料中的2條類煙產品破除包裝后,將煙支充分混勻,隨機抽取52支煙支(類煙產品)為初始樣品,以隨機抽取的2019年某品牌成品卷煙的標準樣品為對照,采用能區分煙與茶的SSR引物,按童治軍[14]的方法進行待檢樣品的基因組DNA提取、純化及PCR擴增,擴增產物用6%非變性聚丙烯酰胺凝膠電泳檢測,最終獲得清晰的特異性條帶。
2 結果與分析
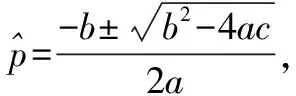
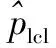
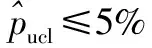
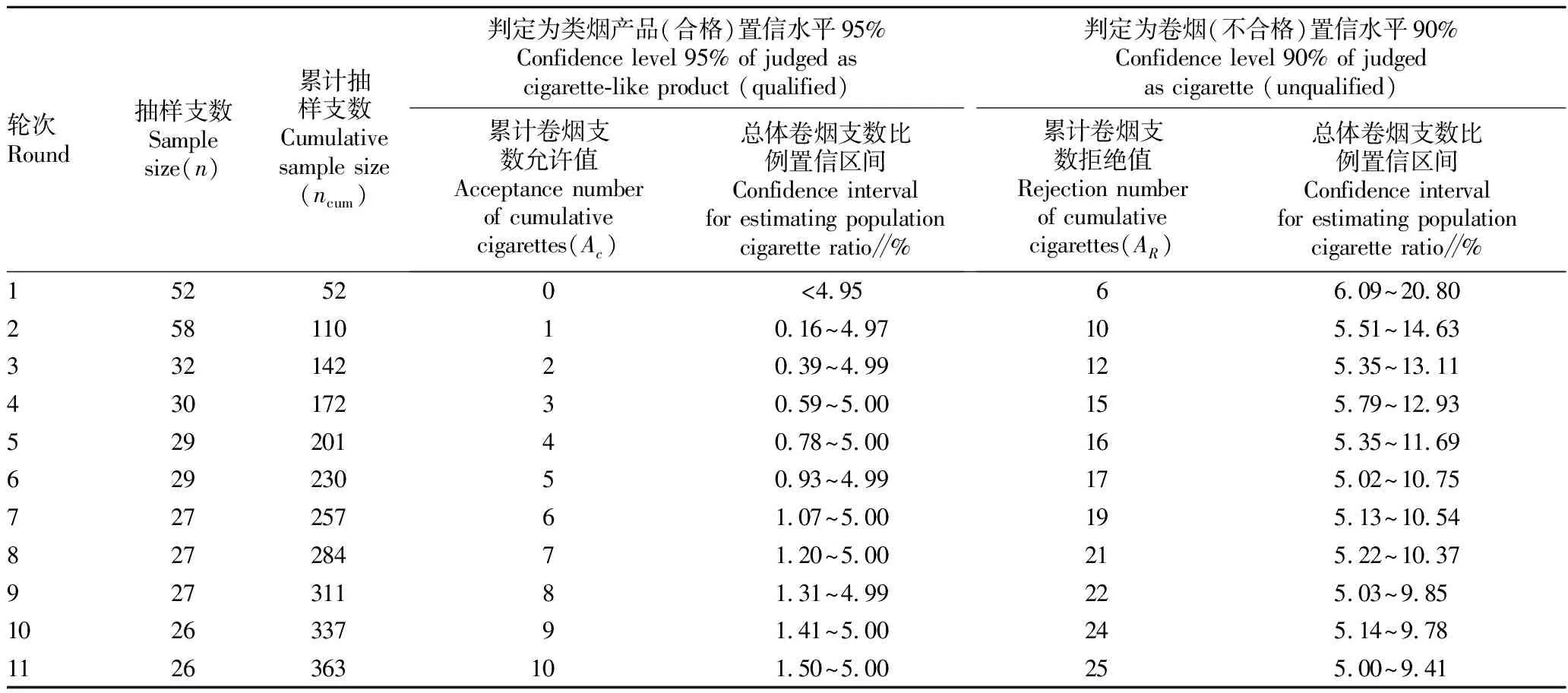
表1 序貫抽樣參考(雙尾)Table 1 Reference of sequential sampling (two tail)
2.4 DNA分子標記鑒別驗證類煙產品由圖2可知,DNA分子標記在卷煙標準樣品(S)中250 bp分子量處擴增出特異性條帶,而初次抽樣的52個類煙產品(n1~n52)均未出現特異性條帶,驗證了序貫抽樣的52個卷煙產品為類煙產品。
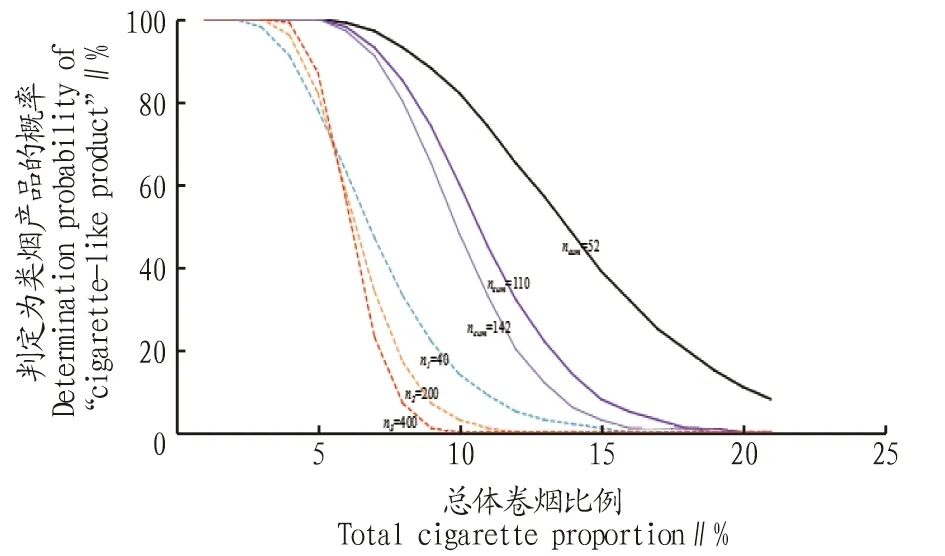
圖1 序貫抽樣ncum為52、110、142和一次抽樣n為80、200、400的OC曲線 Fig.1 OC curve (ncum=52,110,142 and n=80,200,400)

注:M為DNA Marker分子量為100~1 500 bp,S為卷煙標準樣品擴增結果,n1~n52為初次抽樣類煙產品樣品1~52擴增結果 Note:M is the DNA marker with molecular weight of 100-1 500 bp,S is the amplification result of cigarette standard sample,n1-n52 is the amplification result of 1 - 52 of the first sample of cigarette-like products圖2 初次抽樣(nmin=52)煙草SSR特異性引物擴增結果Fig.2 Amplification results of tobacco specificity SSR primer pairs on original sampling (nmin=52)
3 討論
抽樣檢驗是從一批產品中抽取一些樣品進行測量、考核、檢驗或與規定要求相比,最終依據所得結果決定整批產品或過程是否合格的質量檢驗方法,目的是在短時間內、以較低的成本、正確地判斷產品是否符合技術標準[15]。序貫抽樣方法需要每次抽樣結束后進行檢驗,判斷是否進行進一步檢驗,與隨機抽樣、分層抽樣等方法相比,存在一定誤判風險,對檢驗人員的專業技術熟練度要求相對較高[16]。當檢驗接近判定閾值的批次時,會導致鑒別檢驗周期延長,需平衡時間和經濟成本。在該研究中,無論是卷煙還是類煙產品均屬于經工藝和機械加工后的工業產品,其質量有一定的穩定性,也就是說產品的相對一致性是較好的。因此,鑒別檢驗過程中,煙支含煙草特征性成分的類煙產品數量較少,即混有卷煙的類煙產品在生產過程中被嚴格控制,大多數的被檢樣品相對一致性較高,只需檢驗很小的樣本就能通過。從現有的一次抽樣方案來看,抽取52支檢驗,如果假煙大于或等于6支,則該批卷煙判定為不合格,而且以90%的把握認為該批卷煙產品總體卷煙支數比例在區間(6.09%,20.80%),說明當樣本較少時,置信區間過寬,對總體的估計偏差增大,抽樣精確度下降,存在抽樣取證的“風險”。該研究中的OC曲線也表明,抽樣方案在較小抽樣量的基礎上,隨著樣品數量的增加比一次抽樣具有更佳的靈敏度和確定度。該研究中經過序貫抽樣確定nmin為52,此時停止抽取樣品進行DNA鑒定,判定52支卷煙均為類煙產品,說明此鑒別方法較為可行。
4 結論
該研究構建了類煙產品序貫抽樣方案,以訴訟方風險α=0.05、嫌疑人風險β=0.10、總體的卷煙比例≤5%為接收標準,確定了雙尾檢驗最小理論抽樣量為52,最大抽樣量為363,最多需要檢驗11次。經序貫抽樣后確定的供檢材料再進行DNA檢驗,可提高鑒別結果的準確性和客觀性。

