阻塞性睡眠呼吸暫停低通氣綜合征患者合并認知障礙的影響因素及尿液阿爾茨海默病相關神經絲蛋白水平對其診斷價值
郭芋妙,康美美,樊曉軍,張連國,王蓉,聶秀紅
阻塞性睡眠呼吸暫停低通氣綜合征(obstructive sleep apnea hypopnea syndrome,OSAHS)是一種常見的能引起全身多個系統及器官功能損傷的慢性睡眠呼吸障礙性疾病,隨著肥胖及老齡人口的增加,其發病率逐年上升[1]。輕度認知障礙(mild cognitive impairment,MCI)是OSAHS患者神經系統的早期并發癥,發生率可達26%[2]。MCI起病隱匿,早期癥狀輕微,易被忽視,一旦病情惡化則易進展為阿爾茨海默病(Alzheimer's disease,AD),給家庭和社會帶來沉重負擔[3]。目前臨床常用蒙特利爾認知評估(Montreal Cognitive Assessment,MoCA)量表對OSAHS患者是否存在認知障礙進行篩查,但量表易受主觀因素影響且操作復雜而耗時,應用價值有限[4]。生物標志物在機體內的變化常早于組織結構的變化及臨床癥狀的出現,因此,探究OSAHS合并認知障礙的影響因素,尋找靈敏度及特異度高的生物標志物對于疾病的早期診斷具有很高的臨床價值。近年來,基于血液、腦脊液的相關生物標志物得到廣泛關注,但因其取材難度大、操作有創、患者依從性差等原因,未在臨床中廣泛應用。阿爾茨海默病相關神經絲蛋白(Alzheimer's disease-associated neurofilament protein,AD7c-NTP)是神經絲蛋白家族的一員,與大腦神經元損傷密切相關,且尿液AD7c-NTP水平檢測能達到與腦脊液相同的效果,對AD/MCI的診斷具有較高的特異度及靈敏度[5-7]。還有研究指出,OSAHS患者尿液AD7c-NTP水平明顯升高[8],因此推測AD7c-NTP在OSAHS患者認知功能損傷的發生中亦扮演了重要角色,但仍需進一步研究證實。本研究旨在探討OSAHS患者合并認知障礙的影響因素及尿液AD7c-NTP水平對其診斷價值,以期為臨床合并認知障礙的高危OSAHS患者的早期篩查提供新方法。
1 對象與方法
1.1 研究對象 選擇2019年6—12月就診于首都醫科大學宣武醫院呼吸與危重癥醫學科并經多導睡眠圖(polysomnography,PSG)監測確診為OSAHS的患者116例,均符合中華醫學會呼吸病學分會睡眠呼吸障礙學組制定的《阻塞性睡眠呼吸暫停低通氣綜合征診治指南(2011年修訂版)》[9]中OSAHS的診斷標準。根據MoCA量表評分,將患者分為認知正常組80例(MoCA量表評分≥26分)和認知障礙組36例(MoCA量表評分<26分)。選取同期以打鼾為主訴就診于首都醫科大學宣武醫院呼吸與危重癥醫學科并經PSG監測排除OSAHS的正常成年人32例作為對照組。納入標準:(1)年齡>18歲,文化水平在小學及以上;(2)對本研究知情并同意,可以配合進行PSG監測、認知功能評估及中段尿標本的留取。排除標準:(1)非初診,經過治療者;(2)患有內分泌系統疾病,如糖尿病、甲狀腺功能異常等者;(3)存在能引起認知障礙的其他神經系統疾病,如帕金森病、癲癇、精神障礙等者;(4)存在嚴重的心血管事件者;(5)患有腫瘤、近1個月內行大型手術、存在嚴重感染及肝腎功能不全者;(6)正在服用鎮靜催眠、抗精神病類藥物及大量飲酒者。本研究通過首都醫科大學宣武醫院醫學倫理委員會批準(倫理號:臨研申[2021]165號)。
1.2 研究方法
1.2.1 一般資料收集 收集受試者一般資料,包括性別、年齡、BMI、受教育年限、吸煙史、飲酒史。
1.2.2 PSG監測 所有受試者在首都醫科大學宣武醫院呼吸與危重癥醫學科采用澳大利亞Compumedics公司生產的多導睡眠監測系統進行徹夜的PSG監測。記錄口鼻氣流、鼾聲、體位、胸腹運動、指端血氧飽和度等。進行PSG監測前24 h禁酒、咖啡及禁止服用影響睡眠的藥物,計算機自動分析的睡眠呼吸事件由專人進行校正,記錄呼吸暫停低通氣指數(apnea hypopnea index,AHI)、最長呼吸暫停時間(longest apnea time,LAT)、睡眠時血氧飽和度<90%的時間占睡眠總時間的百分比(percentage of sleep time spend when oxygen saturation lower than 90%,SLT90%)、睡眠時最低血氧飽和度(lowest arterial oxygen saturation,LSaO2)、氧減指數(oxygen desaturation index,ODI)(睡眠時血氧飽和度下降≥4%的次數)。根據美國睡眠醫學會制定的睡眠分期標準[10],將睡眠分為Ⅰ期、Ⅱ期、Ⅲ期和快速眼動睡眠(rapid eye movement,REM)期,計算Ⅰ+Ⅱ期睡眠時間占總睡眠時間的百分比(percentage of stageⅠ+Ⅱin total sleep time,Ⅰ+Ⅱ%)、Ⅲ期睡眠時間占總睡眠時間的百分比(percentage of stage Ⅲ in total sleep time,Ⅲ%)及REM期睡眠時間占總睡眠時間的百分比(percentage of REM stage in total sleep time,REM%),所有監測結果必須經過專科臨床醫師審核。
1.2.3 認知功能評估 使用MoCA量表[11]進行認知功能評估,總分為30分,得分≥26分為認知功能正常,得分<26分為認知障礙,對于受教育年限≤12年的患者,最終得分加1分以校正偏差。
1.2.4 尿液AD7c-NTP水平檢測 所有受試者于PSG監測第2天清晨留取中段尿,棄去渾濁或顏色很深的尿液標本,選取清亮的標本,采用加入硼酸防腐劑的塑料試管密封保存于2~8 ℃冰箱備用(不超過1周)。采用酶聯免疫吸附試驗檢測尿液AD7c-NTP水平,由專人嚴格按照試劑盒說明書進行操作。
1.3 統計學方法 采用SPSS 23.0統計軟件進行數據分析。對所有計量資料進行正態性檢驗,服從正態分布的計量資料以(±s)表示,多組間比較采用單因素方差分析,組間兩兩比較采用LSD-t檢驗;不服從正態分布的計量資料以M(P25,P75)表示,多組間比較采用Kruskal-Wallis檢驗,組間兩兩比較采用Mann-WhitneyU檢驗;計數資料以相對數表示,組間比較采用χ2檢驗;兩變量間的相關性分析采用Spearman秩相關分析;采用多因素Logistic回歸分析探討OSAHS患者合并認知障礙的影響因素;采用ROC曲線分析尿液AD7c-NTP水平對OSAHS患者合并認知障礙的診斷價值。以P<0.05為差異有統計學意義。
2 結果
2.1 三組一般資料、PSG監測指標、MoCA量表評分、尿液AD7c-NTP水平比較 三組性別、受教育年限、有吸煙史者占比、有飲酒史者占比比較,差異無統計學意義(P>0.05);三組年齡、BMI、AHI、LAT、SLT90%、LSaO2、ODI、Ⅰ+Ⅱ%、Ⅲ%、REM%、尿液AD7c-NTP水平比較,差異有統計學意義(P<0.05)。認知正常組BMI、AHI、SLT90%、ODI高于對照組,LAT長于對照組,LSaO2、REM%低于對照組,差異有統計學意義(P<0.05);認知障礙組年齡、BMI、AHI、SLT90%、ODI、尿液AD7c-NTP水平高于對照組,LAT長于對照組,LSaO2、REM%低于對照組,差異有統計學意義(P<0.05);認知障礙組BMI、AHI、SLT90%、ODI、Ⅰ+Ⅱ%、尿液AD7c-NTP水平高于認知正常組,LAT長于認知正常組,LSaO2、Ⅲ%低于認知正常組,差異有統計學意義(P<0.05),見表1。
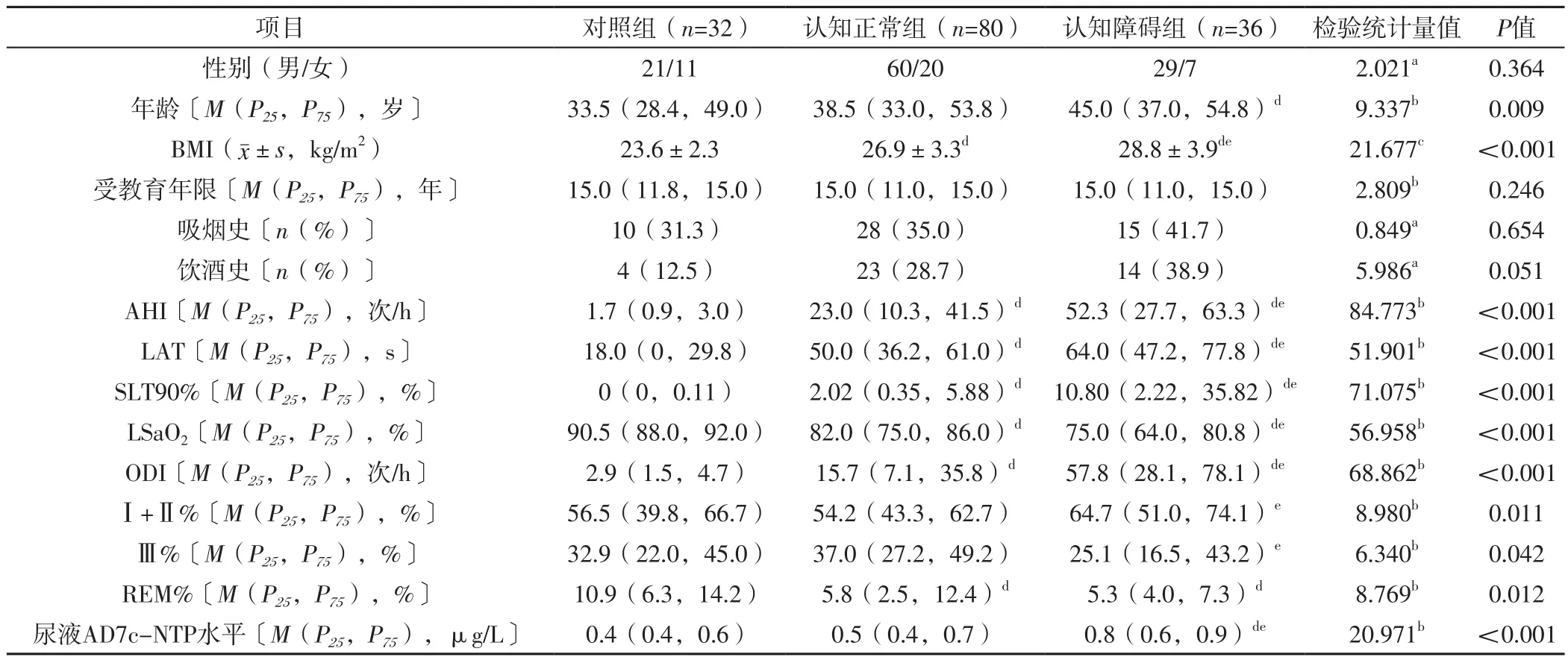
表1 三組一般資料、PSG監測指標、尿液AD7c-NTP水平比較Table 1 Comparison of general data,PSG monitoring indexes and urine AD7c-NTP level among the three groups
2.2 OSAHS患者尿液AD7c-NTP水平與MoCA量表評分的相關性 OSAHS患者尿液AD7c-NTP水平為0.6(0.4,0.8)μg/L,MoCA量表評分為26.0(25.0,27.0)分。Spearman秩相關分析結果顯示,OSAHS患者尿液AD7c-NTP水平與MoCA量表評分呈負相關(rs=-0.461,P<0.001),見圖1。
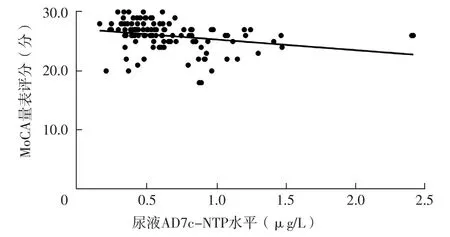
圖1 OSAHS患者尿液AD7c-NTP水平與MoCA量表評分的相關性Figure 1 Correlation between urine AD7c-NTP level and MoCA Scale score in OSAHS patients
2.3 OSAHS患者合并認知障礙影響因素的多因素Logistic回歸分析 以BMI、AHI、LAT、SLT90%、LSaO2、ODI、Ⅰ+Ⅱ%、Ⅲ%、尿液AD7c-NTP水平為自變量(實測值),OSAHS患者是否合并認知障礙為因變量(賦值:否=0,是=1),進行多因素Logistic回歸分析,結果顯示,ODI、Ⅲ%及尿液AD7c-NTP水平是OSAHS患者合并認知障礙的獨立影響因素(P<0.05),見表2。
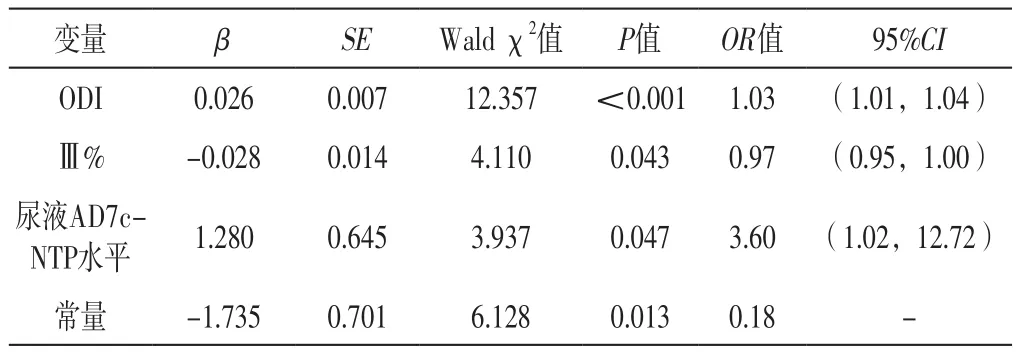
表2 OSAHS患者合并認知障礙影響因素的多因素Logistic回歸分析Table 2 Multivariate Logistic regression analysis of influencing factors of cognitive impairment in patients with OSAHS
2.4 尿液AD7c-NTP水平對OSAHS患者合并認知障礙的診斷價值 ROC曲線分析結果顯示,尿液AD7c-NTP水平診斷OSAHS患者合并認知障礙的AUC為0.716〔95%CI(0.612,0.819)〕,最佳截斷值為0.5 μg/L,靈敏度為80.6%,特異度為61.3%,約登指數為0.471,見圖2。
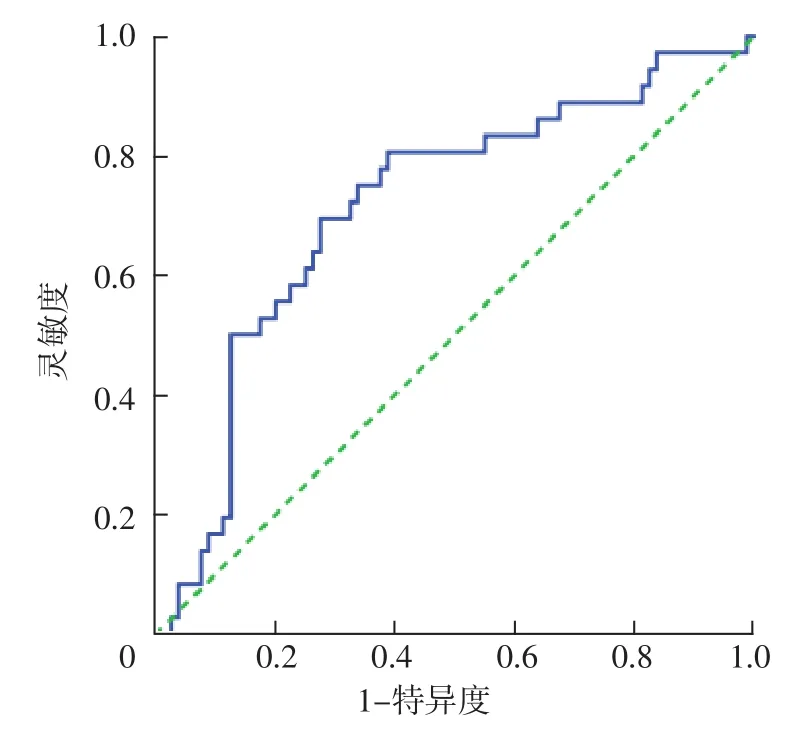
圖2 尿液AD7c-NTP水平診斷OSAHS患者合并認知障礙的ROC曲線Figure 2 ROC curve of urine AD7c-NTP level for the diagnosis of cognitive impairment in patients with OSAHS
3 討論
OSAHS患者因睡眠過程中反復出現呼吸暫停和低通氣,常引起慢性間歇性低氧、高碳酸血癥以及睡眠結構紊亂,是MCI和AD的獨立危險因素[12]。MCI向AD的年轉化率為10%~15%,是正常老年人的10倍[13],其作為AD的早期預警已得到廣泛認同,且早期識別及干預MCI可以延緩疾病進展、預防AD的發生。既往研究證實,尿液AD7c-NTP水平檢測能達到與腦脊液相同的效果,其診斷AD/MCI具有很高的特異度及靈敏度[6-7]。鑒于尿液標本采集方便、可重復性強、患者依從性好,如尿液AD7c-NTP水平能作為OSAHS患者合并認知障礙的篩查指標,將有很大的臨床價值。然而,目前在OSAHS患者中檢測尿液AD7c-NTP水平的研究甚少。本研究旨在探討OSAHS患者合并認知障礙的影響因素及尿液AD7c-NTP水平對其診斷價值。
OSAHS患者發生認知障礙是多因素共同作用的結果,加強對危險因素的認識,對于疾病的預測以及更好的防治十分重要。大多數研究證實,年齡、BMI、受教育年限是OSAHS患者合并認知障礙的危險因素[14-15]。趙阿敏等[16]研究發現,OSAHS患者年齡越大,認知功能越差,這可能與多巴胺水平下降及大腦失用、大腦容量減低及功能退化有關。而LAVIE等[17]卻認為,在老年患者中,輕度OSAHS對心腦血管有一定的保護作用,可能降低認知功能損傷的風險。本研究結果顯示,認知障礙組年齡高于對照組,與認知正常組比較無統計學差異,與既往研究結果存在差異,可能是由于本研究樣本量較小,納入的老年受試者較少,對老年OSAHS患者的認知功能評估有限,后期仍需擴大樣本量,進一步探討年齡對OSAHS患者合并認知障礙的影響。GUNSTAD等[15]報道顯示,超重和肥胖的人群較正常體質量人群執行能力差,而且這種差異不受年齡的影響;另外,高脂飲食引起的肥胖癥與海馬依賴型記憶障礙相關,持續高脂飲食喂養的小鼠空間記憶能力受損,且與記憶整合有關的基因表達減少[18-19]。本研究結果顯示,認知正常組、認知障礙組BMI高于對照組,且認知障礙組BMI高于認知正常組,提示OSAHS患者無論是否合并認知障礙,其BMI均升高,而合并認知障礙的OSAHS患者BMI升高更明顯,表明BMI可能是OSAHS及認知障礙的影響因素。研究顯示,高文化水平可以降低OSAHS患者出現認知障礙的風險[14],這可能是因為高學歷人群在平時工作、學習時用腦更多,大腦細胞更加活躍,而這或許可以減緩大腦老化的速度;另一方面,高學歷人群可能有更多的途徑來了解及關注疾病知識,從而采取相應的措施來減少認知障礙的發生風險。但本研究結果顯示,三組受教育年限比較無統計學差異,可能與本研究受試者大多來自北京,且均為自行就醫者,文化水平普遍較高有關。
既往研究認為,夜間低氧/低通氣是OSAHS患者發生認知障礙的重要原因。長期缺氧可引發OSAHS患者海馬及大腦皮質損傷,從而導致認知功能特別是記憶力受損[20-21]。此外,OSAHS患者夜間反復出現呼吸暫停,造成大腦間歇性低氧而引起氧化應激反應,導致細胞氧化-抗氧化、凋亡-抗凋亡機制失衡,腦細胞內自由基瀑布式增加,出現選擇性腦細胞壞死及凋亡,從而影響認知及記憶功能[22-23]。本研究結果顯示,認知正常組、認知障礙組AHI、SLT90%、ODI高于對照組,LAT長于對照組,LSaO2低于對照組,提示OSAHS可引起呼吸暫停和低通氣,從而引起缺氧。認知障礙組AHI、SLT90%、ODI高于認知正常組,LAT長于認知正常組,LSaO2低于認知正常組,提示OSAHS病情嚴重程度、呼吸暫停和低通氣時間、缺氧與認知功能密切相關,且多因素Logistic回歸分析結果顯示,ODI是OSAHS合并認知障礙的獨立危險因素,與張永林等[24]研究結果一致。
睡眠結構紊亂是OSAHS患者出現認知障礙的另一關鍵因素[25]。在睡眠分期中REM期睡眠被稱為“黃金睡眠”,負責清理腦組織代謝產物,制備機體活動所需的蛋白質和神經遞質,在解除疲勞、促進學習記憶及記憶鞏固等方面起關鍵作用[26]。而深睡眠能促進生長和體力恢復,缺乏深睡眠可導致日間嗜睡、精力差等一系列癥狀[26-27],因此,長期深睡眠、REM期睡眠時間減少及淺睡眠時間延長會導致認知功能受損。本研究結果顯示,認知障礙組Ⅰ+Ⅱ%高于認知正常組,Ⅲ%低于認知正常組,提示淺睡眠時間延長、深睡眠時間縮短可能是OSAHS患者合并認知障礙的影響因素;多因素Logistic回歸分析結果顯示,Ⅲ%升高是OSAHS患者認知功能的保護因素,即深睡眠時間縮短是OSAHS患者合并認知障礙的獨立危險因素,這與KIM等[28]、ZHU等[29]研究結果一致。認知正常組、認知障礙組REM%低于對照組,提示OSAHS患者REM期睡眠時間減少;但認知正常組與認識障礙組REM%比較差異無統計學意義,與既往研究結果[30]不一致,考慮可能與樣本量較小、受試人群選擇差異有關。
AD7c-NTP最早是由麻省總醫院的de la Monte教授課題組在晚期AD患者的顳葉腦組織中分離得到并命名的,其表達于神經元的軸突上,能特異性反映大腦神經元的損傷程度[5]。AD7c-NTP在神經元的異常表達可促進神經炎癥及神經元的死亡,從而參與AD的發生。由于AD7c-NTP可通過血-腦脊液屏障并經腎小球濾過排出,因此,尿液AD7c-NTP水平能準確反映腦脊液中該指標的水平,其或許可作為協助診斷MCI/AD的生物標志物[6]。JIN等[31]通過檢測1 805名健康人尿液AD7c-NTP水平發現,尿液AD7c-NTP水平不受人口統計學因素及非神經系統常見慢性疾病的影響,說明其作為診斷MCI的生物標志物具有良好的穩定性。朱鳳娟等[8]研究發現,OSAHS患者尿液AD7c-NTP水平明顯升高,且與OSAHS病情嚴重程度密切相關,提示AD7c-NTP可能參與了OSAHS發生發展的過程。本研究結果顯示,認知障礙組尿液AD7c-NTP水平高于認知正常組、對照組,提示尿液AD7c-NTP水平可能是OSAHS患者合并認知障礙的影響因素。Spearman秩相關分析結果顯示,OSAHS患者尿液AD7c-NTP水平與MoCA量表評分呈負相關,提示尿液AD7c-NTP水平越高,認知功能損傷越嚴重,與既往研究結果[32]一致。多因素Logistic回歸分析結果顯示,尿液AD7c-NTP水平是OSAHS患者合并認知障礙的獨立影響因素;且ROC曲線分析結果顯示,尿液AD7c-NTP水平診斷OSAHS患者合并認知障礙的AUC為0.716,提示尿液AD7c-NTP水平對OSAHS患者合并認知障礙具有一定診斷價值,這為臨床中MCI的早期識別及客觀評估提供了新方法。
綜上所述,ODI、尿液AD7c-NTP水平升高是OSAHS患者合并認知障礙的危險因素,Ⅲ%升高是OSAHS患者合并認知障礙的保護因素,且尿液AD7c-NTP水平對OSAHS患者合并認知障礙具有一定診斷價值,這有助于臨床早期預測OSAHS患者合并認知障礙的風險,并盡早給予相應的干預措施,以延緩疾病進展。但本研究尚存在一定局限性:本研究為單中心研究,樣本量小;本研究為橫斷面研究,未對受試者進行隨訪;本研究未對受試者性別、年齡進行詳細劃分。此外,尿液AD7c-NTP水平在MCI及AD中的作用機制尚不明確,仍需進行多中心、大樣本量、前瞻性臨床及基礎研究進一步驗證。
作者貢獻:郭芋妙進行文章的構思與設計;郭芋妙、康美美進行數據的收集、資料的整理、統計學處理、結果的分析與解釋;郭芋妙進行論文的撰寫與修訂;樊曉軍、張連國進行研究的實施及可行性分析;王蓉、聶秀紅負責文章的質量控制及審校,對文章整體負責、監督管理。
本文無利益沖突。

