重組人生長激素在FET周期中治療薄型子宮內膜的應用
黃柳靜,莫鳳媚,巫晶晶,周艷群,李西,李榮
(廣西醫科大學第三附屬醫院生殖醫療中心,南寧 530031)
在體外受精-胚胎移植(IVF-ET)治療中,胚胎質量和子宮內膜狀態是成功妊娠的兩大關鍵因素[1],其中子宮內膜因素占2/3,胚胎因素占1/3[2]。臨床上,有一部分患者因子宮內膜薄導致反復胚胎種植失敗,經多種方法治療仍不能有效增加子宮內膜厚度。近年來,有研究顯示重組人生長激素(rhGH)可以改善薄型子宮內膜患者的子宮內膜容受性,進而提高臨床妊娠率,改善妊娠結局[3]。本研究通過分析rhGH不同給藥方式對子宮內膜厚度、內膜體積、血流情況以及凍融胚胎移植(FET)臨床結局的影響,探討rhGH在薄型子宮內膜患者中的應用價值,以期為臨床治療提供參考。
資料和方法
一、研究對象
收集2018年1月至2020年12月在廣西醫科大學第三附屬醫院生殖醫療中心行FET治療的薄型子宮內膜患者74例為研究對象。
納入標準:(1)月經周期規律者:有自然排卵,排卵期內膜厚度<7 mm;月經周期不規律者:使用外源性雌激素≥20 d內膜厚度仍<7 mm;(2)行IVF或ICSI后,有優質胚胎凍存;(3)宮腔粘連者行宮腔鏡下宮腔粘連分離術并復查宮腔鏡確認無粘連復發。
排除標準:(1)合并子宮腺肌病、子宮畸形、子宮內膜癌、子宮內膜非典型增生、子宮內膜結核、粘膜下子宮肌瘤、宮腔積液;(2)合并甲狀腺功能異常;(3)存在血栓傾向性疾病。
本研究經本院倫理委員會批準(Y201811),患者充分知情同意后簽署知情同意書。
本研究擬設置激素替代治療(HRT)+宮腔灌注rhGH、HRT+皮下注射rhGH和單純HRT三種方案治療薄型子宮內膜,研究所需樣本量通過樣本量計算公式計算。經過預試驗和樣本量計算,得出每組最少約需觀察24例患者。
二、分組及處理
1.研究對象分組:所有納入患者均行HRT方案準備內膜。根據所需樣本量及HRT啟動時間不同對患者進行分組:周一、周四啟動HRT者納入宮腔灌注組(24例);周二、周五啟動者納入皮下注射組(25例);周三、周六啟動者納入對照組(25例)。
2.薄型子宮內膜治療:(1)對照組:單純HRT方案。月經第3天開始給予戊酸雌二醇(補佳樂,拜耳醫藥,德國)6 mg/d+阿司匹林腸溶片(拜阿司匹靈,拜耳醫藥,德國)100 mg/d;(2)宮腔灌注組:HRT第8~10天開始給予宮腔灌注rhGH(賽增,4.5 U/支,長春金賽藥業)4.5 U,Qod;(3)皮下注射組:HRT第1天開始予皮下注射rhGH 4.5 U,Qd。三組均采用同樣的HRT方案,對照組僅行HRT,不添加rhGH。
HRT治療10 d后測量子宮內膜厚度,如未達8 mm,予芬嗎通(雌二醇片/雌二醇地屈孕酮片,雅培,荷蘭)白片1 mg,陰道給藥,Qd。3~5 d后再復查B超,當子宮內膜厚度達到或超過8 mm,行黃體酮轉化;如HRT已達20 d而內膜厚度仍<8 mm也行黃體酮轉化,轉化當日停用rhGH。在黃體酮轉化的第4天移植復蘇卵裂期胚胎,轉化的第6天移植復蘇囊胚。
3.rhGH給藥:(1)宮腔灌注方法:患者取膀胱截石位,消毒外陰、陰道和宮頸后,生理鹽水抹洗陰道壁及宮頸,使用注射器抽取1 ml 0.9%生理鹽水溶解rhGH,連接一次性人工授精管(太平洋康泰科學儀器濟南有限公司),授精管前端進入宮頸內口上方后緩慢注入宮腔。灌注完畢,將患者臀部抬高15~30°,臥床休息10 min。(2)皮下注射方法:rhGH溶解方法同宮腔灌注組,于腹壁臍周皮下注射。
4.黃體支持及隨訪:內膜轉化日即開始進行黃體支持,給予黃體酮注射液(浙江仙琚制藥)60 mg/d肌肉注射;移植日開始添加地屈孕酮(雅培,荷蘭)口服,10 mg/次,Bid。補佳樂、芬嗎通及阿司匹林量同前。移植后14 d抽血測β-HCG,如HCG陽性,停芬嗎通,余用藥同前。如未妊娠,則停所有藥物。孕8周左右停補佳樂。黃體支持至孕10周左右。
移植后14~16 d抽血檢測β-HCG>25 U/L為HCG陽性;移植后4~5周B超檢查探及妊娠囊為臨床妊娠;發生在妊娠12周以前的流產為早期流產。
5.觀察指標及測量方法:主要觀察指標有子宮內膜厚度、體積、內膜分型及血流參數、妊娠結局等。納入患者入組時測量的相關數據為治療前數據,黃體酮轉化內膜當日測量的為治療后數據。
子宮內膜各參數測量均使用美國GE Voluson E10超聲診斷儀進行,測量由同一人操作。(1)內膜厚度:在子宮矢狀面測量垂直子宮中線的子宮內膜與子宮肌層分界處外緣的最大經線。(2)內膜體積:啟用3D功能鍵,選用多平面模式,體積角度120°,取樣框盡可能將內膜完全包于框內,啟動容積掃查,獲取三平面容積數據,應用VOCAL分析軟件對內膜進行體積分析。手動測量功能:設置提取容積數據每一切面間角度為30°進行勾畫,每個圖像共測量6次,獲取內膜體積數據。(3)內膜分型:A型:呈典型“三線征”,內膜功能層表現為低回聲,基底層和宮腔線表現為高回聲;B型:呈均勻的中等回聲,宮腔線連續不清;C型:呈均勻高回聲,無明顯宮腔線中線回聲。(4)內膜血流類型:獲取子宮灰階正中長軸切面,檢測子宮內膜及內膜下血流灌注情況:Ⅰ型:內膜區域可見血流信號,并接近宮腔中線;Ⅱ型:內膜區域可見血流信號,但≤1/2單層內膜;Ⅲ型:內膜下區域可見血流信號[4](本研究將內膜下區域設定為內膜邊緣外1 mm[5])。如超聲下在內膜和內膜下區域均未探及明顯血流信號,則記為“無”。(5)內膜血流參數:在子宮矢狀面內膜與肌層交界的暗帶區域、彩色血流最明亮處獲取內膜下血流脈沖多普勒頻譜,所有血流至少連續顯示3~5個心動周期,自動獲得收縮期峰值血流速度(PSV)、舒張末期血流速度(EDV)、搏動指數(PI)、阻力指數(RI)及PSV與EDV比值(S/D值)。(6)內膜和內膜下容積三維能量:內膜容積三維能量的檢測應用三維能量直方圖分析軟件,獲得血管化指數(VI)(以百分率表示)、血流指數(FI)(數值范圍0~100)、血管化血流指數(VFI)(數值范圍0~100);內膜下容積三維能量的檢測應用外殼成像(shell-imaging)系統,獲得內膜下VI、FI、VFI[5-6]。
三、統計學方法
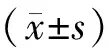
結 果
一、患者一般資料比較
3組患者間年齡、不孕年限、體質量指數(BMI)、抗苗勒管激素(AMH)、基礎卵泡刺激素(bFSH)、補佳樂和芬嗎通的使用天數均無顯著性差異(P>0.05)(表1)。
二、移植胚胎情況比較
3組患者間移植胚胎類型和平均移植胚胎數均無顯著性差異(P>0.05)(表2)。
表1 各組患者的一般情況比較(-±s)
表2 各組患者移植胚胎情況比較 [(-±s),%]
三、治療前、后子宮內膜各參數比較
1.內膜形態:3組患者間治療前子宮內膜厚度、內膜體積均無顯著性差異(P>0.05)。宮腔灌注組、皮下注射組治療后的內膜厚度、內膜體積均顯著高于治療前(P<0.05),而對照組治療前后的內膜厚度、內膜體積無顯著性差異(P>0.05)。宮腔灌注組和皮下注射組治療后內膜厚度、內膜厚度增幅均顯著高于對照組(P<0.05);3組患者間治療后內膜體積均無顯著性差異(P>0.05),但皮下注射組的內膜體積增幅顯著高于對照組(P<0.05)。3組患者間治療前后內膜類型均無顯著性差異(P>0.05)(表3)。
表3 各組患者治療前后內膜狀況比較[(-±s),n(%)]
2.內膜血流:3組患者間治療前后內膜血流類型及血流參數比較均無顯著性差異(P>0.05)(表4)。
3.內膜和內膜下容積三維能量:宮腔灌注組治療后內膜下FI顯著高于治療前,皮下注射組治療后內膜FI和內膜下VI均顯著高于治療前(P<0.05)(表5)。
四、妊娠結局比較
本研究共納入74例患者的74個FET周期。3組患者間HCG陽性率、臨床妊娠率、胚胎著床率、早期流產率均無顯著性差異(P>0.05)(表6)。
表4 各組患者治療前后內膜血流類型/參數比較[(-±s),n(%)]
表5 各組患者治療前后內膜和內膜下容積三維能量比較(-±s)
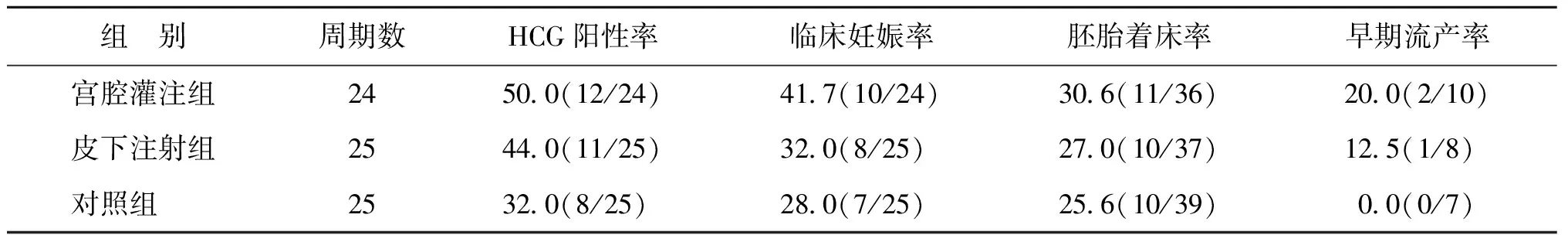
表6 各組患者妊娠結局比較(%)
討 論
薄型子宮內膜是指子宮內膜厚度低于胚胎能夠種植的閾厚度,目前尚無統一的診斷標準,普遍觀點認為排卵日或給予黃體支持當天,子宮內膜厚度<7 mm可視為薄型子宮內膜[7]。薄型子宮內膜的容受性明顯降低。當子宮內膜基底層受損嚴重時,子宮內膜成體干細胞數量減少或功能異常,增殖能力下降,導致內膜過薄而不能支持胚胎種植。常用于治療薄型子宮內膜的方法有大劑量雌激素治療、抑制血小板聚集藥物(阿司匹林)或血管擴張藥物(西地那非)等的應用[8]。有一部分患者得益于這些治療方法,但仍有一部分患者收效甚微。
人體內的生長激素(GH)是由腦垂體前葉嗜酸性細胞分泌的一種蛋白質激素,參與細胞生長代謝,對生殖系統功能維持也有重要作用,包括改善卵巢反應性、提高卵子質量和胚胎質量[9-10]、促進子宮內膜生長、改善子宮內膜容受性等[11-12],最終提高胚胎著床率和臨床妊娠率[13]。還有研究發現宮腔灌注GH能增加薄型子宮內膜患者的子宮內膜厚度,提高妊娠率[3,14]。本研究將rhGH用于宮腔灌注或者皮下注射,與對照組(未使用GH)相比,結果顯示,無論是宮腔灌注組還是皮下注射組,子宮內膜厚度均顯著增加(P<0.05),對照組則無明顯增長。胡淑敏等[15]的研究也發現,激素替代聯合宮腔灌注或皮下注射GH能降低子宮內膜PI、RI及S/D值,改善內膜血流,增加內膜厚度,提高妊娠率;但其結果提示宮腔灌注較皮下給藥和單純雌激素治療,可以更好地促進子宮內膜的發育,與本研究結果并不完全一致。本研究中,皮下注射組的厚度增幅比宮腔灌注組稍大,但差異尚無統計學意義(P>0.05)。
除了子宮內膜厚度,子宮內膜容受性還與子宮內膜體積、形態有關。有研究認為,內膜體積<1 ml時很難受孕,體積>2 ml時受孕率顯著提高[16]。在本研究中,治療前3組患者的子宮內膜體積均<2 ml,經過GH治療,宮腔灌注組的子宮內膜體積達(1.86±0.81) ml,皮下注射組達(2.01±0.85) ml。使用GH的兩組內膜體積增幅均有高于對照組的趨勢,其中皮下注射組與對照組比較有顯著性差異(P<0.05)。在不同內膜分型中,A型、B型子宮內膜容受性較C型好。本研究發現,GH有助于增加子宮內膜厚度和體積,但對內膜類型無明顯影響,與馬新想等[17]研究結果一致。
子宮內膜容受性還與子宮內膜血流灌注有關。目前陰道彩超已廣泛應用于評估子宮內膜血流灌注情況。Raine-Fenning等[18]通過三維超聲發現子宮內膜和內膜下的血管在增生期增加,在排卵前3 d達到峰值,在排卵后5 d降至最低點。子宮內膜血流參數中,PI反應血管的彈性和順應性,正常范圍1~1.5;PI<2時,容受性最好;PI>3時,妊娠率幾乎為零[19];RI反應血流阻力,孫瑩璞等[20]研究發現當RI>0.8時,妊娠率從47.12%銳減至15.38%。本研究中3組患者的PI、RI和S/D值在治療前后均無明顯改變。子宮內膜Ⅰ型血流是比較理想的血流類型,提示子宮內膜的血運較為豐富。本研究中,經過GH治療,宮腔灌注組和皮下注射組的Ⅰ型血流率均較治療前有所增加,但尚無顯著性差異(P>0.05)。
內膜和內膜下區域三維能量中,VI代表目標容積內血管數目多少,主要用于觀察血管的空間分布情況;FI代表目標容積內血流信號的強度,主要用于評估血流的平均速度;VFI是血管信息與血流信息的結合,可以根據流量的估計推算血供情況[21]。Kim等[22]在研究中發現妊娠組子宮內膜的VI、FI、VFI較非妊娠組顯著升高(P<0.05),成功妊娠的VI、FI、VFI臨界值分別為0.95、12.94、0.15,而兩組內膜下VI、FI、VFI差異均無統計學意義(P>0.05)。有學者認為內膜下FI是最能預測妊娠結局的指標[5]。王錦惠等[23]認為內膜和內膜下的二維、三維超聲血流參數可作為評價子宮內膜容受性以及預測IVF-ET妊娠結局的客觀指標,其中PI具有較好的預測價值,內膜及內膜下VI有一定的預測價值。李杏嬋等[24]對64例中重度宮腔粘連分離術后的患者進行研究發現,人工周期聯合GH治療,子宮內膜的血流信號較對照組(僅人工周期)更為豐富,RI和PI均顯著低于對照組,VI、FI、VFI、內膜厚度和體積均顯著高于對照組(P均<0.05)。本研究結果顯示,宮腔灌注組的內膜下FI顯著高于治療前,皮下注射組的內膜FI和內膜下VI顯著高于治療前(P<0.05),提示無論宮腔灌注還是皮下注射rhGH,均有利于改善子宮內膜的血流灌注。
眾多研究表明GH的應用有利于改善臨床結局,Wang等[25]對240例行FET的患者進行研究發現,HRT同時添加rhGH可改善FET的妊娠結局,使用rhGH較長時間組比使用時間較短組和未使用rhGH組的子宮內膜厚度、E2、胰島素樣生長因子1(IGF-1)和血管內皮生長因子(VEGF)的血清水平顯著增加,PI、RI、S/D值顯著降低(P均<0.05),提示HRT聯合rhGH可增加子宮內膜血流灌注,促進與子宮內膜容受性相關的細胞因子表達,改善FET臨床結局。Yang等[26]對擬行FET的薄型子宮內膜患者(內膜厚度<8 mm)進行研究發現,GH組在黃體酮轉化內膜當日至胚胎移植日皮下注射GH,臨床妊娠率和胚胎著床率均較對照組顯著增高(P<0.05)。但本研究中,3組患者的臨床妊娠率、胚胎著床率、早期流產率差異均無統計學意義(P>0.05),僅數據顯示宮腔灌注組的臨床妊娠率、胚胎著床率有高于皮下注射組的趨勢,皮下注射組有高于對照組的趨勢。這和之前研究的結論不一致,考慮與本研究樣本量較小有關。
受到臨床中實際操作條件的限制,納入的樣本量較小是本研究的不足之處,因此研究結論可能存在一定的局限性,后續應繼續完善研究設計,開展更大樣本量的前瞻性研究以及隨機對照試驗加以驗證。
綜上所述,HRT聯合宮腔灌注或皮下注射rhGH均能顯著增加薄型子宮內膜患者的內膜厚度和體積,改善內膜的血流灌注,并有改善FET臨床結局的趨勢。宮腔灌注或皮下注射兩種方式給予GH在增加內膜厚度和體積、改善血流灌注方面,療效相似。宮腔灌注與皮下注射相比,患者需往返醫院的次數少,但宮腔灌注為侵入性操作,增加了感染的風險;皮下注射則增加了患者注射的痛苦,故在臨床上應綜合考慮患者的實際情況和自身意愿來選擇GH的給藥方式。

