輔助生殖技術新鮮及凍融周期異位妊娠相關因素分析
曾倩凌,劉能輝,燕 怡,李艷萍,趙 靜
(1.中南大學湘雅醫院生殖醫學中心,湖南 長沙 410008;2.湖南省人民醫院生殖醫學中心,湖南 長沙 410000;3.湖南省女性生殖健康臨床醫學研究中心,湖南 長沙 410008)
自1978年第1例試管嬰兒Louise Brown誕生至今,輔助生殖技術(assisted reproductive technology,ART)發展日新月異,從最初的體外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET),到其衍生技術凍融胚胎移植(frozen-thawed embryo transfer,FET),再到卵胞漿內單精子注射(intracytoplasmic sperm injection,ICSI)、經皮附睪/睪丸穿刺取精術(percutaneous epididymal sperm aspiration/testicular sperm extraction,PESA/TESE)及胚胎植入前遺傳學診斷/篩查(preimplantation genetic diagnosis/screen,PGD/PGS)等技術,為各種不孕原因的夫婦解決了生育難題。隨著ART的廣泛應用,人們逐漸認識到ART在給人們帶來福音的同時,也增加了不孕夫婦不良妊娠結局的風險;其中ART后異位妊娠發生風險高達2.1%~8.6%,顯著高于自然妊娠中異位妊娠發生率的1%~2%[1]。如未及時發現異位妊娠,最嚴重可導致致死性休克,危及孕婦生命。因此對ART中異位妊娠相關因素進行研究分析,并根據研究對治療方法進行改進,從而降低異位妊娠發生率尤為重要。
目前有一些關于ART后異位妊娠相關因素的報道顯示,在不孕因素中,輸卵管因素是公認的異位妊娠獨立危險因素,而多囊卵巢綜合征(polycystic ovarian syndrome,PCOS)對異位妊娠的影響尚存爭議,PCOS患者僅在新鮮胚胎移植周期中為異位妊娠的高危因素[2]。有研究指出,子宮內膜厚度(endometrium thickness,EMT)是異位妊娠發生的相關因素,胚胎移植前EMT>12mm的患者異位妊娠風險下降[3]。移植周期類型和移植胚胎類別對異位妊娠的影響存在爭議,部分研究認為FET和移植囊胚可以減少異位妊娠發生的幾率;也有研究提示兩者之間并無相關性[1,4]。但目前分別分析新鮮胚胎移植周期(新鮮周期)和凍融胚胎移植周期(凍融周期)異位妊娠相關因素的研究較少,且較多研究納入因素不全。本研究同時將亞生育因素及ART治療相關因素納入研究,并分別分析新鮮周期和凍融周期中與異位妊娠相關的因素,有望更好地發現影響因素,進而優化ART治療程序。
1 研究對象與方法
1.1 研究對象
選取2015年5月至2019年1月在中南大學湘雅醫院生殖醫學中心行ART治療并獲得臨床妊娠的病例為研究對象,研究獲得倫理批準。納入標準:①行IVF/ICSI/FET助孕者;②獲得臨床妊娠者;③臨床資料及隨訪記錄完整。排除標準:①合并嚴重基礎疾病,如高血壓、糖尿病、肝病等內科疾病;②夫妻任何一方染色體異常。根據標準,納入到異位妊娠組的病例為170例,選取同一時期宮內妊娠的病例1 999例為對照組;其中宮內妊娠合并宮外妊娠納入異位妊娠組,樣本量的確定:最小樣本量為自變量數目的15倍。
1.2 資料的收集
從中南大學湘雅醫院生殖醫學中心電子病歷系統采集病例的一般情況、治療過程、實驗室結果及妊娠結局等資料。
納入的影響因素指標包括:患者的一般情況[年齡、身體質量指數(body mass index,BMI)、吸煙史]、不孕相關因素(基礎性激素、不孕年限、不孕類型、異位妊娠史、流產史、剖宮產史、不孕因素)、ART相關因素(周期類型、促排卵方案、內膜準備方案、周期數、扳機日/內膜轉化日EMT、受精方式、移植胚胎數、胚胎類型、胚胎質量)。
1.3 治療方式
1.4 診斷標準
1.4.1 胚胎質量評估
1.4.1.1 卵裂期胚胎 卵裂期胚胎評分標準如下:Ⅰ級,細胞大小均勻,形狀規則,透明帶完整,碎片率<5%;Ⅱ級,細胞大小稍不均勻,形狀稍不規則,碎片率為10%~20%;Ⅲ級,細胞大小明顯不均勻,碎片率為21%~50%;Ⅳ級,細胞大小嚴重不均勻,碎片率>50%。優質卵裂期胚胎定義為卵裂球數目8~9個,評級為1~2級的胚胎,其余胚胎為非優質卵裂期胚胎[5-6]。
1.4.1.2 囊胚 按照Gardner評分系統對囊胚進行評級。優質囊胚的標準定義為3期及3期以上、內細胞團及滋養層細胞均為B級及以上,其余囊胚為非優質囊胚[5-6]。
1.4.2 妊娠結局
臨床妊娠:移植后28天超聲檢查見妊娠囊則判斷為臨床妊娠,2個或2個以上妊娠囊定義為多胎妊娠(包含異位妊娠)。異位妊娠:受精卵在子宮體腔以外著床者。
1.5 統計學方法
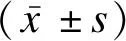
2 結果
2.1 妊娠結局情況
2015年5 月到2019年1月在中南大學湘雅醫院生殖中心經IVF/ICSI/FET助孕并獲得臨床妊娠周期5 654個,其中失訪311例。在隨訪到的5 343個臨床妊娠周期中,異位妊娠194例,占臨床妊娠的3.63%。
2.2 異位妊娠相關因素
2.2.1 兩組的一般情況和不孕因素及ART相關因素
2)知識目標:了解方言與普通話的關系,結合方言與普通話進行自我介紹。掌握普通話的形成、發展及與方言之間的聯系等相關知識及要點。
異位妊娠組與對照組比較,女方年齡和BMI、基礎卵泡刺激素(basic follicle-stimulating hormone,bFSH)、基礎雌二醇(basic estradiol,bE2)、基礎黃體生長素(basic luteinizing hormone,bLH)、不孕年限,流產史、剖宮產史、PCOS、子宮內膜異位癥、DOR、宮腔粘連、子宮畸形、子宮內膜息肉的分布,周期類型、受精方式、移植胚胎數、移植胚胎類型、移植胚胎質量,以及男方年齡和BMI,差異均無統計學意義(P>0.05);兩組的男方吸煙史、不孕類型、異位妊娠史、輸卵管炎癥分布,以及周期數和扳機日/內膜轉化日EMT比較差異均有統計學意義(P<0.05),見表1、表2。
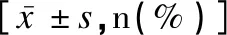
表1 異位妊娠組與對照組的基線資料、妊娠史及不孕原因的比較Table 1 Comparison of baseline data,pregnancy history and causes of infertility between the ectopic and intrauterine pregnancy

表2 異位妊娠組與對照組ART相關因素的比較Table 2 Comparison of ART related factors between ectopic pregnancy group and intrauterine pregnancy
2.2.2 異位妊娠的多因素分析及風險預測模型的構建
不區分新鮮周期與凍融周期,經多因素分析顯示,與異位妊娠相關的獨立影響因素包括男方吸煙史、異位妊娠史、輸卵管炎癥、周期數和扳機日/內膜轉化日EMT,見表3。
將這些因素帶入回歸公式構建風險預測模型:LogitP=0.410×男方吸煙史+0.513×EMT(<8mm)/(-0.682)×EMT(≥13mm)+0.815×輸卵管炎癥+0.712×異位妊娠史+0.164×周期數-2.708,對模型行似然比檢驗,回歸方程有統計學意義(χ2=52.433,P<0.001);對模型做判別能力評估,ROC曲線評估曲線下面積為0.671,標準誤=0.021,P<0.001,見圖1。
2.2.3 新鮮周期中異位妊娠的多因素分析及風險預測模型的構建
新鮮周期中與異位妊娠相關的獨立影響因素包括異位妊娠史、剖宮產史、輸卵管炎癥、PCOS、扳機日EMT及促排卵方案,見表4。
將這些因素帶入回歸公式構建風險預測模型:LogitP=1.047×有異位妊娠史(保守手術)+0.801×剖宮產史+1.308×輸卵管炎癥+0.734×PCOS-1.111×卵泡期長方案+0.946×EMT(<8mm)-4.382,對模型行似然比檢驗,回歸方程有統計學意義(χ2=80.396,P<0.001);對模型做判別能力評估,ROC曲線評估曲線下面積為0.746,標準誤=0.027,P<0.001,見圖2。
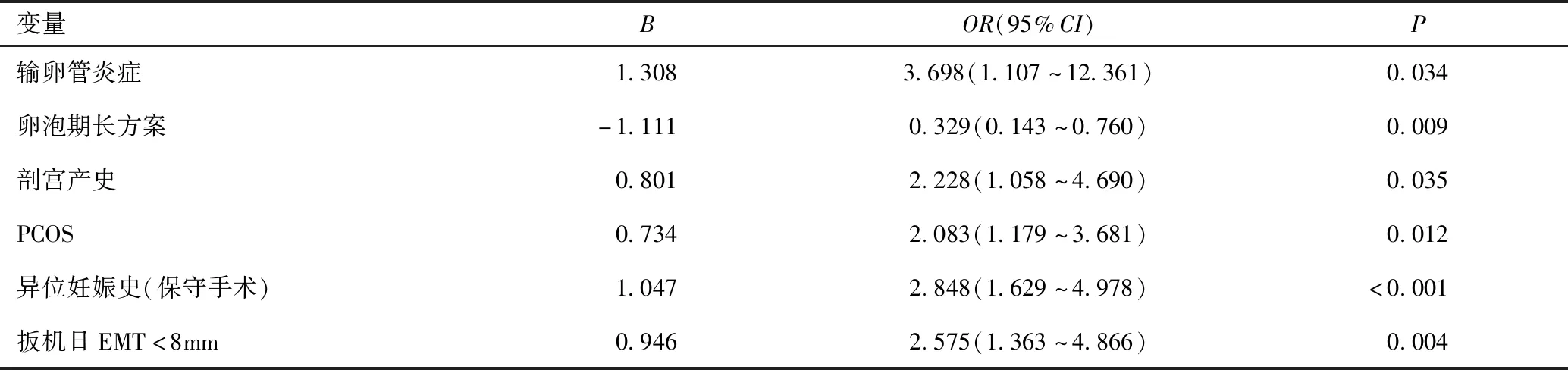
表4 在新鮮周期中對異位妊娠進行多因素Logistic回歸分析Table 4 Multi-factor logistic regression analysis of ectopic pregnancy in fresh cycle
2.2.4 凍融周期中異位妊娠的多因素分析及風險預測模型的構建
凍融周期中與異位妊娠相關的獨立影響因素包括輸卵管炎癥、周期數及內膜準備方案,見表5。
將這些因素帶入回歸公式構建風險預測模型:LogitP=1.114×輸卵管炎癥+0.306×周期數-0.671×內膜準備方案(自然周期)-4.071,對模型行似然比檢驗,回歸方程有統計學意義(χ2=25.368,P=0.005);對模型做判別能力評估,ROC曲線評估曲線下面積為0.674,標準誤=0.031,P<0.001,見圖3。

表5 在凍融周期中對異位妊娠進行多因素Logistic回歸分析Table 5 Multi-factor logistic regression analysis of ectopic pregnancy in FET cycle
3 討論
3.1 ART中輸卵管炎癥及異位妊娠手術史與異位妊娠
1976 年報道了第1例IVF-ET術后異位妊娠的病例,之后有越來越多的IVF-ET術后異位妊娠的報道,異位妊娠是IVF-ET術公認的并發癥[7];且特殊類型的異位妊娠,如卵巢妊娠、宮內合并宮外妊娠、宮頸妊娠等,在ART術后也大大增加[8-10]。1989年就有研究指出,在胚胎移植進入宮腔的過程中,由于推力的作用,44%的胚胎進入輸卵管,如果輸卵管功能受損則無法將胚胎送回宮腔而導致輸卵管妊娠[7]。國內有研究指出,有過異位妊娠史的女性在IVF/ICSI-ET治療結局中更容易再發異位妊娠,而異位妊娠保守手術治療與輸卵管切除手術治療對IVF/ICSI-ET術后妊娠再發異位妊娠的幾率無差別[11]。Jacob等[12]的一項大樣本研究中回顧性分析了既往婦科手術史對異位妊娠的影響,發現既往異位妊娠及生殖器手術與異位妊娠密切相關,這些對盆腔的操作均可能導致盆腔炎癥,從而影響輸卵管的運輸功能。一項回顧性研究指出,輸卵管性不孕癥與異位妊娠密切相關,該研究指出,既往有過異位妊娠史再次異位妊娠風險增加,但未說明既往異位妊娠是否切除輸卵管[13]。本研究顯示,既往異位妊娠保守手術治療后再次異位妊娠的風險增加,而異位妊娠后切除輸卵管則未增加異位妊娠的發生率;但在凍融周期中,有異位妊娠史(保守手術)不再是異位妊娠的獨立影響因素,可能的原因是凍融周期中激素幾乎無超生理水平,子宮內膜容受性較新鮮周期好。目前,切除輸卵管后對卵巢儲備的影響存在爭議,Noventa等[14]對29篇關于輸卵管切除后對ART妊娠結局及卵巢儲備影響的文章進行分析指出,對于輸卵管疾病,以單側輸卵管切除術為基礎的手術方式是安全的,不會對卵巢儲備功能及卵巢控制性促排卵反應產生負面影響,而對妊娠率有積極的影響。
3.2 ART中子宮內膜容受性及促排卵方案與異位妊娠
良好的子宮內膜容受性是胚胎正常著床的關鍵,EMT是評判子宮內膜容受性的最佳指標。本研究顯示,EMT偏薄(<8mm)患者異位妊娠風險增加了1.671倍(95%CI:1.053~2.650),而EMT偏厚(≥13mm)是異位妊娠的保護因素。在一項病例對照研究中指出,與EMT<8mm相比,EMT在8~12mm之間并不會增加宮內臨床妊娠率,然而,EMT>12mm是對異位妊娠的強大保護因素[3],與本研究結果存在一致性。一項前瞻性研究表明,EMT預測宮內妊娠的最佳截斷值為10mm,其靈敏度和特異度分別為93.6%和34.5%[15]。Liu等[16]的一項研究指出,與EMT≥14mm相比,內膜越薄,異位妊娠的風險越高,該研究提到內膜偏薄導致較高異位妊娠率的原因可能與氧分壓的差異有關,偏薄的EMT意味著植入的胚胎將更接近基底子宮內膜層的螺旋動脈,因此由于活性氧的產生,胚胎將暴露在更高的氧濃度中,較高的氧濃度會抑制胚胎的生長,而輸卵管內氧濃度較低,因此導致胚胎進入輸卵管內種植,從而發生異位妊娠。本研究中剖宮產手術史是新鮮周期中異位妊娠的危險因素,可能的原因是剖宮產術后導致切口憩室形成,降低了子宮內膜容受性,且有研究發現與無瘢痕子宮相比,瘢痕子宮血管化明顯減少,白細胞浸潤減少和子宮內膜成熟延遲,這表明剖宮產后子宮內膜容受性受損[17]。盧紅瓊等[18]研究了自然妊娠中200例異位妊娠患者潛在的發病相關因素指出,分娩方式是影響異位妊娠的相關因素,異位妊娠組的既往剖宮產率接近宮內妊娠組的2倍。有研究指出,對于新鮮周期中EMT較薄的女性,凍融周期中額外的E2刺激可能有助于子宮內膜的充分發育[19]。本研究單獨分析了凍融周期中異位妊娠的相關因素顯示,單因素分析中EMT<8mm是異位妊娠的危險因素,但在多因素分析調整混雜因素后,EMT不是異位妊娠的獨立影響因素,原因可能是凍融周期中激素替代治療在一定程度上增加了EMT,因此凍融周期中整體的EMT較新鮮周期厚;而本研究凍融周期中自然周期內膜準備方案是異位妊娠的保護因素,可能的原因在于行自然周期的人群本身內膜容受性較行激素替代周期好。在本生殖中心,通常對既往有規律排卵及子宮內膜生長良好者才納入自然周期,而對自然周期失敗、有排卵障礙者,或者既往有規律排卵但EMT偏薄的患者納入激素替代組。本研究顯示,新鮮周期中卵泡期長方案是異位妊娠的保護因素。有研究指出,在卵巢儲備功能下降的年輕患者中,早卵泡期長方案較拮抗劑方案EMT厚,提示其可提高子宮內膜容受性[20]。另有一項研究指出,在PCOS患者中卵泡期長方案較拮抗劑方案及黃體期長方案EMT顯著增厚,臨床妊娠率增加[21]。還有一項研究比較了卵泡期長方案與黃體期長效長方案及短效長方案臨床結局,顯示卵泡期長方案有更高的胚胎著床率及臨床妊娠率;提示卵泡期長方案可能改善了子宮內膜容受性,幫助胚胎著床,但3種促排卵方案的異位妊娠率及流產率無明顯差異[22]。本文為病例對照研究,即由果推因,在調整了其他因素的情況下得出卵泡期長方案是異位妊娠的保護因素,提示卵泡期長方案可能改善了患者子宮內膜容受性及盆腔微環境。但本研究樣本量有限,尚需更大樣本量的隨訪研究加以證實。
3.3 ART中PCOS與異位妊娠
目前關于PCOS與ART后異位妊娠的關系尚不明確。有研究報道PCOS患者ART治療后異位妊娠的發生率從0~10%不等[2]。一項研究分析了PCOS與異位妊娠的關系發現,對非PCOS患者,扳機日高E2水平會增加異位妊娠的風險;而對PCOS患者,較低的E2水平就會增加異位妊娠的風險;可能的解釋是患有PCOS者對雌激素作用更敏感,對超生理E2水平有較低的閾值,并且在該研究中發現PCOS僅在新鮮周期中增加異位妊娠的發生風險[2]。E2可以調節輸卵管的生理過程,這些生理過程包括纖毛擺動頻率、輸卵管蛋白分泌和胚胎運動。高E2水平可以促進宮頸向宮底方向蠕動,而孕激素則是不同的效應[2,23]。本研究在調整了混雜因素后發現,PCOS在新鮮周期中是異位妊娠的獨立危險因素,而在凍融周期中無顯著性意義。
3.4 ART中移植胚胎類型與異位妊娠
本研究中未發現胚胎類型與異位妊娠之間存在相關性。Smith等[1]研究了13 654例新鮮周期妊娠,比較囊胚移植和卵裂期胚胎移植后的異位妊娠風險,表明卵裂期胚胎移植的異位妊娠風險與囊胚移植相比無差異。與之相反,Fang等[4]發現凍囊胚移植比卵裂期凍融胚胎移植及新鮮周期胚胎移植的異位妊娠率低。囊胚移植結局優于卵裂期胚胎移植,這既是因為它與自然周期的妊娠生理相似,也是因為囊胚具有更高的植入潛力[24]。目前研究的結論存在矛盾,因此囊胚移植作為異位妊娠的保護因素仍然需要進一步的研究來論證。
綜上所述,行ART助孕的患者相對自然妊娠而言更復雜,不僅包括自身的不孕因素,還有ART助孕過程中各種因素的影響。不孕患者妊娠很寶貴,如何最大限度地降低不良妊娠率及增加活產率是醫生和患者的共同目標。本研究發現輸卵管炎癥、異位妊娠保守手術史、EMT薄(<8mm)及治療周期數目越多的患者行ART治療時異位妊娠發生風險增加,卵泡期長方案可能改善子宮內膜容受性,降低異位妊娠的發生風險,PCOS對異位妊娠的影響在新鮮周期中更顯著,其可為臨床工作帶來一定的參考價值,但仍需要多中心前瞻性隨機對照研究進一步證實。

