金花茶葉皂苷對α-淀粉酶抑制機制及效果
藍小河,吳雪輝*,陳嘉慧,陳雪梅,黃永芳,謝克娜
1. 華南農業大學食品學院(廣州 510642);2. 佛山市林業科學研究所(佛山 528000);3. 華南農業大學 林學與風景園林學院(廣州 510642)
金花茶是山茶科山茶屬植物,是藥食兩用植物,在我國廣西、云南等地分布,有很高的藥用價值[1]。由于金花茶不同部位所含有的主要化學成分不同,其藥理活性也不同,而金花茶葉中主要含有皂苷、黃酮和多酚等活性物質,具有良好的降血糖作用[2-3]。蘇琳等[4]研究發現,金花茶葉皂苷能調節糖代謝,降低生物體的血糖水平。
皂苷是類固醇或三萜天然糖苷類重要活性成分,廣泛存在于人參、三七、黃芪等多種中藥材中[5],可以通過抑制口腔和腸道中α-淀粉酶活性,從而減少碳水化合物的分解和消化,降低生物體的血糖水平,是天然的α-淀粉酶抑制劑[6]。包瑞敏等[7]研究顯示黃精總皂苷對α-淀粉酶抑制率達82%,高于糖尿病臨床使用的酶抑制劑阿卡波糖,是良好的α-淀粉酶抑制劑。Kamal等[8]通過研究發現摩洛哥堅果皂苷提取物與阿卡波糖相比,具有更好的α-淀粉酶抑制活性,對肝臟的損害更小。
目前,對于皂苷的α-淀粉酶抑制活性的研究主要集中于三七、遠志等中藥皂苷[9],而關于金花茶葉皂苷對α-淀粉酶抑制作用的研究鮮見報道,因而該研究以金花茶葉皂苷為原料,探究其對α-淀粉酶的抑制機制及效果,以期為金花茶葉皂苷作為天然α-淀粉酶抑制劑以及金花茶葉資源的開發利用提供一定參考。
1 材料與方法
1.1 材料與儀器
金花茶葉(廣東省佛山市林業科學研究所金花茶示范林);α-淀粉酶(美國Sigma-Aldrich公司);乙醇(分析純,天津市富宇精細化工有限公司);可溶性淀粉(天津市科密歐化學試劑有限公司);3, 5-二硝基水楊酸(純度≥98%,國藥集團化學試劑有限公司)。
DK-8D型電熱恒溫水浴鍋(上海森信實驗儀器有限公司);UV-5200型紫外可見分光光度計(上海元析儀器有限公司)。
1.2 試驗方法
1.2.1 金花茶葉皂苷樣品制備
選取無病蟲害,無腐爛、枯萎的金花茶葉,于50℃烘干、粉碎,采用60%乙醇溶液提取皂苷,粗提液經LX-213大孔樹脂和HP-20大孔樹脂純化分離,蒸發濃縮后干燥得到金花茶葉皂苷樣品[10]。
1.2.2 金花茶葉皂苷對α-淀粉酶的抑制試驗
參考范銘[11]的方法,取已配制成一定質量濃度的金花茶葉皂苷溶液、質量濃度為0.5 mg/mL的α-淀粉酶溶液以及緩沖溶液各0.5 mL混合均勻,于37 ℃中恒溫水浴10 min后,加入0.5 mL的1%可溶性淀粉溶液繼續水浴10 min,最后加0.5 mL的3, 5-二硝基水楊酸顯色劑在沸水浴中加熱10 min,冷卻并稀釋一定倍數,置于540 nm處測定吸光度。以緩沖溶液代替α-淀粉酶溶液作為試驗空白組、代替皂苷溶液作為對照組、代替皂苷溶液和α-淀粉酶溶液2種溶液作為背景組,按式(1)計算α-淀粉酶的抑制率。

式中:A為試驗組吸光度;B為試驗空白組吸光度;C為對照組吸光度;D為背景組吸光度。
1.2.3 金花茶葉皂苷質量濃度對α-淀粉酶活性的影響
固定金花茶葉皂苷溶液與α-淀粉酶溶液的反應時間10 min、反應pH 7.0,測定不同質量濃度的皂苷溶液與α-淀粉酶溶液反應后溶液的吸光度,計算抑制率并繪制抑制效果曲線。
1.2.4 金花茶葉皂苷與α-淀粉酶反應pH對α-淀粉酶活性的影響
固定金花茶葉皂苷溶液質量濃度0.5 mg/mL、與α-淀粉酶溶液反應時間10 min,分別測定金花茶葉皂苷溶液與α-淀粉酶溶液在pH為6.0,6.5,7.0,7.5和8.0條件下反應后溶液的吸光度,計算抑制率并繪制抑制效果曲線。
1.2.5 金花茶葉皂苷與α-淀粉酶反應時間對α-淀粉酶活性的影響
固定金花茶葉皂苷溶液質量濃度0.5 mg/mL、反應pH 7.0,分別測定金花茶葉皂苷溶液與α-淀粉酶溶液在反應時間為0,5,10,15和20 min條件下反應后溶液的吸光度,計算抑制率并繪制抑制效果曲線。
1.2.6 金花茶葉皂苷對α-淀粉酶抑制類型的研究
金花茶葉皂苷溶液質量濃度設置為0,0.5和1.0 mg/mL,以1%可溶性淀粉溶液為底物,分別與0.3,0.4,0.5,0.6和0.7 mg/mL的α-淀粉酶溶液反應10 min,測定反應體系的吸光度變化,以酶質量濃度對反應速率作圖。不可逆抑制的速率直線不通過坐標原點,不加抑制劑和可逆性抑制的速率直線均通過坐標原點,且可逆性抑制的速率直線斜率比不加抑制劑的直線斜率小,確定金花茶葉皂苷對α-淀粉酶的抑制類型為可逆或不可逆。
為了進一步確定金花茶葉皂苷對α-淀粉酶的具體抑制類型,金花茶葉皂苷溶液質量濃度設置為0,0.5和1.0 mg/mL,分別與0.5%,0.75%,1%,1.25%和1.5%的可溶性淀粉溶液反應,測定反應體系的吸光度變化,作雙倒數圖。從雙倒數圖中的直線相交于x軸或y軸可以判斷其屬于可逆的非競爭性或競爭性抑制,如直線均不相交則為反競爭性抑制,確定金花茶葉皂苷溶液對α-淀粉酶溶液的具體抑制類型[12]。
1.3 數據統計及分析
所有試驗重復3次,試驗數據均以(x±s)表示,使用Origin 2019軟件作圖,使用Excel和SPSS軟件進行數據分析及處理。
2 結果與分析
2.1 不同金花茶葉皂苷質量濃度對α-淀粉酶活性影響
不同金花茶葉皂苷溶液質量濃度對α-淀粉酶活性影響如圖1所示。由圖1可知,金花茶葉皂苷對α-淀粉酶具有抑制作用,且皂苷溶液質量濃度與α-淀粉酶抑制率呈一定劑量依賴關系。當金花茶葉皂苷質量濃度從0.5 mg/mL增加到5 mg/mL時,α-淀粉酶的抑制率上升較快;超過5 mg/mL后,隨著皂苷質量濃度的增加,α-淀粉酶的抑制率增加減緩;皂苷質量濃度為8 mg/mL時,α-淀粉酶的抑制率達到54.69%,IC50值為7.974 mg/mL。與徐艷陽等[13]研究的黑果腺肋花楸多酚溶液對α-淀粉酶的抑制率隨多酚溶液質量濃度變化趨勢相似。

圖1 金花茶葉皂苷質量濃度對α-淀粉酶抑制作用的影響
2.2 金花茶葉皂苷和α-淀粉酶反應pH對α-淀粉酶活性大小影響
不同反應pH對α-淀粉酶抑制率的影響如圖2所示。金花茶葉皂苷溶液對α-淀粉酶溶液的抑制率隨著pH的增加先升高后下降。當pH為7.0時,其對α-淀粉酶的抑制率達到最大,此時皂苷對α-淀粉酶的抑制效果最佳,pH繼續升高,金花茶葉皂苷對α-淀粉酶的抑制率逐漸減小。α-淀粉酶在人體腸道中水解碳水化合物,將其分解成適合吸收的單糖,而金花茶葉皂苷抑制α-淀粉酶效果最好時的pH為7.0,與腸道的pH接近[14],因此可認為金花茶葉皂苷在人體內能夠較好地發揮其對α-淀粉酶的抑制作用。

圖2 不同反應pH對α-淀粉酶抑制作用的影響
2.3 金花茶葉皂苷和α-淀粉酶反應時間對α-淀粉酶活性大小影響
不同反應時間對α-淀粉酶活性影響如圖3所示。由圖3可知,隨著反應時間的延長,金花茶葉皂苷溶液對α-淀粉酶溶液的抑制率先增加后下降。當反應時間為10 min時,皂苷溶液與α-淀粉酶溶液反應較為完全,α-淀粉酶受到最大程度的抑制;反應時間繼續延長,由于皂苷溶液和α-淀粉酶溶液的質量濃度逐漸減小,結合速率降低,皂苷溶液對α-淀粉酶溶液的抑制率逐漸下降[15],因此可認為反應時間為10 min有利于金花茶葉皂苷發揮其對α-淀粉酶的抑制作用。

圖3 不同反應時間對α-淀粉酶抑制作用的影響
2.4 金花茶葉皂苷對α-淀粉酶的抑制類型
圖4為金花茶葉皂苷對α-淀粉酶抑制作用的抑制動力學曲線。如圖4所示,不同皂苷溶液質量濃度的3條直線近似穿過坐標原點,加入皂苷溶液后的速率直線斜率較不加皂苷溶液時低,說明金花茶葉皂苷溶液對α-淀粉酶溶液的抑制類型為可逆性抑制[16]。金花茶葉皂苷與α-淀粉酶通過非共價鍵可逆性結合,從而使α-淀粉酶活性降低或喪失,可以通過透析等方法去除抑制劑后使α-淀粉酶活性得到恢復。
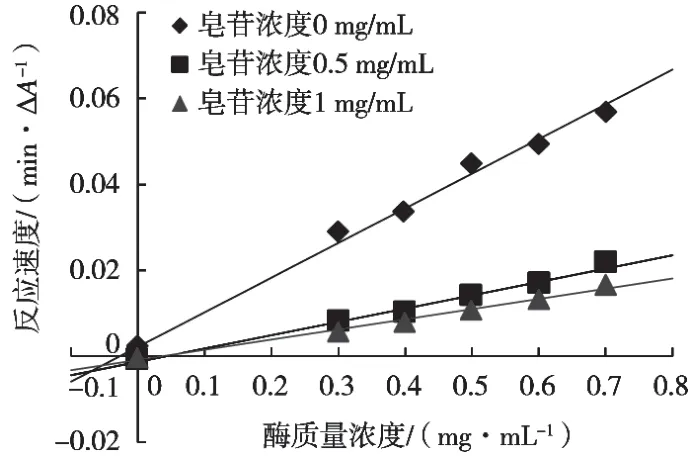
圖4 金花茶葉皂苷對α-淀粉酶抑制動力學曲線
圖5為金花茶葉皂苷對α-淀粉酶抑制作用的雙倒數曲線。由圖5可知,不同皂苷溶液質量濃度的3條直線相交且交點位于x軸,說明金花茶葉皂苷溶液對α-淀粉酶溶液的抑制作用不影響酶促反應的米氏常數,不會改變α-淀粉酶對底物的親和力;加入的皂苷溶液的質量濃度越大,其對應直線的斜率越小,說明金花茶葉皂苷溶液的存在會降低酶促反應的最大反應速度,因此判斷金花茶葉皂苷對α-淀粉酶的抑制類型為可逆的非競爭性抑制[17]。金花茶葉皂苷與α-淀粉酶活性中心以外的基團結合,底物質量濃度不影響皂苷對α-淀粉酶的抑制作用,抑制過程取決于抑制劑的質量濃度,與劉雪輝[18]研究發現武靴藤中皂苷類化合物對α-淀粉酶抑制的作用機制一致。

圖5 金花茶葉皂苷對α-淀粉酶的雙倒數曲線
3 結論
通過金花茶葉皂苷對α-淀粉酶抑制活性的抑制作用條件以及抑制類型進行探究,試驗發現金花茶葉皂苷對α-淀粉酶有一定抑制作用,且抑制效果與皂苷質量濃度呈一定劑量依賴關系,當pH為7.0、反應時間為10 min時,皂苷抑制α-淀粉酶活性的效果最佳,此條件下皂苷質量濃度為8 mg/mL時,金花茶葉皂苷對α-淀粉酶的抑制率可達54.69%,IC50值為7.974 mg/mL,金花茶葉皂苷對α-淀粉酶的抑制類型為可逆的非競爭性抑制,研究結果可為金花茶葉皂苷在α-淀粉酶抑制劑領域的開發利用提供一定參考。

