基于巨噬細胞焦亡探討心脈康方抗動脈粥樣硬化機制
馮文偉,葉健烽,呂洪雪,周智慧,陳麗萍,葉小漢
(廣州中醫藥大學東莞醫院心血管內科,廣東 東莞 523808)
目前,動脈粥樣硬化性心血管疾病(arteriosclerotic cardiovascular disease)的發病率和死亡率仍不斷增長,已經成為全球死亡的首位原因[1-2]。動脈粥樣硬化(atherosclerosis)已被證實是一種慢性炎癥性的動脈血管壁的脂肪病變,是動脈粥樣硬化性心血管疾病發病的重要病理生理基礎[3]。他汀類藥物是治療動脈粥樣硬化的主要藥物,但仍難以有效終止動脈粥樣硬化的進展。
動脈粥樣硬化屬于中醫學“脈痹”范疇。本課題組前期研究提出痰濁、瘀血是導致動脈粥樣硬化的關鍵病理因素,廣東省名中醫葉小漢主任醫師結合嶺南地區特點對鱉甲煎丸進行加減,衍生了心脈康方[4]。心脈康方有化痰消積、軟堅散結的功效,前期臨床研究表明,其能改善冠心病患者的癥狀、炎癥指標及血脂水平[5-6]。前期動物實驗表明,心脈康方能抑制新西蘭兔粥樣硬化斑塊形成,下調白細胞介素6(IL-6)和白細胞介素1β(IL-1β)等炎癥因子和Toll樣受體4(TLR4)的表達[7-8],但其具體分子機制仍不明確。有研究[9]表明,TLR4/核苷酸結合寡聚化結構域樣受體蛋白3(NLRP3)介導的巨噬細胞焦亡在調節動脈粥樣硬化炎癥反應中起重要的作用。本研究旨在進一步探討心脈康方通過抑制TLR4/NLRP3介導巨噬細胞焦亡對動脈粥樣硬化的改善作用,以期為臨床應用提供實驗依據,現將研究結果報道如下。
1 材料與方法
1.1 細胞J774A.1小鼠單核巨噬細胞(來源于BABL/cN小鼠),由廣州吉妮歐生物科技有限公司提供。
1.2 藥物、試劑與儀器心脈康方由醋鱉甲15 g、枳實12 g、三棱10 g、膽南星6 g、醋莪術10 g、生牡蠣30 g、黨參15 g、地龍10 g組成,中藥材由廣州中醫藥大學東莞醫院中藥房提供;阿托伐他汀鈣片(樂普制藥科技有限公司生產,批號:202004105C)。胎牛血清、青霉素和鏈霉素(美國Hyclone公司);DMEM培養基(美國Gibco公司);TLR4過表達質粒(廣州吉妮歐生物科技有限公司);氧化低密度脂蛋白(ox-LDL)試劑(北京協生生物科技有限責任公司);總膽固醇(TC)、甘油三酯(TG)、游離膽固醇(FC)及膽固醇酯(CE)等檢測試劑盒(南京建成生物工程研究所);油紅O染色液和碘化丙啶(PI)染色液(北京索萊寶科技有限公司);乳酸脫氫酶(LDH)檢測試劑盒(沈陽萬類生物科技有限公司);兔抗IL-1β抗體和兔抗GAPDH抗體(美國Abcam公司);兔抗TLR4、NLRP3、含CARD結構域的凋亡相關顆粒樣蛋白(ASC)、白細胞介素18(IL-18)、消皮素D-N端(GSDMD-N)、半胱氨酸蛋白水解酶1(Caspase-1)等抗體和辣根過氧 化 物 酶(HRP)標 記 的 山 羊 抗 兔IgG(H+L)(Affinity,中國);TRIzol(美國Invitrogen公司);逆轉錄和實時定量多聚酶鏈反應(qPCR)試劑盒(TaKaRa,中國)。Multiskan FC酶標儀(美國Thermo Fisher公司);BX53M倒置顯微鏡(日本Olympus公司);CFX96 qPCR儀(美國Bio-Rad公司)。
1.3 含藥血清制備將18只SD大鼠(體質量約200 g)隨機分為空白組、心脈康方組和阿托伐他汀組,每組6只。根據70 kg成人每日口服用藥的臨床推薦劑量,按照成人與大鼠的等效劑量換算系數折算成大鼠灌胃給藥劑量,心脈康方組給予心脈康方9.72 g·kg-1·d-1灌胃,阿托伐他汀組給予1.80 mg·kg-1·d-1[10]灌胃,空白組給予等體積生理鹽水灌胃,每12 h 1次,連續灌胃7 d。末次給藥后1 h,無菌取血制備含藥血清。經56℃滅活30 min后,凍存管分裝,-20℃冰箱保存備用。使用時以DMEM培養液稀釋成所需濃度。
1.4 細胞培養及藥物處理用含有10%胎牛血清的DMEM培養基在37℃、5%CO2的條件下培養J774A.1巨噬細胞。加藥前1 d,以2×105/孔細胞接種到6孔板中,分組:對照組(10%胎牛血清),ox-LDL組(100 μg·mL-1ox-LDL[11]),阿托伐他汀組(100 μg·mL-1ox-LDL+10%阿托伐他汀含藥血清),心脈康方低濃度組(100 μg·mL-1ox-LDL+5%心脈康方含藥血清),心脈康方中濃度組(100 μg·mL-1ox-LDL+10%心脈康方含藥血清),心脈康方高濃度組(100 μg·mL-1ox-LDL+20%心脈康方含藥血清)。阿托伐他汀和不同濃度的心脈康方含藥血清分別與100 μg·mL-1ox-LDL共同處理J774A.1巨噬細胞48 h后,收集細胞沉淀和培養上清液。
繼而進行恢復實驗,實驗分組:對照組(10%胎牛血清)、ox-LDL組(100 μg·mL-1ox-LDL)、心脈康方組(100 μg·mL-1ox-LDL+20%心脈康方含藥血清)、阿托伐他汀組(100 μg·mL-1ox-LDL+10%阿托伐他汀含藥血清)、心脈康方+TLR4組(100 μg·mL-1ox-LDL+20%心脈康方含藥血清+2 μg·mL-1TLR4過表達質粒[12])、阿托伐他汀+TLR4組(100 μg·mL-1ox-LDL+10%阿托伐他汀含藥血清+2 μg·mL-1TLR4過表達質粒)。
1.5 觀察指標與方法
1.5.1 脂質檢測藥物處理方法同“1.4”項。收集細胞沉淀,用超聲波破碎儀裂解細胞,以400g離心5 min后,收集上清液。用TC、TG、FC檢測試劑盒檢測TC、TG、FC以及CE(CE=TC-FC)的水平,評估細胞中脂質累積情況。
1.5.2 qPCR法檢測細胞焦亡通路相關信號分子的基因表達藥物處理方法同“1.4”項。收集細胞沉淀,采用TRIzol提取總RNA,并將總RNA逆轉錄成cDNA。進行qPCR擴增,每個樣品重復3次。qPCR反應程序:熱變性95℃2 min,進入循環,95℃15 s,60℃30 s,反應45個循環后退出,進入溶解曲線60~95℃。采用2-ΔΔCt方法分析目的基因表達量。TLR4、NLRP3、Caspase-1、IL-18、IL-1β及β-actin(為內參)引物序列見表1。

表1 PCR引物序列Table 1 PCR primer sequences
1.5.3 Western Blot法檢測細胞焦亡通路相關信號分子的蛋白表達藥物處理方法同“1.4”項。收集細胞沉淀,加入放射免疫沉淀分析(RIPA)裂解液抽提總蛋白,用二喹啉甲酸(BCA)定量試劑盒測定蛋白濃度。上樣,進行十二烷基硫酸鈉(SDS)-聚丙烯酰胺凝膠電泳(PAGE)分離蛋白并轉移到PVDF膜上,用5%脫脂奶粉封閉液在室溫下封閉1 h后,分別加入以下一抗稀釋液[TLR4(1∶800)、NLRP3(1∶800)、Caspase-1(1∶500),ASC(1∶500)、GSDMD-N(1∶500),IL-18(1∶1 000)、IL-1β(1∶1 000)、GAPDH(1∶1 000)],4℃孵育過夜。TBST洗膜3次,每次5 min,然后與HRP標記的山羊抗兔IgG(H+L)二抗稀釋液(1∶5 000)進行室溫孵育2 h,再用TBST洗膜3次,每次5 min,最后用電化學發光試劑(ECL)進行顯影,沖洗膠片。
1.5.4油紅O染色法觀察巨噬細胞脂質積聚和泡沫化情況藥物處理方法同“1.4”項。藥物處理細胞48 h后,取0.5%油紅O/異丙醇儲存液與蒸餾水按照3∶2比例混勻,靜置10 min后過濾獲得油紅O染液。將不同組別干預處理48 h的細胞加入60%異丙醇浸泡5 min,倒去異丙醇后,換0.5%油紅O溶液浸染15 min,倒去油紅O溶液后,換85%異丙醇溶液清洗3 min至背景無色后換蒸餾水清洗。最后倒置顯微鏡下觀察和拍照。
1.5.5 碘化丙啶(PI)染色法觀察細胞死亡情況藥物處理方法同“1.4”項。藥物處理細胞48 h后,加入1 μg·mL-1Heochst 33342染色液,37℃孵育10 min,再棄去染液后,加入1.0 mL PI染液,4℃避光染色15 min,倒置熒光顯微鏡下觀察和拍照。
1.5.6 微量酶標法檢測細胞上清LDH含量藥物處理方法同“1.4”項。收集細胞培養上清液,用LDH試劑盒(微量酶標法)檢測細胞培養上清液中的LDH水平。
1.6 統計方法采用SPSS 22.0和GraphPad Prism 9.0統計軟件進行數據分析,計量資料以均數±標準差(±s)表示,多組比較采用單因素方差分析以及事后檢驗Tukey HSD法。以P<0.05為差異有統計學意義。
2 結果
2.1 心脈康方含藥血清抑制ox-LDL誘導的巨噬細胞脂質積聚和泡沫化TC、TG、FC以及CE/TC水平升高是脂質累積的重要指標。與對照組比較,ox-LDL組中TC、TG、FC和CE/TC水平明顯升高;而各濃度心脈康方含藥血清和阿托伐他汀抑制了ox-LDL誘導的TC、TG、FC和CE/TC水平升高,且抑制作用呈濃度依賴性。提示心脈康方能抑制ox-LDL誘導的巨噬細胞脂質積聚。見圖1。
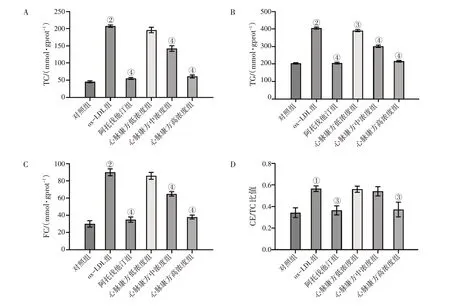
圖1 心脈康方含藥血清對ox-LDL誘導巨噬細胞脂質積聚的影響Figure 1 Effect of Xinmai Kang Formula-containing serum on lipid accumulation in ox-LDL-induced macrophages
巨噬細胞泡沫化是早期動脈粥樣硬化進展的主要標志。油紅O染色結果顯示:對照組大部分細胞沒有脂滴,少數細胞含有少量的脂滴;ox-LDL組細胞體積增大變圓,細胞質中含有大量紅色脂滴;與ox-LDL組相比較,阿托伐他汀組和不同濃度的心脈康方含藥血清組脂滴含量逐漸下降,呈濃度依賴性。提示心脈康方能夠抑制ox-LDL誘導的巨噬細胞泡沫化。見圖2。
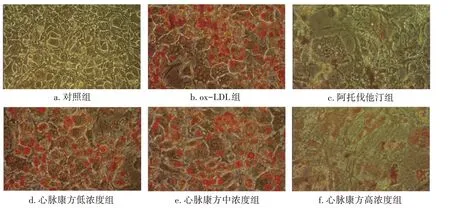
圖2 心脈康方含藥血清對ox-LDL誘導巨噬細胞泡沫化的影響(油紅O染色法)Figure 2 Effect of Xinmai Kang Formula-containing serum on foaming in ox-LDL-induced macrophages(by oil red O staining method)
2.2 心脈康方含藥血清抑制ox-LDL誘導巨噬細胞焦亡與對照組比較,ox-LDL組中IL-1β、IL-18 mRNA和蛋白水平以及GSDMD-N蛋白表達水平顯著上升;與ox-LDL組比較,阿托伐他汀組和不同濃度的心脈康方含藥血清組上述各指標水平均呈下降趨勢,且呈濃度依賴性。具體結果見圖3-A~F。
圖3-G結果顯示,ox-LDL能夠誘導巨噬細胞培養上清液中LDH含量明顯地增高,經阿托伐他汀或者不同濃度的心脈康方含藥血清干預后,這種上升趨勢得到逆轉,且逆轉的程度與心脈康方含藥血清濃度呈正相關性。

圖3 心脈康方含藥血清對ox-LDL誘導巨噬細胞焦亡的影響Figure 3 Effect of Xinmai Kang Formula-containing serum on pyroptosis of ox-LDL-induced macrophages
PI染色結果顯示,與對照組相比較,ox-LDL組中PI陽性細胞數量急劇上升,但在阿托伐他汀或者不同濃度的心脈康方含藥血清的干預下,PI陽性細胞數量呈下降趨勢,且呈濃度依賴性。具體結果見圖4。

圖4 心脈康方含藥血清對ox-LDL誘導巨噬細胞焦亡的影響(PI染色法)Figure 4 Effect of Xinmai Kang Formula-containing serum on pyroptosis of ox-LDL-induced macrophages(by PI staining method)
以上實驗結果提示,心脈康方能夠阻遏ox-LDL誘導的巨噬細胞焦亡。
2.3 心脈康方含藥血清抑制ox-LDL誘導巨噬細胞TLR4/NLRP3信號通路的激活采用qPCR實驗檢測焦亡相關信號通路基因表達。結果顯示,ox-LDL可明顯地上調巨噬細胞中TLR4、NLRP3和Caspase-1 mRNA表達水平,經阿托伐他汀或者不同濃度的心脈康方含藥血清干預后,可明顯逆轉ox-LDL誘導巨噬細胞中TLR4、NLRP3和Caspase-1 mRNA表達水平的升高,且心脈康方含藥血清濃度越高,抑制效果越明顯。具體結果見圖5-A~C。
繼而采用Western Blot實驗檢測焦亡相關信號通路的激活情況。結果顯示,與對照組相比較,ox-LDL組中TLR4、NLRP3、ASC以及Caspase-1的蛋白表達水平顯著上升,在阿托伐他汀或者不同濃度的心脈康方含藥血清的作用下,這種上升趨勢得以逆轉,且逆轉效果與心脈康方含藥血清的濃度呈正相關。具體結果見圖5-D~H。
以上實驗結果提示,心脈康方能夠阻止ox-LDL誘導巨噬細胞中TLR4/NLRP3信號通路的激活。
2.4 TLR4過表達逆轉心脈康方含藥血清對ox-LDL誘導巨噬細胞TLR4/NLRP3信號通路的抑制作用為了探討心脈康方含藥血清是否通過TLR4/NLRP3信號通路來調控巨噬細胞焦亡,本研究首先將TLR4過表達質粒、ox-LDL和心脈康方含藥血清共同處理巨噬細胞48 h,并通過qPCR和Western Blot實驗檢測各組細胞中TLR4、NLRP3、Caspase-1的表達水平。qPCR結果顯示,TLR4過表達能夠顯著地逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞中TLR4、NLRP3、Caspase-1 mRNA水平的降低作用,具體結果見圖6-A~C。
Western Blot實驗結果也顯示,TLR4過表達能夠明顯地逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞中TLR4、NLRP3、ASC和Caspase-1蛋白水平的下調作用,具體結果見圖6-D~H。

圖6 TLR4過表達與心脈康方含藥血清共同作用對ox-LDL誘導巨噬細胞中TLR4/NLRP3信號通路的影響Figure 6 Effect of TLR4 overexpression in combination with Xinmai Kang Formula-containing serum on pyroptosis of ox-LDL-induced macrophages
2.5 TLR4過表達逆轉心脈康方含藥血清對ox-LDL誘導巨噬細胞脂質積聚和泡沫化的抑制作用本研究通過檢測TC、TG、FC水平,及采用油紅O染色觀察各組中脂質積累和泡沫化情況,結果顯示,TLR4過表達能夠顯著地逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞脂質積聚的減少作用,具體結果見圖7。同時,TLR4過表達也能夠明顯地逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞泡沫化的抑制作用,具體結果見圖8。

圖7 TLR4過表達與心脈康方含藥血清共同作用對ox-LDL誘導巨噬細胞脂質積聚的影響Figure 7 Effect of TLR4 overexpression in combination with Xinmai Kang Formula-containing serum on lipid accumulation in ox-LDL-induced macrophages
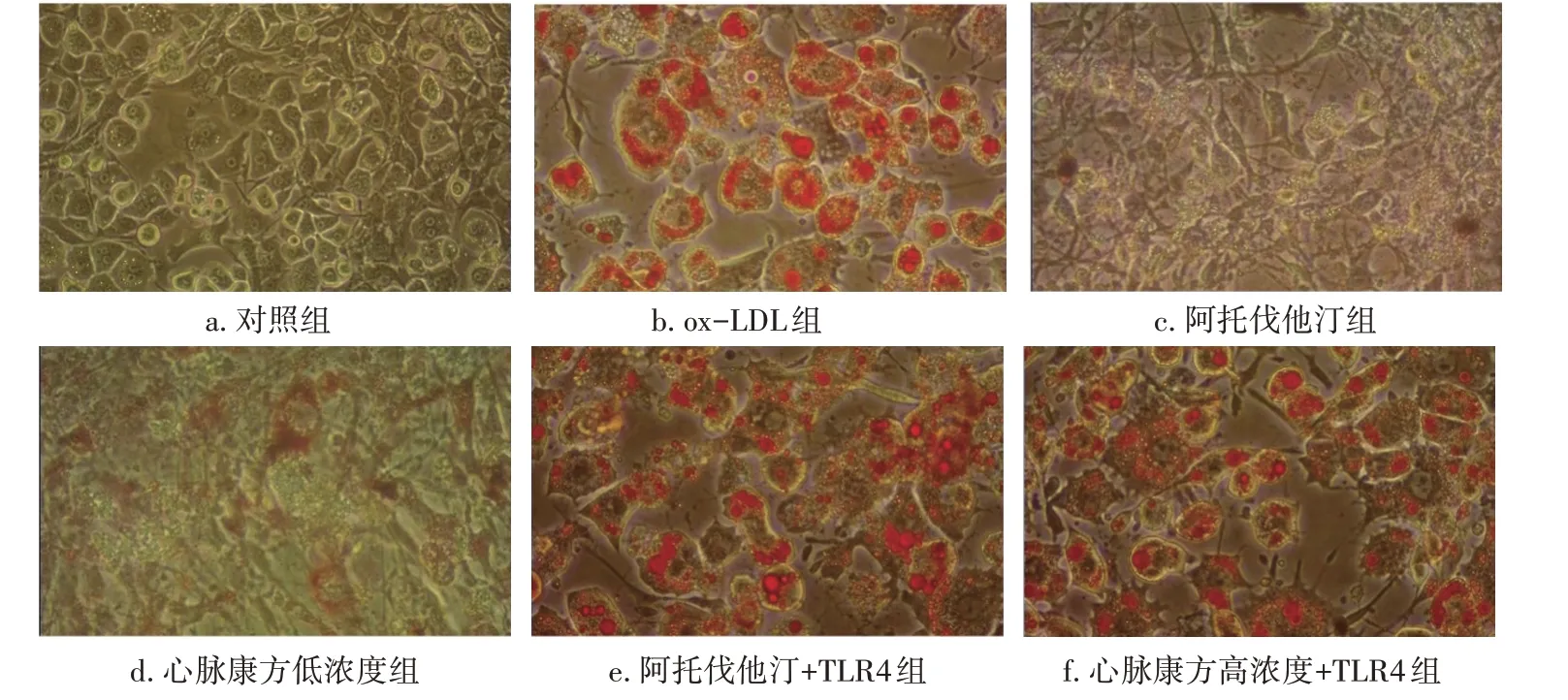
圖8 TLR4過表達與心脈康方含藥血清共同作用對ox-LDL誘導巨噬細胞泡沫化的影響(油紅O染色法)Figure 8 Effect of TLR4 overexpression in combination with Xinmai Kang Formula-containing serum on foaming of ox-LDL-induced macrophages(by Oil Red O staining method)
2.6 TLR4過表達逆轉心脈康方含藥血清對ox-LDL誘導巨噬細胞焦亡的抑制作用采用qPCR和Western Blot法檢測各組中細胞焦亡相關下游基因和蛋白的表達以及采用LDH試劑盒和IP染色檢測各組中細胞焦亡情況,結果顯示,TLR4過表達能夠逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞焦亡相關下游基因IL-1β和IL-18 mRNA表達水平以及IL-1β、IL-18和GSDMD-N蛋白表達水平的下降作用,具體結果見圖9-A~F。TLR4過表達也能夠逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導巨噬細胞釋放LDH水平的減少作用,具體結果見圖9-G。此外,TLR4過表達能夠逆轉阿托伐他汀或者心脈康方含藥血清對ox-LDL誘導PI陽性細胞數量的降低作用,具體結果見圖10。

圖9 TLR4過表達與心脈康方含藥血清共同作用對ox-LDL誘導巨噬細胞焦亡的影響Figure 9 Effect of TLR4 overexpression in combination with Xinmai Kang Formula-containing serum on pyroptosis of ox-LDL-induced macrophages
3 討論
動脈粥樣硬化的病變特點為由于機體內脂質代謝受損引起的動脈壁內膜易損斑塊沉積,斑塊中含有大量炎癥細胞(巨噬細胞、激活的T細胞等),少量平滑肌細胞及較多新生血管。炎癥作為免疫應答的關鍵環節,貫穿動脈粥樣硬化發病的整個過程,影響動脈粥樣硬化的形成和進展[3]。因此,干預炎癥因子逐漸成為防治動脈粥樣硬化的有效手段[13-14]。
心脈康方中:鱉甲滋陰清熱、軟堅散結,為君藥;三棱、莪術行氣破血,牡蠣、地龍軟堅消積,共為臣藥;枳實破氣化痰消積,膽南星化痰,為佐藥;再佐以黨參益氣健脾,使破氣不傷正和傷胃。諸藥合用,共奏化痰消積、軟堅散結之功。現代藥理學研究表明:莪術、三棱能夠抑制炎癥,阻止血栓形成[15];黨參多糖、地龍可調節免疫反應,抑制細胞炎癥因子表達[16-17]。
動脈粥樣硬化的始動環節是血管內皮損傷,脂質積聚,巨噬細胞吞噬脂質后變成巨噬泡沫細胞。本研究結果顯示,ox-LDL能夠誘導巨噬細胞脂質沉積和泡沫化,與文獻報道[18-19]一致。血脂異常為動脈粥樣硬化的主要危險因素,巨噬細胞泡沫化是早期動脈粥樣硬化進展的主要標志。本研究結果顯示,心脈康方含藥血清中、高濃度均能改善TC、TG、FC和CE/TC水平,呈濃度依賴性。油紅O染色結果顯示,心脈康方含藥血清可減少ox-LDL誘導巨噬細胞中紅色脂滴的積聚,隨著藥物濃度的增加,效果更為明顯。表明心脈康方含藥血清能夠抑制ox-LDL誘導的巨噬細胞泡沫化,從而發揮其改善動脈粥樣硬化的作用。
巨噬細胞功能障礙被認為是動脈粥樣硬化發展的關鍵步驟。在動脈粥樣硬化的進展中,病變巨噬細胞的死亡和死細胞的吞噬清除功能缺陷促進了斑塊壞死的形成[20]。據報道,細胞焦亡(pyroptosis)與人類巨噬細胞死亡有關,提示細胞焦亡在動脈粥樣硬化中發揮重要的作用[4]。細胞焦亡又稱細胞炎性壞死,是一種促炎癥性程序性細胞死亡方式,其特點是氣泡狀突起形成,GSDMD在細胞膜形成孔,胞內LDH等物質流出,最終導致細胞腫脹,膜破裂,造成IL-18和IL-1β等炎癥因子的大量釋放。因此,活化的GSDMD蛋白是引起細胞焦亡的關鍵步驟,而檢測LDH可評估細胞滲漏程度。有研究證實,動脈粥樣硬化斑塊中IL-18和IL-1β的表達均升高,而在不穩定斑塊中,其表達更為明顯[21]。本研究結果顯示,模型組中LDH含量,PI陽性細胞數,GSDMD-N、IL-1β和IL-18水平均顯著升高,而心脈康含藥血清可使PI陽性細胞呈下降趨勢,降低GSDMD-N的表達和上清液中LDH含量,以及下調IL-18和IL-1β等炎癥因子的表達,且趨勢呈濃度依賴性,這表明心脈康方含藥血清有效地抑制了巨噬細胞焦亡。
ox-LDL可被巨噬細胞中的TLR-4所識別,進而誘導巨噬細胞中NLRP3、pro-Caspase-1、GSDMD、pro-IL-1β和pro-IL-18的上調,NLRP3受到刺激活化后,與ASC相結合,募集pro-Caspase-1并誘導自我剪切成Caspase-1。Caspase-1的激活介導后續消皮素D(GSDMD)蛋白的活化,導致焦亡的發生[11]。由此可見,TLR4/NLRP3信號通路在細胞焦亡的調控中發揮著重要作用。有學者報道,抑制該通路可減少細胞焦亡及改善動脈粥樣硬化[22-23]。本研究結果顯示,不同濃度的心脈康方含藥血清均可降低ox-LDL誘導巨噬細胞中TLR4、NLRP3、ASC和Caspase-1的表達,并且隨著心脈康方含藥血清濃度的升高其表達量逐漸下降。這提示心脈康方可能通過阻止TLR4/NLRP3信號通路的激活,抑制了ox-LDL誘導巨噬細胞焦亡,從而發揮改善動脈粥樣硬化的作用。為了進一步探討心脈康方含藥血清是否通過TLR4/NLRP3信號通路來調控巨噬細胞焦亡抗動脈粥樣硬化,本研究進行了一系列的細胞恢復實驗。結果表明,TLR4過表達能夠逆轉心脈康方含藥血清對ox-LDL誘導巨噬細胞脂質積聚、泡沫化、焦亡和炎癥反應的抑制作用,進一步證實了心脈康方對巨噬細胞焦亡的抑制作用與TLR4/NLRP3通路有關。
綜上所述,心脈康方可通過調控TLR4/NLRP3信號通路的活化抑制ox-LDL誘導巨噬細胞脂質累積、泡沫化和焦亡,從而起到抗動脈粥樣硬化的作用。

