導向深度學習的化合物性質實驗教學
楊歡 貝偉浩 藍仁敏



【摘要】本文以教學碳酸氫鈉自偶電離為例,論述導向深度學習的化合物性質實驗教學設計的方法,通過分析教學主題內容及教學現狀,找尋教學創新點,合理定位評價目標,根據真實學情整合學科知識,從而解決學生提出的問題,驅動學生開展深度學習。
【關鍵詞】深度學習 實驗課堂 碳酸氫鈉 自偶電離 高中化學教學
【中圖分類號】G63 【文獻標識碼】A
【文章編號】0450-9889(2022)26-0120-05
深度學習是促進學生能力發展、提升學生核心素養的重要方式和可靠路徑。胡久華教授等人在《指向“深度學習”的化學教學實踐改進》一文中指出,化學學科的深度學習需要在教師引領下,學生圍繞具有挑戰性的學習主題,開展以化學實驗為主的多種探究活動,從宏微結合、變化守恒的視角,運用證據推理與模型認知的思維方式,解決綜合復雜問題,獲得結構化的化學核心知識,建立運用化學學科思想解決問題的思路方法,培養學生的創新精神和實踐能力,促進學生核心素養的發展。筆者以教學碳酸氫鈉自偶電離為例,論述通過化學實驗促進學生深度學習的途徑。
一、教學主題內容及教學現狀分析
(一)教學主題內容
碳酸氫鈉自偶電離一課是人教版高中化學選擇性必修1《化學反應原理》第三章《水溶液中的離子反應與平衡》的單元復習課。學生在學完《溶液中的離子平衡》一章后,對溶液中的三大平衡有了初步的認識,但利用相關知識分析和解決實際問題的能力仍有待加強。
碳酸氫鈉是人教版高中化學必修第一冊第二章《海水中的重要元素——鈉和氯》第一節“鈉及其化合物”中的教學內容。教材只簡單介紹了碳酸氫鈉與酸反應、受熱分解這兩個化學性質,并未涉及碳酸氫根在溶液中的電離水解等知識。而利用碳酸氫鹽沉淀金屬離子是工業生產中的常用方法,顯然學生僅掌握課本上講述的碳酸氫鈉的性質無法深入理解這一反應的原理。
本節課通過整合水溶液中的離子平衡與碳酸氫鹽知識,幫助學生學習用平衡原理研究物質性質的方法,同時深入理解碳酸氫鹽的化學性質。
(二)研究現狀
用碳酸氫鹽沉淀金屬離子是工業生產常用的方法,如利用碳酸氫銨沉錳、沉鈰等,這一方法也是高考考查熱點。但碳酸氫鹽可以與金屬離子反應這一知識在教材中并未出現。在目前的教學中,大多教師遇到此類試題往往會就題論題,導致學生對反應原理的理解流于表面,不能舉一反三。有教師設計了相關教學嘗試解決這一問題,如利用碳酸氫鈉與氯化鈣發生反應,檢驗沉淀和上層清液的成分書寫反應方程式,但并沒有對反應原理進行深入解釋;有教師通過探究碳酸氫鈉與氯化鈣反應生成的沉淀,并通過計算分析生成相應產物的可能性,理論上可行但實際上計算對學生而言難度較大,并且采用這種方式對反應原理也缺乏深入解釋。此外,在生物光合作用實驗中,會利用碳酸氫鈉溶液作為二氧化碳的緩沖劑,教師和學生都對這一原理表示不解。由于反應釋放和吸收二氧化碳的量較少,傳統實驗很難直觀觀察到二氧化碳釋放和吸收的過程。為分析二氧化碳緩沖溶液的緩沖原理,有教師設計了數字化解析實驗,借助這一實驗,可以將碳酸氫鈉吸收和釋放二氧化碳的過程具象化。
二、教學思想與創新點
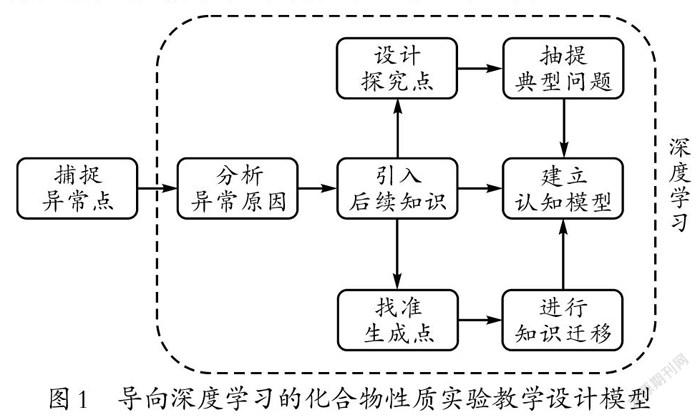
化學實驗是化學探究的載體。貝偉浩老師曾提出由“探究點”“品質點”“異常點”“生成點”構成的化學課堂“四要素設計模式”。從這一模型出發,以碳酸氫鈉與氯化鈣的反應會產生不同現象這一與學生預期不符的異常點為引子引入課程,能夠激發學生的學習興趣。尋找生物學實驗中的化學知識,并將其作為條件變換的探究點,抽象出化學學科本原性的典型實驗問題并據此設計課程,能夠促進學生深度學習。基于此,筆者構建了導向深度學習的化合物性質實驗教學設計模型(如圖1所示)。
三、教學目標
通過解讀課程標準的內容要求、學業要求,結合學情,筆者制訂如下教學目標。
(一)利用平衡移動的知識,分析碳酸氫鈉與氯化鈣的反應,以及碳酸氫鈉溶液作為二氧化碳緩沖劑的反應原理,用方程式表示反應過程,培養“宏觀辨識與微觀探析”“變化觀念與平衡思想”的化學學科核心素養。
(二)設計實驗,探究碳酸氫鈉與氯化鈣反應的產物,證實碳酸氫鈉溶液能夠吸收或釋放二氧化碳氣體,并能作為二氧化碳緩沖劑使用,從而培養學生“科學探究與創新意識”的化學學科核心素養。
(三)根據反應原理,建構水溶液中碳酸氫鈉自偶電離的反應模型,培養“證據推理與模型認知”的化學學科核心素養。
四、評價目標
通過解讀課程標準的內容要求、學業要求,結合學情,筆者制訂了如下評價目標。
(一)通過觀察學生分析與解釋實驗現象的情況,診斷并發展學生宏微結合、證據推理、變化平衡的認知能力。
(二)通過觀察學生討論、設計實驗的課堂表現,診斷并發展學生科學探究的能力。
(三)通過對實驗及平衡原理的歸納總結,推導出碳酸氫根自偶電離的模型,診斷并發展學生證據推理的能力。
五、教學流程
筆者共設計了四個教學環節,具體內容如表1所示。
六、教學實錄
(一)實驗引入
師:可以利用氯化鈣溶液鑒別碳酸鈉與碳酸氫鈉溶液嗎?為什么?
生1:可以。因為氯化鈣與碳酸鈉可以反應生成碳酸鈣沉淀,而氯化鈣與碳酸氫鈉不反應,所以可以利用是否產生白色沉淀來區分碳酸鈉與碳酸氫鈉溶液。
師:真的是這樣嗎?請利用桌面上老師所給藥品與器材進行分組實驗。分別向氯化鈣溶液中滴入碳酸鈉與碳酸氫鈉溶液,然后匯報實驗結果。
(學生活動:學生分組實驗,并匯報實驗結果。)
學生小組1:我們向氯化鈣溶液中滴加碳酸鈉溶液,發現生成了白色沉淀。
學生小組2:我們向氯化鈣溶液中滴加碳酸氫鈉溶液,無明顯現象。
學生小組3:我們的結果跟上一個小組不一樣。向氯化鈣溶液中滴加碳酸氫鈉溶液后,也有白色沉淀生成。
學生小組4:我們的結果跟前面兩個小組都不一樣。向氯化鈣溶液中滴加碳酸氫鈉溶液后,除了有白色沉淀生成,還有氣體生成。
(a)學生小組2? ? (b)學生小組3? ? (c)學生小組4
師:同樣是碳酸氫鈉溶液與氯化鈣溶液反應,為什么三個小組的實驗現象各不相同?
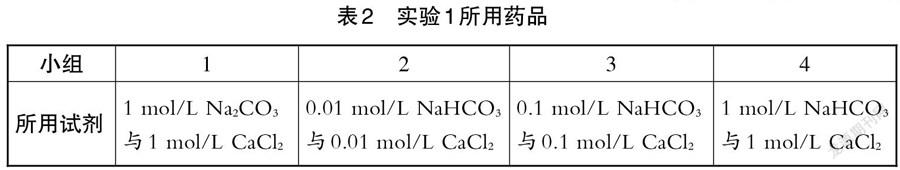
(學生對比之后發現,四個小組中有三個小組所用的溶液濃度不同。四個小組所用藥品信息如表2所示。)
師:為什么溶液濃度不同,實驗現象會有區別?
由此引入第二環節的內容。
(二)理論分析與實驗驗證
師:請根據實驗結果,利用平衡移動原理,分析產生沉淀和氣體的原因。
生1:碳酸氫根在水溶液中會電離生成氫離子與碳酸根,碳酸根與鈣離子結合生成碳酸鈣,觀察到生成白色沉淀;氫離子與另一個碳酸氫根結合,生成碳酸,碳酸進一步分解生成二氧化碳和水,觀察到有氣體生成。沉淀和氣體的生成又能促使碳酸氫根的電離平衡正移,反應從而持續進行。
師:為什么碳酸氫鈉溶液濃度不同時會生成不同的實驗現象呢?
生2:反應物的濃度較小時,電離產生的碳酸根與鈣離子的離子濃度的乘積小于Ksp,所以觀察不到沉淀。氫離子與碳酸氫根結合生成碳酸,碳酸再分解生成二氧化碳和水,只有當溶液中的二氧化碳達到飽和之后,才會有二氧化碳氣體從溶液中逸出,所以只有反應物溶液濃度大的時候才能觀察到有氣體生成。
師:你能設計實驗檢驗生成的氣體確實是二氧化碳嗎?
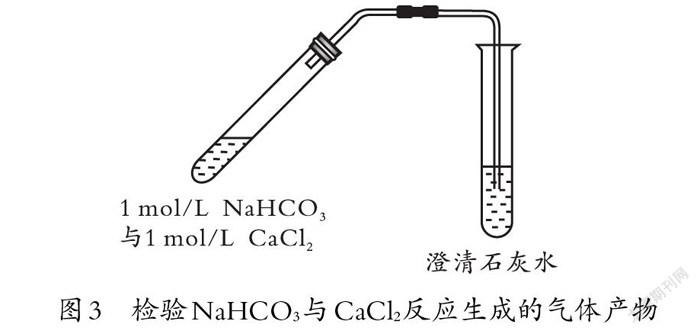
[學生活動:設計出實驗2(如圖3所示),用澄清石灰水檢驗生成的氣體,卻發現澄清石灰水沒有變渾濁。學生分析原因并改進實驗。]
生3:澄清石灰水沒有變渾濁的原因可能是參與反應的溶液濃度不夠大,生成的二氧化碳較少未進入澄清石灰水。可以嘗試增大反應溶液的濃度,產生更多的二氧化碳。
(學生活動:改用飽和碳酸氫鈉溶液和飽和氯化鈣溶液進行實驗3,能夠明顯觀察到澄清石灰水變渾濁,從而證明產生的氣體是二氧化碳,且實現現象不同是受反應物濃度影響。)
師:請根據以上實驗現象,書寫實驗3的離子反應方程式。
(學生活動:書寫方程式2HCO+Ca?HO+CO↑+CaCO↓)
師:這一反應過程,可以看作是碳酸氫根結合了另一個碳酸氫根電離產生的氫離子,鈣離子的加入促進了這一平衡的正移。在沒有鈣離子存在時,這一反應也能發生嗎?
(三)分析碳酸氫鈉作為二氧化碳緩沖劑的原理并實驗驗證
師:在生物學的光合作用實驗中(如圖4所示),常用碳酸氫鈉溶液作為二氧化碳的緩沖劑。請分析碳酸氫鈉溶液吸收或釋放二氧化碳的反應原理,并設計實驗驗證。
生4:推測原理跟碳酸氫鈉和氯化鈣的反應類似,即碳酸氫根電離出的氫離子與另一個碳酸氫根結合,生成碳酸,碳酸再分解得到二氧化碳,即2HCO?HO+CO↑+CO。
生5:按照以上分析,碳酸氫鈉溶液吸收二氧化碳可通過兩個實驗驗證。一個實驗是將二氧化碳通入碳酸氫鈉溶液中,觀察碳酸氫鈉是否能夠吸收二氧化碳氣體,同時測量溶液的pH值是否降低;另一個實驗是檢驗碳酸氫鈉溶液是否能釋放CO2氣體,同時測定溶液的pH值是否升高。
師:利用數字化實驗儀器,可以方便地測量氣體含量和溶液pH值的細微變化。
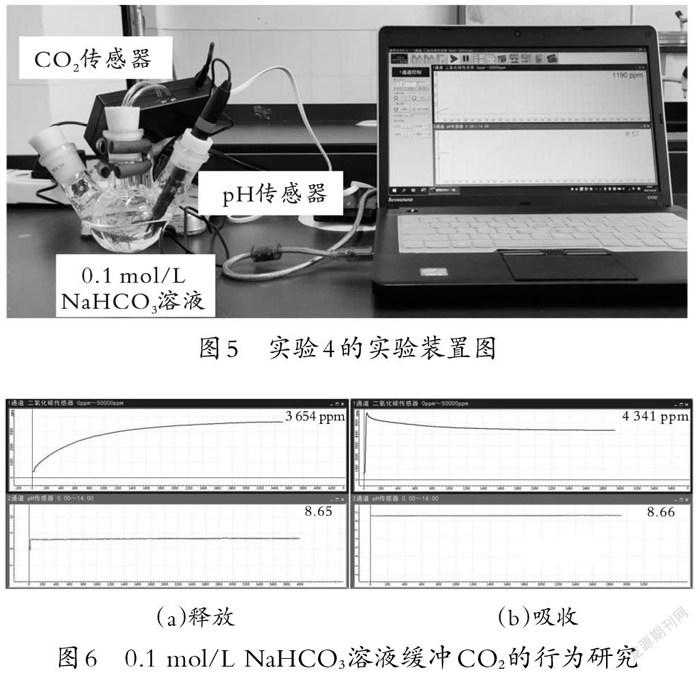
(教師向學生介紹二氧化碳傳感器和pH傳感器,設計實驗4,如圖5所示,實驗結果如圖6所示。實驗結果證明學生的推測正確。)
師:(小結)碳酸氫鈉溶液中,存在碳酸氫根電離出的氫離子與另一個碳酸氫根結合,生成二氧化碳、水和碳酸根的過程。這一過程就是碳酸氫根自偶電離的過程,廣泛存在于碳酸氫鹽溶液中,該反應的K約為10-4,反應程度并不算小。向碳酸氫鈉溶液中加入氯化鈣溶液,生成碳酸鈣沉淀,降低了碳酸氫根的濃度,使自偶電離平衡正移。其他外界條件的改變也會使平衡移動。
師:加熱碳酸氫鈉溶液會發生什么反應?為什么?
生6:會生成二氧化碳和碳酸鈉。加熱促使二氧化碳揮發,使自偶電離平衡正移。
(四)分析工業生產原理
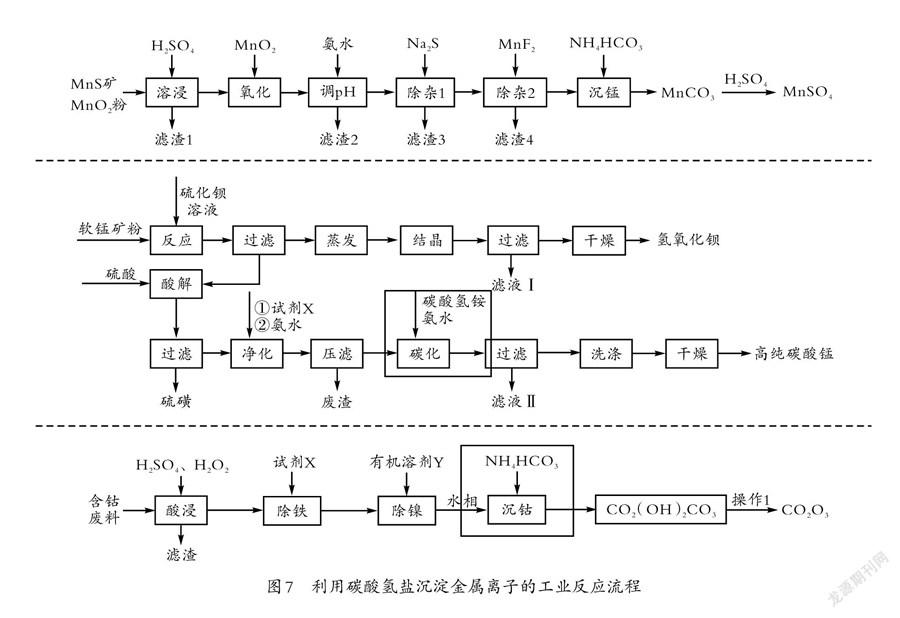
師:請分析工業流程中(如圖7所示)相應步驟的反應原理,寫出離子方程式。
(學生活動:書寫相關步驟的離子方程式。)
學生基本都能正確寫出沉錳的離子方程式:Mn+2HCO=MnCO↓+CO↑+HO以及碳化反應的方程式:Mn+HCO+NH·HO=MnCO↓+NH+HO,學生都能分析出發生了碳酸根與錳離子結合生成碳酸錳沉淀,以及氨水會與碳酸發生中和反應,但不太確定碳酸錳之外的另一產物;沉鈷反應的方程式為2CO+4HCO=CO(OH)CO↓+3CO↑+HO,學生都能分析出有碳酸鈷和二氧化碳生成,但是由于對堿式碳酸鹽的形成原理不夠明確,方程式的書寫正確率不高。
七、教學效果與反思
溶液中的離子平衡問題復雜且抽象,學生不能很好地利用平衡移動原理分析溶液中離子平衡問題。教師可以根據這一真實學情,整合學科知識,結合物質性質與反應原理,解決學生的問題。
實際教學關注真實問題的解決,選取的兩個情境都是學生在學習時真實遇到的,并且還與其他學科關聯,能夠很好地激發學生的學習興趣。
教師通過設計巧妙的實驗,將抽象的原理具象化,能夠幫助學生自主建立自偶電離模型,而不是讓學生被動地接受教師傳遞的信息。在本節課之前,學生不認為碳酸氫鈉能夠與氯化鈣反應生成沉淀,導致不能很好地分析碳酸氫鹽沉淀金屬離子的問題;本節課后,學生能敏銳地識別可以利用碳酸氫根自偶電離模型解決的問題,說明他們較好地內化了相關內容。
此外,在有外加條件干擾時,學生書寫方程式容易出現錯誤,說明他們利用平衡移動的知識解決實際問題的能力仍有待加強。教師后續可以通過引導學生解決更多的真實問題,從而提升他們解決實際問題的能力。
參考文獻
[1]胡久華,羅濱,陳穎.指向“深度學習”的化學教學實踐改進[J].課程·教材·教法,2017(3).
[2]郝緯.探究化工流程題中碳酸氫鹽作沉淀劑的反應原理[J].高中數理化,2020(2).
[3]朱壯麗,邳宏偉,姜序敏,等.二氧化碳緩沖溶液緩沖原理的數字化解析實驗[J].化學教育(中英文),2020(15).
[4]貝偉浩,藍仁敏,張金恒.化學實驗教學“四要素設計模式”研究[J].廣西教育,2021(1).
(責編 劉小瑗)

