多重耐藥菌感染患者清創(chuàng)術后內(nèi)鏡滅菌方法研究
馬久紅,周夢嬌,李賢煌,畢正琴,何榮攀,胡 露,黃 茜
(1. 南昌大學第一附屬醫(yī)院消化內(nèi)鏡中心,江西 南昌 330006; 2. 荊州市第一人民醫(yī)院消化內(nèi)鏡中心,湖北 荊州 434200; 3. 南充市中心醫(yī)院呼吸內(nèi)科,四川 南充 637000)
胰腺包裹性壞死(wall-off necrosis,WON)是急性胰腺炎常見的并發(fā)癥,根據(jù)新亞特蘭大分類將其定義為囊腔含有固體壞死物質、急性胰腺炎病程大于4周且成熟囊壁有胰周積液[1-2]。WON并多重耐藥菌(multidrug-resistant organism, MDRO)感染率達63%,成為急性胰腺炎患者主要死因[3-4]。(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術是將內(nèi)鏡操縱到壞死腔的不同延伸部分,利用活檢鉗、圈套器等器械,達到徹底清除壞死組織碎片的效果,具有病死率低、胰瘺發(fā)生率低等優(yōu)點,已成為WON首選的治療方案[5-7]。MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術使用的副送水內(nèi)鏡除有鉗子管道和送氣/送水管道,增加了副送水管道,實現(xiàn)對術中創(chuàng)面實時沖洗,獲得更清晰的視野,以提高治療效率。然而,副送水管道細小,清洗消毒過程中不能直接刷洗,僅依靠注射器反復注氣注液,清洗消毒難度大,更容易引起MDRO在腔道內(nèi)的殘留。
過去十幾年間,國外研究報道各大醫(yī)院超過25起軟式內(nèi)鏡再處理不合格導致的MDRO感染暴發(fā)[8]。2014年,美國西雅圖一家醫(yī)院內(nèi)鏡逆行胰膽管造影術(endoscopic retrograde cholangiopancreatography, ERCP)后16例患者因感染MDRO死亡。Ross等[9]分析原因發(fā)現(xiàn),現(xiàn)有的軟式內(nèi)鏡再處理指南存在不足,即使嚴格按照廠家指南進行清洗消毒,仍有2%的軟式內(nèi)鏡再處理不合格。因軟式內(nèi)鏡再處理不合格引起MDRO醫(yī)院感染或暴發(fā)的危險因素包括:內(nèi)鏡管腔結構復雜清洗不徹底、存在刮痕刮絲等損傷、消毒滅菌劑使用不規(guī)范等[10-12]。鑒于MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術使用的副送水內(nèi)鏡結構更復雜,國內(nèi)尚缺乏相應的再處理數(shù)據(jù)。本研究采用過氧乙酸浸泡滅菌和環(huán)氧乙烷低溫滅菌兩種方法對用于MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術的副送水內(nèi)鏡進行消毒滅菌,對消毒滅菌后內(nèi)鏡的鉗子管道、送氣/送水管道和副送水管道3個位點進行微生物采樣研究,初步了解不同方法對MDRO WON(經(jīng)皮經(jīng)胃)內(nèi)鏡下清創(chuàng)術內(nèi)鏡的滅菌效果,以期為該類內(nèi)鏡甚至不同用途內(nèi)鏡的消毒滅菌方式提供參考依據(jù)。
1 對象與方法
1.1 研究對象 本研究共納入(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術的GIF-260J帶副送水功能的內(nèi)鏡78條,均為2020年1月—2021年12月某院在胰腺ICU住院且根據(jù)引流物培養(yǎng)結果明確為MDRO感染的WON患者手術使用。
1.2 滅菌方法 A組按照WS 507—2016《軟式內(nèi)鏡清洗消毒技術規(guī)范》[13](以下簡稱《規(guī)范》)對內(nèi)鏡進行預處理、測漏、手工清洗、漂洗、0.225%過氧乙酸浸泡滅菌15 min、無菌水終末漂洗、干燥;B組根據(jù)《規(guī)范》對內(nèi)鏡進行預處理、測漏、手工清洗、漂洗、干燥、環(huán)氧乙烷低溫滅菌。
1.3 分組及采樣方法 根據(jù)不同滅菌方法,采用隨機數(shù)字表法分為A組過氧乙酸浸泡滅菌組和B組環(huán)氧乙烷低溫滅菌組,各39條,分別對內(nèi)鏡的鉗子管道、送氣/送水管道和副送水管道3個位點進行微生物培養(yǎng)和菌落計數(shù)。按照GB15982—2012《醫(yī)院消毒衛(wèi)生標準》[14](以下簡稱《標準》)的要求,嚴格進行無菌操作。使用無菌注射器抽取50 mL硫代硫酸鈉中和劑分別對消毒滅菌后的鉗子管道、送氣/送水管道和副送水管道進行沖洗,遠端部由全量收集器收集。收集完畢2 h內(nèi)送至實驗室進行微生物學監(jiān)測。取洗脫液1 mL接種營養(yǎng)瓊脂平皿,再取1 mL重復上步驟接種于平皿,將剩余48 mL洗脫液用濾膜(0.45 μm)過濾濃縮,將濾膜接種于平皿上,置36℃±1℃溫箱培養(yǎng)48 h后進行菌落計數(shù)。挑出典型單個菌落進行革蘭染色,光學顯微鏡下觀察細菌形態(tài)并分類,采用微生物自動分析系統(tǒng)進行細菌鑒定和藥敏試驗。
1.4 滅菌效果評價 按照《規(guī)范》滅菌后的內(nèi)鏡不能檢出任何微生物,3個管道采樣有任一位點檢測出微生物即為此內(nèi)鏡滅菌不合格。(1)滅菌合格率(%)=滅菌合格條數(shù)/采樣條數(shù)×100%。(2)菌落數(shù):當濾膜法不可計數(shù)時, 菌落總數(shù)(CFU/位點)=平皿的平均菌落數(shù)×50。當濾膜法可計數(shù)時, 菌落總數(shù)(CFU/位點)=平皿總菌落數(shù)+濾膜總菌落數(shù)[15]。
1.5 質量控制
1.5.1 患者一般資料一致性 系統(tǒng)后臺導出每例患者性別、年齡、病因和感染病原菌耐藥情況,比較兩組患者一般資料的一致性。
1.5.2 內(nèi)鏡一致性 本試驗的內(nèi)鏡均為同一批次購入,使用年限和型號均相同(GIF-260J)。試驗前內(nèi)鏡均行微生物學監(jiān)測,菌落計數(shù)為0則納入研究。
1.5.3 工作人員一致性 1名專職清洗消毒護士負責本試驗內(nèi)鏡的清洗消毒工作,1名專職護士負責清洗消毒流程質量控制。2名采樣護士負責本試驗內(nèi)鏡的采樣工作。
2 結果
2.1 兩組患者的一般資料 兩組患者性別、年齡、病因及耐藥菌比較,差異均無統(tǒng)計學意義(P>0.05),見表1。

表1 兩組患者一般資料比較
2.2 不同滅菌方法處理后內(nèi)鏡滅菌合格率比較 A組內(nèi)鏡滅菌合格率為61.54%(24/39),B組內(nèi)鏡滅菌合格率為100%(39/39),兩組比較,差異具有統(tǒng)計學意義(χ2=18.571,P<0.001)。
2.3 不同滅菌方法處理后各位點滅菌合格率比較 A組鉗子管道滅菌合格率為82.05%,送氣/送水管道滅菌合格率為89.74%,副送水管道滅菌合格率為74.36%,B組3個位點滅菌合格率均為100%。鉗子管道和副送水管道2個位點組間滅菌合格率比較,差異均有統(tǒng)計學意義(均P<0.05)。送氣/送水管道兩組內(nèi)鏡滅菌合格率比較,差異無統(tǒng)計學意義(P>0.05)。見表2。其中,A組有3條(7.69%)內(nèi)鏡的3個位點同時檢出細菌,有2條(5.13%)內(nèi)鏡的鉗子管道和副送水管道2個位點同時檢出細菌。

表2 不同滅菌方法處理后內(nèi)鏡各位點滅菌合格率比較 [例(%)]
2.4 不同滅菌方法處理后各位點菌落數(shù)比較 3個位點細菌菌落數(shù)A組和B組間比較,差異均有統(tǒng)計學意義(均P<0.05)。A組內(nèi)鏡過氧乙酸浸泡滅菌后各位點的菌落總數(shù)分布范圍不同,鉗子管道、送氣/送水管道和副送水管道菌落總數(shù)范圍分別為0~6 、0~112、0~23 CFU。見表3。

表3 不同滅菌方法處理后內(nèi)鏡各位點菌落數(shù)比較(CFU)
2.5 過氧乙酸浸泡滅菌后內(nèi)鏡各位點檢出MDRO情況 A組117份標本分離到36株MDRO,其中多重耐藥銅綠假單胞菌占38.89%(14株),多重耐藥肺炎克雷伯菌占27.78%(10株),耐甲氧西林金黃色葡萄球菌占19.44%(7株),多重耐藥鮑曼不動桿菌占5.56%(2株)。見表4。
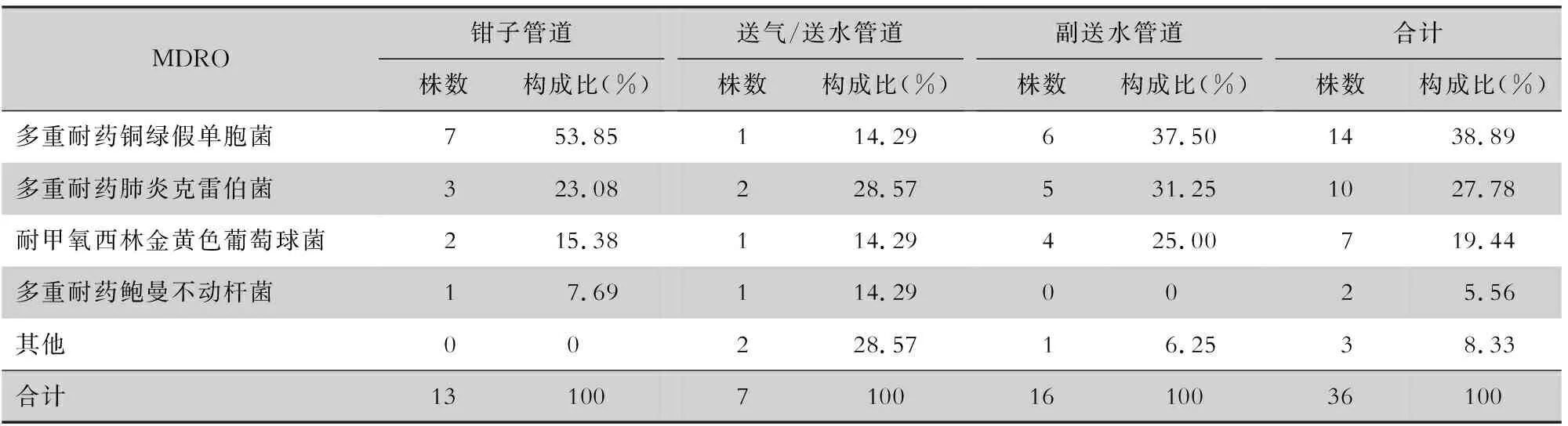
表4 過氧乙酸浸泡滅菌內(nèi)鏡各位點檢出MDRO情況
2.6 不合格內(nèi)鏡轉為環(huán)氧乙烷低溫滅菌后各位點合格情況 本研究A組檢測到15條內(nèi)鏡滅菌不合格,將該15條內(nèi)鏡轉為環(huán)氧乙烷低溫滅菌,結果顯示鉗子管道、送氣/送水管道、副送水管道微生物學監(jiān)測滅菌合格率達100%。
3 討論
隨著內(nèi)鏡下微創(chuàng)診療技術的發(fā)展,軟式內(nèi)鏡應用領域也不斷拓展,不僅用于“看見內(nèi)部”,還用于無菌腔體內(nèi)的治療手術[16]。斯波丁分類規(guī)定,凡接觸無菌組織的軟式內(nèi)鏡均應滅菌[17]。過氧乙酸是近年軟式內(nèi)鏡再處理過程中使用較為廣泛的消毒劑和滅菌劑,理論上能殺滅一切細菌繁殖體,包括分枝桿菌、病毒、真菌及其孢子和絕大多數(shù)細菌芽孢,具有效率高、時間短、周轉快等特點。本研究顯示,MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術內(nèi)鏡經(jīng)過氧乙酸浸泡滅菌方法滅菌合格率為61.54%。從117份標本中分離到36株MDRO,其中多重耐藥銅綠假單胞菌檢出率最高。該結果考慮與內(nèi)鏡管腔結構復雜、易受磨損等原因導致手工清洗合格率低,內(nèi)鏡生物負載大,化學消毒劑浸泡殺菌效果差, 以及MDRO對過氧乙酸產(chǎn)生抗性有關[18-20]。
本研究關注帶副送水功能的內(nèi)鏡,其結構復雜,包括鉗子管道、送氣/送水管道和副送水管道。鉗子管道是內(nèi)鏡器械進出同時吸引空腔內(nèi)容物的管道。送氣/送水管道通過注氣充盈空腔,注水沖洗內(nèi)鏡可視鏡面,保持鏡面干凈清晰。副送水管道通過注入生理鹽水等液體對創(chuàng)面進行沖洗,以保持清晰的治療視野。A組內(nèi)鏡各位點合格率顯示,送氣/送水管道滅菌情況優(yōu)于鉗子管道和副送水管道。各位點細菌鑒定結果顯示,送氣/送水管道細菌檢出株數(shù)少于鉗子管道和副送水管道,可能和送氣/送水管道的功能和設計有關。使用內(nèi)鏡時送氣/送水管道在正壓情況下通過內(nèi)鏡先端部極小的側孔注入滅菌水和空氣,這種設計可以減少污染物進入水氣腔道的概率;但送氣/送水管道細小,清洗刷無法進入管道內(nèi),在床旁預處理和手工清洗時,只能依靠專用清洗接頭和灌流裝置進行沖洗,一旦污染就難以清洗干凈,影響消毒滅菌效果。A組各位點菌落數(shù)結果顯示,1條內(nèi)鏡送氣/送水管道菌落數(shù)高達112 CFU。由此可見,送氣/送水管道菌落計數(shù)差異較大,該結果與國外其他學者研究結果[21]一致。
本組試驗數(shù)據(jù)顯示,過氧乙酸浸泡滅菌后副送水管道的滅菌合格率最低(74.36%),細菌檢出率最高,與劉軍等[22]研究結果一致。帶副送水內(nèi)鏡的副送水管道極細小狹長,內(nèi)徑為1 mm,直接開口于內(nèi)鏡先端部,使用中存在液體反流倒灌的可能,污染風險高。對副送水管道的清洗,目前只能通過手工方法連接專用管道,使用注射器推注水或清洗液進行清洗,難以達到內(nèi)鏡清洗消毒的較高要求。因此,使用過氧乙酸浸泡滅菌方法時需加強對送氣/送水管道和副送水管道污染狀況的微生物學監(jiān)測,以保證滅菌合格,未來也應設計新的清洗方法,降低感染風險。
2013—2014年美國暴發(fā)歷史上最大一次因十二指腸鏡抬鉗器污染引起的MDRO感染事件,其中35例患者被確診,隨后采取環(huán)氧乙烷對十二指腸鏡滅菌才得以終止暴發(fā)[23-24]。Smith等[25]對ERCP術前直腸拭子檢查結果顯示,MDRO感染或化膿性膽管炎患者使用的十二指腸鏡感染傳播風險高,被定義為高風險內(nèi)鏡。對該類高風險內(nèi)鏡采用環(huán)氧乙烷低溫滅菌結果顯示該處理可阻斷MDRO通過十二指腸鏡交叉感染。本研究中環(huán)氧乙烷低溫滅菌對MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術內(nèi)鏡消毒總合格率達100%,3個位點的合格率均為100%,沒有檢出微生物。將15條過氧乙酸滅菌法滅菌不合格的內(nèi)鏡轉為環(huán)氧乙烷低溫滅菌后,微生物檢測滅菌合格率達100%,阻斷了MDRO 通過內(nèi)鏡下清創(chuàng)術的副送水內(nèi)鏡感染傳播的風險。上述結果提示,MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術的內(nèi)鏡可認定為高風險內(nèi)鏡,建議采取環(huán)氧乙烷低溫滅菌方法以保證臨床使用安全,避免感染風險。
MDRO WON(經(jīng)皮/經(jīng)胃)內(nèi)鏡下清創(chuàng)術內(nèi)鏡再處理的質量控制仍是一大挑戰(zhàn),建議消毒滅菌前必須對內(nèi)鏡進行徹底地手工清洗。為防止MDRO在清洗消毒過程中對周圍環(huán)境的污染,應注意手衛(wèi)生以及穿好隔離衣,加強對診療間及周圍環(huán)境的終末消毒,防止交叉感染。對內(nèi)鏡的微生物學監(jiān)測不能僅局限于鉗子管道的監(jiān)測,帶副送水內(nèi)鏡需監(jiān)測副送水管道,以降低感染風險。未來應對臨床常見MDRO的消毒劑和滅菌劑抗性進行研究,為臨床合理選擇消毒滅菌方法提供依據(jù)。
利益沖突:所有作者均聲明不存在利益沖突。

