調和肝脾類中藥治療“腸-肝”軸相關疾病作用機制的研究進展
賈可欣,李 寒,劉閏平
1.北京中醫藥大學中藥學院,北京 100029
2.北京中醫藥大學生命科學學院,北京 100029
現代醫學認為肝臟和胃腸道在解剖學和功能上存在內在聯系,它們之間可通過膽道、門靜脈和體循環等進行雙向交流,“腸-肝”軸體現了肝臟和胃腸道及腸道微生物群落間的相互作用[1-2]。“腸-肝”軸具備相互串擾的生理病理基礎,其穩態主要依賴肝腸間的免疫交流和膽汁酸-腸道微生物軸的穩定,其內涵在于維持腸道微生態平衡、腸道黏膜屏障功能的完整以及肝臟生理功能的正常發揮[2-3]。一方面,腸道屏障構建了機體同外源性異物接觸的第1道“防線”;而肝臟則提供針對逃逸腸黏膜免疫監控的抗原、炎性因子以及內毒素的第2 道“防線”[4]。肝臟受腸道菌群失調、腸屏障功能損傷后所致免疫逃逸的影響,可接觸腸源性的食物抗原和腸道菌群產生的內毒素等,并不可避免地在腸道穩態破壞后發生免疫狀態改變,包括免疫不足引起的慢性感染和癌癥以及免疫過度誘發的無菌性肝臟炎癥[2],可表現為肝纖維化、肝硬化、酒精性脂肪肝病(alcoholic liver disease,ALD)、非酒精性脂肪肝病(nonalcoholic fatty liver disease,NAFLD)和原發性硬化性膽管炎(primary sclerosing cholangitis,PSC)等[5-6]。另一方面,肝臟受損后,免疫細胞激活釋放大量細胞因子并伴隨膽汁酸分泌異常,這些肝源性炎性因子及異常膽汁酸信號傳導不僅對肝臟本身造成二次打擊[7],亦可損傷腸黏膜屏障功能,影響腸道生態和免疫耐受平衡,形成病理性惡性循環,加重潰瘍性結腸炎(ulcerative colitis,UC)、腸易激綜合征(irritable bowel syndrome,IBS)等消化道疾病[4]。因此,正確認識“腸-肝”軸之間的密切關系及探索二者間微妙的雙向平衡和有利于為“腸-肝”軸疾病的防治提供新的診療理念。
“腸-肝”軸學說與中醫以五臟為核心的中醫經典藏象理論中的“肝脾”理論有異源同理之妙。生理狀態下,負責消化吸收及轉運營養物質的胃、腸等器官與主運化,敷布精微,生化輸布氣血之“脾”相類;而“肝”主疏泄,本身即具有調暢脾胃運化、化生排泄膽汁的功能。病理狀態下,作為聯系緊密的臟腑系統,“肝脾”與“腸-肝”軸均存在相互影響,疾病互傳的特點。《金匱要略》云:“見肝之病,知肝傳脾,必先實脾”。脾失健運,胃腸失司,土病及木,肝失調達,則肝脈不暢,致慢性肝病形成;而肝失疏泄,氣血郁滯,濁邪內阻,木郁乘土,又致脾失健運,則脾虛濕蘊,形成類似“腸-肝”軸中發生的病理循環[4]。在治療上,“腸-肝”軸疾病如肝纖維化發展到一定病理階段,常見少食、乏力、腹脹、脅痛及右上腹觸及包塊等,重者可見腹水。中醫辨證多為肝脾失和、肝郁脾虛。治療上當以調和肝脾為要。研究表明,許多腸道和肝臟疾病的發病與“腸-肝”軸功能穩態失衡相關,對于UC 和IBS等具有肝郁脾虛證表現的腸道疾病,治宜疏肝理脾,常以調和肝脾代表方如四逆散、痛瀉要方等隨證化裁,并可取得治療成效[8]。因此,肝脾理論是中醫對“腸-肝”軸認識的重要組成部分,“腸-肝”軸學說也是對中醫“肝脾”相關理論的豐富和延伸[9],調和肝脾類中藥的藥理學作用可能與其對“腸-肝”軸的調控密不可分。
傳統中醫藥以整體觀和辨證論治為基石,以調和肝脾為要進行“肝脾”相關疾病的診治,并在現代消化系統疾病,尤其是與“腸-肝”軸相關疾病的應用中取得了明確治療效果。本文對調和肝脾類中藥通過調節腸道微生態及免疫微環境、保護腸道機械屏障、平衡膽汁酸穩態、調節神經遞質治療“腸-肝”軸相關疾病進行系統性回顧,闡述其藥理作用機制與“腸-肝”軸間的關聯,旨為調和肝脾類中藥的證治應用提供科學理論依據,同時從傳統中醫藥角度為“腸-肝”軸相關疾病拓寬診療思路及藥物選擇。
1 調節腸道微生態及免疫微環境
大量研究表明,NAFLD、ALD、UC、IBS 等疾病與腸道微生物的結構和功能改變有關,腸道共生群落失調也極易誘發包括宿主肝臟在內的免疫系統響應[10],因此調節腸道菌群,維持腸道穩態,一直是治療“腸-肝”軸相關疾病的重要策略。相應的,調和肝脾類中藥可通過調控腸道微生態改善“腸-肝”軸疾病。
1.1 中藥復方
1.1.1 四逆散 四逆散為疏肝理脾之基礎方,功擅透邪解郁、疏肝理脾,為肝脾不和病證之主方。該方君藥柴胡疏肝解郁、臣藥白芍斂陰柔肝,二者適肝體而合肝用;佐藥枳實理氣解郁,伍柴胡升降相承,共使氣血調暢,肝脾同調,以愈四逆,臨床可用于治療NAFLD 等肝臟疾病及UC、IBS 等胃腸疾病。
調肝理脾經典方四逆散治療NAFLD 多通過作用于“腸-肝”軸來改善腸道和肝臟病理變化。Cheng等[11]采用四逆散干預高脂飲食誘導的NAFLD 大鼠,可降低模型動物血清天門冬氨酸氨基轉移酶(aspartate aminotransferase,AST)和丙氨酸氨基轉移酶(alanine aminotransferase,ALT),以及肝臟總膽固醇、三酰甘油、游離脂肪酸和白細胞介素-6(interleukin-6,IL-6)水平,顯著減輕脂質的肝內蓄積及肝臟炎癥。此外,腸道微生物群分析表明,四逆散組與高脂肪飲食組相比,其腸道細菌組成和功能不同,并且表示顫螺菌屬可能是四逆散組小鼠腸道細菌生物標志物;另外四逆散組小鼠體質量、肝臟指數、內臟脂肪指數、血清ALT、肝臟腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)和三酰甘油均有降低,說明四逆散可改善小鼠腸道菌群紊亂和內毒素血癥,減輕肝內脂肪變和炎癥反應,可通過調節“腸-肝”軸的病理變化發揮保護肝損傷作用。Zhu 等[12]研究也證實四逆散可通過抗炎和改變腸道微生物群以改善高脂飲食誘導的NAFLD。
四逆散對UC 和IBS 同樣具有良好緩解作用,可有效抑制腸道炎癥反應,減輕腹瀉、腹部拘急疼痛癥狀。Sun 等[13]研究發現四逆散和甘草甜素干預三硝基苯磺酸誘導的UC 小鼠后,可降低促炎因子如γ 干擾素、IL-12、TNF-α 和IL-17 等,并促進小鼠結腸中抗炎因子IL-10 的產生,提示四逆散可通過調節促炎和抗炎因子的平衡,顯著改善小鼠結腸炎的病變程度。Tang 等[14]運用網絡藥理學分析四逆散潛在活性成分及預測其治療IBS 的作用機制,發現四逆散治療IBS 可能與神經活性配體-受體相互作用、內臟鈣離子信號傳導和HIF-1 信號通路有關。此外,Cai 等[15]基于葡聚糖硫酸鈉誘導慢性實驗性結腸炎小鼠模型,發現四逆散不僅通過調節TANK結合激酶1(TANK binding kinase 1,TBK1)和干擾素調節因子3(interferon regulatory factor 3,IRF3)選擇性抑制干擾素基因刺激蛋白(stimulator of interferon genes,STING)和視黃酸誘導基因蛋白-I(retinoic acid inducible-gene-I,IRG-I)通路介導的I型干擾素反應,還可直接影響信號傳導及轉錄激活因子1(signal transducer and activator of transcription 1,STAT1)和STAT2 的激活來抑制干擾素刺激基因的表達,該研究不僅為I型干擾素反應在UC 中的致病作用提供了新的見解,而且提示四逆散或可通過干擾I型干擾素介導的免疫應答以改善慢性結腸炎。
由此可見,四逆散不僅可有效調節腸道免疫穩態,抑制腸道炎癥反應;還可改善腸道菌群紊亂進一步減輕NAFLD 肝臟脂肪蓄積以及炎癥反應,是通過調節“腸-肝”軸病理機制發揮異病同治特色的代表方劑。
1.1.2 當歸芍藥散 當歸芍藥散為仲景調和肝脾之祖方,具調肝養血、健脾利濕之功效,主治肝脾兩虛、血瘀濕滯之證。方中川芎、當歸、芍藥活血疏肝、益血之虛、柔肝緩急;茯苓、白術、澤瀉益氣運脾、運濕泄濁;合用則肝脾同調,疏瘀血、散蓄水,臨床用治肝纖維化、NAFLD 及功能性消化不良等疾病。
當歸芍藥散可通過調節腸道微生態改善肝損傷。劉禮劍等[16]給予肝硬化患者該方連續治療1 個月后,發現患者肝臟儲備功能及肝功能指標水平(ALT、AST、總膽紅素)顯著改善,其治療總有效率為86.67%(26/30),且患者腸道雙歧桿菌水平升高,大腸桿菌水平降低,因此當歸芍藥散加味可通過調節腸道微生態失衡,修復腸道黏膜屏障以及改善內毒素血癥等多個方面治療肝硬化;此外,當歸芍藥散可顯著抑制刀豆蛋白A誘導的小鼠免疫性肝損傷,這種保護作用與其降低小鼠血清中TNF-α、γ 干擾素、IL-4 及IL-6 等炎性因子表達水平及上調核因子E2 相關因子(nuclear factor erythroid 2-related factor,Nrf2)信號通路有關[17]。
當歸芍藥散在臨床亦可通過改善腸道免疫生態用于治療IBS。回顧性分析研究表明當歸芍藥散可改善腹瀉型IBS(肝郁脾虛型)患者的腹部疼痛、排便異常、急躁易怒、脅肋脹滿、納呆食少、體倦乏力等癥狀,明顯降低患者IBS 病情嚴重程度,治療總有效率達90%[18];同時,網絡藥理學分析結果表明,當歸芍藥散治療IBS 的核心靶點有IL-6、禽肉瘤病毒17 原癌基因、前列腺素內過氧化物合酶2等;主要生物學通路有TNF 信號通路、鈣離子信號通路、5-羥色胺(5-hydroxytryptamine,5-HT)信號通路;分子對接結果表明當歸芍藥散化合物核心活性成分山柰酚、豆甾醇、楊梅酮、喜樹堿等和靶蛋白結合穩定且質量較高,預測了當歸芍藥散治療IBS 的核心活性組分及潛在機制[18]。
此外,當歸芍藥散亦被報道對高脂飲食誘導的NAFLD 大鼠腸黏膜機械屏障具有保護作用,可改善大鼠血清總膽固醇、三酰甘油、ALT、AST 水平和肝臟游離脂肪酸含量,減輕肝臟脂肪蓄積及回結腸黏膜上皮細胞水腫,降低腸道通透性,這種作用或與其升高回腸和結腸組織閉合蛋白(occludin)、閉鎖小帶蛋白-1(zonula occludens protein-1,ZO-1)表達有關[19]。
1.1.3 柔肝化纖顆粒 柔肝化纖顆粒由王振常教授在壯肝逐瘀煎的基礎上化裁而來,可滋陰柔肝、活血化瘀、健脾消積。本方黃精、枸杞滋補肝腎、養陰生津;生牡蠣、鱉甲滋陰潛陽、軟堅散結,澤蘭活血祛瘀,5 藥合用,肝腎同治。黃精、黃芪補肺益氣健脾,黑棗補中益氣養胃,正氣充盛以祛邪外出,并助生血行津。合薏苡仁、虎杖清熱利濕解毒,雞內金健脾消積化瘀,陳皮理氣化痰。全方合用則肝腎同治、實脾治肝、補虛瀉實。
柔肝化纖顆粒可用于治療肝纖維化及肝硬化。陳美岑[20]在研究柔肝化纖顆粒對乙肝肝硬化代償期肝腎陰虛證治療效果時發現,該成方能有效調控腸道菌群的分布,提高雙歧桿菌、乳酸桿菌,而降低腸球菌、腸桿菌,并降低內毒素水平,從而減輕對肝臟的腸源性打擊;另外還可改善此證型患者肝功能、肝纖維化、凝血功能、中醫癥候積分等,并減小門靜脈內徑,具有較好的臨床療效及安全性。同時有研究提示柔肝化纖顆粒能調節成纖維細胞基質金屬蛋白酶抑制酶2/基質金屬蛋白酶2 的值,抑制肝組織激活素A 的表達,提高血清卵泡抑素的水平,從而抑制肝細胞凋亡,促進肝細胞再生,改善肝組織病理以治療大鼠肝纖維化[21-22]。
1.2 單味藥
1.2.1 黃芪 補氣藥黃芪可改善腸道微生態紊亂,研究發現黃芪可以通過與甘草配伍發揮恢復腸道微生物群多樣性、調節菌群豐度和結構、降低炎性小體NOD 樣受體熱蛋白結構域相關蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)等表達的作用,從而改善3,5-二乙氧基羰基-1,4-二氫-2,4,6-三甲基吡啶誘導的小鼠肝臟炎癥和膽汁淤積性肝損傷[23]。另外,也有報道稱其成分黃芪多糖和黃芪皂苷可通過調節肝臟脂質積累、炎癥以及調節腸道微生物群而改善NAFLD,或通過改善肝臟和血清脂質沉積、氧化應激反應、炎癥反應和腸道菌群紊亂以緩解ALD[24-25];其活性組分黃芪甲苷還可通過降低Th17 細胞反應及促進Treg細胞反應以重塑免疫平衡來改善潰瘍形成、炎癥細胞浸潤,從而發揮緩解UC 的藥理作用[26]。
1.2.2 茯苓 研究發現茯苓可通過調節腸道菌群改善肝臟脂肪變性,其成分茯苓多糖能夠通過調節腸道丁酸鹽水平或降低內毒素水平以調節腸道菌群,并影響肝臟脂肪合成或下調炎性通路維持免疫穩態,從而發揮改善高血糖、高脂血癥以及NALFD 肝脂肪變性的作用[27-28];另外,茯苓寡糖也可通過調節腸道微生物群和腸道代謝物以改善高脂飲食誘導的小鼠糖脂代謝紊亂[29];茯苓多糖和茯苓三萜酸還可通過降低變形菌、藍細菌、瘤胃球菌科和螺桿菌科等病原菌的豐度及促進丹毒絲菌科和普雷沃菌科等益生菌豐度以調節腸道微生物群和代謝譜,從而緩解順鉑誘導的腸道損傷[30]。
1.2.3 柴胡 疏肝解郁代表藥物柴胡具有抗炎和抗感染活性,其活性組分柴胡皂苷A 和柴胡皂苷D 可通過調節腸道微生物群結構和多樣性,顯著抑制TNF-α、IL-6和IL-1β等促炎因子mRNA 水平,提高抗炎因子IL-10表達水平,并通過抑制核因子-κB抑制蛋白(inhibitor of nuclear factor-κB,IκB)的降解和磷酸化而抑制核因子-κB(nuclear factor-κB,NFκB)活化,通過增加黏蛋白mRNA 水平保護腸道屏障以改善右旋糖酐硫酸鈉誘導的小鼠UC[31-32]。此外,柴胡石油醚部位可增加慢性溫和不可預知應激模型(chronic unpredictable mild stress,CUMS)大鼠腸道微生物群多樣性,回調微生物中羅斯氏菌屬、毛形桿菌屬、蒼白桿菌屬、普雷沃氏菌屬、貪銅菌屬的相對豐度,通過調節腸道菌群結構發揮療效[33]。
1.2.4 陳皮 理氣健脾藥陳皮可通過調節腸道菌群治療番瀉葉誘導的小鼠腹瀉,降低小鼠排便率及稀便級和腹瀉指數,并改善小鼠淀粉酶和脂肪酶活性,高通量測序技術亦表明陳皮可提高腸道菌群多樣性指數,糾正門及屬水平優勢物種,從而改善小鼠腹瀉[34];此外,佟常青等[35]通過16S rRNA 測序技術證明,陳皮可促進擬桿菌門相關細菌繁殖,抑制厚壁菌門、變形菌門和藍藻菌門部分細菌生長以改善創傷后應激障礙大鼠的腸道菌群環境。
2 保護腸道機械屏障
腸道機械屏障又稱為腸道物理屏障,作為抵御微生物入侵的第1 道防線,在腸道屏障結構中占據中心地位,其由腸道上皮細胞及細胞間連接組成,可防止腸腔中的大分子物質如細菌和毒素等進入到血液循環中,對維持腸道正常形態和功能具有重要意義[36]。近年來一些調和肝脾類經方及中藥保護腸道機械屏障的療效和優勢逐漸得到認可,為治療“腸-肝”軸疾病提供了新的方向和選擇。
2.1 中藥復方
2.1.1 疏肝理脾方 疏肝理脾方源于柴芍六君湯,具有疏肝理氣、健脾化濕之功,可用于治療肝郁脾虛、痰濁濕熱蘊結之證[37]。方中君藥柴胡疏肝理氣;臣藥茯苓益氣健脾;佐藥茜草、白茅根清熱涼血,地龍、鱉甲滋陰潛陽,湘曲、砂仁健脾化濕;使藥白芍養血柔肝,共奏疏肝健脾化濕之功。臨床常用于治療非酒精性脂肪肝炎(nonalcoholic steatohepatitis,NASH)及非特異性UC。
張茜茜等[5]研究發現疏肝理脾方可通過改善NASH 大鼠腸黏膜屏障功能和肝組織病理學變化,抑制“腸-肝”軸病態進展,從而阻止NASH 進一步惡化。基于蛋氨酸及膽堿缺乏飲食誘導的NASH 大鼠模型,研究者通過計算肝組織炎癥活動、脂肪變性及纖維化評分,分析肝臟脂肪變性程度以及腸腔微絨毛長度及寬度的變化,證明疏肝理脾方可修復模型大鼠腸微絨毛形態,并減輕肝細胞脂肪變、氣球樣變及纖維化病變,由此改善NASH 大鼠的肝損傷程度,有效減輕炎癥范圍及纖維化程度[5]。除此之外,江澄[37]發現疏肝理脾方還可改善腸道微絨毛排列形態,修復腸黏膜上皮組織結構,使腸黏膜結構更清晰,并減輕腸上皮線粒體、內質網等細胞器的損傷。
而對于特制飼料及夾尾刺激法誘導的模擬小兒厭食癥的厭食模型大鼠,疏肝理脾方可改善大鼠排泄率和腸碳末推進率,緩解大鼠進食量及體質量的下降程度,組織病理學結果表明,該方給藥后可改善胃及小腸腺體萎縮情況,修復胃腸黏膜結構,保護胃腸道黏膜的完整,從而促進大鼠食欲,增加其攝食量、體質量,并促進模型動物的小腸運動及吸收功能[36]。
2.1.2 健脾活血方 健脾活血方為北京地壇醫院治療ALD 協定處方,有健脾益氣、活血解毒之功。方中黨參、白術、生黃芪健脾益氣化濕,丹參、郁金行氣活血化瘀,葛根、黃芩、黃連重在分消酒蘊濕熱、清腸解毒。全方解毒不傷正,又兼活血健脾,可治療ALD 及慢性萎縮性胃炎等“腸-肝”軸疾病。
臨床病例分析顯示,健脾活血方有助于改善慢性萎縮性胃炎,該方協同復合維生素B 溶液加慶大霉素針劑,對慢性萎縮性胃炎有效率達91.2%(68 例治愈42 例,好轉20 例)。健脾活血方可通過改善微循環,加快血流速度,改善組織營養,促進局部炎癥吸收,恢復和再生萎縮腺體及細胞,促進腸上皮化生的異型增生消退,對胃黏膜、腸上皮化生和異型增生均有不同程度的逆轉作用,同時對幽門螺旋桿菌也有抑制作用[26]。
藥理研究發現,健脾活血方對酒精性肝病小鼠具有良好治療效果,可以降低酒精性肝病小鼠血清AST、ALT,改善肝功能;減輕肝脂肪變性和炎性細胞浸潤,改善肝小葉結構排列形態,保護肝損傷,其治療效果與陽性對照藥谷氨酰胺效果相當[38]。研究人員亦發現,健脾活血方可使小鼠小腸組織形態紊亂狀況減輕、上皮層杯狀細胞和上皮細胞數量減少,并且腸道ZO-1、occludin 蛋白上調,相對于模型組小鼠小腸病理有明顯改善;從而進一步揭示了健脾活血方可能通過“腸-肝”軸機制,改善腸道屏障功能受損,降低血漿內毒素及TNF-α 水平,進而減輕肝損傷來治療酒精性肝病小鼠[38]。
2.2 單味藥
2.2.1 白芍 柔肝養血藥白芍多有助于維持腸道屏障結構及功能。白芍水提液可改善小鼠腸道微生物群的多樣性和增加有益細菌的相對豐度來改善腸道微生物穩態和恢復腸道機械屏障,并能通過IL-23/IL-17 軸抑制炎癥反應以調節免疫狀態來緩解UC[39];白芍提取物還可通過調節腸道微生物群,維持腸道完整性,以及降低Toll 樣受體介導的炎癥通路維持免疫平衡來改善高脂高糖喂養小鼠的體質量增加、肝脂肪變性、葡萄糖耐量和全身炎癥狀況,從而發揮治療小鼠NAFLD 的作用[40];其活性組分白芍總苷也被報道可改善腸缺血再灌注大鼠的腸道黏膜間水腫及充血,其保護機制可能與通過III型受體酪氨酸激酶及干細胞生長因子受體信號通路維持Cajal 間質細胞線粒體的結構和功能穩定性有關。
3 平衡膽汁酸穩態
膽汁酸是膽汁的重要成分,在腸道和肝臟信號級聯中不可或缺,膽汁酸穩態深深影響腸道屏障和肝腸免疫響應[41],其中法尼醇X 受體(foresaid X receptor,FXR)[42]作為核心膽汁酸受體已成為“腸-肝”軸疾病中不可忽視的治療靶點。調和肝脾類中藥可通過調節膽汁酸相關信號通路治療“腸-肝”軸疾病。
3.1 中藥復方
3.1.1 茵陳蒿湯 茵陳蒿湯為傳統醫藥治療黃疸的經典方劑,由張仲景創制,方中君藥茵陳苦寒,清熱利濕,臣藥梔子引濕熱從小便去,佐藥大黃瀉熱通便,導瘀熱從大便而下,共建清熱、利濕、退黃之功。本方可用于治療原發性膽汁性膽管炎(primary biliary cholangitis,PBC)、NAFLD、肝纖維化等疾病。
茵陳蒿湯在臨床常用于治療PBC,臨床病例分析表明,茵陳蒿湯聯合熊去氧膽酸有助于降低患者ALT、AST、堿性磷酸酶水平,并改善皮膚瘙癢、疲乏、脅肋脹痛、食欲減退、口苦等癥狀,提高熊去氧膽酸生化學應答率緩解PBC,這種作用與其升高血清成纖維細胞生長因子19 水平,從而發揮激素樣作用,調節患者膽囊充盈及膽汁酸代謝有關[43]。
3.1.2 柴胡疏肝散 柴胡疏肝散即四逆散加川芎、香附,主治肝氣郁滯諸證。方中君藥柴胡疏肝解郁,臣藥香附、川芎活血行氣止痛,并助柴胡解肝經郁滯;佐藥陳皮、枳殼理氣行滯,芍藥、甘草養血柔肝;使藥甘草調和諸藥,全方共奏疏肝行氣、活血止痛之效。柴胡疏肝散在臨床被廣泛用于治療胃腸及肝膽疾病。
臨床報道柴胡疏肝散可用于治療急性結石性膽囊炎[44],其聯合熊去氧膽酸給藥后療效確切,可減輕患者腹部疼痛狀況,明顯降低患者疼痛分級指數、Mc Gill 疼痛量表評分和目測類比定級法評分,其發揮緩解急性膽囊炎效果或與輔助熊去氧膽酸促進內源性膽汁酸排泄并抑制其重吸收,拮抗疏水膽酸細胞毒作用,保護肝細胞抑制肝臟膽固醇生成,并促進其排泄和轉化,從而溶解膽固醇性結石有關[45];此外,該方對膽汁反流性胃炎具有良好治療效果,可緩解患者心煩不寐、口苦、納差等表現,并改善患者胃動力指標(促胃液素、胃動素等),總有效率達95.74%,可明顯減輕膽汁反流性胃炎患者臨床癥狀[46]。
基礎研究表明,柴胡疏肝散可緩解α-萘異硫氰酸酯誘導的肝內膽汁淤積大鼠肝損傷,降低模型大鼠肝臟病理炎性浸潤和壞死情況,改善肝損傷大鼠的膽汁流量及肝功水平,這種治療效果與柴胡疏肝散調控FXR/Nrf2/抗氧化反應元件信號通路有關[47]。
3.2 單味藥
3.2.1 大黃 研究表明,大黃及其代表活性成分大黃素均可改善急性肝內膽汁淤積性損傷。基于異硫氰酸萘酯誘導的大鼠急性肝內膽汁淤積模型,大黃浸煎液可改善血清ALT、AST、ALP、總膽紅素及總膽汁酸等肝功指標水平并減輕大鼠肝臟病理損傷,這種保護作用與大黃調控大鼠肝組織FXR 及膽汁酸轉運體表達有關[48];另外,多項研究表明,大黃活性組分大黃素對膽汁淤積性肝損傷具有良好療效,通過調控FXR 相關信號通路,調節膽汁酸代謝和脂質代謝,保護肝細胞結構及功能,從而緩解膽源性肝損傷有關[49-51]。
3.2.2 牛黃 傳統中藥牛黃作為一種特殊動物藥,源于動物牛膽囊、膽管或肝管中干燥的膽結石,其主要核心成分膽汁酸在“腸-肝”軸疾病中發揮重要作用。研究發現,牛磺熊去氧膽酸和熊去氧膽酸這2 類代表性膽汁酸成分,可明顯促進大鼠膽汁分泌及總膽汁酸和膽紅素分泌,減小膽固醇濃度,促使游離膽固醇結晶溶解而達到抑制膽固醇型膽結石的作用[52];此外,該藥可影響NAFLD 小鼠肝臟膽汁酸代謝輪廓,牛黃給藥后有效緩解NAFLD 小鼠肝臟脂質累積并能改善其膽汁酸變化異常,這種保肝效果依賴于牛黃修復肝臟膽汁酸合成和轉化途徑,增加結合型膽汁酸含量作用的發揮[53]。
4 調節神經遞質
4.1 中藥復方
4.1.1 逍遙散 逍遙散為四逆散之變方,擅調和肝脾,有疏肝解郁、養血健脾之功。主治肝郁血虛脾弱之證。方中君藥柴胡疏肝解郁、調達肝氣;臣藥當歸養血和血,白芍養血斂陰柔肝;佐藥白術、茯苓健脾化濕,炙甘草補脾益氣、柔肝緩急;薄荷疏肝郁、透肝熱;燒生姜降逆和中、辛散達郁,為佐藥;柴胡為肝經引經藥,又兼使藥之用,共奏調和肝脾之功。逍遙散在臨床廣泛用于消化系統疾病的治療。
現代藥理研究發現,逍遙散能改善胃腸道蠕動以減少有害菌及內毒素的腸道潴留,從而有效保護肝功能,豐富了“以腸治肝”的機制內涵。徐嘉蔚等[54]將逍遙散拆方干預牛血清白蛋白注射誘導的肝硬化模型大鼠,并設立去除健脾藥物組(去白術、茯苓、生姜、甘草),結果表明逍遙散能保護肝功能,同時減輕內毒素血癥,并促進血清胃動素和胃竇及小腸平滑肌細胞胃動素受體的表達,以增強胃腸道運動,相較于原方組別,去除健脾藥物組大鼠胃竇平滑肌胃動素受體表達明顯減少,肝保護作用減弱;表明逍遙散方中健脾藥能通過促進胃腸道蠕動排空,減輕細菌及有害毒素在腸道的潴留,而改善腸源性內毒素對肝臟的打擊,即健脾以調“肝”,通過調節“腸-肝”軸的病理變化以緩解肝纖維化。
4.1.2 痛瀉要方 痛瀉要方擅補脾疏肝、祛濕止瀉,主治肝郁脾虛之痛瀉,方中君藥白術苦溫、補脾燥濕;臣藥白芍柔肝緩急止痛;佐使藥陳皮理氣燥濕醒脾,防風則燥濕以助止瀉,為脾經引經藥,共治痛瀉肝郁脾虛之證。對于現代醫學的UC、IBS 等“痛瀉”之證,臨床常表現為瀉必腹痛、瀉后痛減。中醫認為其多因脾虛肝郁所致,故常用痛瀉要方以調和肝脾;該方治療UC 緩解期肝郁脾虛證效果顯著,而UC 等腸道疾病肝郁脾虛證發病與“腦-腸”軸和“腸-肝”軸假說密切相關[55]。
現代藥理研究表明,痛瀉要方對于5-HT 信號傳導的調節具有顯著作用,通過干預5-HT 和5-HT受體(5-HT receptor,5-HTR)的結合,調節腸道蠕動和分泌,降低腸道敏感性,緩解腸道潰瘍,從而達到腸肝同調效果。研究表明,5-HT 激活有利于增強腸道敏感性,促進腸道的分泌和運動功能,5-HT 可與腸道受體直接結合,通過作用于5-HT1R~5-HT4R 以及5-HT7R 5 種受體,調節腸道分泌和蠕動,痛瀉要方可能通過調節5-HT 信號系統治療肝郁脾虛型UC[56]。痛瀉要方也可抑制5-HT 的分泌,降低血清中5-HT 濃度,抑制胃腸道蠕動[55,57],通過調節腸道內5-HTR 的表達,影響腸道敏感性而改善肝郁脾虛型腸病。任婷婷等[58]、林震群等[59]研究發現痛瀉要方可下調腸黏膜5-HT1R 和5-HT3R的過度表達;并下調腸道5-HT3RmRNA 表達水平,抑制5-HT3R 的活化,從而降低IBS 模型大鼠的結腸高敏感性。另外,對于經乳鼠結腸刺激方法復制的內臟高敏感性大鼠,其腸道5-HT4、5-HT4RmRNA 的表達水平降低,而痛瀉要方可以增強內臟高敏感性大鼠結腸5-HT4R 蛋白表達以降低5-HT的釋放[60],并顯著上調經直腸擴張刺激后大鼠結腸中5-HT4RmRNA 水平,從而降低結腸敏感性[61]。蔣志濱等[62]研究顯示肝郁脾虛型UC 大鼠肝組織5-HT2R 表達上調,但經痛瀉要方干預后大鼠肝內5-HT2R 表達下降,腸道5-HT 水平降低,說明痛瀉要方可能通過抑制肝內5-HT 與5-HTR 的結合而改善結腸炎性癥潰瘍性病變。
5 結語與展望
調和肝脾類中藥通過改善“腸-肝”軸的病理發揮作用,對“腸-肝”軸系統相關疾病肝脾不和證的病理和癥狀治療效果較佳[63]。調和肝脾類中藥改善“腸-肝”軸的作用機制如圖1所示。針對NAFLD、ALD、肝硬化等疾病,調和肝脾類中藥可以通過改善腸道菌群失調,促進胃腸道蠕動,減輕腸黏膜機械屏障損傷,從而抑制腸源性內毒素血癥和肝臟炎癥因子如TNF-α 的釋放,減輕腸源性肝打擊,發揮以腸治肝的功效。而對于UC、IBS 等疾病,調和肝脾類方劑如痛瀉要方等能夠調節5-HT 信號傳導,可以通過抑制肝內炎性因子的釋放以及5-HT與相應5-HTR 的結合,減輕肝源性腸道損傷,抑制腸道炎癥反應,發揮以肝治腸的功效。中醫基于臟腑、五行理論,講究治肝實脾、扶土抑木、疏補相成。而“腸-肝”軸系統則有以腸治肝、以肝治腸之妙,其根本上在于改善腸道屏障功能。另外,健脾方藥還可通過“腦-腸”軸調控腸道菌群和5-HT系統緩解炎癥性腸病的情志激動、焦慮狀態,亦豐富了中醫理論培土以抑木、補土以疏木的內涵[55]。
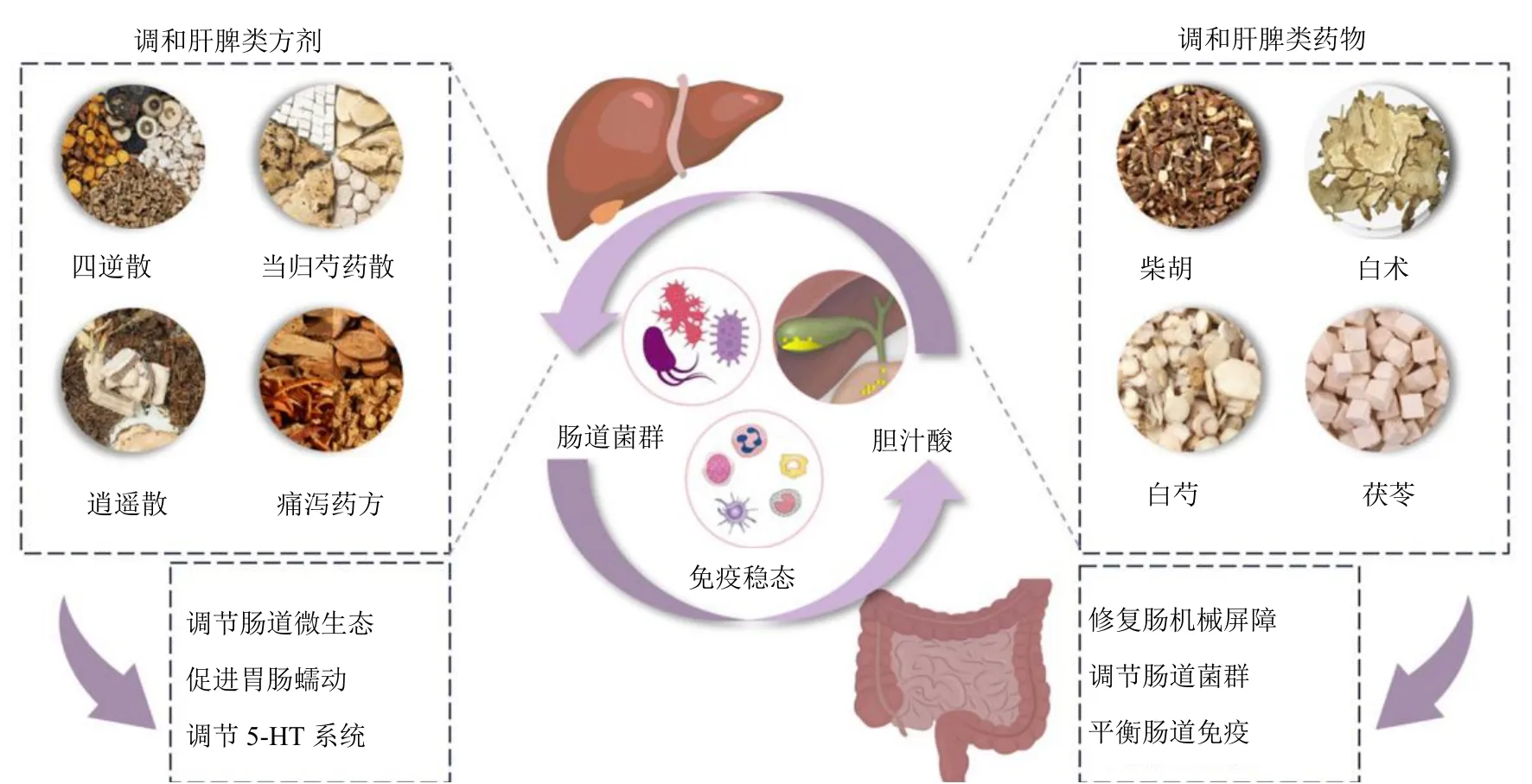
圖1 調和肝脾類中藥改善“腸-肝”軸的作用機制Fig.1 Mechanism of regulating liver and spleen traditional Chinese medicine to improve “gut-liver” axis
而在調和肝脾類單味中藥,出現頻次最高的依次為白芍、白術、柴胡等入肝經和(或)脾經的藥物,見表1。其中,具有改善胃腸道功能障礙從而發揮緩解便秘、UC 及IBS 等胃腸疾病的單味中藥多具有調節腸道菌群、恢復腸道屏障、平衡免疫反應的功能。改善肝臟病變的單味中藥則不僅可直接不僅可直接減輕肝臟脂肪變,也可間接調節腸道菌群結構和水平、抑制炎癥活動,進而通過調節“腸-肝”軸交流機制而“以腸治肝”,減輕肝損傷。如補脾類中藥黃芪側重于調節炎癥反應以恢復腸道屏障和平衡腸道免疫穩態;健脾類中藥茯苓和陳皮更依賴于調節腸道菌群紊亂以維持腸道微生態;補益藥黃芪,調肝類中藥柴胡和白芍則在維持腸道免疫平衡和腸道菌群穩定方面均有良好效果。有趣的是,柴胡、白芍為調和肝脾代表方的基礎藥對,二者補肝之體、適肝之用,共奏調和肝脾之效。因此,調和肝脾類方劑中高頻中藥的藥理作用集中在維持肝臟和(或)腸道的免疫環境及維持腸道微生態平衡,這不僅驗證了調和肝脾類方劑中高頻中藥的潛在藥理作用與調節“腸-肝”軸穩態有關,也為后續“腸-肝”軸疾病的基礎探索和臨床診療提供參考。
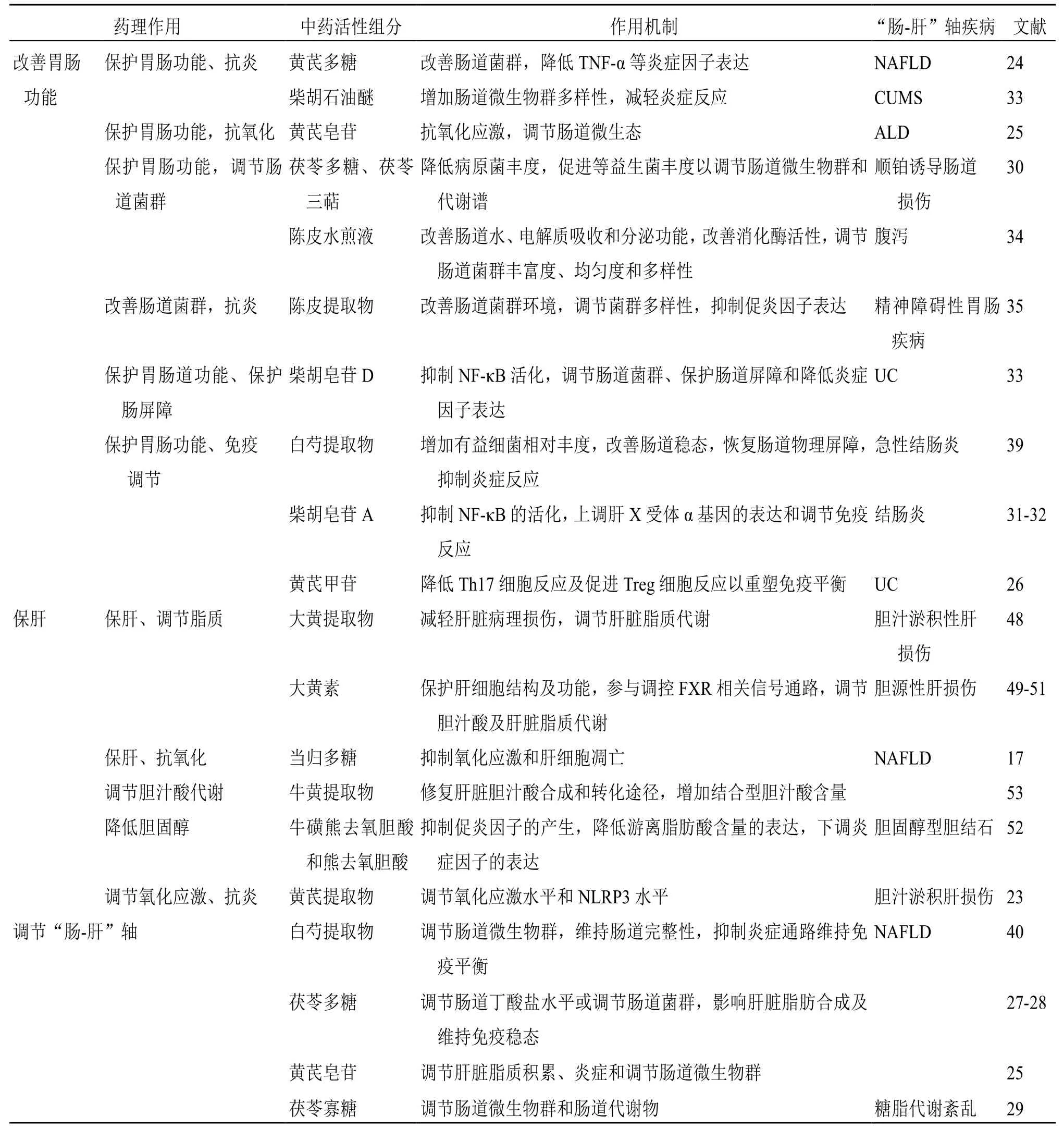
表1 調和肝脾類方中高頻次藥物信息Table 1 Information of high-frequency traditional Chinese medicine in classical formulae of harmonizing liver and spleen
綜上所述,本文對調和肝脾及其代表方劑和中藥參與“腸-肝”軸疾病證治情況及藥理研究進展進行了歸納和合理性闡述,發現調和肝脾類中藥有“以肝治腸”和“以腸治肝”的鮮明特色,這與中醫“肝脾同調,治肝實脾”的理念相契合。闡明調和肝脾類中藥治療功效的科學內涵將為中醫藥診治“腸-肝”軸相關疾病提供思路,同時拓寬臨床治療用藥選擇。
利益沖突所有作者均聲明不存在利益沖突

