大明膠囊治療高脂血癥的網絡藥理學分析及分子對接驗證研究
張越 張卉青 楊提 徐春梅

[關鍵詞]大明膠囊;高脂血癥;網絡藥理學;靶點預測;分子對接
高脂血癥是由于脂肪代謝或轉運異常而導致的血漿中脂質結構紊亂[1]。高脂血癥是心血管疾病發病和病死的主要危險因素。他汀類是血脂異常的首選治療藥物,盡管他汀類藥物治療對心血管事件有積極作用,但患者的依從性往往較差[2]。因此,探索不良反應較低且作用有效的降脂藥物具有重要意義。
中藥治療高脂血癥具有療效確切、毒性相對較低、成本低等優點,因此得到越來越多人的關注。大明膠囊是經國家食品藥品監督管理局批準的具有活血化瘀作用的中成藥。大明膠囊由6味中藥,即大黃、決明子、丹參、陳皮、人參和茯苓組成,對高脂血癥患者有確切療效[3-4]。但由于大明膠囊所含成分復雜,其治療高脂血癥的關鍵活性成分及潛在分子機制至今尚不明確。本研究通過網絡藥理學研究方法,分析大明膠囊治療高脂血癥的分子機制,為后續研究提供理論基礎。
1 方法
1.1 大明膠囊相關靶點篩選
通過中藥系統藥理學數據庫與分析平臺(TCMSP)獲得中成藥大明膠囊成分的化學組分,根據口服生物利用度(oralbioavailability,OB)≥30%且類藥性(drug-likeness,DL)≥0.18的2個ADME屬性值進行初步篩選以獲得活性成分及各活性成分的蛋白質靶點,并根據已發表的文獻報道補充未檢索到的活性成分的已知靶點。最后使用UniProt蛋白質數據庫對活性成分的蛋白質靶點名稱進行統一規范。
1.2 高脂血癥相關靶點的篩選
以“hyperlipemia”為關鍵詞,利用GeneCards、DisGeNET數據庫獲取高脂血癥的潛在治療靶點,并以DrugBank數據庫中臨床一線治療藥物的靶點為補充。合并3個數據庫得到的靶點后,刪除重復值得到高脂血癥的潛在治療靶點。
1.3 大明膠囊成分-高脂血癥共有靶點蛋白質相互作用(protein-proteininteraction,PPI)網絡構建
利用Venny2.1對大明膠囊成分相關靶點與高脂血癥靶點取交集并繪制韋恩圖。通過STRING數據庫構建交集靶點蛋白相互作用網絡模型,將生物類型設定為“homosapiens”,最小互作閾值設定為“highestconfidence>0.9”,其余選項設為默認值,得到大明膠囊成分-高脂血癥靶點PPI網絡。
1.4 基因本體(geneontology,GO)與京都基因與基因組百科全書(Kyotoencyclopediaofgenesandgenomes,KEGG)富集分析
GO對基因和蛋白質功能進行限定和描述,將基因功能分為三個部分:細胞組分(cellularcomponent,CC)、分子功能(molecularfunction,MF)、生物過程(biologicalprocess,BP)[5]。KEGG是一個整合基因組、化學和系統功能信息的數據庫[6]。應用R語言軟件中ClusterProfilerGO.R插件及Perl語言對大明膠囊活性成分及藥物-疾病共有靶點進行GO和KEGG通路富集,對結果進行可視化分析,得到大明膠囊治療高脂血癥的生物功能和信號通路。
1.5 大明膠囊成分-高脂血癥靶點-通路網絡圖的構建
運用Cytoscape3.7.2構建大明膠囊成分-高脂血癥靶點-通路網絡圖,利用Cytoscape3.7.2內置工具包分析成分及靶點的網絡拓撲參數,包括連接度、介度及緊密度等,并根據網絡拓撲學參數篩選核心靶點及發揮藥效的主要活性成分。
1.6 分子對接驗證
利用軟件AutoDockVina對確定的大明膠囊活性成分和核心靶點進行分子對接驗證,研究其結合方式和結合程度。
2 結果
2.1 大明膠囊活性成分靶點的獲取
通過TCMSP數據庫初步獲取、ADME篩選得到陳皮、大黃、丹參、茯苓、決明子、人參的活性成分分別為5、10、19、6、13、17種。活性成分的作用靶點分別為69、70、103、22、67、115個,合并刪除重復值后共得到靶點196個。
2.2 高脂血癥相關靶點的獲取
通過GeneCards數據庫共得到高脂血癥潛在靶點1463個。根據經驗設定Score≥2倍中位數的目標靶點為高脂血癥的潛在靶點,通過GeneCards所得高脂血癥靶點Score最大值為45.99,最小值為0.12,中位數為0.50,故設定Score≥1的靶點為高脂血癥的潛在靶點。結合DisGeNET、DrugBank數據庫補充,合并刪除重復值后,得到541個高脂血癥相關靶點。
2.3 大明膠囊活性成分-高脂血癥靶點PPI網絡構建
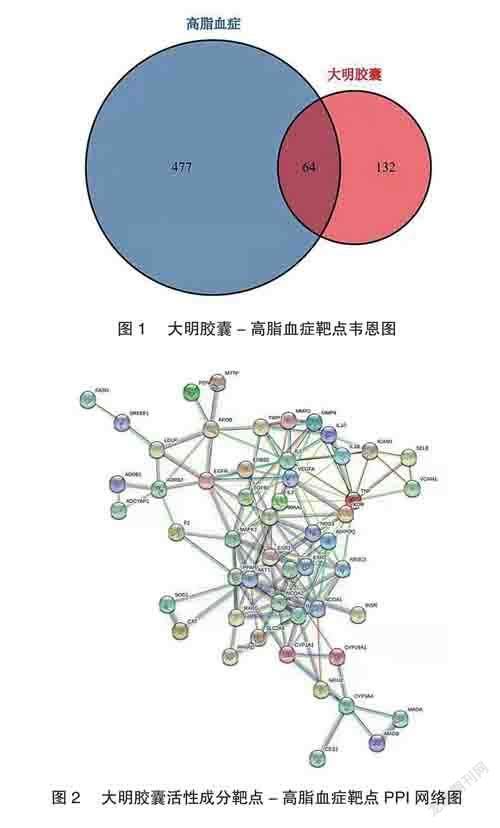
將篩選的大明膠囊活性成分與高脂血癥靶點取交集繪制韋恩圖,得到64個共有靶點,見圖1。在STRING平臺中錄入共有靶點得到大明膠囊活性成分靶點-高脂血癥靶點PPI網絡,見圖2。
2.4 靶點功能與通路的富集分析
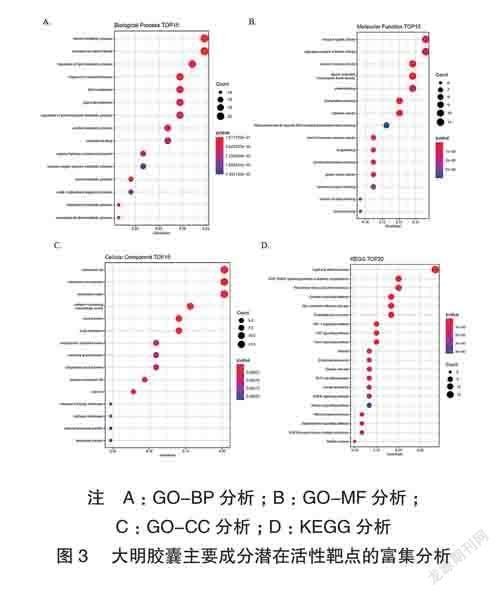
應用R語言軟件ClusterProfilerGO.R插件對大明膠囊治療高脂血癥的潛在作用靶點進行GO和KEGG分析,并對結果進行可視化。
生物過程分析顯示,這些靶點主要富集于類固醇代謝過程、營養水平的應答等,見圖3A。分子功能分析顯示,其靶點主要涉及受體配體活性、信號受體激活因子活性等,見圖3B。細胞組分分析表明,這些靶點主要涉及膜筏、膜微區、膜區等,見圖3C。
KEGG通路分析提示,大明膠囊治療高脂血癥的機制可能與脂質和動脈粥樣硬化信號通路、糖尿病并發癥AGE-RAGE信號通路等有關,見圖3D。
2.5 大明膠囊成分-高脂血癥靶點-通路網絡圖的構建
運用Cytoscape3.7.2軟件構建大明膠囊成分-高脂血癥靶點-通路網絡,見圖4。再通過軟件內置的NetworkAnalyzer工具分析大明膠囊調血脂網絡拓撲學參數,得到核心成分及核心靶點。Cytoscape網絡分析結果表明山柰酚(kaempferol)連接度、介度、緊密度最高,分別為21、0.15、0.45,預測山柰酚為大明膠囊治療高脂血癥的主要成分。HSP90AA1在靶點網絡中的連接度、介度、緊密度最高,分別為35、0.25、0.48,預測其為大明膠囊治療高脂血癥的最重要靶點。NCOA2、AKT1、ADRB2、RXRA、TNF、NCOA1、PPARG、MAPK1、IL-6、IL-1β、ESR1亦為相對重要靶點。
2.6 分子對接驗證
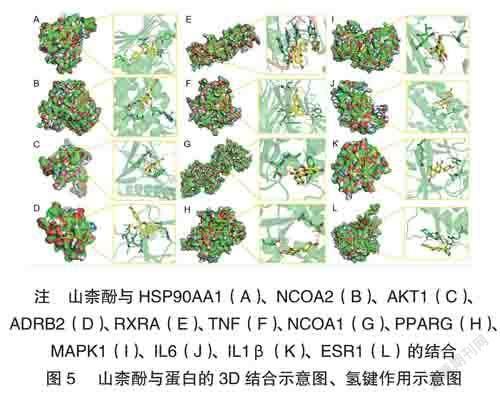
上述結果表明,大明膠囊治療高脂血癥的核心靶點為HSP90AA1、NCOA2、AKT1、ADRB2、RXRA、TNF、NCOA1、PPARG、MAPK1、IL-6、IL-1β、ESR1,主要成分為山柰酚。利用AutoDockVina軟件將山柰酚與核心靶點相互作用進行分子對接預測。AutoDockVina軟件對預測模型進行打分,即Affinity(kcal/mol),其值越小越易與蛋白質結合。預測結果顯示,山柰酚與HSP90AA1、NCOA2、AKT1、ADRB2、RXRA、TNF、NCOA1、PPARG、MAPK1、IL-6、IL-1β、ESR1的結合能分別為-5.8、-3.95、-5.64、-5.76、-5.04、-5.59、-4.07、-5.7、-4.91、-5.29、-6.67、-4.68kcal/mol,均在-3.95~-6.67kcal/mol,說明山柰酚與核心靶點均具有較強的結合能力。其中山柰酚與IL-1β的結合能為-6.67kcal/mol,表明其結合能力最強,見圖5。
3 討論
大明膠囊具有清熱降濁、活血化瘀之功效,適用于熱郁血瘀型高脂血癥的輔助治療。既往研究表明,蒽醌類化合物蘆薈大黃素作為大明膠囊的潛在有效成分之一,具有調節血脂、降低膽固醇的作用[7]。網絡藥理學是建立在系統生物學理論基礎上的一門新的學科,它分析生物系統的網絡,選擇特定的信號節點來設計多靶點藥物分子[8]。本研究通過網絡藥理學研究方法從整體角度探索大明膠囊治療高脂血癥的活性成分及其分子作用機制,結果預測黃酮類化合物山柰酚可能為大明膠囊治療高脂血癥的主要成分。山柰酚是各種植物性食品中主要的膳食類黃酮,具有抗癌、抗氧化和抗動脈粥樣硬化等多種有益特性[9]。山柰酚可通過抑制Akt和激活PPARα、PPARδ發揮降低三酰甘油的作用[10],還可通過TLR4/NF-κB信號通路的失活上調miR-26a-5p緩解ox-LDL誘導的內皮細胞凋亡[11]。上述研究表明山柰酚具有調節血脂、改善動脈粥樣硬化的作用。
3.1 大明膠囊治療高脂血癥關鍵靶點分析
根據上述研究結果,大明膠囊治療高脂血癥的關鍵靶點為HSP90AA1、NCOA2、AKT1、ADRB2、RXRA、TNF、NCOA1、PPARG、MAPK1、IL-6、IL-1β、ESR1。根據分子對接結果,IL-1β與山柰酚的結合能力最強,可能是大明膠囊治療高脂血癥的關鍵靶點。炎癥反應伴隨著高脂血癥的發生發展,TNF-α、IL-1β、IL-6等炎癥因子均與高脂血癥有著密切的聯系[12]。IL-1β是炎癥反應的關鍵介質,其對宿主反應和抵抗病原體至關重要,且能夠加劇急性和慢性疾病的組織損傷[13]。在一項小鼠實驗中,ApoE和IL-1β雙敲除小鼠主動脈竇動脈粥樣硬化病變的大小和硬化面積比明顯小于單敲除ApoE小鼠[14]。IL-1β通過抑制炎癥因子的表達,調節動脈粥樣硬化的炎癥反應,可減少脂質過氧化物的產生,進而改善血管內皮細胞功能[15]。
3.2 通路與生物進程分析
GO-CC富集結果表明,大明膠囊主要在細胞膜上發揮其降血脂作用,且主要分布于膜閥、膜微結構域。膜閥及膜微結構域是高度動態且富含甾醇和鞘磷脂的結構域[16-17],在信號傳導、響應外部刺激等方面起著至關重要的作用[18]。GO-MF結果表明,大明膠囊的降血脂作用主要與細胞內受體配體活動及信號受體激活因子等有關。大明膠囊能夠通過激活AMPK通路使血清和肝臟中的脂質減少。AMPK的激活可增強PPARα的表達和脂蛋白脂肪酶的轉錄,導致三酰甘油水解;也可增強低密度脂蛋白受體蛋白表達促進脂質代謝[19]。大明膠囊還可通過SIRT1/AMPK信號通路增加心肌細胞自噬,抑制氧化應激和炎癥反應,從而改善心肌梗死后的心功能[4]。KEGG結果表明,大明膠囊降血脂作用涉及的主要信號通路包括脂質和動脈粥樣硬化信號通路、糖尿病并發癥中的AGE-RAGE信號通路等,亦證明大明膠囊通過作用于多個信號通路共同發揮其治療高脂血癥的作用,其主要與IL-6、PPARG、TNF、NOS3、VCAM1、AKT、MAPK1等炎癥、氧化應激相關信號因子有關。
本研究通過網絡藥理學研究方法,篩選了大明膠囊治療高脂血癥的主要化學成分及核心靶點,發現了山柰酚在大明膠囊降血脂中發揮重要的作用,并推測其治療高脂血癥的藥理學機制可能是通過調控炎癥反應及氧化應激因子實現的,為今后大明膠囊治療高脂血癥的深入研究提供了理論基礎。

