血清IL-32 sRAGE及NLR與多發性骨髓瘤合并腎損傷的相關性分析
姜 銘, 徐 娟, 丁林林, 賁海祥, 尹 紅
(1.江蘇省如皋市人民醫院, 江蘇 如皋 226500 2.南通大學附屬醫院血液病研究室, 江蘇 南通 226000)
多發性骨髓瘤(Multiple myeloma,MM)是一種由惡性漿細胞克隆性增殖所致[1]。其中腎損傷為MM常見并發癥,同時也是導致MM患者死亡的重要原因[2]。因此及早發現MM患者并發腎損傷對控制病情發展和改善預后具有重要意義。有研究指出,血清白細胞介素-32(Interleukin 32,IL-32)、可溶性晚期糖基化終末產物受體(Soluble advanced glycation end product receptor,sRAGE)參與了MM的發生發展。也有研究表示,中性粒細胞/淋巴細胞比值(Neutrophil/lymphocyte ratio,NLR)在MM作用下呈高表達趨勢。但對于IL-32、sRAGE及NLR是否參與了MM患者并發腎損傷過程尚無統一定論。故而本研究選取82例MM患者作為研究對象,探討MM并發腎損傷與IL-32、sRAGE、NLR的相關性。結果如下。
1 資料與方法
1.1臨床資料:選取2020年6月至2022年6月如皋市人民醫院診治的82例MM患者作為研究對象,設立為觀察組,并根據患者腎功能情況分為腎損傷組(n=27)和非腎損傷組(n=55),同期選取41例健康體檢者設立為健康對照組。診斷標準:符合“中國多發性骨髓瘤診治指南(2022年修訂)”[3]中的診斷標準,骨髓單克隆漿細胞比例≥10%,經活檢證實骨或髓外組織內存在漿細胞瘤。腎損傷標準:以腎小球濾過率(eGFR)<60mL/(min×1.73m2)判定MM合并腎損傷。觀察組納入標準:①經臨床確診為MM;②初次就診,入組前未接受治療;③認知功能正常;④年齡>18歲。對照組納入標準:①身體健康,無慢性疾病;②認知功能正常;③均接受血清IL-32、sRAGE及NLR等指標測定。排除標準:①心肝功能不全者;②患有其他惡性腫瘤者。腎損傷組中,男性13例、女性14例,年齡48~75歲,平均值(62.85±5.74)歲,BMI 19~24kg/m2,平均值(23.52±2.41)kg/m2,依據國際分期系統(International Staging System。ISS):Ⅰ期4例、Ⅱ期14例、Ⅲ期9例;非腎損傷組中,男性29例、女性26例,年齡32~69歲,平均值(52.88±5.65)歲,BMI 19~25kg/m2,平均值(23.58±2.35)kg/m2,依據國際分期系統(International Staging System。ISS):Ⅰ期18例、Ⅱ期24例、Ⅲ期13例;健康對照組中,男性21例、女性20例,年齡45~72歲,平均值(62.81±5.79)歲,BMI 20~23kg/m2,平均值(23.45±2.48)kg/m2;三組一般資料比較,差異無統計學意義(P>0.05)。
1.2方法:于入院時采集MM患者靜脈血5mL,健康體檢者于入院體檢當天采集靜脈血5mL,經3000r/min離心10min取上清液待檢;采用Infinite F50酶標儀(瑞士TECAN公司),選擇酶聯免疫吸附法測定IL-32、sRAGE;采用全自動血細胞分析儀及配套試劑測定中性粒細胞、淋巴細胞,并計算NLR。
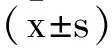
2 結 果
2.1觀察組與健康對照組的血清IL-32、sRAGE、NLR比較:觀察組的IL-32、NLR均高于健康對照組,而sRAGE低于健康對照組(P<0.05)。見表1。

表1 觀察組與健康對照組的血清IL-32 sRAGE NLR比較
2.2腎損傷組與非腎損傷組的血清IL-32、sRAGE、NLR比較:腎損傷組的IL-32、NLR均高于非腎損傷組,而sRAGE低于非腎損傷組(P<0.05)。見表2。

表2 腎損傷組與非腎損傷組的血清IL-32 sRAGE NLR比較
2.3二元Logistic回歸分析:以腎功能是否損傷為因變量(1=損傷,2=未損傷),以“IL-32、sRAGE、NLR”為協變量,納入Logistic回歸中分析,結果顯示IL-32、NLR水平升高和sRAGE水平下降是影響MM患者并發腎損傷的獨立危險因素(P<0.05)。見表3。

表3 IL-32 sRAGE NLR對MM患者并發腎損傷的二元Logistic回歸分析
2.4預效能分析:ROC曲線分析顯示,血清IL-32、sRAGE、NLR預測MM患者并發腎損傷的AUC值分別為(0.761、0.765、0.802,P<0.05);敏感度分別為100.00%、100.00%、48.10%;特異度分別為50.90%、49.10%、100.00%。見表4和圖1。

圖1 血清IL-32、sRAGE、NLR預測MM患者并發腎損傷的ROC曲線分析

表4 血清IL-32 sRAGE NLR預測MM患者并發腎損傷的效能分析
3 討 論
MM為惡性漿細胞病常見類型。經流行病學調查,其發病率約占所有血液系統惡性腫瘤的10.00%[4]。目前臨床對于MM發病機制尚未完全闡明,認為它的出現可能與電離輻射、遺傳因素、病毒感染等有關[5]。針對MM分析,發現該類患者初期多見于貧血、骨痛、感染等臨床表現,隨病情進展,可出現腎功能異常。據臨床調查,在MM病情進展中,約有20.00%~50.00%的患者出現不同程度的腎臟損害,且在確診MM時已出現腎損害的患者高達10.00%~40.00%,可能與其早期表現不明顯有關,易造成患者就診延遲。有研究指出,MM患者并發腎損傷可能與免疫球蛋白輕鏈、多糖復合物沉淀組織器官致腎臟淀粉樣變性等有關[6]。也有文獻報道,MM患者并發腎損傷可能與惡性漿細胞大量產生單克隆輕鏈而阻塞、損傷腎小管有關[7]。雖然臨床對MM患者采用自體干細胞移植和蛋白酶體抑制劑等方法治療有利于延長患者的生存期,但合并腎損害尚無特異性治療方案。有研究表示,慢性腎臟損傷和腎功能不全是MM患者致死的重要原因。在此情況下及早發現MM患者并發腎損害顯得尤為重要,有利于改善預后。
IL-32是一種呈促炎特性的因子,由病原體和促炎因子誘導漿細胞、單核細胞及調節性T細胞產生,能通過激活巨噬細胞的殺傷活性,抑制炎性介質釋放。據臨床研究發現,IL-32參與了MM的發生發展。可能是通過抑制多種促炎因子在MM的發生與發展過程中而發揮作用[8]。同時在MM發病過程中,骨髓瘤的擴散能通過破壞機體局部組織,誘發或增加炎癥反應,而炎癥反應的增加或出現又能通過促進IL-32大量表達發揮抑炎作用[9]。在本研究結果中可見,MM患者的血清IL-32呈高表達趨勢,即高于健康體檢者,說明受MM影響,會使血清IL-32水平升高。上述已說到腎損害為MM并發癥,本文在IL-32的進一步研究中發現,其表達水平會隨MM患者并發腎損害而上升,提示IL-32升高可能參與了MM患者腎損害的發展。sRAGE為RAGE的抑制性配體。既往研究發現,其具有延緩動脈粥樣硬化進展、保護缺血再灌注損傷和抗炎等作用。但隨著臨床對sRAGE的進一步研究,發現其在MM患者中呈低表達。在正常生理狀態下,sRAGE能通過競爭性抑制RAGE-配體,阻滯腫瘤增殖,并延緩病情進展。但骨髓內漿細胞惡性增生能力的不斷增加,能導致sRAGE水平下降,當其表達降低時,可能會加劇骨髓瘤細胞的轉移和播散,并在病情的進一步發展下,產生更多的游離輕鏈損傷腎功能;同時sRAGE水平的下降也無法抑制異常免疫球蛋白生成而發揮保護腎功能作用。
NLR是指中性粒細胞與淋巴細胞比值,其中前者可反映機體炎性反映程度,在腫瘤所致炎癥反應影響下,能促使中性粒細胞激活,而該細胞的激活又能通過增加血管內皮生長因子、炎癥介質分泌,使癌細胞轉移和血管生成;另外,中性粒細胞水平的上調也能通過釋放大量的彈性蛋白酶而阻斷腫瘤細胞凋亡途徑,為腫瘤細胞不受限制而大量分化、增殖。而后者淋巴細胞可反映機體抗腫瘤免疫抑制功能[10]。據臨床研究發現,MM患者受病情影響,存在機體免疫功能紊亂情況,當骨髓內MM細胞大量克隆增殖,能通過減少B淋巴細胞和T淋巴細胞分泌,影響機體免疫功能;同時也能通過激活神經內分泌系統、氧化應激及炎癥反應,促使皮質醇激素和兒茶酚胺大量釋放,引起骨髓抑制及反向調節淋巴細胞增殖、分化,而在這一系列作用下能導致淋巴細胞凋亡加劇。故而臨床常通過監測NLR變化來觀察MM患者機體炎性反應程度和抗腫瘤免疫抑制功能狀態。
本文針對IL-32、sRAGE及NLR進一步研究,發現MM患者并發腎損傷會使IL-32、HLR水平進一步升高和促使sRAGE表達下降。研究結果顯示,腎損傷組的IL-32、NLR水平顯著高于非腎損傷組,而sRAGE低于非腎損傷組;且本文Logistic回歸分析也顯示,IL-32、sRAGE、NLR水平是影響MM患者并發腎損傷的獨立危險因素,與姜倩倩等學者結果一致,進一步證實了上述指標對MM患者并發腎損傷的影響。
綜上所述,血清IL-32、sRAGE、NLR表達與MM患者并發腎損傷具有一定相關性,動態監測其水平變化有利于預測MM患者并發腎損傷提供重要參考依據。

