羥考酮與瑞芬太尼復合丙泊酚對顱腦損傷術患者血流動力學神經功能及預后的影響
喬 燕, 廖興志, 陳 湉, 施冬冬, 肖驥鋒
(聯勤保障部隊第904醫院麻醉科, 江蘇 無錫 214044)
顱腦損傷系外力所致腦組織損傷,具有起病急及發病率、死亡率高等特點[1]。目前,外科手術仍為治療顱腦損傷的主要方式,但因顱腦的特殊結構,對術中麻醉的要求相對更高。良好麻醉效果不但能確保手術順利進行,而且可使術后并發癥風險降低。瑞芬太尼和丙泊酚均系臨床常用麻醉藥之一,前者為高強度鎮痛藥,可在極短時間內發揮鎮痛效果,但過量使用會加劇腦組織氧化應激損傷,不利于患者預后;后者可降低顱內壓、保護腦組織,但其鎮痛效果不理想[2]。羥考酮系鎮痛機制和嗎啡相似,具有起效快、作用效果持久、生物利用率高等特點。目前,已有較多關于羥考酮與瑞芬太尼分別復合丙泊酚應用于顱腦損傷手術中的報道,但鮮有比較羥考酮復合丙泊酚與瑞芬太尼復合丙泊酚應用于顱腦損傷手術報道。為此,本研究就以上兩種麻醉方式進行比較,分析其對顱腦損傷手術患者血流動力學、神經功能及預后的影響,報道如下。
1 資料與方法
1.1一般資料:選取2019年9月至2021年9月收治的150例行顱腦損傷手術患者為研究對象,隨機分成研究組和對照組,各75例。納入標準:①均存在明確的顱腦外傷癥狀體征,且經CT檢查確診;②受傷至入院治療時間<12h;③格拉斯哥昏迷評分(Glasgow coma score,GCS)<9分;④患者家屬知情并簽署知情協議書。排除標準:①過往顱腦手術史;②入組前合并神經、血液系統疾病;③嚴重肝腎功能障礙;④對本研究選用藥物禁忌。研究組男41例、女34例,年齡為28~63歲,平均(45.73±7.86)歲,受傷原因:40例交通事故、27例高處墜落、8例暴力外傷。對照組男43例、女32例,年齡為29~63歲,平均(45.71±7.76)歲,受傷原因:38例交通事故、24例高處墜落、13例暴力外傷。兩組一般資料比較,差異無統計學意義(P>0.05)。本研究遵循《世界醫學協會赫爾辛基宣言》有關原則。
1.2方 法
1.2.1術前準備:兩組患者術前均接受常規處置:開放中心靜脈通路、保持氣道通暢、留置胃管、予以利尿藥物、監測心電、血壓等,并視患者血腫部位、大小、身體狀況選擇手術類型。所有手術均由同一組高年資神經外科醫師完成。
1.2.2麻醉方法:麻醉開始前行動脈穿刺直接測壓和深靜脈置管操作。麻醉誘導:兩組患者均予以2.0mg/kg丙泊酚、0.6μg/kg枸櫞酸舒芬太尼注射液、0.6mg/kg羅庫溴銨靜脈推注。麻醉誘導完畢,氣管插管予以機械通氣。麻醉維持:研究組予以0.10~0.15mg·kg-1·h-1羥考酮、4~8mg·kg-1·h-1丙泊酚。對照組予以0.10~0.15μg·kg-1·min-1瑞芬太尼、4~8mg·kg-1·h-1丙泊酚。兩組麻醉劑量視患者術中心率、呼吸頻率、血壓等情況適當調整,并吸入1.5%~2.0%七氟烷維持麻醉,間斷注射羅庫溴銨維持肌松。術畢前20min停用七氟烷,并逐漸減少丙泊酚用量。
1.2.3術后鎮痛:術畢前15min,研究組予以0.08mg/kg羥考酮預先鎮痛,并將0.6mg/kg羥考酮+100mL鹽酸托烷司瓊氯化鈉注射液入泵;對照組予以0.15μg/kg舒芬太尼預先鎮痛,并將2μg/kg舒芬太尼+10.0mg托烷司瓊配置成100mL入泵。兩組鎮痛泵均經生理鹽水稀釋后以2mL/h速率于術畢前15min開始泵入。手術完成后移送患者至恢復室。
1.3觀察指標:分別于術前(T0)、麻醉后30min(T1)、術畢即刻(T2)、術后24h(T3)時以心電監護儀(邁瑞,T6型)檢測血氧飽和度(Oxygen saturation,SpO2)、平均動脈壓(Mean arterial pressure,MAP)、心率(Heart rate,HR)水平。分別于T0與T3時抽取靜脈血,分離血清,以酶聯免疫吸附法檢測Tau蛋白(Microtubule-associated protein tau,Tau)、神經元特異性烯醇化酶(Neuron-specific enolase,NSE)、膠質纖維酸性蛋白(Glial fibrillary acidic protein,GFAP)水平。術后隨訪3個月,以格拉斯哥預后評分(Glasgow Outcome Scale,GOS)評估患者預后情況[3]:Ⅰ級:死亡;Ⅱ級:植物生存且僅有最小反應;Ⅲ級:重度殘疾,無法正常生活,需他人照顧;Ⅳ級:輕度殘疾但可獨立生活,可于保護下工作;Ⅴ級:恢復良好,僅有輕度缺陷。
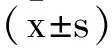
2 結 果
2.1兩組患者圍術期不同時點血流動力學水平變化比較:兩組間、不同時點間SpO2、MAP、HR的差別及時間與分組的交互作用均有統計學意義(P<0.05)。見表1。

表1 兩組患者圍術期不同時點血流動力學水平變化比較
2.2兩組患者手術前后神經功能水平比較:T0時,兩組血清Tau、NSE、GFAP水平比較無差異(P>0.05);T3時,兩組血清Tau、NSE、GFAP水平均低于T0時,且研究組降低程度大于對照組(P<0.05)。見表2。

表2 兩組患者手術前后神經功能水平比較
2.3兩組患者預后情況比較:兩組均未出現死亡病例,研究組預后情況優于對照組(P<0.05)。見表3。
3 討 論
近年來顱腦損傷發病率逐年升高,神經及認知功能障礙系顱腦損傷患者常見合并癥,預后較差。目前,顱腦外科手術仍為治療顱腦損傷最為有效手段,可迅速解除患者顱內高壓狀態、清除血腫,促進腦組織代謝,防止腦組織再次損傷,對改善患者預后具有重要意義[4]。但顱腦外科手術操作難度大,對麻醉及手術操作要求極高,因此,理想的麻醉方式不但要滿足手術需求,還應具備保護患者腦組組免受二次損傷的功效[5]。
丙泊酚與瑞芬太尼均為顱腦外科手術常用麻醉藥,其中丙泊酚具備較強脂溶性,可迅速發揮功效,但缺點是親和力不足,需大劑量方可發揮其鎮痛功能,易導致呼吸抑制;瑞芬太尼達到血腦平衡僅需1min,并快速水解發揮作用,但同樣會對呼吸具有一定抑制作用,延長術后拔管時間[6,7]。羥考酮可對阿片k、μ受體產生激動作用,且能以主動轉運形式通過血腦屏障進入至中樞神經系統內,并刺激其中的阿片受體,阻斷痛覺傳導,從而發揮強鎮痛功效,且因其給藥途徑多,在臨床中廣泛應用。羥考酮復合丙泊酚后能增強丙泊酚對腦局部藥效,一定程度上填補了丙泊酚親和力不足。
手術作為應激源一種,會使得患者產生較強烈應激反應,從而改變血流動力學水平。良好的麻醉需減少手術帶來應激反應保持相對穩定的血流動力學水平。本研究結果表明,兩組圍術期SpO2、MAP、HR等血流動力學指標水平均呈現出先顯著升高后逐漸下降趨勢,且在整個變化過程中研究組波動幅度較對照組相對更小,提示羥考酮復合丙泊酚相較于瑞芬太尼復合丙泊酚應用于顱腦損傷手術患者可獲得更為穩定的血流動力學水平。分析原因為:羥考酮血藥濃度和其藥效具有明顯關聯性,而其可主動轉運至腦脊液內,使得其在血藥濃度較低時亦可發揮較強鎮痛作用,復合丙泊酚應用還可有效抑制組胺、皮質醇、睪酮等分泌及氧自由基合成,從而減輕腦組織局部氧化應激反應,從而保持相對穩定血流動力學水平。
顱腦損傷和血腫壓迫均會導致血腦屏障破壞,大量神經損傷因子進入血液循環中,從而對大腦神經功能造成影響[8]。Tau為一種磷蛋白,主要分布于神經細胞軸突內,腦細胞功能受損時,其水平會異常升高;NSE為廣泛分布烯醇化酶之一,當神經元受損、功能異常時,會通過血腦屏障流入血液中;GFAP為分布于星形膠質細胞內的一種特異性酸性蛋白,當神經系統損傷時,其水平會明顯上升[9]。本研究結果顯示,術后24h兩組血清Tau、NSE、GFAP水平均較術前明顯降低,且研究組降低程度大于對照組,提示羥考酮復合丙泊酚相較于瑞芬太尼復合丙泊酚應用于顱腦損傷手術患者可明顯改善患者神經功能。此外,本研究結果表明,研究組預后情況更佳,說明羥考酮復合丙泊酚相較于瑞芬太尼復合丙泊酚應用于顱腦損傷手術患者可明顯改善患者預后情況。
綜上所述,羥考酮復合丙泊酚相較于瑞芬太尼復合丙泊酚應用于顱腦損傷手術患者可獲得更為穩定的血流動力學水平,且能明顯改善患者神經功能及預后,更值得臨床應用。

