維持性血液透析患者高磷血癥的危險因素研究*
姜曉鳳,張 明,孫福州,高琛妮
(1.山東省棗莊市立醫院腎臟內科,山東 棗莊 277110;2.上海交通大學醫學院附屬瑞金醫院腎臟內科,上海 200025)
礦物質與骨異常(mineral and bone disorder,MBD)是慢性腎臟病(chronic kidney disease,CKD)患者常見的并發癥之一,可導致CKD患者全因死亡率和心血管死亡率明顯增加[1]。鈣磷代謝紊亂是MBD重要的特征,我國55%的維持性血液透析(maintenance hemodialysis,MHD)患者血磷達到或超過5.6 mg/dL[2]。高磷血癥被認為是MHD患者異位鈣化的始動因素,也是CKD患者發生全因死亡和心血管死亡的獨立危險因素[3]。
充分了解鈣磷代謝現狀是糾正MBD的第一步,本文通過橫斷面調查形式,分析山東省棗莊市立醫院血液透析中心MHD患者MBD相關實驗室檢驗結果,并分析血磷控制情況及影響因素,以期更好了解本中心MHD患者鈣磷代謝紊亂現狀,為日后采取預防和干預措施打好基礎,現報道如下。
1 對象與方法
1.1 研究對象
符合條件的MHD患者152例。其中男性87例(57.2%),女性65例(42.8%),男女比例1.34∶1。平均年齡(57.6±13.4)歲,平均確診CKD(82.5±73.5)月,中位透析齡22月(14~32月)。所有患者均定期接受限制飲食磷攝入的健康宣教。分為高磷血癥組107例,非高磷血癥組45例。
本研究納入本中心進行規律血液透析的患者,納入標準:(1)年齡超過18歲;(2)接受規律血液透析時間≥3個月;(3)每周透析至少2次。排除標準:(1)臨床資料或實驗室檢查結果不完整;(2)曾行甲狀旁腺手術;(3)罹患惡性腫瘤;(4)不愿意參加研究。本研究經山東省棗莊市立醫院倫理委員會批準,入組患者均簽署書面知情同意書。
1.2 研究方法
1.2.1 臨床資料
記錄透析患者人口學資料、確診CKD時間、透析齡、透析通路、每周透析頻次、透析時長、透析前收縮壓、透析前舒張壓、透析前及透析后體重等臨床資料。
1.2.2 實驗室檢查
收集并記錄患者透析前血紅蛋白、前白蛋白、白蛋白、堿性磷酸酶、血尿素氮、血清肌酐、血尿酸、血鈣、血清矯正鈣、血磷、鈣磷乘積、甲狀旁腺素(parathyroid hormone,PTH)等實驗室檢查結果。使用單室尿素清除指數(single-pool Kt/V,spKt/V)評價透析充分性。
其中,血清矯正鈣=血清鈣濃度+0.02×(40-血清白蛋白); spKt/V=-ln[透后血尿素氮/透前血尿素氮-0.008×治療時間]+[4-3.5×透后血尿素氮/透前血尿素氮]×(透前體重-透后體重)/透后體重。
根據《中國慢性腎臟病礦物質和骨異常診治指南》[4],定義MHD患者鈣磷代謝實驗室指標達標標準:血清矯正鈣2.10~2.37 mmol/L,血磷1.13~1.78 mmol/L,鈣磷乘積≤55 mg/dL,PTH 150~300 pg/mL。
1.3 統計學方法
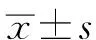
2 結果
2.1 達標情況
本中心152例患者中,鈣達標81例(53.3%),磷達標42例(27.6%),PTH達標41例(27.0%),三項指標均達標的患者8例(5.3%),見表1。

表1 本院MHD患者CKD-MBD指標達標情況
2.2 不同血磷水平患者的一般情況及實驗室指標比較
根據血磷水平將患者分為高磷血癥組(血磷≥1.78 mmol/L)及非高磷血癥組(血磷<1.78 mmol/L)。2組之間的臨床指標比較,見表2。與非高磷血癥組相比,高磷血癥組的MHD患者更年輕、前白蛋白、白蛋白、尿素氮、肌酐、尿酸、堿性磷酸酶及PTH水平更高(P<0.05),見表2。

表2 不同血磷水平患者的一般情況及實驗室指標比較
2.3 磷結合劑使用情況
152例患者中,127例(83.6%)服用磷結合劑。其中106例(69.7%)服用含鈣磷結合劑,60例(39.6%)服用非含鈣磷結合劑,39例(25.7%)患者同時服用含鈣及非含鈣磷結合劑。服用磷結合劑及未服用磷結合劑患者的平均血清矯正鈣、血磷、鈣磷乘積和PTH水平無統計學差異,見表3。

表3 服用磷結合劑與未服用磷結合劑患者的鈣磷代謝指標比較
2.4 不同透析充分性患者的血磷水平比較
將本中心MHD患者按照Kt/V分為透析充分組(Kt/V≥1.2,n=84)及透析不充分組(Kt/V<1.2,n=68)。透析充分組患者的血磷及鈣磷乘積顯著低于透析不充分組,見表4。

表4 不同透析充分性患者鈣磷代謝指標比較
2.5 高磷血癥的相關危險因素分析
Spearman相關性分析結果顯示,MHD患者是否合并高磷血癥與年齡、Kt/V、堿性磷酸酶呈負相關,與前白蛋白、白蛋白、尿素氮、血肌酐、尿酸、PTH呈正相關,見表5。

表5 高磷血癥相關危險因素分析
3 討論
高磷血癥是我國MHD患者常見并發癥,我國MHD患者磷達標率在16.8%~60.2%之間[5,6]。CKD患者高磷血癥往往是多因素的。本研究提示,MHD患者血磷水平與年齡呈負相關,這可能與老年MHD患者進食量相對較少、飲食磷攝入較低有關。有研究證實,MHD患者采用高通量血透、血液透析濾過治療可以更有效地改善CKD-MBD[7]。本研究中,血磷水平與Kt/V呈負相關,且透析充分組患者血磷顯著低于透析不充分組,提示改善透析充分性,包括延長透析時間、增加透析頻率、聯合血液濾過或血液灌流等方法,有助于降低MHD患者的血磷水平。
一項納入820例CKD 3~5期患者的研究結果顯示,男性及CKD 5期是高磷血癥的獨立危險因素[8]。本研究并未發現高磷血癥與性別有相關性,可能與本研究納入人數相對較少有關。高磷血癥患者的代謝性指標如前白蛋白、白蛋白、尿素氮、肌酐、尿酸等明顯高于非高磷者,與曹聰等[9]人的研究結果一致。進一步分析提示,血磷與血肌酐、尿酸呈正相關,多因素回歸分析也證實血肌酐與尿酸是MHD患者高磷血癥的獨立危險因素。這可能因為高磷血癥患者存在飲食控制不佳,攝入較多蛋白及嘌呤,以及殘腎功能差有關,提示我們需要按照控磷“3D”原則[10],關注MHD患者飲食。飲食控制是治療高磷血癥的基礎,接受規范的飲食控磷教育,可使透析患者血磷有顯著下降[11]。
綜上,本研究結果提示,高水平肌酐和尿酸是MHD患者高磷血癥的獨立危險因素。對MHD患者進行飲食宣教、改善透析充分性,為有效控制血磷提供依據。

