嗜酸性粒細胞計數和嗜酸性粒細胞與淋巴細胞比率對腺病毒肺炎診斷及預后的影響*
張小珍 陳 娟 崔莉娜 黃義雙 丘小其 劉曉萍
廣東省深圳市寶安區婦幼保健院急診兒科 518102
腺病毒肺炎(Adenovirus pneumonia,AdVP)常發生于嬰幼兒時期,人腺病毒(Human adenovirus,HAdV)感染相關肺炎病死率約為50%,具有病情進展快、治療難度大、預后差等特點,易引發膿毒癥、急性呼吸窘迫綜合征等嚴重并發癥[1]。HAdV傳統診斷方法為呼吸道樣本多重HAdV聚合酶鏈反應,但具有一定局限性,未能識別早期下呼吸道HAdV感染,因而尋找AdVP診斷方法具有重要意義。嗜酸性粒細胞(EOS)可引起肺泡上皮、肺毛細血管內皮損傷,并可反映肺組織損傷、呼吸衰竭嚴重程度,且對感染相關器官功能障礙具有一定預測價值[2]。EOS屬于免疫炎性細胞,其與氣道重塑、氣道高反應性、膿毒癥、哮喘等炎性疾病有關,并可促進炎性因子、趨化因子、細胞因子釋放,引起氣道炎性反應[3]。嗜酸性粒細胞與淋巴細胞比率(ELR)變化可反映哮喘、氣道炎性疾病嚴重程度[4]。目前EOS、ELR與AdVP相關研究較少,本研究主要檢測AdVP患兒外周血中EOS、ELR,分析其對AdVP診斷價值及預后的影響,為改善AdVP患兒預后提供參考依據。
1 資料與方法
1.1 一般資料 選取2016年9月—2021年8月本院收治的肺炎患兒200例為研究對象,分為肺炎支原體肺炎(MPP)組124例、AdVP組76例,根據28d住院期間AdVP患兒預后情況[5]分為2個亞組:預后良好患兒53例、預后不良患兒23例。MPP組:男63例、女61例,年齡1~8(4.46±0.32)歲,體質量3~17(10.03±2.03)kg;肺部斑片狀滲出108例、肺部實性改變15例。AdVP組:男40例、女36例,年齡2~8(4.52±0.35)歲,體質量2~16(9.83±1.97)kg;肺部斑片狀滲出63例、肺部實性改變13例。兩組一般資料比較無明顯差異(P>0.05),具有可比性。研究經本院倫理委員會批準。
1.2 納入與排除標準 納入標準:符合AdVP、MPP診斷標準[6],經病原學檢測確診為HAdV陽性;近期未服用免疫抑制劑、糖皮質激素;生命體征平穩;既往無肺部手術史者;未合并肺部其他病變者;家屬知情且簽署同意書。排除標準:合并造血系統、腦血管等原發性疾病者;合并免疫系統疾病者;其他病原學檢查結果顯示陽性者;營養不良者;出現難以控制呼吸衰竭者;合并先天性疾病者。
1.3 方法 (1)收集肺炎患兒臨床資料:包括性別、年齡、發病季節、機械通氣、免疫功能、血常規、炎性指標[白細胞(WBC)、C反應蛋白(CRP)、中性粒細胞比值(N)、淋巴細胞比值(L)、紅細胞沉降率(ESR)]等。(2)治療方法:依據AdVP治療標準,予以排痰、平喘、降溫、并發癥防治等對癥治療,依據病情需要予以肝腎保護,針對繼發性感染者給予抗菌藥物治療。治療7d后評價治療效果:若癥狀、體征消失且經胸部影像學檢查顯示病灶完全吸收視為治愈,若癥狀、體征明顯減輕且病灶明顯吸收視為好轉,若癥狀、體征及病灶無明顯變化甚至惡化視為無效,其中治愈、好轉提示預后良好,無效提示預后不良。(3)檢測EOS、ELR:受試者入組后(24h內)采集靜脈血3ml,加入抗凝試管(EDTA),使用Sysmex XT4000-i全自動血細胞分析儀(希森美康公司)檢測EOS、淋巴細胞計數,并計算ELR。
1.4 觀察指標 (1)比較入組后各組EOS、ELR,分析其與炎性指標相關性。(2)分析EOS、ELR聯合CRP、ESR對AdVP的診斷價值。(3)分析EOS、ELR與AdVP患兒預后相關性,及其相關影響因素。(4)基于影響AdVP患兒預后的危險因素建立列線圖預測模型,并進行外部驗證,觀察內容包括一致性指數(C-index)、區分度(Discrimination)、校準度(Calibration)。
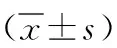
2 結果
2.1 MPP組、AdVP組EOS、ELR及炎性指標結果 與MPP組比較,AdVP組EOS、ELR、CRP、ESR升高(P<0.05),見表1。
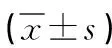
表1 MPP組、AdVP組EOS、ELR及炎性指標結果
2.2 EOS、ELR與炎性指標相關性分析 EOS、ELR與CRP、ESR呈正相關(P<0.05),見表2。

表2 EOS、ELR與炎性指標相關性分析
2.3 EOS、ELR、CRP、ESR對AdVP的診斷價值 以AdVP組76為陽性樣本,以MPP組124例為陰性樣本,繪制ROC曲線,結果顯示EOS、ELR、CRP、ESR診斷AdVP的AUC分別為0.774、0.802、0.749、0.703,見圖1、表3。

表3 EOS、ELR、CRP、ESR對AdVP的診斷價值
2.4 EOS、ELR聯合CRP、ESR對AdVP的診斷價值 以AdVP組76為陽性樣本,以MPP組124例為陰性樣本,繪制ROC曲線,結果顯示EOS+ELR、EOS+ELR+CRP、EOS+ELR+CRP+ESR診斷AdVP的AUC高于單個指標診斷(P<0.05),見圖2、表4。

表4 EOS、ELR聯合CRP、ESR對AdVP的診斷價值
2.5 不同預后患兒EOS、ELR及臨床特征比較 與預后良好患兒比較,預后不良患兒乳酸脫氫酶、EOS、ELR、CRP、ESR水平升高(P<0.05),總膽紅素、IgA、IgM水平降低(P<0.05),見表5。

表5 不同預后患兒EOS、ELR及臨床特征比較
2.6 Logistic回歸分析影響AdVP患兒預后的危險因素 以AdVP患兒預后為因變量,以總膽紅素、乳酸脫氫酶、EOS、ELR、IgA、IgM、CRP、ESR為自變量,Logistic回歸分析影響AdVP患兒預后的危險因素,結果顯示,EOS、ELR、CRP、ESR是患兒預后不良的危險因素(P<0.05),見表6。

表6 Logistic回歸分析影響AdVP患兒預后的危險因素
2.7 AdVP預后不良的列線圖預測模型及外部驗證 納入2.6中分析所得相關影響因素,繪制預測AdVP預后不良(預后不良患兒23例)的列線圖,見圖3,C-index為0.985(95% CI:0.421~0.993)。采用200例肺炎患兒作為外部驗證數據集對列線圖進行驗證,結果顯示,Discrimination為0.730,Calibration為0.822,見圖4。

圖3 AdVP預后不良的列線圖預測模型

圖4 列線圖預測模型的外部驗證
3 討論
EOS、炎性因子與淋巴細胞計數、血小板計數呈正相關,并可用于評估新型冠狀病毒肺炎(COVID-19)恢復情況[7]。本研究中AdVP組EOS、ELR、CRP、ESR水平高于MPP組,EOS、ELR與CRP、ESR呈正相關,表明EOS、ELR升高可增加CRP、ESR生成量,引起細胞免疫功能紊亂,誘發氣道炎性損傷,參與AdVP發生發展過程。CRP、ESR可增加肺部血管通透性,誘發壞死性細支氣管炎,可能作為早期診斷AdVP的標志物[8]。提示EOS、ELR可反映氣道炎性反應水平,EOS可遷移至炎性部位,以自分泌/旁分泌形成生成ESR等炎性因子,引發炎性級聯反應,在AdVP氣道炎性反應中發揮重要作用,控制EOS活化的內源性途徑可能控制AdVP發展進程。同時本研究嘗試性分析EOS、ELR聯合CRP、ESR對AdVP的診斷價值,結果顯示EOS、ELR聯合CRP、ESR診斷AdVP的AUC高于單個指標診斷價值。表明HAdV感染可激活機體免疫系統,增加炎性介質、細胞因子生成量,檢測外周血EOS、ELR、CRP、ESR,可為臨床早期診斷AdVP及治療提供參考。
EOS可促進T細胞增殖、分化,調節輔助性T細胞1(Th1)/Th2極化,參與機體免疫反應過程,研究表明EOS計數增加、ELR升高與呼吸衰竭、多器官功能障礙有關[9]。本研究顯示,預后不良患兒乳酸脫氫酶、EOS、ELR、CRP、ESR水平高于預后良好患兒,總膽紅素、IgA、IgM水平低于預后良好患兒。其原因可能為EOS、ELR升高可釋放Th2細胞因子,誘發Th2免疫反應,引起機體免疫失衡、細胞免疫功能障礙,并可激活趨化因子受體3,募集炎性因子聚集于氣道,引起氣道炎癥反應,促進肺組織損傷,導致患兒預后不良。ELR可作為多種炎性疾病的診斷標志物[10]。本研究分析顯示,EOS、ELR是AdVP患兒預后不良的危險因素。本研究納入預后不良的相關因素建立列線圖預測模型,結果顯示C-index為0.985,進一步對列線圖模型進行驗證,結果發現該模型具有預測精確度、良好區分度、校準度。
綜上所述,AdVP患兒外周血中EOS、ELR升高,可作為早期診斷AdVP的生物標志物,聯合CRP、ESR可提高其診斷價值,基于EOS、ELR、CRP、ESR建立的列線圖模型可準確預測AdVP患兒預后狀態,為臨床制定個性化治療方案提供參考。

