痛風(fēng)患者達(dá)標(biāo)治療降尿酸藥物劑量的影響因素分析
李建斌 蔡芬 吳銳
【摘 要】目的:探究痛風(fēng)患者實(shí)現(xiàn)達(dá)標(biāo)治療所需要的降尿酸藥物用量的影響因素。方法:收集2017年6月至2018年6月在南昌大學(xué)第一附屬醫(yī)院風(fēng)濕免疫科就診的123例原發(fā)性痛風(fēng)患者的臨床資料,根據(jù)痛風(fēng)患者對(duì)降尿素藥物劑量的需求將其分為敏感組、次敏感組和耐藥組。在達(dá)標(biāo)之前2~4周隨訪1次,達(dá)標(biāo)后1~3個(gè)月隨訪1次,持續(xù)1年。收集并分析不同組別患者的一般資料、個(gè)人史、合并癥、實(shí)驗(yàn)室檢查等臨床資料。結(jié)果:敏感組29例(23.58%),次敏感組44例(35.77%),耐藥組50例(40.65%);單因素分析顯示,病程、年齡、體質(zhì)量指數(shù)(BMI)、家族史、初始血肌酐值、初始紅細(xì)胞沉降率、糖尿病、腦卒中與痛風(fēng)患者的達(dá)標(biāo)治療相關(guān)(P < 0.05)。多因素分析結(jié)果顯示,BMI、初始血肌酐值和家族史是痛風(fēng)達(dá)標(biāo)治療的獨(dú)立影響因素(P < 0.05)。結(jié)論:存在高BMI、家族中有痛風(fēng)史以及高血肌酐的痛風(fēng)患者對(duì)現(xiàn)有的降尿酸藥物反應(yīng)較差,臨床中需兼顧痛風(fēng)患者BMI及血肌酐的管理,個(gè)體化制定降尿酸藥物劑量,做到精準(zhǔn)化達(dá)標(biāo)治療。
【關(guān)鍵詞】 痛風(fēng);降尿酸藥物;影響因素;達(dá)標(biāo)治療
Analysis of Influencing Factors on the Dosage of Uric Acid Lowering Drugs for Gout Patients Undergoing Standard Treatment
LI Jian-bin,CAI Fen,WU Rui
【ABSTRACT】Objective:To explore the influencing factors of the dosage of uric acid lowering drugs required for gout patients to achieve standard treatment.Methods:Clinical data of 123 patients with primary gout who had visited the Department of Rheumatology and Immunology at the First Affiliated Hospital of Nanchang University from June 2017 to June 2018 were collected.Gout patients were divided into a sensitive group,a sub sensitive group,and a drug resistant group based on their demand for the dosage of urea lowering drugs.Follow up once 2~4 weeks before reaching the standard,and once 1~3 months after reaching the standard,lasting for 1 year.
General information,personal history,comorbidities,laboratory tests,and other clinical characteristics of patients in different groups were collected and analyzed.Results:There were 29 cases(23.58%)in the sensitive group,
44 cases(35.77%)in the sub sensitive group,and 50 cases(40.65%)in the drug resistant group.Univariate analysis showed that the course of disease,age,body mass index(BMI),family history,initial blood creatinine value,initial erythrocyte sedimentation rate,diabetes and stroke were related to the standard treatment of gout patients(P < 0.05).Multivariate analysis showed that BMI,initial blood creatinine value and family history were independent influencing factors for gout treatment(P < 0.05).Conclusion:Gout patients with high BMI,a family history of gout,and high blood creatinine have poor response to existing uric acid lowering drugs.In clinical practice,it is necessary to balance the management of BMI and blood creatinine in gout patients,and tailor the dosage of uric acid lowering drugs to achieve precise and
standardized treatment.
【Keywords】 gout;uric acid lowering drugs;influencing factors;standard treatment
痛風(fēng)是一種代謝性疾病,其主要特征為尿酸代謝紊亂,導(dǎo)致尿酸水平升高,引發(fā)關(guān)節(jié)炎和尿酸結(jié)晶沉積的炎癥反應(yīng)。針狀尿酸結(jié)晶沉積可在全身各組織中引發(fā)多種并發(fā)癥,如關(guān)節(jié)急性炎癥、尿路結(jié)石、腎功能衰竭、心血管疾病等[1]。高尿酸血癥也被認(rèn)為是心血管和代謝性疾病的獨(dú)立危險(xiǎn)因
素[2-3]。研究發(fā)現(xiàn),尿酸結(jié)晶的溶解與血尿酸水平呈反比[4],且保持血尿酸水平在目標(biāo)范圍內(nèi)的痛風(fēng)患者,其結(jié)石數(shù)量和尺寸有所改善[5]。特別是腎功能不全患者,維持血尿酸在目標(biāo)范圍內(nèi)能顯著降低長(zhǎng)期透析的需求[6]。控制血尿酸水平對(duì)減少急性關(guān)節(jié)炎發(fā)作及改善并發(fā)癥至關(guān)重要[7]。美國(guó)風(fēng)濕病學(xué)會(huì)(ACR)2012年提出“達(dá)標(biāo)治療”的概念,強(qiáng)調(diào)降低尿酸水平以維持血尿酸在
360 μmol·L-1以下[8]。降尿酸藥物包括抑制尿酸合成藥和促進(jìn)尿酸排泄藥,兩者臨床應(yīng)用安全有
效[9]。然而,痛風(fēng)患者對(duì)這些藥物的敏感性存在差異,部分患者需要更大劑量或聯(lián)合用藥。本研究回顧性分析了痛風(fēng)患者降尿酸藥物治療的劑量與臨床特征的相關(guān)性,旨在提供更精準(zhǔn)的治療指導(dǎo)。
1 資料與方法
1.1 研究對(duì)象 收集2017年6月至2018年6月在南昌大學(xué)第一附屬醫(yī)院風(fēng)濕免疫科住院的123例痛風(fēng)患者臨床資料。在達(dá)標(biāo)之前2~4周隨訪1次,達(dá)標(biāo)后1~3個(gè)月隨訪1次,持續(xù)1年。所有患者符合2015年ACR和歐洲抗風(fēng)濕病聯(lián)盟(EULAR)制定的痛風(fēng)診斷標(biāo)準(zhǔn)[10],年齡18~75歲,未合并其他腫瘤疾病,并排除繼發(fā)性痛風(fēng)患者。
1.2 分組方法 將痛風(fēng)患者根據(jù)對(duì)降尿酸藥物的敏感性分為3個(gè)組別:①敏感組:別嘌呤醇≤100 mg,每日1次;苯溴馬隆≤50 mg,每日1次;非布司他≤40 mg,每日1次治療下血尿酸達(dá)標(biāo)患者。②次敏感組:100 mg,每日1次 < 別嘌呤醇≤100 mg,每日2次;50 mg,每日1次 < 苯溴馬隆≤75 mg,每日1次;40 mg,每日1次 < 非布司他≤60 mg,每日1次治療下血尿酸達(dá)標(biāo)患者。③耐藥組:100 mg,每日1次 < 別嘌呤醇≤100 mg,每日2次;75 mg,每日1次 < 苯溴馬隆≤100 mg,每日1次;60 mg,每日1次 < 非布司他≤80 mg,每日1次,或聯(lián)合治療血尿酸達(dá)標(biāo)患者,及聯(lián)合治療血尿酸持續(xù)不達(dá)標(biāo)患者。
1.3 研究方法 收集患者的臨床資料,包括年齡、性別、家族史、紅細(xì)胞沉降率(ESR)、C反應(yīng)蛋白(CRP)、吸煙史、病程、飲酒史、血尿素氮、血尿酸、血肌酐、痛風(fēng)石發(fā)生情況、體質(zhì)量指數(shù)(BMI),是否合并腦卒中、高血壓病、腎結(jié)石、高脂血癥、糖尿病、慢性腎功能不全、心臟冠狀動(dòng)脈疾病和動(dòng)脈硬化等臨床疾病。
1.4 統(tǒng)計(jì)學(xué)方法 采用SPSS 26.0軟件進(jìn)行統(tǒng)計(jì)分析。計(jì)量資料符合正態(tài)分布以表示,采用獨(dú)立樣本t檢驗(yàn);不符合正態(tài)分布以中位數(shù)和四分位數(shù)間距[M(P25,P75)]表示,采用非參數(shù)檢驗(yàn)。計(jì)數(shù)資料以例數(shù)和百分比(%)表示,采用χ2檢驗(yàn);多組等級(jí)資料比較采用Kruskal-Wallis H檢驗(yàn)。危險(xiǎn)因素納入多元有序Logistic回歸分析。以P < 0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié) 果
2.1 一般情況 共納入123例痛風(fēng)患者,男115例,女8例。敏感組29例(23.58%),其中服用別嘌呤醇11例(37.93%),苯溴馬隆9例(31.03%),非布司他9例(31.03%);次敏感組44例(35.77%),其中服用別嘌呤醇14例(31.82%),苯溴馬隆
9例(20.45%),非布司他21例(47.73%);耐藥組50例(40.65%),其中服用別嘌呤醇8例(16.00%),苯溴馬隆8例(16.00%),非布司他10例(20.00%),聯(lián)合用藥血尿酸達(dá)標(biāo)9例(18.00%),聯(lián)合用藥血尿酸持續(xù)不達(dá)標(biāo)15例(30.00%)。
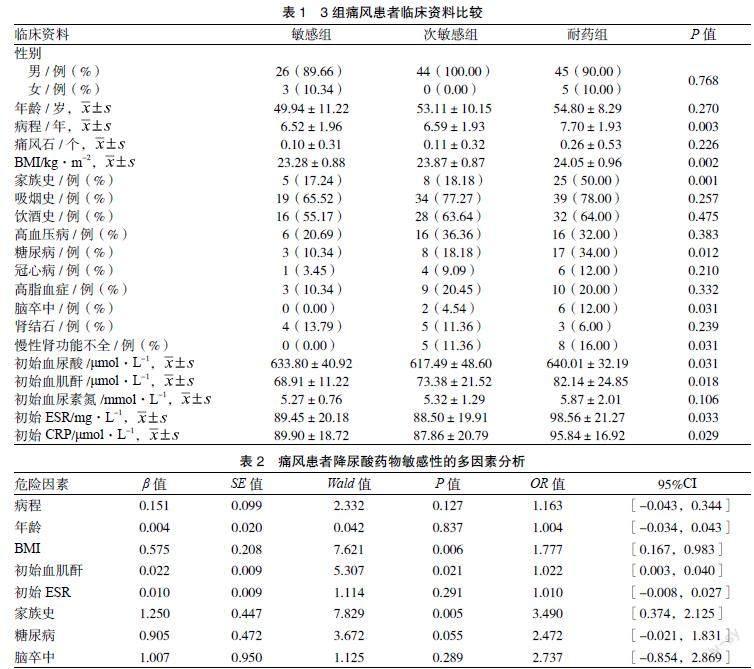
2.2 3組痛風(fēng)患者臨床資料比較 3組痛風(fēng)患者在ESR、CRP、病程、血尿酸、BMI、血肌酐、家族史、腦卒中、慢性腎功能不全和糖尿病等方面比較,差異有統(tǒng)計(jì)學(xué)意義(P < 0.05)。但在痛風(fēng)石、年齡、飲酒史、初始血尿素氮、性別、高血壓病、吸煙史、腎結(jié)石、高脂血癥和冠心病方面比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P > 0.05)。見(jiàn)表1。
2.3 痛風(fēng)患者降尿酸藥物敏感性的影響因素分析 單因素分析顯示,痛風(fēng)患者的達(dá)標(biāo)治療與病程、年齡、BMI、初始血肌酐值、初始ESR、家族史、糖尿病、腦卒中等多個(gè)影響因素相關(guān)(P < 0.05);多因素回歸分析顯示,痛風(fēng)患者的達(dá)標(biāo)治療與患者BMI、初始血肌酐值和家族史相關(guān)(P < 0.05)。見(jiàn)表2。
3 討 論
痛風(fēng)是由于關(guān)節(jié)內(nèi)尿酸鹽晶體沉積所導(dǎo)致,與嘌呤代謝紊亂以及腎臟尿酸排泄功能障礙所致的高尿酸血癥直接相關(guān)。血尿酸控制不佳會(huì)引起腎功能受損、關(guān)節(jié)內(nèi)尿酸鹽沉積、心血管問(wèn)題等并發(fā)癥[11]。多項(xiàng)研究證實(shí),痛風(fēng)達(dá)標(biāo)治療將血尿酸水平持續(xù)降至 < 360 μmol·L-1(6 mg·dL-1)對(duì)改善痛風(fēng)患者預(yù)后,降低并發(fā)癥有重要意義。據(jù)流行病學(xué)調(diào)查,我國(guó)痛風(fēng)發(fā)病率從1998年的0.34%逐漸升至
2008年的1.33%,每年增長(zhǎng)率高達(dá)9.7%,截至2020年,我國(guó)痛風(fēng)患者數(shù)量已達(dá)到1億[12]。作為代謝類(lèi)疾病,痛風(fēng)已經(jīng)成為中國(guó)僅次于糖尿病的第二常見(jiàn)疾病。但我國(guó)痛風(fēng)治療3個(gè)月血尿酸達(dá)標(biāo)率僅29.12%,6個(gè)月血尿酸達(dá)標(biāo)率為38.20%,依從性差、不良生活嗜好(飲酒)及治療不規(guī)范是導(dǎo)致痛風(fēng)患者達(dá)標(biāo)率低的重要原因[13]。本研究顯示,即使規(guī)范用藥甚至聯(lián)合用藥,仍有部分患者(12.2%)血尿酸不能達(dá)標(biāo);而影響痛風(fēng)患者降尿酸藥物達(dá)標(biāo)治療劑量的獨(dú)立因素有家族史、BMI、初始血肌酐。
家族聚集的明顯趨勢(shì)在不同地區(qū)和人種中表現(xiàn)出特定的特征,這些特征與高尿酸血癥、痛風(fēng)相關(guān)。研究表明,遺傳基礎(chǔ)存在于10%~25%的原發(fā)性痛風(fēng)患者中[14]。遺傳易感性不僅在痛風(fēng)的發(fā)生和發(fā)展過(guò)程中扮演關(guān)鍵角色[15],而且可能導(dǎo)致對(duì)降尿酸藥物的治療劑量需求增加。這是因?yàn)槟蛩猁}的處理存在遺傳缺陷,而許多藥物通過(guò)影響腎臟尿酸鹽轉(zhuǎn)運(yùn)影響血尿酸水平[16]。韓國(guó)的一項(xiàng)隊(duì)列研究發(fā)現(xiàn),痛風(fēng)相關(guān)的遺傳因素與肥胖/飲酒之間存在相互作用的可能性[17]。中國(guó)山東地區(qū)進(jìn)行了一項(xiàng)跨斷面研究,結(jié)果顯示,BMI、血糖升高以及有痛風(fēng)的家族史與高尿酸血癥風(fēng)險(xiǎn)增加相關(guān)[18]。另有研究表明,與未受影響的直系親屬相比,有痛風(fēng)影響的個(gè)體患病風(fēng)險(xiǎn)增加了2.42倍。有痛風(fēng)家族史且超重,與疾病風(fēng)險(xiǎn)明顯增加有關(guān)[17]。
血肌酐是許多疾病的重要生物標(biāo)志物,如痛風(fēng)、高尿酸血癥、腎臟疾病和心臟病。研究發(fā)現(xiàn),與無(wú)痛風(fēng)石的參與者相比,有痛風(fēng)石患者年齡更大,病程更長(zhǎng),血清肌酐更高[19]。而別嘌呤醇可降低高尿酸血癥患者的肌酐水平[20]。在對(duì)照組(單獨(dú)使用非布司他)和聯(lián)合組(非布司他聯(lián)合關(guān)節(jié)鏡手術(shù))的研究中發(fā)現(xiàn),聯(lián)合組血清肌酐顯著降低,2組血清尿酸和急性痛風(fēng)發(fā)作時(shí)間均顯著降低。在2組隨訪終點(diǎn)的比較中,聯(lián)合組血清肌酐和尿酸水平低于對(duì)照組[21]。
就痛風(fēng)患者對(duì)降尿酸藥物的反應(yīng)性而言,BMI被確認(rèn)為影響因素之一,這與本研究結(jié)果一致。腹部肥胖被視為高尿酸血癥的危險(xiǎn)因素之一。在一項(xiàng)研究中,對(duì)無(wú)癥狀高尿酸血癥人群進(jìn)行了痛風(fēng)風(fēng)險(xiǎn)因素的篩查,發(fā)現(xiàn)隨著腰圍的增加,高尿酸血癥轉(zhuǎn)化為痛風(fēng)的風(fēng)險(xiǎn)增加9%[22]。研究顯示,BMI增加與痛風(fēng)發(fā)病風(fēng)險(xiǎn)逐漸上升密切相關(guān)[23]。ACR發(fā)現(xiàn),解決過(guò)度肥胖和其他關(guān)鍵的可改變因素,有可能預(yù)防大多數(shù)男性痛風(fēng)的發(fā)生。肥胖癥的男性可能不會(huì)從其他改變中受益,除非解決了自身的肥胖問(wèn)題[24]。研究表明,每增加1個(gè)BMI單位,痛風(fēng)風(fēng)險(xiǎn)增加48.95倍[25]。在痛風(fēng)負(fù)擔(dān)和社會(huì)人口學(xué)指數(shù)之間觀察到一種非線性關(guān)系,當(dāng)社會(huì)人口學(xué)指數(shù)值約為0.6時(shí),對(duì)痛風(fēng)負(fù)擔(dān)的估計(jì)最低。高BMI是痛風(fēng)負(fù)擔(dān)的主要風(fēng)險(xiǎn)因素[26]。
綜上所述,具有痛風(fēng)家族史、高血肌酐和高BMI的患者對(duì)現(xiàn)有降尿酸藥物的反應(yīng)性較差。在臨床實(shí)踐中,需要綜合考慮痛風(fēng)患者的BMI和糖尿病管理,制定個(gè)體化的降尿酸藥物劑量,以實(shí)現(xiàn)精準(zhǔn)的治療目標(biāo)。需要指出的是,由于本研究樣本有限,并且是單中心的回顧性臨床研究設(shè)計(jì),因此結(jié)果的適用性受到一定程度的限制。未來(lái)的研究需增加樣本量、進(jìn)行前瞻性研究,以探究痛風(fēng)患者達(dá)標(biāo)治療的影響因素和相關(guān)機(jī)制。
參考文獻(xiàn)
[1] BORGHI C,AGABITI-ROSEI E,JOHNSON RJ,et al.
Hyperuricaemia and gout in cardiovascular,metabolic and kidney disease[J].Eur J Intern Med,2020,80(1):
1-11.
[2] PEREZ-RUIZ F,MORENO-LLEDO A,URIONAGUENA I,et al.Treat to target in gout[J].Rheumatology(Oxford),2018,57(Suppl 1):20-26.
[3] KIMURA Y,TSUKUI D,KONO H.Uric acid in inflammation and the pathogenesis of atherosclerosis[J].Int J Mol Sci,2021,22(22):12394-12412.
[4] GUPTA MK,SINGH JA.Cardiovascular disease in gout and the protective effect of treatments including urate-lowering therapy[J].Drugs,2019,79(5):531-541.
[5] DALBETH N,MERRIMAN TR,STAMP LK.Gout[J].Lancet,2016,388(10055):2039-2052.
[6] 唐羽裳,劉宏,劉必成.高尿酸血癥流行病學(xué)數(shù)據(jù)的變遷及反思[J].藥品評(píng)價(jià),2015,12(7):8-13.
[7] MAZZA A,LENTI S,SCHIAVON L,et al.Asymptomatic hyperuricemia is a strong risk factor for resistant hypertension in elderly subjects from general popul-
ation[J].Biomed Pharmacother,2017,86(1):590-594.
[8] KHANNA D,F(xiàn)ITZGERALD JD,KHANNA PP,et al.
2012 American College of Rheumatology guidelines for management of gout.Part 1:systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia[J].Arthritis Care Res(Hoboken),2012,64(10):1431-1446.
[9] PIANI F,AGNOLETTI D,BORGHI C.Advances in pharmacotherapies for hyperuricemia[J].Expert Opin Pharmacother,2023,24(6):737-745.
[10] DEJACO C,SINGH YP,PEREL P,et al.2015 recommendations for the management of polymyalgia rheumatica:a European League Against Rheumatism/American College of Rheumatology collaborative initiative[J].Arthritis Rheumatol,2015,67(10):2569-2580.
[11] COPUR S,DEMIRAY A,KANBAY M.Uric acid in metabolic syndrome:does uric acid have a definitive
role?[J].Eur J Intern Med,2022,103(1):4-12.
[12] 趙敏,陳婷,黃振光.1990—2019年中國(guó)痛風(fēng)疾病負(fù)擔(dān)研究[J].現(xiàn)代預(yù)防醫(yī)學(xué),2021,48(21):3974-3978.
[13] 田新平,曾小峰.加強(qiáng)痛風(fēng)的長(zhǎng)期規(guī)范化管理改善痛風(fēng)患者的長(zhǎng)遠(yuǎn)預(yù)后[J].浙江醫(yī)學(xué),2017,39(4):243-244.
[14] NAKAYAMA A,NAKAOKA H,YAMAMOTO K,et al.
GWAS of clinically defined gout and subtypes identifies multiple susceptibility loci that include urate transporter genes[J].Ann Rheum Dis,2017,76(5):869-877.
[15] ZHAO J,GUO S,SCHRODI SJ,et al.Trends in the contribution of genetic susceptibility loci to hyperuricemia and gout and associated novel mechanisms[J].Front Cell Dev Biol,2022,10(1):937855-937871.
[16] 胡有元.血尿酸正常痛風(fēng)的機(jī)制研究進(jìn)展[J].甘肅醫(yī)藥,2021,40(4):299-301.
[17] KIM KH,CHOI IA,KIM HJ,et al.Familial risk of gout and interaction with obesity and alcohol consumption:a population-based cohort study in Korea[J].Arthritis Care Res(Hoboken),2023,75(9):1955-1966.
[18] LU J,SUN W,CUI L,et al.A cross-sectional study on uric acid levels among Chinese adolescents[J].Pediatr Nephrol,2020,35(3):441-446.
[19] HE W,PHIPPS-GREEN A,STAMP LK,et al.Population-specific association between ABCG2 variants and tophaceous disease in people with gout[J].Arthritis Res Ther,2017,19(1):43-48.
[20] QU LH,JIANG H,CHEN JH.Effect of uric acid-lowering therapy on blood pressure:systematic review and Meta-analysis[J].Ann Med,2017,49(2):142-156.
[21] GONG Z,XIA L,XU R,et al.The clinical effects of febuxostat alone or combined with arthroscopic surgery for gout:a single-center retrospective study[J].J Inflamm Res,2021,14(1):4509-4517.
[22] 李?lèi)偅瑮畛埃瑥埿ぃ?肥胖與高尿酸血癥的相關(guān)研究現(xiàn)況[J].世界最新醫(yī)學(xué)信息文摘,2019,19(98):128-129.
[23] JURASCHEK SP,MILLER ER 3rd,GELBER AC.Body mass index,obesity,and prevalent gout in the United States in 1988—1994 and 2007—2010[J].Arthritis Care Res(Hoboken),2013,65(1):127-132.
[24] MCCORMICK N,RAI SK,LU N,et al.Estimation of primary prevention of gout in men through modification of obesity and other key life style factors[J].JAMA Netw Open,2020,3(11):e2027421-e2027432.
[25] LIU K,YAO Y,CHEN W,et al.Modifiable risk factors and incidence of gout:estimation of population attributable fraction in the US[J].Semin Arthritis Rheum,2022,55(1):152040-15048.
[26] XIA Y,WU Q,WANG H,et al.Global,regional and national burden of gout,1990—2017:a systematic analysis of the Global Burden of Disease Study[J].Rheumatology(Oxford),2020,59(7):1529-1538.
收稿日期:2023-08-19;修回日期:2023-10-05
 風(fēng)濕病與關(guān)節(jié)炎2024年2期
風(fēng)濕病與關(guān)節(jié)炎2024年2期
- 風(fēng)濕病與關(guān)節(jié)炎的其它文章
- 基于“玄府理論”淺析開(kāi)玄通絡(luò)辨治強(qiáng)直性脊柱炎
- 王宏坤教授運(yùn)用經(jīng)方處理唑來(lái)膦酸不良反應(yīng)的經(jīng)驗(yàn)
- 彭江云教授運(yùn)用桂枝湯類(lèi)方辨治成人Still病經(jīng)驗(yàn)
- 全身炎癥反應(yīng)指數(shù)與痛風(fēng)石形成的相關(guān)性分析
- 強(qiáng)直性脊柱炎睡眠質(zhì)量與中醫(yī)證型分析
- 基于經(jīng)筋理論的膝骨關(guān)節(jié)炎患者“筋結(jié)點(diǎn)”超聲解剖學(xué)特征分析與針刀治療的療效評(píng)價(jià)研究
