2′-巖藻糖基乳糖功能及其微生物生產菌種構建研究進展
劉琳,趙藤,高俊哲,李俊眾,2,孫雪,2,宗劍飛,劉逸寒,2,李玉,2*,李慶剛,2*
(1.天津科技大學生物工程學院,天津 300457;2.天津科技大學工業發酵微生物教育部重點實驗室/天津市工業微生物重點實驗室/工業酶國家工程實驗室,天津 300457;3.山東合成遠景生物科技有限公司,山東濰坊 262500)
母乳富含多種營養物質和生物活性成分,是新生兒最主要的營養和能量來源。世界衛生組織和聯合國兒童基金會建議,母乳喂養可持續至嬰兒兩歲或更長,這對于新生兒的健康保護意義重大[1]。人乳寡糖,即母乳低聚糖(human milk oligosaccharides,HMOs),是母乳中含有的一類碳水化合物,在母乳固體營養物中的含量位于第三,僅次于乳糖和脂質。HMOs 具有重要的營養價值,可以通過防止病原體在腸道內的黏附、調節免疫反應等方式來改善新生兒的健康[2]。HMOs 的種類豐富多樣,包括2′-巖藻糖基乳糖(2′-fucosyllactose,2′-FL)、乳酰-N-新四糖(lacto-N-neotetraose,LNnT)、3-巖藻糖基乳糖(3-fucosyllactose,3-FL)、6′-唾液酸乳糖(6′-sialyllactose,6′-SL)和3′-唾液酸乳糖(3′-Lactose sialic acid,3′-SL)等,其中,分泌型母乳中含量最高的為2′-巖藻糖基乳糖(2′-fucosyllactose,2′-FL),其在HMOs 總量中占比可達30%[3]。
2′-FL 是由一分子巖藻糖與一分子乳糖通過α-1,2 糖苷鍵連接而成,結構如圖1 所示。
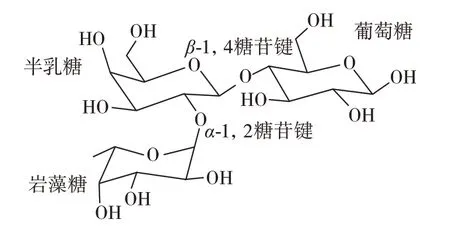
圖1 2′-FL 結構示意圖Fig.1 Structure of 2′-FL
2′-FL 可作為益生元,促進雙歧桿菌、擬桿菌等益生菌生長,同時有效抑制病原體與腸道黏膜的結合與定殖,提高嬰兒免疫力[4]。2′-FL 對人體的作用主要包括調節腸道菌群生態、阻斷病原體黏附靶細胞、調節免疫系統和促進大腦發育等。
1 2′-巖藻糖基乳糖的功能及其作用機制
巖藻糖基乳糖的功能及其作用機制如圖2 所示。
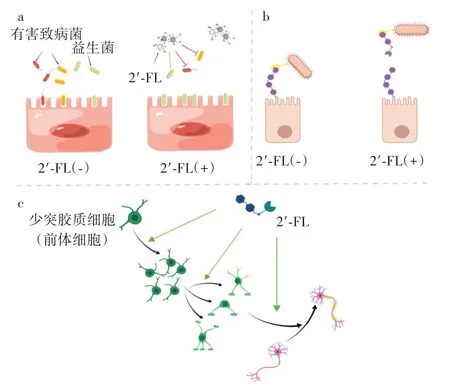
圖2 2′-巖藻糖基乳糖的功能及其作用機制Fig.2 The function and mechanism of 2′-fucosyllactose
1.1 調節腸道菌群生態
益生元是通過選擇性地刺激一種或幾種細菌的生長或活性,從而產生對寄主有益影響的成分,2′-FL 符合作為益生元的前提條件。采用全自動細菌培養系統監測細菌生長情況,發現2′-FL 是具有高度選擇性的碳源,可以作為腸道益生菌菌群的唯一碳源促進其生長,而不被潛在致病菌吸收利用[5],從而有利于嬰兒腸道菌群的進化(圖2a)。
雙歧桿菌是一種腸道益生菌,Lewis 等[6]測定了母乳喂養嬰兒糞便菌群的組成結構,結果顯示嬰兒糞便中雙歧桿菌的百分含量與母乳中HMOs 的含量呈正相關。Mao 等[7]對具有代謝2′-FL 能力的雙歧桿菌進行研究,結果證實了雙歧桿菌聯合2′-FL 能夠顯著提高腸道菌群的物種豐富度。此外,雙歧桿菌在代謝過程中能夠產生豐富的乳酸和短鏈脂肪酸,使得腸道環境pH 值顯著降低,從而抑制了產氣莢膜梭菌等有害菌的繁殖及毒素的分泌,降低了誘發嬰兒分泌性腹瀉的風險[8-9]。
1.2 阻斷病原體黏附靶細胞
細菌、病毒的感染是導致嬰幼兒患病的常見原因,大多數病原體感染宿主的第一步是通過凝集素或黏附素與腸道上皮細胞表面的糖蛋白結合,而2′-FL 與宿主細胞表面的糖蛋白結構相似,能夠作為可溶性誘餌受體與病原體結合(圖2b),從而阻止了病原體在靶細胞表面的定植,最終被排出體外[10]。通過體外實驗證明了2′-FL 可以抑制空腸彎曲桿菌、腸致病性大腸桿菌、沙門氏菌血清變種和銅綠假單胞菌對人腸道細胞Caco-2 的黏附,并且2′-FL 顯著抑制了銅綠假單胞菌對人呼吸道上皮細胞系A549 的黏附,抑制率為24%[11]。
1.3 調節免疫系統
2′-FL 對免疫系統也具有一定的積極影響,可作為免疫因子在全身發揮作用。Eiwegger 等[12]測試了2′-FL 對免疫系統的影響,結果顯示2′-FL 使Th1 細胞顯著增加,同時還促進γ 干擾素的分泌、抑制白細胞介素的產生,這表明2′-FL 具有抗炎作用,有助于降低嬰兒炎性疾病的發生率。2′-FL 還與腸道上皮細胞Ag-IgE復合物激活的調節相關,能夠抑制炎癥細胞流入腸道,減輕食物過敏癥狀[13]。
2′-FL 對于疫苗接種的免疫應答具有一定的改善作用。食用添加2′-FL 飼糧的小鼠,其疫苗特異性遲發型過敏(delayed-type hypersensitivity,DTH)反應顯著增強,血清中疫苗特異性免疫球蛋白水平升高[14]。與對照組相比,喂養2′-FL 小鼠的脾臟B 細胞活化標志物CD27 表達增加,體外再刺激后,脾細胞疫苗特異性CD4+和CD8+T 細胞數量和γ 干擾素的產生也顯著增加。另外還證實了2′-FL 對骨髓來源樹突狀細胞成熟狀態和抗原提呈能力的直接影響。
1.4 促進大腦發育
在嬰兒的早期神經發育過程中,神經細胞髓鞘化對腦連接和行為認知功能的產生起著至關重要的作用,研究發現2′-FL 在促進少突膠質祖細胞增殖、成熟、分化過程中發揮著重要作用,證實了2′-FL 能夠促進神經細胞髓鞘化發育[15](圖2c)。早期攝入2′-FL 對增強嬰兒的認知發展和學習記憶是十分重要的,而并未發現其他HMOs 成分與嬰兒認知發展相關[16]。事實上,2′-FL 可以滋養腸道微生物,并可能通過以下幾種機制促進嬰兒的認知發育:1)防止腸道生態失衡,減少隨后從未成熟的腸道到發育中大腦的炎癥的發生,避免早期認知缺陷[17];2)提高腸道微生物擬桿菌和乳桿菌的豐度,增強腦信號傳導底物——短鏈脂肪酸的產生[18]。
在動物實驗中,Oliveros 等[19]以小鼠為模型檢驗了2′-FL 對大腦發育的影響,喂養了2′-FL 的小鼠在Y 形迷宮與莫里斯水迷宮中的表現都更好,而且補充了2′-FL 的大鼠長期增益效應(long-term potentiation,LTP)比對照組更強烈且持續時間更長。研究發現,小鼠認知能力的提高是通過長期增強大腦海馬區來促進空間學習和記憶的,并檢測到2′-FL 增加了與新獲得記憶存儲相關分子的表達(如突觸后密度蛋白、磷酸化鈣/鈣調素依賴性激酶II 等),表明2′-FL 會影響嚙齒動物的認知領域,并改善學習和記憶[20]。
1.5 其他作用
病毒對于人類健康有著巨大的威脅,許多人類致死性傳染疾病通過病毒傳播,2′-FL 可起到預防病毒感染的功效。鑒定發現2′-FL 主要通過阻斷病毒的吸附和內化來抑制柯薩奇病毒A 組9 型分離株(CV-A9)BUCT01 對人體細胞的感染,10 mg/mL 的2′-FL 對CVA9 有顯著的抑制作用且無細胞毒性,與對照組相比,2′-FL 阻斷了病毒的進入,使病毒在橫紋肌肉瘤細胞中的感染顯著減少[21]。
皮膚在老化或紫外線照射等因素的作用下易出現色素沉著的現象,研究發現2′-FL 能夠誘導微管關聯蛋白1A 和1B(microtubule-associated proteins 1A/1B,MAP1LC3,LC3)的Ⅰ型轉化為自噬激活標志物LC3Ⅱ,隨后形成LC3Ⅱ+/PMEL+自噬體[22]。此外,2′-FL 激活了AMP 依賴的蛋白激酶(adenosine 5′-monophosphate-activated protein kinase,AMPK)在Thr172 位點的磷酸化以及ULK1 在Ser555 位點的磷酸化,而這種磷酸化在AMPK 特異性抑制劑dorsmorphin 的存在下被逆轉,從而使得2′-FL 介導的色素沉著減少,表明2′-FL 通過AMPK-ULK1 軸誘導細胞自噬以促進黑色素降解。
近期研究表明,2′-FL 還具有一定的抗腫瘤與解毒作用。Li 等[23]在荷瘤裸鼠模型中,選擇結腸癌細胞HCT116 作為敏感細胞株,使用5-氟尿嘧啶(5-fluorouracil,5-Fu)作為陽性藥物對HCT116 細胞進行處理。與對照組相比,2′-FL 組與2′-FL/5-Fu 組的腫瘤質量均顯著降低,并發現了2′-FL 通過VEGFA/VEGFR2/PI3K/Akt/Caspase3 通路進行調控,從而實現新生血管數量的減少、腫瘤惡性程度的降低,證實了2′-FL 有一定的抗腫瘤及減輕肝腎組織毒性的作用。
2 2′-巖藻糖基乳糖的應用領域及生產現狀
隨著生活水平的日益提高以及對更健康的膳食結構的需求,2′-FL 因其優越的性能被廣泛應用于各個領域。目前對2′-FL 最重要的應用為添加到嬰幼兒配方奶粉中,此外,2′-FL 還可以添加到功能性食品和飲料中或用作醫療輔劑等。
2.1 嬰幼兒配方奶粉
2′-FL 不僅被美國食品及藥品管理局認定為公認安全(generally recognized as safe,GRAS),而且被歐洲食品安全局批準為一種新型食品(novel food,NF),并進一步研究得出結論:將1.2 g/L 2′-FL、0.6 g/L LNnT聯合添加到嬰兒配方奶粉中時,2′-FL 對嬰兒是安全的[24]。2′-FL 可以顯著降低母乳喂養嬰兒腹瀉的發生率,作為益生元改善嬰兒的腸道健康,且較高濃度的2′-FL 可降低母乳喂養嬰兒的死亡率[25]。
2.2 功能性食品和飲料
近年來,具有益生元特性的功能性食品和飲料需求較高,研究與市場報告預計,到2027 年全球功能性食品和飲料市場達到2 291 億美元,且保持6.3%的復合年增長率。2′-FL 具有多種益生功效,添加到食品或者飲料中,能夠起到改善腸道菌群、增強免疫力等作用。因此,作為功能性原料的2′-FL 將在未來的食品和飲料領域具有廣闊的發展前景。
2.3 醫療輔劑
近期研究發現,使用2′-FL 能夠減輕咪喹莫特(imiquimod,IMQ)誘導的銀屑病小鼠的皮損炎癥。2′-FL 能夠抑制輔助性T 細胞17(T helper cell 17,Th17)免疫應答并減少Th17 相關的細胞因子產生,2′-FL 干預后顯著減輕了IMQ 引起的皮膚紅斑和皮損增厚,同時能夠顯著降低皮膚角質層增生并改善皮膚組織病理變化[26]。
另外,在腸道疾病的治療中,2′-FL 也具有一定的輔助改善效果。研究HMOs 改善腸易激綜合征的臨床試驗結果表明,每天定量服用HMOs 混合物對于腸易激綜合征癥狀的減輕具有顯著改善效果。隨著2′-FL多種生物活性的發掘,如何保障2′-FL 供給市場需求是目前亟需解決的問題。
2.4 2′-巖藻糖基乳糖生產現狀
目前,國外多家公司均供應HMOs。同時,我國多家新銳企業已實現2′-FL 的產業化落地,并通過將合成生物學與人工智能算法進行有機整合、建立新的研發路徑、利用機器學習對整條代謝通路進行模塊化整合、采用新一代基因編輯技術對底盤微生物進行基因定向改造等方式來生產HMOs。
當今很多國家和地區已經批準了HMOs 應用于嬰幼兒配方奶粉原料中的相關法規,為HMOs 市場提供了巨大的發展前景。目前,美國食品和藥物管理局、歐洲食品安全局已經批準了5 家公司的十多項與2′-FL 相關的產品[27]。2022 年,2′-FL 獲得了澳新食品標準局批準,可應用于嬰幼兒配方奶粉中。
法規的持續完善為HMOs 市場提供了巨大的發展前景,2018 年HMOs 的全球市場規模為7 882 萬美元,預計到2026 年將達到2.388 億美元,期間復合年增長率將達15.3%。隨著應用領域的擴展以及生產工藝的突破,未來HMOs 市場仍將保持增長態勢,科漢森公司預測到2025 年HMOs 的潛在市場價值將超過4.7 億美元,長期市場價值有望超過12 億美元。
我國在2016 年國家衛計委就發布了2′-FL 作為食品營養強化劑的征求意見,但尚未得到批準。在2021 年,國家衛健委開放了國內轉基因微生物食品添加劑的申報路徑,正式開始受理和審批轉基因微生物食品添加劑新品種;隨后在2022 年,國家發展改革委發布了《“十四五”生物經濟發展規劃》,提出培育壯大生物經濟支柱產業,大力發展合成生物學技術,探索“人造”新型食品的研發。相關政策的制定將進一步加快2′-FL 的合法化進程,在未來我國2′-FL 發展空間進一步擴大的同時,其生產應用也將迎來新的突破。
3 2′-巖藻糖基乳糖的生產方法
目前,生產2′-FL 的方法主要有3 種:化學合成法、酶催化合成法、微生物法。
3.1 化學合成法
化學合成法以L-巖藻糖為底物,進行數十步反應后經過色譜分離,最終得到純度較高的2′-FL 產物。2019 年,Agoston 等[28]實現了2′-FL 的千克級化學合成,過程如圖3 所示。
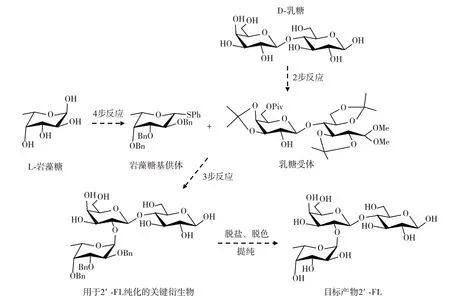
圖3 2′-FL 的化學合成過程Fig.3 Chemical synthesis of 2′-FL
具體分為以下4 步:1)乳糖受體的制備:以D-乳糖為原料進行2 步反應,使用了包括2,2-二甲氧基丙烷、哌戊酰氯、吡啶和二氯甲烷等化學試劑,后進行柱層析獲得純的乳糖受體,得率為52%;2)巖藻糖基供體的制備:以L-巖藻糖為原料,經過乙酰化、引入噻吩基、催化脫除乙酸酯反應后,進一步在N,N-二甲基酰胺中進行芐基化反應,過程中以溴化芐為烷化劑、叔丁醇鉀為堿,最終在以四氫呋喃為溶劑的體系中結晶分離出糖基供體,得率為67%~72%;3)糖基化:使用Lemieux 方法,從乙酸乙酯中結晶分離得到晶體,再用甲醇重結晶進一步純化;4)目標產物的分離:去除保護基團、脫除芐基,2′-FL 以白色無定形固體的形式被分離得到,最終得率僅為19.8%~27.3%。
化學合成法涉及的步驟繁瑣、反應條件嚴苛、產率低、底物成本高,且反應過程中大量使用的有機試劑會對環境造成污染,故化學合成法在2′-FL 生產方面暫未實現較大的應用規模[29]。
3.2 酶催化合成法
酶法合成由于具有能夠進行糖苷鍵的特異性合成以及反應條件溫和等優點,獲得了極大的關注。酶催化反應中涉及到的酶主要包括α-1,2-巖藻糖基轉移酶(α-1,2-fucosyltransferases)和α-L-巖藻糖苷酶(α-L-fucosidase)[30],可使用的底物有鳥苷5′-二磷酸-L-巖藻糖(guanosine 5′-diphospho-L-fucose,GDP-L-fucose)、乳糖和4-硝基苯基-α-L-巖藻糖苷(4-nitrophenyl-α-L-fucosidase,pNP-FUC),通過轉糖基反應完成2′-FL 的催化合成,如圖4 所示。
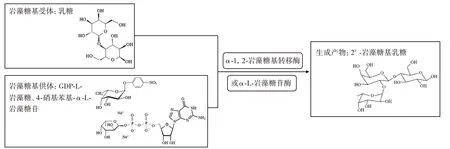
圖4 2′-FL 的酶法合成Fig.4 Enzymatic synthesis of 2′-FL
Shi 等[31]表達了來自土地桿菌屬(Pedobɑctersp.CAU209)的新型α-L-巖藻糖苷酶PbFuc,該酶以pNPFUC 為供體,乳糖為受體催化2′-FL 的合成。該酶對pNP-FUC 及2′-FL 表現出的比活力分別為26.3 U/mg和3.4 U/mg,在pH5.0 和35°C 的條件下,轉化率可達85%,表明PbFuc 在特異性合成2′-FL 方面具有較大的潛力。Liu 等[32]采用計算機輔助設計和篩選與生化試驗相結合的半理性操作,增強了α-1,2-巖藻糖基轉移酶對底物乳糖的識別,與野生型相比,突變體的催化效率提高了100 倍,通過體外酶促法獲得的2′-FL 可達2.56 g/(mL·h)。
與化學法合成相比,酶法合成的反應條件較溫和、易控制,但因當前酶法合成的產量較低、底物GDP-L-巖藻糖成本較高,以及以pNP-FUC 為底物進行合成的產物存在對硝基苯酚污染問題,故其在生產規模及食品領域的應用等方面仍然存在許多限制[33]。未來,繼續發掘能夠替代pNP-FUC 等合成底物的低成本天然底物,同樣是進一步降低酶法合成2′-FL 成本的一種有效方法。
3.3 微生物法
相較于化學法和酶催化法,微生物法合成2′-FL具有易實現大規模生產、可使用廉價原料作為底物等優勢,更容易實現2′-FL 的高水平生產。隨著代謝工程和合成生物學的不斷發展進步,人們不斷探尋微生物中的特定基因,適當地對其加以改造并構建2′-FL合成途徑,在實現2′-FL 工業化、大規模生產方面取得了顯著的成果和突破。
微生物合成2′-FL 的主要代謝途徑包括補救途徑和從頭合成途徑,如圖5 所示。
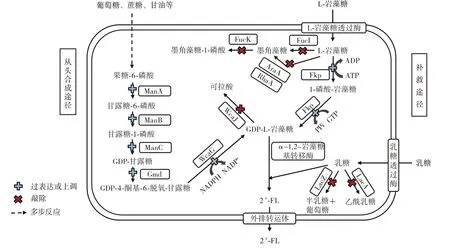
圖5 2′-FL 的從頭合成途徑和補救途徑Fig.5 De novo pathway and salvage pathway of 2′-FL
補救途徑中,首先是具有L-巖藻糖激酶活性和L-巖藻糖-1-磷酸鳥苷酸轉移酶活性的雙功能酶Fkp 將外源添加的巖藻糖轉化為GDP-L-巖藻糖;隨后,乳糖在乳糖透過酶的催化作用下被轉運到宿主細胞內;最后,在外源引入的α-1,2-巖藻糖基轉移酶的催化作用下,巖藻糖殘基從GDP-L-巖藻糖轉移到乳糖上,完成乳糖的巖藻糖基化,最終生成2′-FL[34]。補救途徑以巖藻糖為起始底物,途徑簡單,容易改造,但由于巖藻糖價格昂貴,導致了補救途徑的成本過高而無法實現大規模生產[35]。
從頭合成途徑中,微生物從糖酵解途徑的中間代謝產物果糖-6-磷酸開始合成GDP-L-巖藻糖。該途徑依次經過甘露糖-6-磷酸異構酶、磷酸甘露糖變位酶和甘露糖-1-磷酸鳥苷酸轉移酶的酶促反應得到GDP-甘露糖,然后,在GDP-D-甘露糖-4,6-脫氫酶和GDP-4-酮-6-脫氧-D-甘露糖-3,5-差向異構酶-4-還原酶的催化作用下,生成GDP-L-巖藻糖[36]。最終,由α-1,2-巖藻糖基轉移酶催化乳糖完成巖藻糖基化反應。2′-FL 的從頭合成途徑涉及到的合成步驟相對于補救途徑更復雜一些,但從頭合成途徑可選擇使用蔗糖、葡萄糖、甘油等廉價原料作為底物進行2′-FL 的發酵合成,從而更具有實用價值、更容易實現2′-FL 的規模化生產。
4 2′-巖藻糖基乳糖生產菌種構建
目前,尚未發現能夠自然合成2′-FL 的微生物,需要通過基因工程手段在微生物細胞中構建相關的合成途徑來實現2′-FL 的生產。目前最常用的底盤菌株為大腸桿菌(Escherichiɑcoli),但大腸桿菌不屬于食品安全菌株,對產品純化的要求更高,因此在提高大腸桿菌發酵液的分離純化技術的同時,也在不斷探尋安全性更高的宿主菌株,包括釀酒酵母(Sɑcchɑromycescerevisiɑe)、解脂耶氏酵母(Yɑrrowiɑlipolyticɑ)、枯草芽孢桿菌(Bɑcillussubtilis)、谷氨酸棒桿菌(Corynebɑcterium glutɑmicum)和乳酸乳球菌(Lɑctococcuslɑctis)等。
4.1 大腸桿菌菌種構建
因大腸桿菌具有清晰的遺傳背景、簡單的基因操作被廣泛應用于大規模工業生產中。此外,大腸桿菌自身具有GDP-L-巖藻糖的合成途徑,通過增加GDP-L-巖藻糖的供給和引入α-1,2-巖藻糖轉移酶,就能夠在大腸桿菌中構建2′-FL 合成的代謝途徑[37]。但大腸桿菌本身胞內的GDP-L-巖藻糖積累量少,同時大部分已知的α-1,2-巖藻糖轉移酶活性較低,因此,需要經過大量的代謝工程改造才能實現2′-FL 的高效合成。
4.1.1 提高底物的積累量
2′-FL 合成的關鍵中間體GDP-L-巖藻糖的積累是2′-FL 生產的限制因素,因此通常從加強GDP-L-巖藻糖的合成及阻斷GDP-L-巖藻糖的旁路代謝通量兩個方面進行代謝工程改造。為了提高工程大腸桿菌中GDP-L-巖藻糖的積累量,通常需要過表達2′-FL 從頭合成途徑中的關鍵基因,包括mɑnA、mɑnB、mɑnC、gmd和wcɑG等。此外,作為從頭合成途徑中最后一步WcɑG催化反應的關鍵輔因子NADPH,過表達其合成酶,包括NADH 激酶和葡萄糖-6-磷酸脫氫酶[38],也能夠達到這一目的。在阻斷GDP-L-巖藻糖的旁路代謝通量方面,敲除GDP-L-巖藻糖轉化為可拉酸代謝途徑中的關鍵基因wcɑJ,對巖藻糖的積累具有促進作用[39]。
同時,作為合成2′-FL 另一底物的乳糖,增加其輸入到細胞中的通量也至關重要。但當大腸桿菌以葡萄糖作為細胞生長的碳源,乳糖由乳糖操縱子中的乳糖透過酶(LacY)轉運時,乳糖轉運會受到分解代謝阻遏(catabolite repression,CR),限制了細胞中用于巖藻糖基化反應的乳糖供應,從而減少了2′-FL 的產生。Park 等[40]從E.coliBL21 的lac 操縱子上解除CR,并使用lac 啟動子取代tac 啟動子,使lac 操縱子可以啟動的同時解除了菌株受到的CR 影響,從而顯著提高2′-FL的產量,達到了40 g/L。Ni 等[41]利用lɑcZ突變的E.coliC41(DE3)ΔZ 構建了工程化細胞工廠,并采用了一對正調控因子RcsA 和RcsB 來促進GDP-L-巖藻糖的形成,使2′-FL 產量達到6.86 g/L。
4.1.2 優化2′-FL 合成途徑中的關鍵酶
除了調節GDP-L-巖藻糖的積累量之外,限速酶α-1,2-巖藻糖基轉移酶的活性也是微生物合成2′-FL 的關鍵限制因素。Li 等[42]通過引入多級代謝工程策略,進行GDP-L-巖藻糖合成模塊的基因組合優化,進一步使用RBS 篩選、融合肽段和多拷貝基因克隆等手段提高限速酶的催化性能,并通過分析2′-FL 合成途徑中的關鍵中間體、切斷競爭途徑使得碳通量流向2′-FL的生成,最終在3 L 發酵罐中通過補料分批培養的2′-FL 產量達64.62 g/L。Liu 等[43]采用核糖體結合位點、融合肽和酶基因協同修飾的組合工程策略,增強α-1,2-巖藻糖基轉移酶的可溶性表達并提高其酶活性,在E.coli(DE3)PlySs 中使用優化的核糖體結合位點區域驅動3×FLAG 作為融合伴侶與α-1,2-巖藻糖基轉移酶同時進行表達,最終蛋白產量和酶活顯著提高,分別提高了11.51 倍和13.72 倍,促進了2′-FL 的生產。
目前使用的α-1,2-巖藻糖基轉移酶大多是致病菌幽門螺桿菌來源的FucT2 和FutC,Chin 等[44]使用脆弱擬桿菌來源的WcfB 進行2′-FL 的合成,使其產量提高了10 倍。因此,從其他微生物中挖掘高催化活性的α-1,2-巖藻糖基轉移酶以進一步優化2′-FL 的生物合成,仍是未來研究的重要方向。Chen 等[45]將來自生脂固氮螺菌(Azospirillumlipoferum)的α-1,2-巖藻糖基轉移酶SAMT 整合至大腸桿菌染色體中,同時敲除了lɑcZ和wcɑJ基因并引入調控因子RcsA 和RcsB,在5 L 發酵罐中通過分批補料發酵,使2′-FL 產量達到112.56 g/L。
此外,Chen 等[46]采用空間合成生物學策略,利用能夠相互作用的肽段序列,構建了由相關途徑酶組成的多酶復合物,通過自組裝改善了大腸桿菌中2′-FL 生物合成途徑酶的空間組裝。與表達游離酶和未組裝酶的對照菌株相比,試驗組的2′-FL 合成通量提高了2.1倍,達到25.1 g/L,為2′-FL 的合成提供了新的思路。
4.1.3 補救途徑中的代謝改造
相比于從頭合成途徑,補救途徑生產成本較高,但其途徑簡單、容易改造,在2′-FL 生產方面仍然具有較大的潛力。首先,增強Fkp 的表達是提高補救途徑中胞內GDP-L-巖藻糖含量的主要方法。GTP 是Fkp 的關鍵限速底物,通過過表達gsk基因從而加強GTP 的再生、優化GTP 的供應,已被證實有利于增強2′-FL 的合成[47]。提高α-1,2-巖藻糖基轉移酶的活性、阻斷巖藻糖的分解代謝等措施在補救途徑的代謝改造中同樣適用。Chin 等[48-49]在工程菌株E.coliBL21star(DE3)中引入脆弱擬桿菌(Bɑcteroidesfrɑgilis)來源的Fkp 和幽門螺桿菌(Helicobɑcterpylori)來源的Fuct2 構建了2′-FL 補救途徑,首先使用來自大腸桿菌K12 的含有lacZ△M15 的乳糖操縱子替換了原本的內源性乳糖操縱子,并在FucT2 的N 端加入了3 個天冬氨酸分子進一步提高2′-FL 的合成,發酵后2′-FL 產量為6.4 g/L。考慮到巖藻糖分解代謝途徑中的兩個關鍵酶L-巖藻糖異構酶(L-fucose isomerase,FucI)和L-墨角藻糖激酶(L-fuculose kinase,FucK)會分解巖藻糖并產生相關副產物,在構建了2′-FL 補救途徑的基礎上又敲除了fucIfucK基因簇和編碼降解乳糖的β-半乳糖苷酶基因lɑcZ,最終使2′-FL 胞外濃度達到23.1 g/L。除了FucI和FucK 之外,阿拉伯糖異構酶(arabinose isomerase,AraA)和鼠李糖異構酶(rhamnose isomerase,RhaA)也能夠催化巖藻糖異構化,不利于巖藻糖的積累。Jung等[50]構建了ɑrɑA和rhɑA基因缺失菌株,使2′-FL 的產量達到47 g/L,相比于對照菌株提高了2 倍。
同時構建補救途徑與從頭合成途徑也可以提高2′-FL 的生物合成。Li 等[51]將2′-FL 從頭合成途徑和補救途徑共同構建到單一的工程菌株E.coliBL21(DE3)中,導入了fucT2基因,并利用CRISPR/Cas9 系統使lɑcZ、fucI、fucK和wcɑJ基因失活,通過改變質粒拷貝數對不同的靶基因進行調控以提高2′-FL 的生物合成,使2′-FL 產量達到14.1 g/L。
4.1.4 菌種構建的新思路
近年來,隨著合成生物學與代謝工程的不斷發展,嘗試使用更多的代謝工程方法及工具進行2′-FL 生產菌種的構建。Sun 等[52]采用理性的精細調控途徑基因表達和非理性的實驗室適應性進化組合策略來提高2′-FL 積累,對2′-FL 合成途徑基因的表達進行單拷貝或多拷貝精細調控,并在此基礎上刪除分支途徑基因、過表達2′-FL 外排蛋白SetA 和果糖-1,6-二磷酸酶GlpX,得到的菌株在5 L 發酵罐中的2′-FL 產量為46.06 g/L。隨后進行實驗室適應性進化,獲得了耐受性提高的rpoC基因突變株,該菌株2′-FL 產量為61.06 g/L,生產強度可達1.70 g/(L·h),是目前相關報道的最高生產強度。
除此之外,在合成途徑關鍵基因(如mɑnC-mɑnB和gmd-wcɑG)處利用強組成型啟動子替代原有的啟動子,將額外的wbgL(α-1,2-巖藻糖基轉移酶編碼基因)表達盒整合到recA位點[53];增加futC的基因拷貝數并在FutC 的N 端融合TrxA 標簽[54]等途徑精細調控優化措施已被用來提高2′-FL 合成,并取得了一定成效。為了簡化產物純化過程、避免抗生素在具有營養用途的產品中殘留,Baumg?rtner 等[55]將途徑基因整合到大腸桿菌的染色體上,實現2′-FL 的無抗生素全細胞合成,最終得到2′-FL 濃度為20.28 g/L。使用蛋白質工程對α-1,2-巖藻糖基轉移酶進行改造,通過對FutC-配體底物對接分析,發現了可以提高FutC 溶解度和活性的突變位點,其中4 個突變位點的組合(F40S/Q150H/C151R/Q239S)使2′-FL 產量提高了2.4 倍[40]。
4.2 釀酒酵母菌種構建
釀酒酵母(Sɑcchɑromycescerevisiɑe)作為GRAS 菌株,具有合成2′-FL 的理想特性,如細胞內含有豐富的GDP-巖藻糖前體物質GDP-甘露糖,以及缺乏乳糖的分解代謝能力。在2018 年首次報道了通過代謝工程改造釀酒酵母[56],成功實現了2′-FL 的生物合成,但產量較低,以乙醇為碳源進行發酵獲得的2′-FL 僅有503 mg/L。之后,Xu 等[57]注意到釀酒酵母存在無法攝入乳糖、不能合成GDP-巖藻糖等問題,需要轉入異源乳糖轉運蛋白以及表達GDP-巖藻糖合成相關基因,于是在釀酒酵母中表達大腸桿菌來源的gmd、wɑcj基因,實現了GDP-巖藻糖的有效合成。另外,在α-1,2-巖藻糖基轉移酶的選擇方面,從不同微生物中挖掘鑒定潛在的α-1,2-巖藻糖基轉移酶,其中采用蠟樣芽孢桿菌中的FutBc 實現了較高的2′-FL 產量,比常用的幽門螺桿菌來源的α-1,2-巖藻糖基轉移酶(FutC)提高了1.8 倍。進一步通過強化GDP-甘露糖的合成、敲除半乳糖誘導型啟動子的主要轉錄抑制因子gɑl80后,得到2′-FL 的產量為26.63 g/L[58]。雖然利用釀酒酵母產生的2′-FL 與工程大腸桿菌相比在產量上仍然有一定的差距,但研究結果對于開發食品級微生物細胞工廠、實現2′-FL 的商業化、規模化經濟生產具有巨大潛力。
4.3 枯草芽孢桿菌菌種構建
枯草芽孢桿菌(Bɑcillussubtilis)同樣是GRAS 菌株,在食品級產品的微生物合成中被廣泛使用,通過引入fkp、futC等基因在枯草芽孢桿菌中構建了2′-FL 補救途徑[59],過表達L-巖藻糖轉運蛋白基因(glcP)、引入異源乳糖滲透酶基因(lɑcY、lɑc12)以及消除內源性β-半乳糖苷酶基因(yesZ),改善了L-巖藻糖和乳糖的輸入、避免了乳糖的降解。此外,通過微調輔因子GTP再生模塊基因(gmd、ndk、guɑA、guɑC、ykfN、deoD和xpt)的表達提高了GDP-L-巖藻糖的積累量,最終該菌的2′-FL 產量達到了5.01 g/L。隨后,Zhang 等[60]在枯草芽孢桿菌中引入大腸桿菌和幽門螺旋桿菌來源的mɑnB、mɑnC、gmd、wcɑG和futC基因構建了2′-FL 從頭合成途徑,通過減少競爭性乳糖消耗、增加輔因子GTP 的再生和前體甘露糖-6-磷酸(M6P)的供應進一步提高2′-FL 產量,同時,使用組成型啟動子P7 替換編碼M6P 異構酶的內源性mɑnA基因的天然啟動子,最終在不添加抗生素和化學誘導劑的情況下,使2′-FL產量達到了88.3 g/L。由此可見,通過改造枯草芽孢桿菌工程菌,亦可實現2′-FL 的高效合成。
已報道的部分2′-FL 生產菌株如表1 所示。
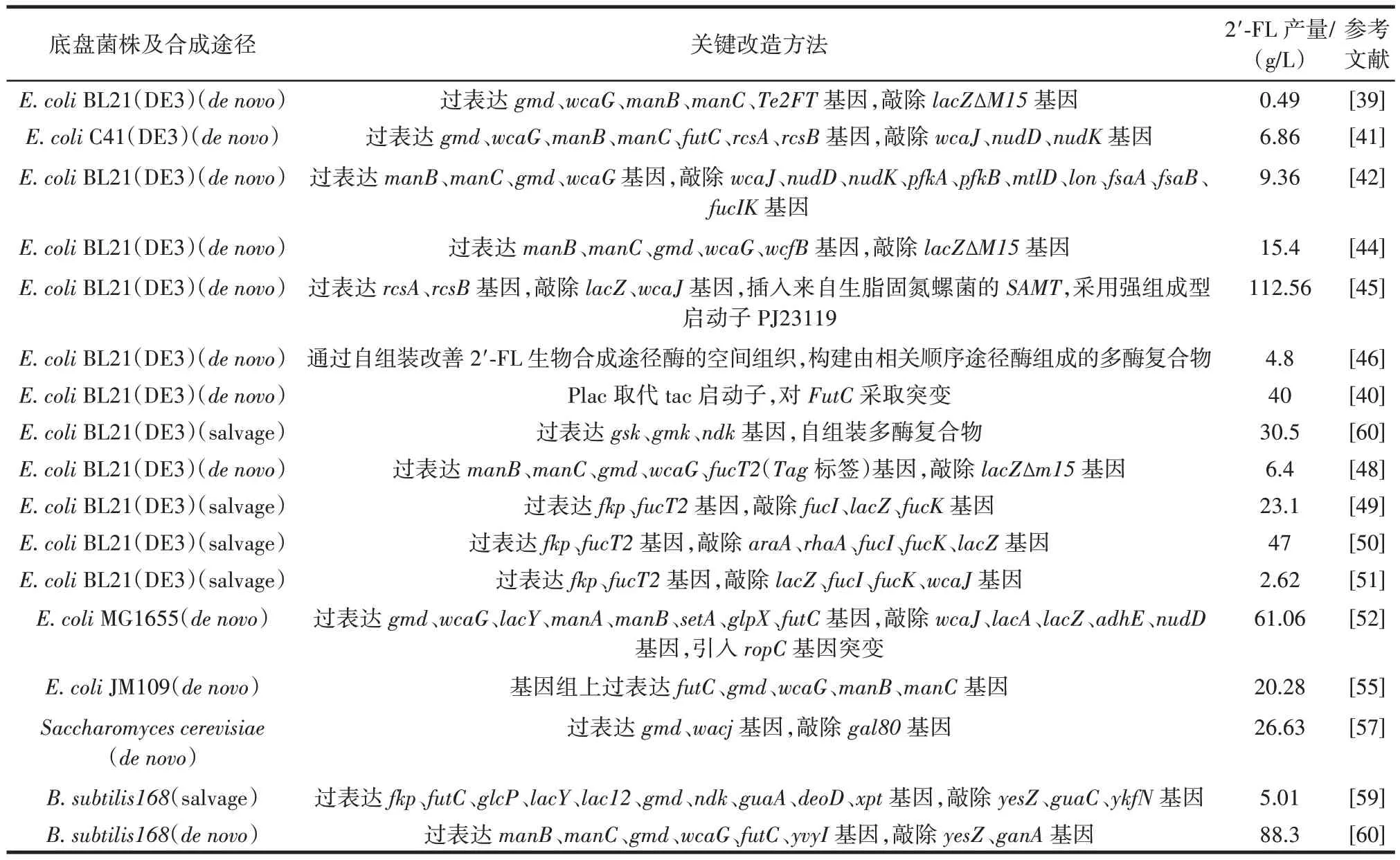
表1 已報道的部分2′-FL 生產菌株Table 1 Some reported 2′-FL producing strains
5 結論與展望
目前,2′-FL 的合成主要通過化學合成、酶法合成和基因工程微生物發酵來實現,其中,構建2′-FL 高產微生物具有易實現大規模生產、可使用廉價原料作為底物等優勢,被認為是極具前景的生產方式。構建高效的重組菌株是2′-FL 工業化生產的重要任務。
大腸桿菌是目前合成2′-FL 最主要的工程菌種,可對其代謝途徑進一步優化以提高其合成效率,包括提高GDP-巖藻糖的積累量、優化2′-FL 合成途徑中的關鍵酶、提高菌種的耐受性等。考慮大腸桿菌不屬于食品安全菌株,已嘗試構建釀酒酵母、枯草芽孢桿菌、谷氨酸棒桿菌等食品安全級的工程菌來進行2′-FL 的生物合成,目前報道的產量較低,但結合代謝工程、啟動子工程、蛋白質工程、發酵工程等多種改造策略,有望進一步提高產量。隨著2′-FL 生產菌株的高效合成、提取技術的優化以及相關應用準則的批準,2′-FL在食品、醫藥等領域具有更加廣闊的應用前景。

