慢性腎臟病非透析患者心臟瓣膜鈣化的影響因素及對預后的影響
陳雅玲 康儒典 張建福
【摘要】 目的:探討慢性腎臟病(chronic kidney disease,CKD)非透析患者心臟瓣膜鈣化(cardiac valve calcification,CVC)的影響因素及對預后的影響。方法:回顧性選取2019年3月—2021年3月福建醫科大學附屬泉州第一醫院收治的CKD非透析患者312例為研究對象,收集患者的一般情況、實驗室檢查及心臟彩超等資料。隨訪截止時間為2022年6月。分析CKD非透析患者CVC的影響因素,以及CVC與預后的關系。結果:CVC組年齡、高血壓史和糖尿病史比例均高于非CVC組(P<0.05);CVC組總膽固醇和腎小球濾過率水平均低于非CVC組(P<0.05);CVC左心室肥厚率高于非CVC組(P<0.05)。logistic回歸結果顯示,年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚均為CVC的影響因素(P<0.05);CVC組患者的全因死亡率34.31%較非CVC組的2.86%高(P<0.05)。結論:年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚均為CKD非透析患者CVC的影響因素,CVC可以增加該類患者的全因死亡率。
【關鍵詞】 慢性腎臟病 非透析 心臟瓣膜鈣化 影響因素 預后
慢性腎臟病(chronic kidney disease,CKD)是指腎功能不全,導致血肌酐水平持續升高,腎小球濾過率(glomerular filtration rate,GFR)降低的一種疾病[1]。CKD患者除了腎臟功能受損外,還伴隨著多種系統性并發癥,其中心臟病是較為常見的一種。心臟瓣膜鈣化(cardiac valve calcification,CVC)是心臟病的一種,其發生率在CKD患者中較高。CKD患者中存在著大量的炎癥因子,這些因子會導致血管內皮細胞的損傷,使得血管壁的通透性增加[2]。同時,CKD患者中存在著大量的代謝產物,這些產物在循環系統中沉積和堆積,導致血管內皮細胞的損傷進一步加劇。這些因素都可能導致CVC的發生。有研究顯示,CVC為CKD患者發生心血管疾病及全因死亡的有效預測因子[3]。因此,研究CKD患者CVC的相關因素及其對預后的影響十分有必要。查閱相關文獻后發現,目前關于CKD患者CVC相關因素的研究以透析治療患者居多,關于非透析患者CVC相關因素的研究較少[4]。基于此,本研究選取2019年3月—2021年3月福建醫科大學附屬泉州第一醫院收治的CKD非透析患者312例為研究對象,分析其CVC的影響因素及對預后的影響,現報道如下。
1 資料與方法
1.1 一般資料
回顧性選取2019年3月—2021年3月本院收治的CKD非透析患者312例為研究對象,收集患者的一般情況、實驗室檢查及心臟彩超等資料。納入標準:均符合CKD的診斷標準[5];年齡≥18歲。排除標準:行透析治療;存在嚴重的感染或合并惡性腫瘤;依從性較差;資料不全;非中國國籍。本研究已經本院醫學倫理委員會批準。
1.2 方法
在全面查閱相關中英文文獻之后,多次向權威專家征詢意見,確定研究的方向和實施的具體方案。收集患者的資料,包括:性別、年齡、高血壓史、糖尿病史;血紅蛋白、血尿素氮、總膽固醇、腎小球濾過率、骨型堿性磷酸酶、血鈣、血磷水平;左室收縮末內徑、左室射血分數、肺動脈內徑、左心室肥厚指標值。
1.3 觀察指標
(1)CVC組和非CVC組一般情況比較。(2)CVC組和非CVC組實驗室檢查指標比較。(3)CVC組和非CVC組患者的心臟彩超比較。(4)CKD非透析患者CVC的多因素分析。(5)CVC組和非CVC組全因死亡率比較。
1.4 統計學處理
采用SPSS 23.0軟件對本次研究收集到的數據進行統計學分析,滿足正態分布的計量資料,采用(x±s)描述,行t檢驗;計數資料以率(%)描述,行字2檢驗。采用logistic回歸分析CKD非透析患者CVC的影響因素。檢驗水準α=0.05,以P<0.05表示差異有統計學意義。
2 結果
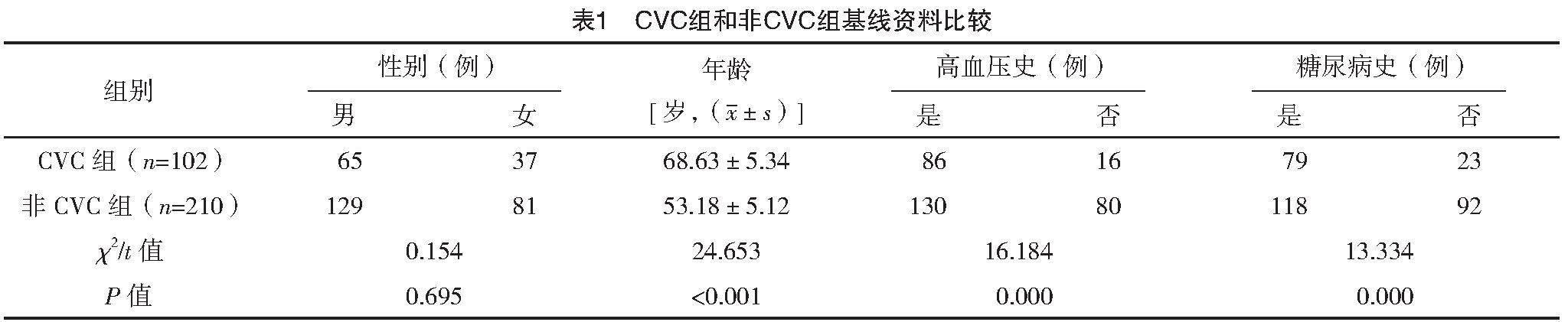
2.1 CVC組和非CVC組基線資料比較
根據CVC情況將患者分為CVC組(n=102)和非CVC組(n=210),CVC發生率為32.69%(102/312)。隨訪截止時間為2022年6月,死亡41例。CVC組年齡、高血壓史和糖尿病史比例均高于非CVC組(P<0.05)。見表1。
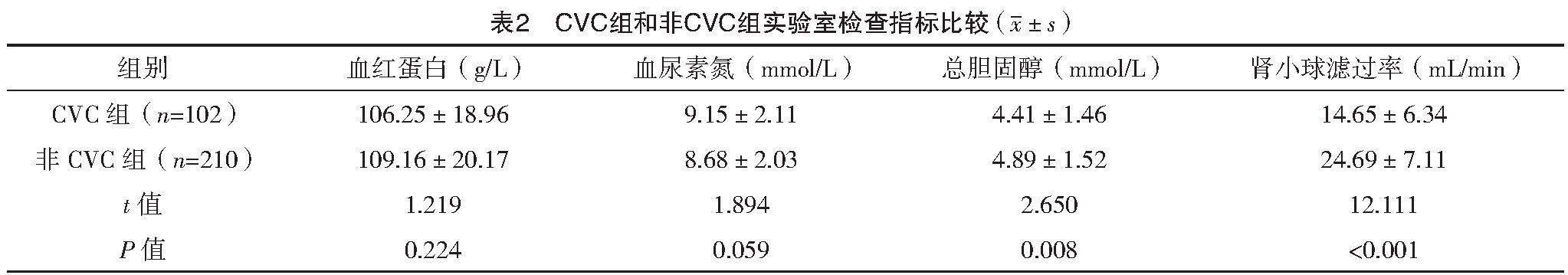
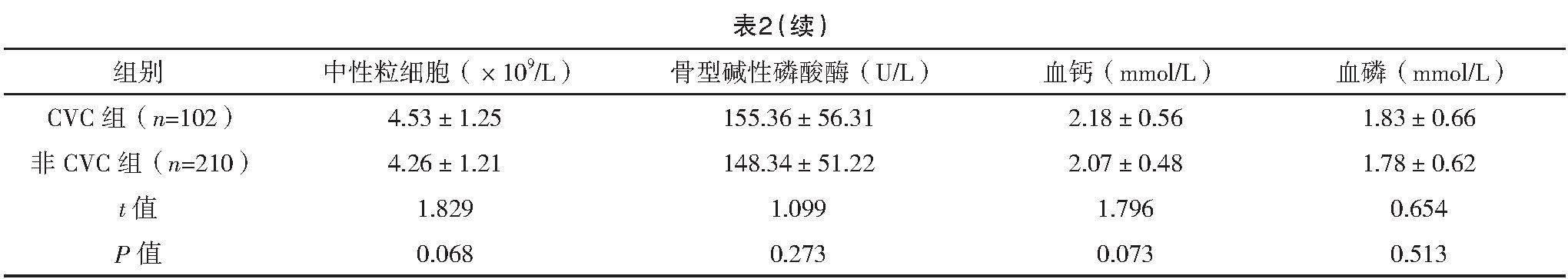
2.2 CVC組和非CVC組實驗室檢查指標比較
CVC組總膽固醇和腎小球濾過率水平均低于非CVC組(P<0.05),見表2。
2.3 CVC組和非CVC組心臟彩超比較
CVC組左心室肥厚率高于非CVC組(P<0.05),見表3。
2.4 CKD非透析患者CVC的多因素分析
以是否患CVC作為應變量(否=0;是=1),將單因素有統計學意義的變量年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚率作為自變量進行賦值。logistic回歸結果顯示,年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚均為CVC的影響因素(P<0.05)。見表4、表5。
2.5 CVC組和非CVC組全因死亡率比較
CVC組全因死亡率34.31%較非CVC組的2.86%高(字2=57.449,P=0.001),見表6。
3 討論
CVC是CKD患者中較為常見的一種心血管并發癥,其發生與CKD中的高磷血癥、高鈣血癥、炎癥反應、血管鈣化、糖尿病等多種因素有關[6]。因此,對于CKD患者,應該加強對心血管并發癥的預防和治療,同時注意控制血磷、血鈣和血糖水平,減輕炎癥反應,從而降低CVC的風險[7]。
本研究結果顯示:CVC組年齡、高血壓史和糖尿病史比例均高于非CVC組(P<0.05);CVC組總膽固醇和腎小球濾過率水平均低于非CVC組(P<0.05);CVC組左心室肥厚率高于非CVC組(P<0.05);logistic回歸結果顯示,年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚均為CVC的影響因素(P<0.05);CVC組患者的全因死亡率34.31%較非CVC組的2.86%高(P<0.05)。以上結果說明,年齡大、高血壓、糖尿病、左心室肥厚率高均會增加CKD非透析患者CVC的發病風險,總膽固醇水平、腎小球濾過率水平更高,越不易發生CVC。李文等[8]的研究顯示,CKD 1~5期非透析患者CVC的發生率為32.32%;高齡、更差的腎功能及合并高脂血癥為CKD患者出現CVC的獨立危險因素,高齡、低蛋白血癥及雙瓣膜鈣化為CKD患者全因死亡的獨立危險因素。與本研究結果近似。同時,還有相關研究顯示,年齡、高血壓、糖尿病、總膽固醇水平等為CKD非透析患者發生CKC的影響因素,與本研究結果近似[9-12]。
分析以上結果產生原因為:(1)隨著年齡的增長,體內的鈣離子含量增高,同時老年人的腎臟功能下降,導致鈣離子代謝紊亂,容易出現心臟瓣膜鈣化[13]。(2)高血壓可導致心血管系統的血管壁受損,血液中的脂質、蛋白質等物質滲入心臟瓣膜組織內,促進鈣鹽沉積,加速瓣膜鈣化進程。此外,高血壓還會增加心臟負荷,導致心室肥厚和左心室增大,從而影響瓣膜的正常功能,進一步促進瓣膜鈣化[14]。因此,伴有高血壓的CKD患者更容易發生CVC。(3)糖尿病是一種慢性代謝性疾病,是CKD的常見病因之一。糖尿病患者中血糖水平持續升高,導致內皮細胞損傷和血管通透性增加,從而導致CVC的發生[15]。(4)膽固醇是心臟瓣膜細胞生長和修復所必需的營養物質。膽固醇水平正常或偏高可使心臟瓣膜細胞正常生長和修復,使得心臟瓣膜不容易受到破壞。此外,膽固醇水平正常或偏高還會減少血管壁的損傷和炎癥反應,進而減少CKC的發生[16]。(5)CKD患者腎小球濾過率水平正常或偏高,患者的腎功能損傷可能較輕微,發生血中鈣、磷等礦物質代謝異常的風險較小。鈣磷代謝異常可導致磷酸鹽沉積于瓣膜組織中,從而引起瓣膜鈣化。此外,腎功能損傷可能導致內分泌系統紊亂,如甲狀腺激素、維生素D等的代謝異常,也會導致CKC的發生[17-18]。(6)左心室肥厚往往是由于高血壓引起的,在高血壓的情況下,心臟需要更大的壓力來推動血液流動,這會導致心臟負擔增加,進而影響心臟功能,使心臟瓣膜結構發生改變。同時,左心室肥厚還與神經內分泌系統失衡密切相關,隨著疾病的進展,會導致產生一系列的代謝和內分泌激素的變化,這些變化會對心臟的瓣膜功能產生影響,造成CKC[19-20]。(7)CVC與心血管事件的發生有關,如心血管死亡、心肌梗死、腦卒中等,因此對CKD患者的預后產生了重要的影響[21]。因此,在CKD患者中進行早期發現和治療CKC、控制危險因素,對保護心血管健康具有重要的臨床價值。尤其是年齡大的CKD患者,需要更加重視CVC的防治工作,合理地控制自身的慢性疾病,改善生活習慣、保持良好的心態和心理狀態,以減少CVC的發生率。
綜上所述,年齡、高血壓史、糖尿病史、總膽固醇、腎小球濾過率、左心室肥厚均為CKD非透析患者CVC的影響因素,CVC可以增加該類患者的全因死亡率。
參考文獻
[1] ZHANG Y,HE D,ZHANG W,et al.ACE Inhibitor benefit to kidney and cardiovascular outcomes for patients with non-dalysis chronic kidney disease stages 3-5: a network meta-analysis of randomised clinical trials[J].Drugs,2020,80(8):797-811.
[2] OTOBE Y,RHEE C M,NGUYEN M,et al.Current status of the assessment of sarcopenia, frailty, physical performance and functional status in chronic kidney disease patients[J].Curr Opin Nephrol Hypertens,2022,31(1):109-128.
[3]陳曉玲,鄭茗丹,向玥.慢性腎臟病病人血鎂水平與心臟瓣膜鈣化的關系探討[J].中西醫結合心腦血管病雜志,2022,20(16):3030-3034.
[4]魏懷志,張蕾.慢性腎臟病與透析患者心臟瓣膜鈣化的研究進展[J/OL].世界最新醫學信息文摘(連續型電子期刊),2019,19(93):78-79.https://d.wanfangdata.com.cn/periodical/ChlQZXJpb2RpY2FsQ0hJTmV3UzIwMjMxMjI2EhFzanp4eXktZTIwMTk5MzAzOBoINGNrNnRyemc%3D.
[5] STEVENS P E,LEVIN A,KIDNEY D I G O.Evaluation and management of chronic kidney disease: synopsis of the kidney disease: improving global outcomes 2012 clinical practice guideline[J].Annals of Internal Medicine,2013,158(11):825-830.
[6] ABDELAZEEM B,SHEHATA J,ABBAS K S,et al.The efficacy and safety of roxadustat for the treatment of anemia in non-dialysis dependent chronic kidney disease patients: an updated systematic review and meta-analysis of randomized clinical trials[J/OL].PLoS One,2022,17(4):e0266243.https://pubmed.ncbi.nlm.nih.gov/35363823/.
[7]汪曉晨,王立婷,湯日寧,等.慢性腎臟病患者心臟瓣膜鈣化的研究進展[J].中華腎臟病雜志,2020,36(11):876-880.
[8]李文,賈林沛,董星彤,等.慢性腎臟病非透析患者心臟瓣膜鈣化的影響因素及對預后的影響[J].中華腎臟病雜志,2022,38(9):794-801.
[9]洪維,肖婧,傅辰生,等.老年慢性腎臟病3~5期非透析患者心臟瓣膜鈣化特點及其與血清骨代謝標志物的相關性[J].中國臨床醫學,2020,27(4):639-644.
[10]湯日寧,汪曉晨,王立婷,等.慢性腎臟病患者心臟瓣膜鈣化新危險因素分析[J].中國全科醫學,2021,24(11):1365-1371.
[11]邵雪,郭永力,張隆業,等.血清骨特異性堿性磷酸酶在慢性腎臟病3~5期患者心臟瓣膜鈣化中的作用[J].國際移植與血液凈化雜志,2022,20(3):13-16.
[12]米紅巖,李澤民.終末期腎臟病和血液透析患者心臟瓣膜鈣化的影響因素分析[J].中國衛生標準管理,2022,13(19):85-89.
[13]鐘瑩瑩,李亞迪.尿毒癥高通量血液透析患者心臟瓣膜鈣化發生情況及其影響因素分析[J].臨床醫學工程,2022,29(12):1775-1776.
[14] BELLIZZI V,GAROFALO C,FERRARA C,et al.Ketoanalogue supplementation in patients with non-dialysis diabetic kidney disease: a systematic review and meta-analysis[J].Nutrients,2022,14(3):441.
[15] ZHENG L,TINA J,LIU D,et al.Efficacy and safety of roxadustat for anaemia in dialysis-dependent and non-dialysis-dependent chronic kidney disease patients: a systematic review and meta-analysis[J].Br J Clin Pharmacol,2022,88(3):919-932.
[16]閆奇奇,郝麗,張森.慢性腎臟病患者血清FGF23水平與鈣磷代謝及臨床相關性[J].安徽醫科大學學報,2019,54(5):776-780.
[17] BRIGUORI C,MATHEW R O,HUANG Z,et al.Dialysis initiation in patients with chronic coronary disease and advanced chronic kidney disease in ISCHEMIA-CKD[J/OL].J Am Heart Assoc,2022,11(6):e022003.https://pubmed.ncbi.nlm.nih.gov/35261290/.
[18]王云丹,王應燈.老年慢性腎臟病患者外周血中性粒細胞/淋巴細胞比值與超敏C反應蛋白及心臟瓣膜鈣化的相關性[J].老年醫學與保健,2020,26(1):29-33.
[19] AKIZAWA T,TANAKA-AMINO K,OTSUKA T,et al.Clinical parameters among patients in Japan with anemia and non-dialysis-dependent chronic kidney disease with and without diabetes mellitus who received roxadustat[J].Clin Exp Nephrol,2022,26(9):843-850.
[20]汪曉晨.慢性腎臟病患者心臟瓣膜鈣化的危險因素分析[D].南京:東南大學,2020.
[21]劉海軍,楊秀芹,宋慶慶,等.慢性腎臟病非透析患者發生心臟瓣膜鈣化的危險因素分析[J].山東醫學高等專科學校學報,2021,43(3):170-172.

