Imoto比色法測定殼寡糖含量的研究
譚佩毅,黃秀錦
(江蘇食品職業技術學院,江蘇淮安 223003)
Imoto比色法測定殼寡糖含量的研究
譚佩毅,黃秀錦
(江蘇食品職業技術學院,江蘇淮安 223003)
從標準品的選擇、波長選定、試劑用量、比色條件、線性關系等方面研究了Imoto比色法測定殼寡糖含量的最佳條件。結果表明,測定波長為438nm,比色最佳條件為10g/L鐵氰化鉀3.5mL、0.5mol/L Na2CO33.5mL、水浴加熱時間85min、加熱溫度95℃;以氨基葡萄糖鹽酸鹽作為標準對照品,濃度在0~60μg/mL范圍內線性關系良好。采用該比色法測得水解液中殼寡糖含量為39.77μg/mL,RSD值為2.15%。
殼寡糖,Imoto比色法,氨基葡萄糖鹽酸鹽
殼聚糖(Chitosan)是甲殼素部分脫乙酰基后的產物[1],具有顯著的生物生理活性[2]和良好的功能性質,已在食品、化妝品、生物制藥、農業、環境保護以及廢水處理等領域中都得到了應用[3]。但由于殼聚糖分子量較大,分子間及分子內存在大量的氫鍵,使得殼聚糖分子結構緊密,且只能溶解于稀乙酸等酸性溶液中形成透明狀的黏液[4-5],因此殼聚糖在以上領域中的應用很大程度上受到了限制。殼寡糖(chitooligosaccharides)又稱寡聚氨基葡糖,是殼聚糖降解后得到的由2~10個氨基葡糖通過β-1,4-糖苷鍵連接而成的低聚糖[6]。殼寡糖是天然糖中唯一大量存在的堿性氨基寡糖[7],由于分子量和聚合度較低,溶解性和吸收率較好,易于被人體、動物及植物機體吸收利用[8],因此,在保健品、營養劑、食品添加劑等方面都具有良好的應用價值。殼寡糖來源廣泛,安全無毒,水溶性好,有多種生物活性,已引起國內外醫藥研究者的廣泛關注。但測定殼寡糖含量的方法尚不成熟,目前基本采用測定D-氨基葡萄糖的方法間接測定殼寡糖含量,目前氨基葡萄糖常見的測定方法有Elson-Morgan法[9-10]、Imoto法[11-12]、苯酚-硫酸法[13]和3,5-二硝基水楊酸法(DNS法)[14]。其中Elson-Morgan法操作繁瑣且回收率低,不適用于氨基糖與乙酰氨基糖混合的體系;苯酚-硫酸法顯色較淺,不適于氨基糖及乙酰氨基糖類物質的測定;DNS法有較好的顯色效果,但此法的靈敏度略低[15];Imoto法具有顯色效果較好,可用于測定氨基糖與乙酰氨基糖混合的體系,且靈敏度較高,穩定性好,重復性好[16]。本實驗分別從標準品的選擇、吸收波長的確定、試劑用量及線性關系等方面進行考察,確定Imoto比色法測定殼寡糖含量的最佳條件,并通過重現性、回收率等實驗對該方法進行考察。
1 材料與方法
1.1 材料與儀器
殼寡糖(黃色粉末) 自制;葡萄糖、氨基葡萄糖、乙酰氨基葡萄糖、氨基葡萄糖鹽酸鹽 Sigma公司;HCl、鐵氰化鉀、無水Na2CO3均為分析純。
TU-1900紫外可見分光光度計 北京普析通用儀器有限責任公司;SHA-C恒溫水浴鍋 上海醫療器械廠;JA1003A電子精密天平 上海倫捷機電儀表有限公司。
1.2 實驗方法
1.2.1 溶液的配制
1.2.1.1 標準溶液的配制 精確稱取40℃真空干燥至恒重的葡萄糖、氨基葡萄糖、乙酰氨基葡萄糖、氨基葡萄糖鹽酸鹽對照品各100.00mg,置于100mL容量瓶中,加水溶解并定容至刻度,搖勻即得1mg/mL對照品儲備液[17]。
1.2.1.2 10g/L鐵氰化鉀溶液的配制 準確稱取1.00g鐵氰化鉀置于100mL棕色容量瓶中,去離子水定容,搖勻備用。
1.2.1.3 0.5mol/L Na2CO3溶液的配制 準確稱取5.30g無水Na2CO3置于100mL容量瓶中,加入50mL溫水,攪拌溶解后冷卻至室溫,加水定容至100mL。
1.2.1.4 殼寡糖溶液的配制 準確稱取1.00g殼寡糖置于100mL容量瓶中,用0.5mol/L乙酸溶液定容至100mL,振蕩溶解后備用。
1.2.2 殼寡糖水解液的制備 準確量取殼寡糖溶液1mL置入小燒杯中,沿壁緩緩加入4mL 6mol/L HCl溶液,混合后置于沸水浴中水浴4h,流水冷卻后備用[5]。1.2.3 比色條件的確定
1.2.3.1 標準品及波長的選擇 分別量取葡萄糖、氨基葡萄糖、乙酰氨基葡萄糖、氨基葡萄糖鹽酸鹽標準溶液和殼寡糖水解液各1.0mL置于25mL比色管中,分別加入3mL鐵氰化鉀和3mL Na2CO3溶液,加水定容至25mL,具塞搖勻,用鋁箔封住比色管口,置于沸水浴中30min[12],冷卻后以去離子水做基線,用紫外-可見分光光度計在300~800nm波長范圍內進行掃描,得到葡萄糖、氨基葡萄糖、乙酰氨基葡萄糖、氨基葡萄糖鹽酸鹽經褪色反應后的吸收光譜,并與殼寡糖水解液經褪色反應后的吸收光譜進行比較,以選擇最適標準品,同時確定最大吸收波長。
1.2.3.2 鐵氰化鉀溶液添加量的確定 取潔凈25mL比色管7支,分別加入殼寡糖水解液各1mL,再依次加入0、1.0、2.0、3.0、4.0、5.0、6.0mL鐵氰化鉀溶液,然后分別加入Na2CO3溶液5mL,按照1.2.3.1所示方法在最大吸收波長處測定吸光度值,考察鐵氰化鉀溶液添加量對褪色效果的影響。
1.2.3.3 Na2CO3溶液添加量的確定 取潔凈25mL比色管7支,分別加入殼寡糖水解液和鐵氰化鉀,再依次加入0、1.0、2.0、3.0、4.0、5.0、6.0mL Na2CO3溶液,按照1.2.3.1所示方法在最大吸收波長處測定吸光度值,考察Na2CO3溶液添加量對褪色效果的影響。
1.2.3.4 水浴加熱時間的確定 取潔凈25mL比色管10支,分別加入殼寡糖水解液、鐵氰化鉀和Na2CO3溶液,按照1.2.3.1所示方法分別置于沸水浴中加熱,每隔10min取出一管在最大吸收波長處測定吸光度值,考察加熱時間對褪色效果的影響。
1.2.3.5 水浴加熱溫度的確定 取潔凈25mL比色管6支,分別加入殼寡糖水解液、鐵氰化鉀和Na2CO3溶液,按照1.2.3.1操作后分別置于50、60、70、80、90、100℃水浴鍋中加熱,取出冷卻后在最大吸收波長處測定吸光度值,考察加熱溫度對褪色效果的影響。
1.2.3.6 正交實驗 依據單因素實驗結果,以鐵氰化鉀添加量、Na2CO3添加量、水浴加熱時間、水浴加熱溫度為考察因素,以吸光度值為考察指標,采用L9(34)正交實驗設計,分析各因素對吸光度的影響,以確定最佳比色條件,正交實驗平行兩次。因素水平見表1。
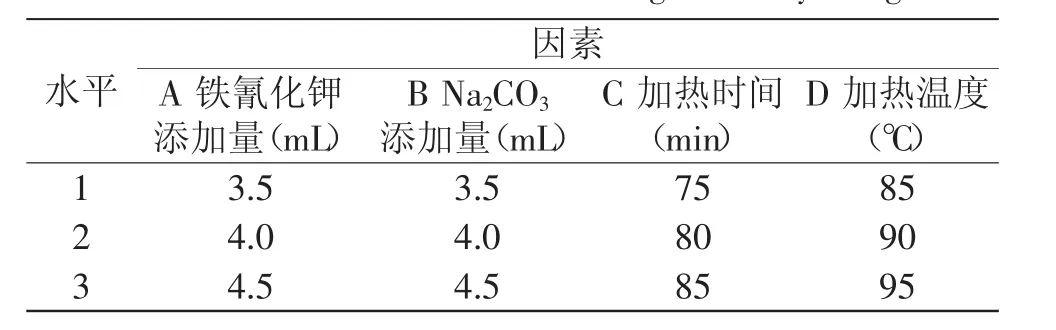
表1 正交試驗因素水平表Table 1 Factors and levels in orthogonal array design
1.2.4 標準曲線的繪制 依據1.2.3確定的各最適條件,分別吸取0、0.50、1.00、1.50、2.00、2.50、3.00mL 1.0mg/mL氨基葡萄糖鹽酸鹽標準溶液于50mL容量瓶中,分別加入鐵氰化鉀和Na2CO3溶液,混勻,水浴加熱后,以去離子水做空白,繪制標準曲線。
1.2.5 回收率實驗 為考察方法的準確度,采用加標回收率法,向已知殼聚糖含量的殼寡糖水解液中加入不同量的標準品,分別測定其殼聚糖含量,并計算其回收率和相對標準偏差,以評價該比色方法的準確度和可靠性。
1.2.6 數據處理分析方法 采用北京普析UVWin5 V 5.1.0進行紫外掃描光譜圖圖繪制,采用Spss Statistics 17.0統計學軟件和Excel軟件對正交實驗結果進行方差分析和極差分析。
2 結果與分析
2.1 比色條件的確定
2.1.1 標準品及波長的選擇 Imoto法的原理是黃綠色鐵氰酸離子在堿性條件下能被還原糖還原成微黃色的亞鐵氰酸離子。若反應中鐵氰化鉀過量,還原糖含量與生成的亞鐵氰化鉀的濃度呈正比關系,與反應液的顏色成反比關系[11]。據文獻報道,各種還原糖和鐵氰化鉀反應情況和最大吸收波長有所不同[18],選擇合適的標準品和合適的最大吸收波長才能準確測量出殼聚糖的含量。
由圖1可知,各標準品和殼寡糖水解液與鐵氰化鉀反應后在420~450nm范圍內有一最大吸收峰。這是因為吸光度主要由殘留的鐵氰酸和生成的亞鐵氰化鉀產生,標準品和水解液發生反應后都是以這兩種物質為主,但各種標準品最大吸收波長略有不同,這可能是因為各種標準品氧化后的產物有一定的吸光度,從而調高或降低了溶液的吸光度。各標準品中,氨基葡萄糖鹽酸鹽的最大吸收波長最大(438nm)、葡萄糖和氨基葡萄糖次之(435nm),乙酰氨基葡萄糖最大吸收波長最小(425nm)。氨基葡萄糖鹽酸鹽和殼寡糖水解液均在438nm處吸收最強,這可能是因為殼寡糖在鹽酸作用下水解的產物以氨基葡萄糖鹽酸鹽為主,與氨基葡萄糖鹽酸鹽結構最為相似,因此選擇以氨基葡萄糖鹽酸鹽為標準品,以438nm為最大吸收測定波長。
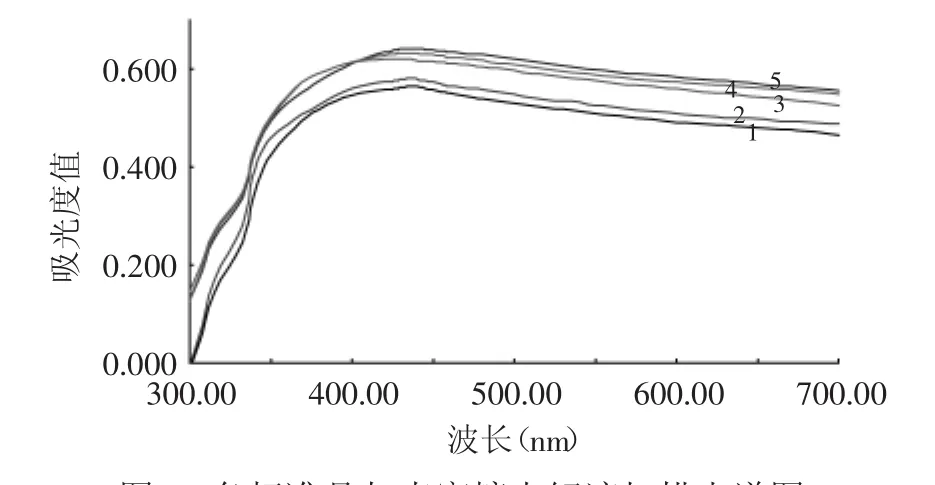
圖1 各標準品與殼寡糖水解液掃描光譜圖Fig.1 Scanning spectrums of 4 standard samples and hydrolysate
2.1.2 鐵氰化鉀溶液添加量的確定 通過添加0.0、1.0、2.0、3.0、4.0、5.0、6.0mL鐵氰化鉀溶液,分別考察對吸光度的影響,結果見圖2。
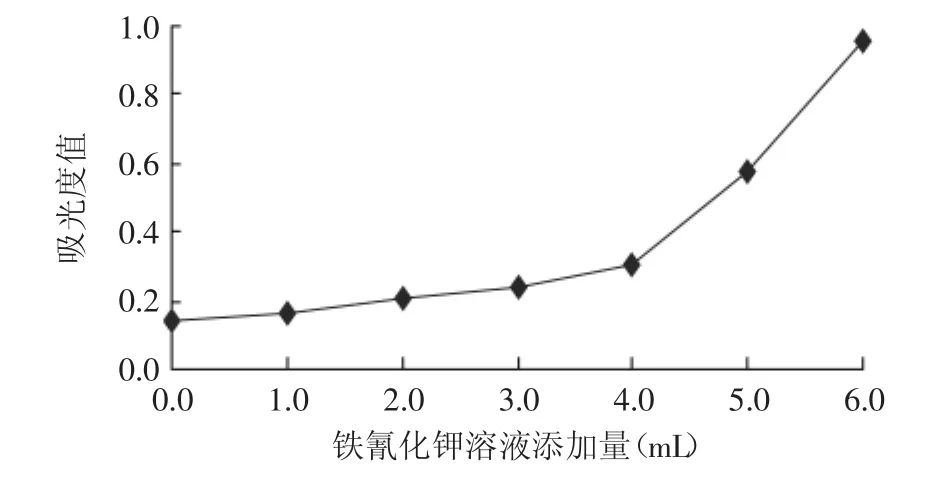
圖2 鐵氰化鉀溶液添加量對吸光度的影響Fig.2 Effect of addition of potassium ferricyanide reagent on absorbency
由圖2可知,隨著鐵氰化鉀溶液添加量的增加,溶液的吸光度值先緩慢增加,而當溶液增加到4.0mL后,吸光度值呈線性增加趨勢。這主要是因為少量的鐵氰化鉀加入后立即與溶液中的氨基葡萄糖鹽酸鹽反應生成吸光度值較小的亞鐵氰化鉀和幾乎沒有吸光度值的氨基葡萄糖酸,而顏色較深吸光度值較大的鐵氰化鉀幾乎沒有殘留,因此吸光度值增加很小;隨著鐵氰化鉀添加量的不斷增加,溶液中幾乎所有的氨基葡萄糖鹽酸鹽都轉變為氨基葡萄糖酸,且加入的鐵氰化鉀不與任何物質發生反應,此時溶液的吸光度隨著鐵氰化鉀的濃度增加而線性增加。但從反應靈敏度和經濟節約兩方面考慮,鐵氰化鉀溶液添加量以4.0mL較好。
2.1.3 Na2CO3溶液添加量的確定 由圖3可知,吸光度值隨著Na2CO3溶液添加量的增加先緩慢降低后迅速降低,當達到最低點后又略有增加。這主要是因為鐵氰化鉀與氨基葡萄糖鹽酸鹽發生反應需在堿性條件下才能順利進行,只添加鐵氰化鉀,不添加Na2CO3溶液基本不會發生反應,因此不添加Na2CO3時,溶液的顏色較深,吸光度值很大;隨著Na2CO3溶液添加量不斷增大,溶液pH逐漸增加,形成的堿性環境越來越適合鐵氰化鉀與氨基葡萄糖鹽酸鹽發生氧化還原反應,溶液顏色褪去速度增加,吸光度值降低加快;但Na2CO3溶液添加量超過4.0mL時,溶液的pH過大,不適合氧化還原反應,溶液顏色褪去較少。因此選擇Na2CO3溶液添加量為4.0mL較好。

圖3 Na2CO3溶液添加量對吸光度的影響Fig.3 Effect of addition of Na2CO3reagent on absorbency
2.1.4 水浴加熱時間的確定 鐵氰化鉀與氨基葡萄糖鹽酸鹽發生氧化還原反應需要一個過程。實驗發現,加入鐵氰化鉀和Na2CO3后進行加熱,溶液顏色開始緩慢變淡,并隨加熱時間增加而逐漸褪色。
由圖4可知,在80min內吸光度值基本以線性速度遞減,褪色反應迅速,反應液顏色逐漸變淺,這反映了鐵氰化鉀和氨基葡萄糖鹽酸鹽較容易發生化學反應,而80min后吸光度值基本保持不變,表明褪色反應基本完全。因此,選定水浴加熱時間為80min。
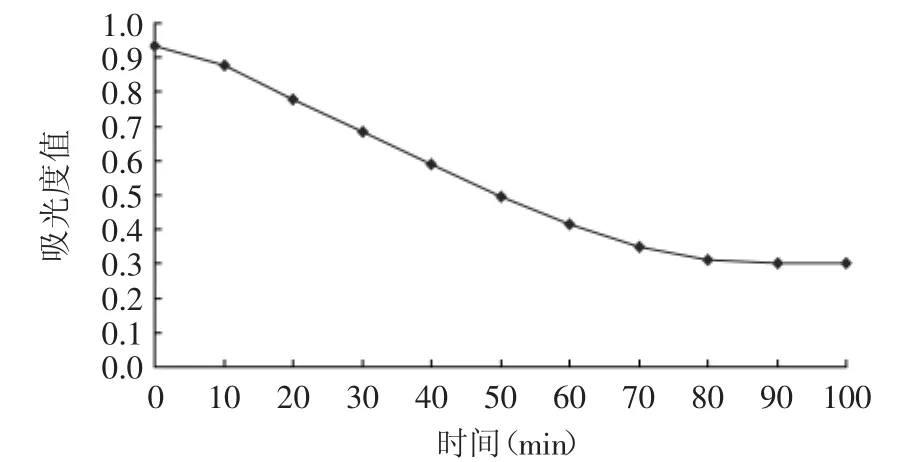
圖4 加熱時間對吸光度的影響Fig.4 Effect of bath time on absorbency
2.1.5 水浴加熱溫度的確定 溫度對顯色反應有很大影響,溫度過低不利于氧化還原反應的進行。由圖5可知,當水浴溫度在60~70℃時,分子能量和運動速度較慢,溶液褪色速度緩慢,吸光度值變化較小。隨著溫度升高,反應速度加快,吸光度值逐漸變小,至90℃時達到最小值,而后當溫度繼續升高時,吸光度值略有增加。這可能是因為長時間的高溫加熱導致水蒸氣增加,溶液濃縮后,顏色亦會有所增加。因此為節省能源,提高實驗準確度,確定水浴加熱溫度為90℃。
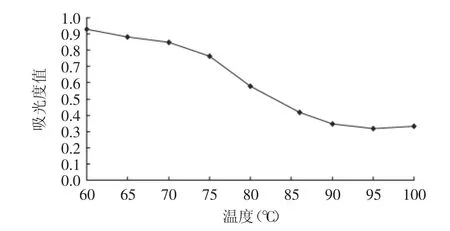
圖5 水浴加熱溫度對吸光度的影響Fig.5 Effect of bath temperature on absorbency
2.1.6 最佳比色條件的確定 在單因素實驗的基礎上,選擇鐵氰化鉀添加量、Na2CO3添加量、水浴加熱時間、水浴加熱溫度為考察因素,進行L9(34)正交實驗,采用Excel 2007對兩次平行實驗結果的均值進行極差分析,結果見表2。利用Spss Statistics 17.0統計學軟件對正交實驗兩次結果及平均值進行方差分析,方差分析結果見表3。
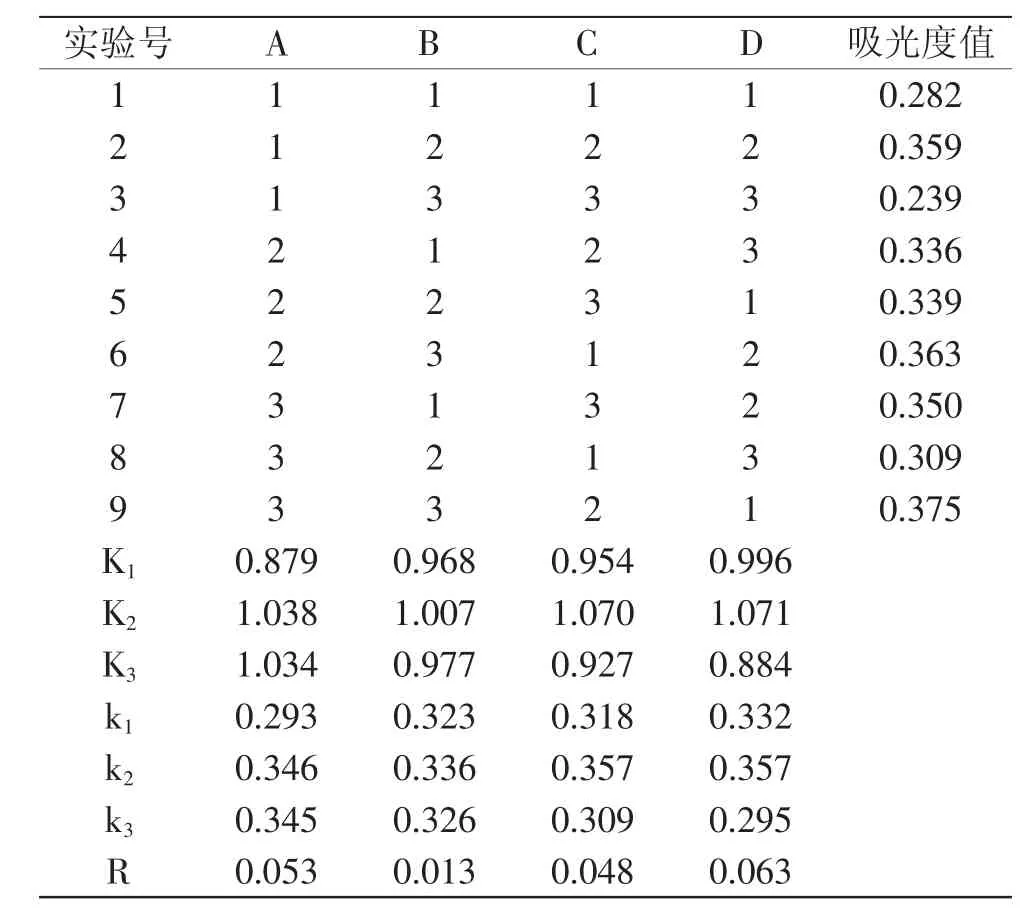
表2 正交實驗結果與極差分析Table 2 Orthogonal test results and range analysis
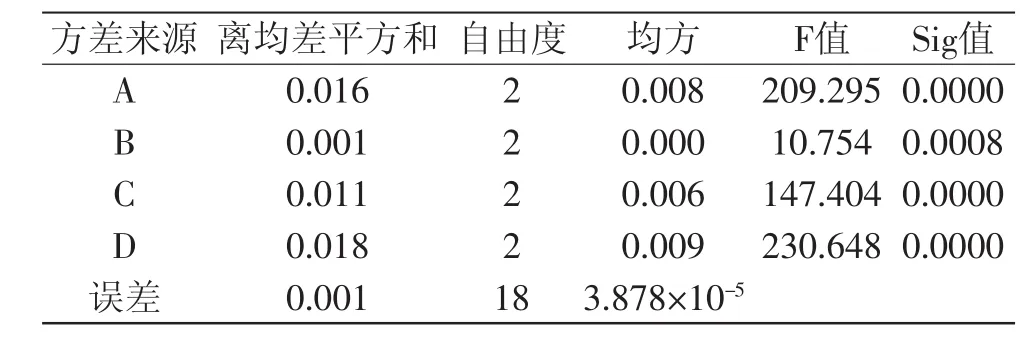
表3 正交實驗結果方差分析Table 3 Analysis of variance of orthogonal test
由表2正交實驗結果中R值可以看出,各因素的影響次序為:D>A>C>B,即加熱溫度對吸光度的影響最大,鐵氰化鉀添加量次之,Na2CO3添加量對吸光度的影響最小。本實驗的最佳組合為A1B1C3D3,即最佳比色條件為:10g/L鐵氰化鉀溶液3.5mL、0.5mol/L Na2CO3溶液3.5mL、水浴加熱時間85min、水浴加熱溫度95℃。
由方差分析結果(表3)可知,誤差項的均方值僅為3.878×10-5,不足均方總和的萬分之一,且四因素對應的Sig值均小于0.01,這說明誤差對吸光度的影響非常小,正交實驗因素選擇正確。表3中四因素對應的F值大小順序為FD>FA>FC>FB,說明四因素對吸光度的影響次序依次為D>A>C>B,與正交實驗極差分析結果相一致。
2.1.7 驗證實驗 A1B1C3D3的比色條件不在正交實驗表中,因此按此比色條件做3次平行實驗進行驗證,結果分別為0.223、0.225、0.222,三數值及平均值(0.223)均小于正交實驗最小值且穩定,即在該條件下,溶液顏色變化最大,為比色的最優條件。
2.2 標準曲線的繪制
根據最佳比色條件,測定不同濃度氨基葡萄糖鹽酸鹽標準品與鐵氰化鉀反應后的吸光度值,并繪制標準曲線(見圖6)。
結果表明,在0~60μg/mL范圍內,其線性回歸方程為y=-0.0137x+0.9288,相關系數R2=0.9990,結果符合朗伯比爾定律,表明線性關系良好。
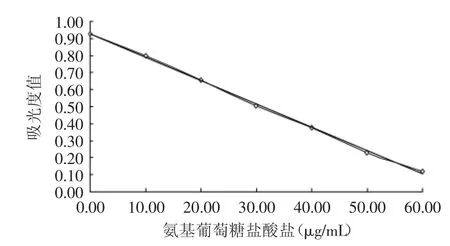
圖6 氨基葡萄糖鹽酸鹽標準曲線Fig.6 Standard curve of glucosamine hydrochloride
2.3 殼寡糖水解液中殼寡糖含量的測定
取殼寡糖水解液進行比色測定(n=7),實驗測得殼寡糖水解液中殼寡糖的平均含量為39.77μg/mL,RSD值為2.15%,表明該測定方法精密度較高,重復性好,能滿足實驗樣品分析的需要。
3 結論
以氨基葡萄糖鹽酸鹽為標準對照品,采用Imoto比色法測定了殼寡糖水解液中殼寡糖的含量,實驗結果表明,氨基葡萄糖鹽酸鹽的最大吸收波長為438nm,且在0~60μg/mL范圍內有良好線性關系;最佳比色條件為:10g/L鐵氰化鉀溶液3.5mL、0.5mol/L Na2CO3溶液3.5mL、水浴加熱時間85min、水浴加熱溫度95℃。
采用Imoto比色法測得殼寡糖水解液中殼寡糖的含量為39.77μg/mL,RSD值為2.15%,表明該方法具有操作簡便、重現性好、回收率較高等優點。
[1]韓永萍,林強.殼聚糖降解制備低聚殼聚糖和殼寡糖的研究進展[J].食品科技,2006(7):35-38.
[2]Kurita K.Chitin and chitosan:functional biopolymers from marine crustaceans[J].Mar Biotechnol,2006,8(3):203-226.
[3]Kim S,Rajapakse N.Enzymatic production and biological activities ofchitosan oligosaccharides(COS):A review[J].Carbohydrate Polymers,2005,62(4):357-368.
[4]孫婷.纖維素酶降解殼聚糖的研究[D].無錫:江南大學,2009.
[5]劉琳,張杰,曾凡駿.過氧化氫法制備特定聚合度殼寡糖的工藝研究[J].食品科技,2011,36(3):88-91.
[6]蔡圣寶,邢榮娥,劉松,等.兩種方法制備殼寡糖平均分子質量與氨基含量分析[J].海洋科學,2009,33(5):70-73.
[7]喬瑩,白雪芳,杜昱光.殼寡糖醫藥保健功能的研究進展[J].中國生化藥物雜志,2008,29(3):210-213.
[8]魏新林,夏文水.甲殼低聚糖的生理活性研究進展[J].中國藥理學通報,2003,19(6):614-617.
[9]李輝,賈宏新,盧桂華.分光光度法測定殼聚糖含量的方法研究[J].中國公共衛生,2002,18(10):1248-1249.
[10]Elson L A,Morgan W T J.A colorimetric method for the determination of glucosamine and chondrosamine[J].Biochemical Journal,1933,27(6):1824-1828.
[11]Imoto T,Yagishita K.A simple activity measurement of lysozyme[J].Agricultural and Biological Chemistry,1971,35(7),1154-1156.
[12]劉靖.纖維素酶水解殼聚糖的特性及機理研究[D].無錫:江南大學,2006.
[13]張惟杰.糖復合物生化研究技術[M].杭州:浙江大學出版社,1999:11.
[14]Miller G L.Use of dinitrosalicylic acid reagentfor determination of reducing sugar[J].Analytical Chemistry,1959,31(3):426-428.
[15]李克成,李鵬程,邢榮娥,等.殼寡糖含量的測定方法比較[J].藥物分析雜志,2011,31(8):1530-1532.
[16]李雪梅,孟慶軍,楊俊慧,等.電化學法測定馬鈴薯全粉中還原糖的含量[J].食品工業科技,2008,29(11):257-259.
[17]張華珺,陳敏.氨基葡萄糖熒光光度分析法的研究[J].食品研究與開發,2009,30(2):100-104.
[18]蘇暢,夏文水,姚惠源.氨基葡萄糖和乙酰氨基葡萄糖的測定方法[J].食品工業科技,2003(6):74-76.
Study on determination of total chitooligosaccharides by Imoto olorimetry
TAN Pei-yi,HUANG Xiu-jin
(Jiangsu Food Science College,Huai’an 223003,China)
A quantitative method for the determination of the total content of chitooligosaccharides was studied by Imoto colorimetry.The method was improved and verified in the aspects of standard sample,wavelength,reagent,colorimetric conditions.The result showed that the chitooligosaccharides content could be well calculated according to their absorption at 438nm by applying 10g/L potassium ferricyanide reagent 3.5mL and 0.5mol/L Na2CO33.5mL at 95℃ for 85min.The linear range of standard curve was 0~60μg/mL with glucosamine hydrochloride as standard.The content of chitooligosaccharides of hydrolysate by the method was 39.77μg/mL(RSD=2.15%).
chitooligosaccharides;Imoto colorimetry;glucosamine hydrochloride
TS254.9
A
1002-0306(2012)22-0071-05
2012-05-10
譚佩毅(1967-),男,碩士,副教授,主要從事應用化學研究。

