60歲以上老年患者肺切除術后并發房顫的危險因素分析
王煜東,李玉,張蘇寧,趙俊剛,魯繼斌
人們的預期壽命增加了,相應地老年肺癌患者的比例也在增加。而手術仍是其首選治療手段。肺癌患者術后并發癥很多,房顫是最常見的一種術后并發癥[1],患者會因此延長住院時間,增加住院費用,甚至誘發腦梗死等嚴重并發癥,因此預防是必要的。有報告顯示,年齡是術后房顫一個獨立的危險因素[2]。為了進一步明確≥60歲老年人肺切除術后房顫的誘因以便及早采取有效的防治措施,有必要對其相關因素進行研究,目前已有一些研究,但結論尚未統一。本研究回顧性分析中國醫科大學附屬第一醫院胸外科過去2年內362例老年患者的臨床資料,對肺切除術后誘發房顫的危險因素進行單因素分析及多因素Logistic回歸分析,為預防術后房顫及治療提供科學依據。
1 材料及方法
1.1 納入標準
2010年12月至2012年12月于中國醫科大學附屬第一醫院胸外科接受肺切除術。年齡≥60歲的老年患者。依據術后心電監護及心電圖結果診斷為房顫,診斷標準以人民衛生出版社第7版《診斷學》教材為依據。
1.2 排除標準
術前發生房顫者,由于難以確定是術中或術后因素所致,因此不計入術后影響房顫因素的分析。
1.3 臨床資料
2010年12月至2012年12月于中國醫科大學附屬第一醫院胸外科接受肺切除術年齡≥60歲的老年患者共370例,其中8例因有術前房顫已被排除。
納入研究中的362例患者年齡60~83歲,平均年齡66歲,其中60~70歲共266例,70歲以上96例;男226例,女136例;有吸煙史172例;飲酒史44例;心律失常病史22例;冠心病病史34例;高血壓病病史84例;糖尿病病史52例;術前心電圖檢查異常者116例;心臟射血分數≤60%72例;FEV2≤70%68例;PaO2≤80 mmHg 77例。
開胸手術350例;全肺手術23例,肺葉切除手術296例,楔形切除43例;左胸切口171例;手術時長大于2 h 140例;心包內操作15例;術中輸血16例;淋巴結清掃303例;惡性病變324例;本組患者除2例死亡(1例心梗,1例肺梗)外,其余經積極治療后均治愈。
1.4 統計分析方法
采用SPSS 19.0統計學軟件進行分析,先采用χ2檢驗進行單因素分析或必要時使用連續校正χ2檢驗,再采用Logistic回歸模型進行多因素分析,P<0.05為差異有統計學意義。
2 結果
本組362例患者中,共52例發生房顫,發生率為14.36%,按照年齡分為2組(≥60且<70歲;≥70歲),分析術后房顫的發生規律,如圖1。
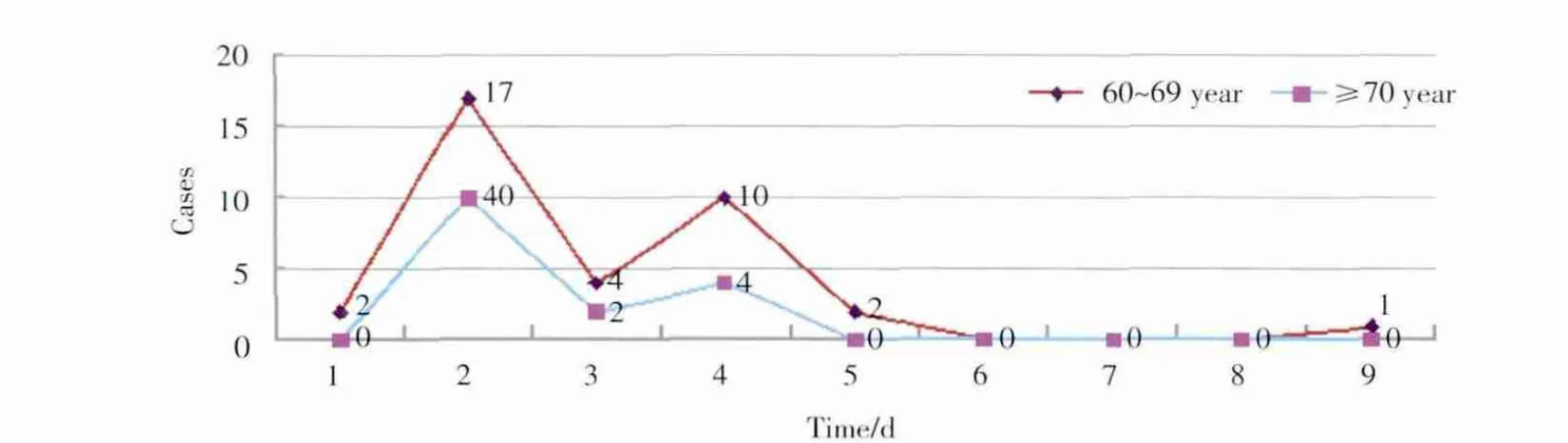
圖1 術后房顫時間分布圖Fig.1 Time distribution of atrial fibrillation after operation
對各個因素進行單因素χ2檢驗(不滿足條件時應用連續校正χ2檢驗或Fisher確切概率),結果顯示:術后房顫與冠心病史、切除范圍、手術入路、心包內操作、淋巴結清掃、病變良惡性相關(P<0.05);與年齡、性別、吸煙史、飲酒史、心律失常史、高血壓史、糖尿病史、ECG異常、射血分數、FEV2、PaO2、手術方式、手術時長、術中輸血無明顯相關性,見表1。
對有意義的結果進行多因素Logistic回歸分析,結果顯示:術后房顫與冠心病史、切除范圍、手術入路、心包內操作相關(P<0.05),見表2。
3 討論
肺癌術后并發癥很多,但房顫為較早期也較常見的一種。肺癌術后發生房顫的原因復雜,目前尚無統一意見,公認的是多因素的,國內外文獻報道的發生率差異也較大。
國內外報道的肺切除術后房顫發生率一般在10%~25%之間,本組362例患者中共52例發生房顫,發生率為14.36%。研究顯示術后出現房顫的高發時間為術后前3 d,3 d后明顯減少[3],有學者認為可能與術后PaO2的波動有關,曾對胸外科患者術后進行動態血氣分析監測,發現剖胸手術后PaO2在術后1~2 d最低,此期最易發生房顫,術后第3天PaO2開始逐漸回升,發生率開始減少。本組患者術后前3 d發生的房顫占總房顫94.2%。
高齡對于肺切除術后發生房顫有很重要的影響,這一點已經被廣泛認同。有研究顯示高齡組與低齡組患者肺切除術后房顫發生率的差異有統計學意義(P<0.05)[4]。人在老化過程中心臟細胞的自律性及傳導性均減退,心房內細胞凋亡及纖維化增多,易發生傳導延遲及傳導折返,從而導致房顫。有研究顯示75歲以上老年人只有10%左右的竇房結細胞具有正常活力[5]。本組研究在此基礎上比較了高齡患者2個亞組分別為60~70歲及70歲以上(80歲以上只有1例),比較后發現這兩個高齡亞組中第二組發生率略高于第一組,但是差異并沒有統計學意義,且兩亞組在術后房顫高峰分布上亦無明顯差別。Hung?Chang等[6]研究發現雖然老年肺癌患者手術后會出現比年輕患者更多的并發癥,尤其是心肺系統并發癥,但其無進展生存期及遠期生存率的結果均比年輕患者更好。身體適合手術的老年患者不應被視為單純地按照年齡肺切除術的禁忌證。
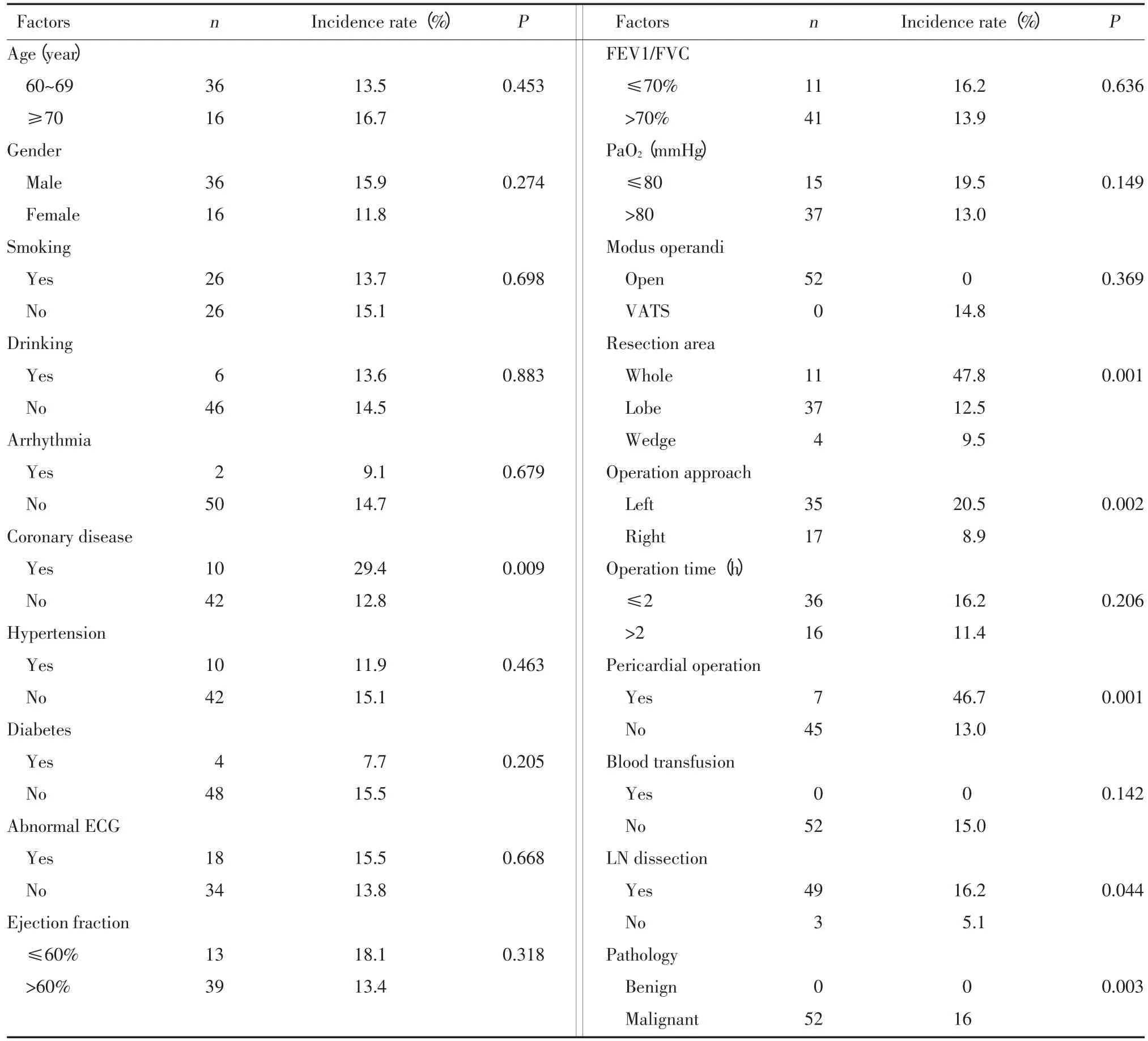
表1 術后房顫單因素分析Tab.1 Single factor analysis of atrial fibrillation after operation

表2 術后房顫多因素Logistic回歸分析Tab.2 Multi?factors analysis of atrial fibrillation after operation
缺血性心臟病對術后房顫有很重要的影響。本組病例中,有冠心病病史組術后房顫發生率明顯高于無冠心病組(P=0.009),差異有統計學意義,可能是由于本研究對象均為老年人。這說明原發的心臟病史對術后房顫有很重要的影響。有研究發現,雖然心血管并發癥會增加手術的風險,但不會影響非小細胞肺癌的肺切除后的患者的長期預后[7]。
術前肺功能對術后房顫的發生有預測作用,術前肺功能差者術后發生并發癥的比例可以高達44%[9]。FEV1/FVC≤70%則提示患者存在明顯的通氣功能障礙,如小氣道痙攣、狹窄、肺氣腫等。本組資料顯示FEV1/FVC≤70%的患者發生房顫的機率稍有增高,但差異無統計學意義(P=0.636)。由于條件有限,如果能獲得房顫發生時的肺功能等指標與術前相比較,也許更有意義。
手術本身對術后房顫的發生有很重要的影響。本組病例中,全肺切除后房顫發生率是47.8%(11/23),明顯高于肺葉切除及楔形或局部切除術(P=0.001)。經左胸手術術后房顫發生率明顯高于經右胸手術(20.5%、8.9%,P=0.002),因該院全肺切除患者中大部分為左全肺切除術,而全肺切除對術后房顫有很大的影響,故左側切口發生率更高,為了降低單因素分析后數據之間干擾,多因素Lo?gistic回歸分析結果顯示,手術切口對術后房顫的影響差異有統計學意義(P=0.034),可能由于左側手術更靠近肺靜脈根部的心房異常起搏點。因為有研究認為肺靜脈是房顫的異常起搏點,高達94%的房顫異位興奮點起源于此,特別是上肺靜脈根部2~4 cm的區域[1]。心房壁與肺靜脈之間相互延伸,互相包繞,肺靜脈根部很可能是心房傳導纖維的通路之一。當切斷結扎肺靜脈根部纖維時,很可能阻斷或者干擾了正常的房室傳導或者興奮激發了異位起搏點,從而產生房顫[5]。另外,有研究認為全肺切除后房顫與肺血管床減少,增加了右心的后負荷,改變了血流動力學穩定有關[8]。
同樣,心包內操作也是通過心包無菌性反應對心房產生刺激造成房顫[8],在本研究中,心包內操作對術后房顫影響的差異有統計學意義(P=0.001)。
有研究表明胸腔鏡手術的術后并發癥總體較開胸手術低[10],本研究顯示,胸腔鏡手術后房顫發生率比開胸手術低,但差異并無有統計學意義(P=0.369)。
本組病例中,淋巴結清掃術后房顫發生率與未行淋巴結清掃術相比,差異有統計學意義(P=0.044)。這可能與縱隔及肺門處自主神經受損有關。心臟受兩側迷走神經和交感神經共同支配,清除淋巴結時極易損傷肺門及縱隔處的迷走和交感神經[11]。
肺癌組術后房顫發生率比肺良性腫瘤組術后房顫發生率高,差異具有統計學意義(P=0.003),但可能并非惡性腫瘤本身所致,首先,惡性腫瘤一般需要擴大切除范圍,相對局部切除術,損傷更大,損失肺功能及肺血管床更多,極易造成心臟負荷增加;其次,惡性腫瘤常常需要廓清淋巴結,有的淋巴結呈侵襲性生長,侵犯周圍心臟相關神經,廓清時損傷神經在所難免。再者,惡性腫瘤患者年齡一般年長較多,身體基礎疾病較多,若合并冠心病等病史,也易誘發術后房顫。多因素分析結果顯示此差異無統計學意義(P=0.998),證實了這種改變由別的因素而來。
綜上所述,60歲以上老年患者肺切除術后發生房顫的高峰時間為術后1~3 d,并且60歲以上老年患者中70歲以下與70歲以上兩組之間肺切除術后房顫發生率無明顯差別,兩組的房顫高峰分布差別亦不明顯。60歲以上老年患者肺切除術后房顫發生率與冠心病史、切除范圍、手術入路、心包內操作相關(P<0.05)。術前采取干預措施,術中減少對心包和肺組織的損傷可以減少術后房顫的發生率。
[1]Góme Z?Caro A,Moradiellos FJ,Ausín P,et al.Risk factors for atri?al fibrillation after thoracic surgery[J].Arch Bronconeumol,2006,42(1):9-13.
[2]Asamura H,Naruke T,Tsuchiya R,et al.What are the risk factors for arrhythmias after thoracic operations?A retro?spective multivari?ate analysis of 267 consecutive thoracic operations[J].J Thorac Car?diovasc Surg,1993,106(6):1104-1110.
[3]Roselli EE,Murthy SC,Rice TW,et al.Atrial fibrillation complicat?ing lung cancer resection[J].J Thorac Cardiovasc Surg,2005,130(2):438-444.
[4]VaporciyanAA,Correa AM,Rice DC,et al.Risk factors associated with atrial fibrillation after noncardiac thoracic surgery:analysis of 2588 patients[J].J Thorac Cardiovasc Surg,2004,127(3):779-786.
[5]Ciriaco P,Mazzone P,Canneto B,et al.Supraventricular arrhythmia following lung resection for non?small cell lung cancer and its treat?ment with amiodarone[J].Eur J Cardiothorac Surg,2000,18(1):12-16.
[6]Liu HC,Huang WC,Wu CL,et al.Surgery for elderly lung cancer[J].Ann Thorac Cardiovasc Surg,2013,19(6):416-422.
[7]Takenaka T,Katsura M,Shikada Y,et al.The impact of cardiovascu?lar comorbidities on the outcome of surgery for non?small?cell lungcancer[J].Inter Cardio Vas Thor Surg,2013,16(3):270-274.
[8]Foroulis CN,Kotoulas C,Lachanas H,et al.Factors associated with cardiac rhythm disturbances in the early post?pneumonectomy peri?od:a study on 259 pneumonectomies[J].Eur J Cardiothorac Surg,2003,23(3):384-389.
[9]Kearney DJ,Lee TH,Reilly JJ,et al.Assessment of operative risk in patients undergoing lung resection.Importance of predicted pulmo?nary function[J].Chest,1994,105(3):753-759.
[10]Park BJ,Zhang H,Rusch VW,et al.Video?assisted thoracic sur?gery does not reduce the incidence of postoperative atrial fibrilla?tion after pulmonary lobectomy[J].J Thorac Cardiovasc Surg,2007,133(3):775-779.
[11]Rena O,Papalia E,Oliaro A,et al.Supraventricular arrhythmias af?ter resection surgery of the lung[J].Eur J Cardiothorac Surg,2001,20(4):688-693.

