福莫司汀預(yù)防完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移療效觀察
黃 堃,鄺先奎,韓 偉,趙向通,閆 焱,董文杰,王麗萍
(1.鄭州大學(xué)第一附屬醫(yī)院腫瘤科,河南 鄭州 450052;
2.項(xiàng)城市第一人民醫(yī)院腫瘤科,河南 周口 466200)
?
福莫司汀預(yù)防完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移療效觀察
黃堃1,鄺先奎2,韓偉1,趙向通1,閆焱1,董文杰1,王麗萍1
(1.鄭州大學(xué)第一附屬醫(yī)院腫瘤科,河南 鄭州 450052;
2.項(xiàng)城市第一人民醫(yī)院腫瘤科,河南 周口 466200)
[摘要]目的觀察福莫司汀對完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移的預(yù)防作用。方法68例完全緩解期小細(xì)胞肺癌患者隨機(jī)分為2組。治療組31例給予福莫司汀100 mg·m-2,靜脈滴注,d1,8,21 d為1周期,重復(fù)2周期;對照組37例給予定期復(fù)查。比較15個(gè)月內(nèi)2組腦轉(zhuǎn)移發(fā)生率、無疾病進(jìn)展生存期、1 a生存率。結(jié)果治療組腦轉(zhuǎn)移發(fā)生率低于對照組,無疾病進(jìn)展生存期長于對照組,差異有統(tǒng)計(jì)學(xué)意義(P均<0.05);2組1 a生存率比較差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)論早期應(yīng)用福莫司汀可降低完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移發(fā)生風(fēng)險(xiǎn),延長患者無疾病進(jìn)展生存期。
[關(guān)鍵詞]小細(xì)胞肺癌;福莫司汀;預(yù)防;完全緩解期;腦轉(zhuǎn)移
小細(xì)胞肺癌屬于神經(jīng)內(nèi)分泌腫瘤,約占肺癌的13%~18%,2013年美國約有31 000例新增小細(xì)胞肺癌病例[1]。小細(xì)胞肺癌惡性程度高,具有倍增時(shí)間快、早期廣泛轉(zhuǎn)移的特征,如未接受治療,生存期一般僅2~4個(gè)月,聯(lián)合化療是治療小細(xì)胞肺癌的基石,目前推薦治療為依托泊苷+順鉑聯(lián)合化療4~6周期方案[2]。初治的廣泛期小細(xì)胞肺癌化療有效反應(yīng)率為60%~70%,中位生存期9個(gè)月,相比之下,局限期患者中位生存可達(dá)18個(gè)月,甚至通過規(guī)律化療、放療的多峰性治療,長期無病生存率可達(dá)20%~25%[3]。小細(xì)胞肺癌具有早期播散趨勢,約25%的患者初診時(shí)已伴發(fā)腦轉(zhuǎn)移,而隨著疾病進(jìn)展,2 a內(nèi)腦轉(zhuǎn)移發(fā)生率可達(dá)到80%,即使是完全緩解期小細(xì)胞肺癌,2 a內(nèi)腦轉(zhuǎn)移發(fā)生率也超過50%,目前,腦轉(zhuǎn)移被認(rèn)為是影響肺癌預(yù)后的一個(gè)獨(dú)立因素[4-5]。因此,預(yù)防中樞神經(jīng)系統(tǒng)轉(zhuǎn)移被公認(rèn)是提高小細(xì)胞肺癌疾病控制的一項(xiàng)重要挑戰(zhàn)。
小細(xì)胞肺癌遠(yuǎn)處轉(zhuǎn)移以腦部為主,主要因?yàn)檠X屏障使腦組織中抗腫瘤藥物濃度明顯低于腦外組織,使腦成為腫瘤細(xì)胞逃避化療藥物殺滅的避難所。福莫司汀為亞硝基脲類中的抑制細(xì)胞增殖的抗腫瘤藥物,具有烷基化和氨甲酰化活性,化學(xué)結(jié)構(gòu)式含有一個(gè)丙氨酸的生物電子等配體(氨基-1-乙基磷酸),具有高脂溶性、游離度低、相對分子質(zhì)量小、易于穿透細(xì)胞和通過血腦屏障等特點(diǎn)[6]。本研究主要觀察福莫司汀對預(yù)防完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移的臨床療效,現(xiàn)將結(jié)果報(bào)道如下。
1資料與方法
1.1臨床資料入組2013年8月至2014年6月鄭州大學(xué)第一附屬醫(yī)院收治經(jīng)病理確診的小細(xì)胞肺癌(包括無腦轉(zhuǎn)移的廣泛期病例)68例,均滿足以下條件:1)年齡20~70歲,ECOG評分0~2分,預(yù)期生存時(shí)間>12周;2)白細(xì)胞≥4×109·L-1,血小板≥100×109·L-1,血紅蛋白≥90 g·L-1;3)肌酐和總膽紅素≤正常上限值1.5倍,谷丙轉(zhuǎn)氨酶、谷草轉(zhuǎn)氨酶升高和堿性磷酸酶≤正常上限值2.5倍;4)至少有一個(gè)在徑線上可精確測量的病灶(記錄為最大直徑);5)均規(guī)律接受依托泊苷+順鉑聯(lián)合化療6周期,根據(jù)WHO實(shí)體瘤療效評價(jià)標(biāo)準(zhǔn),誘導(dǎo)治療療效評價(jià)完全緩解;6)無其他惡性腫瘤病史。排除條件:轉(zhuǎn)移性或原發(fā)性腦轉(zhuǎn)移瘤患者,有嚴(yán)重未控制的內(nèi)科疾病或急性感染者,已知既往多種藥物過敏者,既往對惟一病灶進(jìn)行放療。
1.2分組將68例患者分為治療組(n=31)和對照組(n=37),2組患者的性別、EGFR評分和分期比較差異無統(tǒng)計(jì)學(xué)意義(P>0.05),具有可比性。見表1。
1.3治療方法治療組:過去4周未接受過化療的患者,用4 mL安瓿瓶內(nèi)的無菌乙醇溶液將208 mg福莫司汀完全溶解,根據(jù)患者體表面積,以 100 mg·m-2劑量,將溶液用250 mL的質(zhì)量分?jǐn)?shù)5%等滲葡萄糖溶液稀釋后,避光條件下靜脈滴注,時(shí)間<1 h,d1,8,21 d為1周期,共給予2周期化療。酌情適量給予止吐藥物和重組人粒細(xì)胞集落刺激因子,治療期間每6 d行血常規(guī)、肝功能和腎功能檢查。治療期間每周期第1天復(fù)查胸部CT、頭顱MRI,完成上述治療后第1個(gè)月,重復(fù)上述檢查1次,以后每3個(gè)月重復(fù)檢查1次。對照組:誘導(dǎo)治療療效評價(jià)為完全緩解,前3個(gè)月每個(gè)月定期復(fù)查胸部CT、頭顱MRI,以后每3個(gè)月重復(fù)上述檢查1次。如隨訪期間患者出現(xiàn)頭暈、頭痛、惡心嘔吐,語言障礙、肢體肌力減退、共濟(jì)失調(diào),中樞神經(jīng)系統(tǒng)功能紊亂等疑似腦轉(zhuǎn)移瘤相關(guān)臨床癥狀,可立即行頭顱MRI檢查。
表12組患者的臨床資料比較
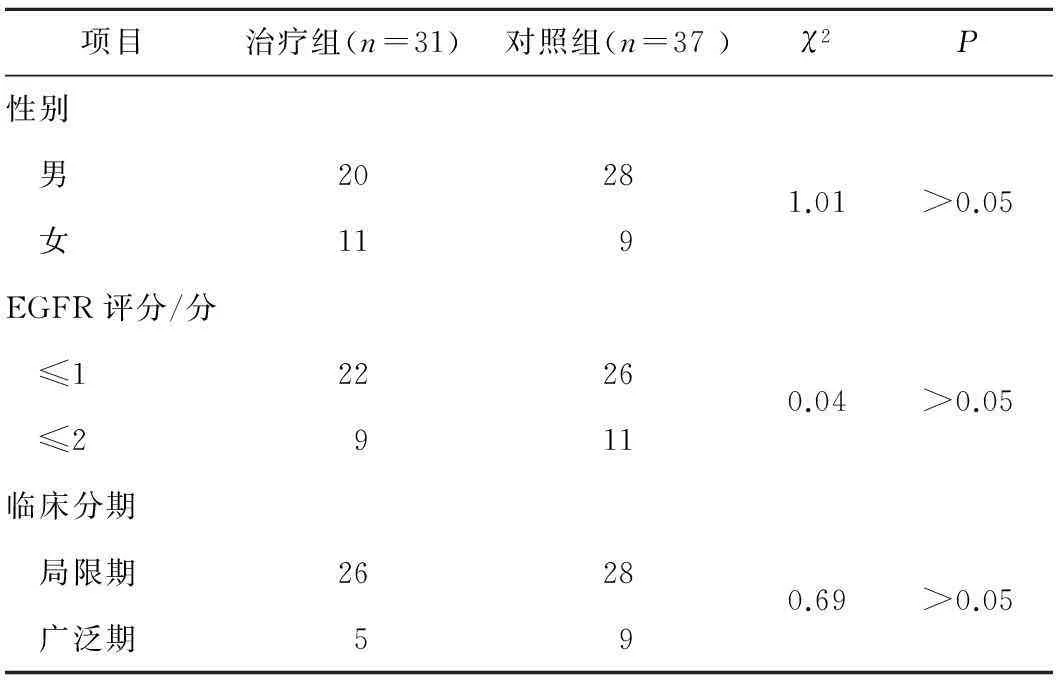
項(xiàng)目治療組(n=31)對照組(n=37)χ2P性別 男20281.01>0.05 女119EGFR評分/分 ≤122260.04>0.05 ≤2911臨床分期 局限期26280.69>0.05 廣泛期59
1.4觀察指標(biāo)和評價(jià)標(biāo)準(zhǔn)所有患者隨訪15個(gè)月,比較2組腦轉(zhuǎn)移發(fā)生率、無進(jìn)展生存期和1 a生存率。1)腦轉(zhuǎn)移發(fā)生率:以化療結(jié)束,療效評價(jià)完全緩解后,MRI發(fā)現(xiàn)腦轉(zhuǎn)移病灶為陽性,未發(fā)生腦轉(zhuǎn)移病灶為陰性,腦轉(zhuǎn)移發(fā)生率=腦轉(zhuǎn)移陽性例數(shù)/總例數(shù)×100%;2)無疾病進(jìn)展生存期:開始接受治療到任何有記錄的腫瘤進(jìn)展或死亡之日的時(shí)間;3)1 a生存率:患者接受治療后1 a時(shí)存活患者占同組患者的概率。
本研究的主要終點(diǎn)指標(biāo)是腦轉(zhuǎn)移發(fā)生率,經(jīng)頭顱MRI證實(shí)發(fā)生腦轉(zhuǎn)移者,次要終點(diǎn)指標(biāo)為生存期,如觀察期間出現(xiàn)腦外轉(zhuǎn)移、局部腫瘤復(fù)發(fā),可予以原方案或二線方案化療,可繼續(xù)觀察腦轉(zhuǎn)移發(fā)生率、1 a生存率。
2結(jié)果
2.12組腦轉(zhuǎn)移發(fā)生率比較治療組腦轉(zhuǎn)移發(fā)生率低于對照組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見表2。
表22組腦轉(zhuǎn)移發(fā)生率比較
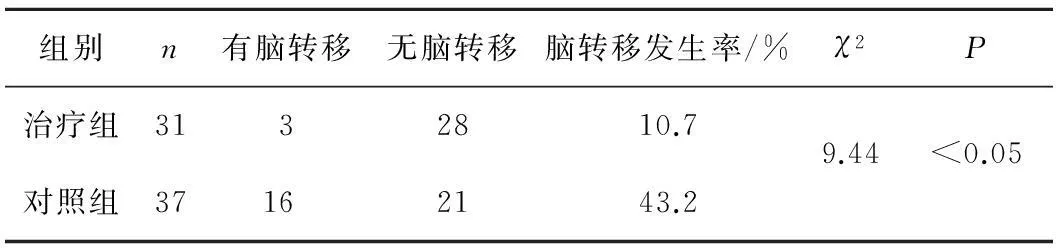
組別n有腦轉(zhuǎn)移無腦轉(zhuǎn)移腦轉(zhuǎn)移發(fā)生率/%χ2P治療組3132810.79.44<0.05對照組37162143.2
2.22組無疾病進(jìn)展生存期比較治療組無疾病進(jìn)展生存期為(7.52±2.95)個(gè)月,長于對照組的(5.89±2.67)個(gè)月,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見圖1、表3。
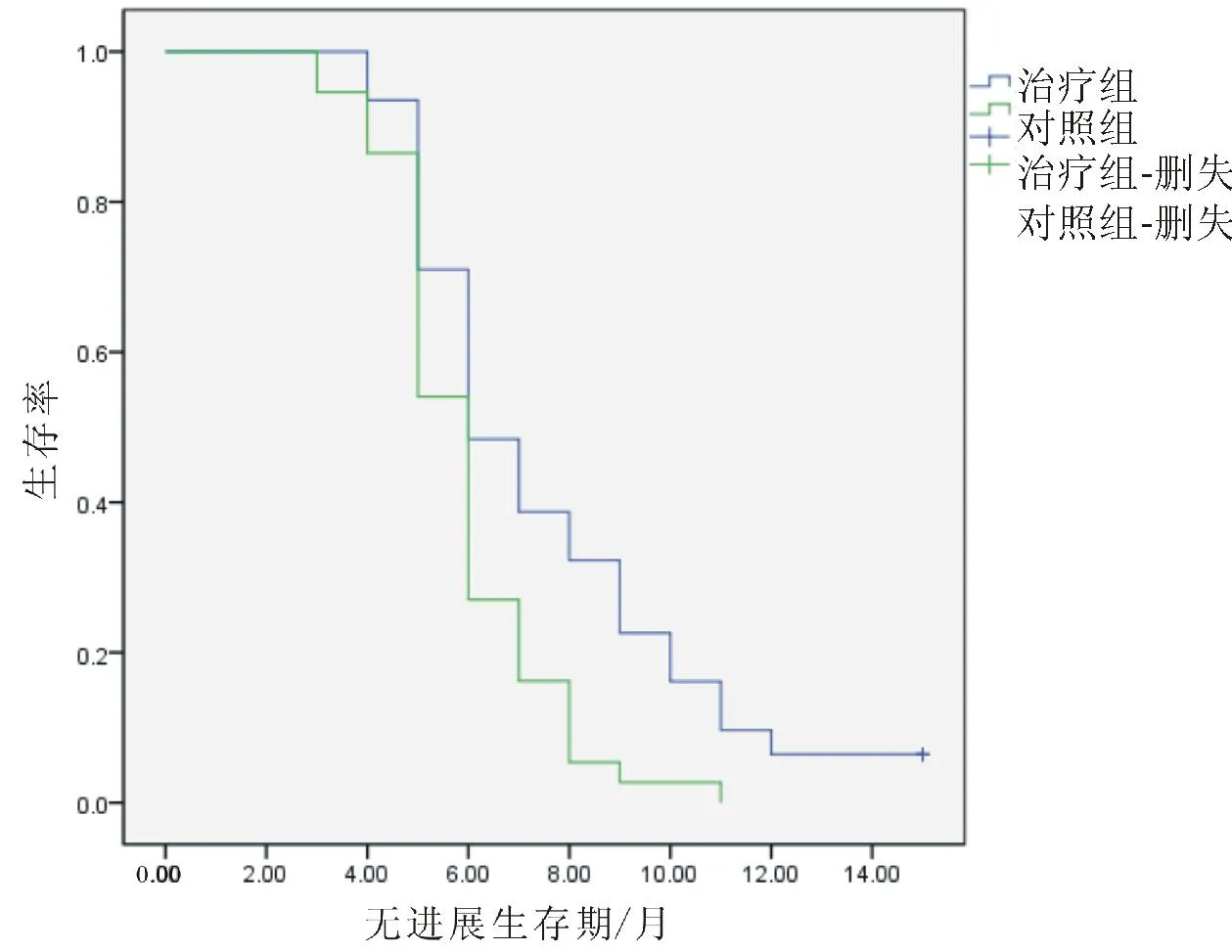
圖1 2組無進(jìn)展生存期比較

組別無疾病進(jìn)展生存期/月治療組7.52±2.95對照組5.89±2.67P<0.05
2.32組1 a生存情況比較治療組1 a生存率為51.6%,對照組為62.1%,比較差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。見表4。

表4 2組1 a生存情況比較 n
3討論
小細(xì)胞肺癌是一種上皮來源性的低分化惡性腫瘤,由細(xì)胞質(zhì)少、細(xì)胞邊界不清、細(xì)顆粒核染色體、無核仁或核仁不明顯的小細(xì)胞構(gòu)成,被歸于高級神經(jīng)內(nèi)分泌腫瘤[7-9]。雖然初治患者對化療敏感,但易于產(chǎn)生耐藥和復(fù)發(fā),且對二線藥物敏感度欠佳,預(yù)后較差,絕大部分患者最終死于復(fù)發(fā)[10]。腦部是小細(xì)胞肺癌最常見的轉(zhuǎn)移播散部位,據(jù)文獻(xiàn)[11]報(bào)道,在尸檢中,50%的小細(xì)胞肺癌患者被發(fā)現(xiàn)腦轉(zhuǎn)移,其中33%患者無任何神經(jīng)系統(tǒng)癥狀。
血腦屏障由無窗孔的毛細(xì)血管內(nèi)皮細(xì)胞及細(xì)胞間緊密連接、基膜、周細(xì)胞、星形膠質(zhì)細(xì)胞足突以及狹小的細(xì)胞外隙共同組成的一個(gè)復(fù)合體,其為中樞神經(jīng)系統(tǒng)提供解剖和生理上的保護(hù),對于保證大腦功能的正常運(yùn)行至關(guān)重要,但也是治療許多中樞神經(jīng)系統(tǒng)疾病的瓶頸,因?yàn)槠淠茏柚?5%的小分子藥物進(jìn)入腦組織腦轉(zhuǎn)移[12]。由于大部分化療藥物不能很好通過血腦屏障,因此,腦部成為腫瘤細(xì)胞的避難所,腦轉(zhuǎn)移成為肺癌復(fù)發(fā)的主要原因之一,諸如局部腫瘤復(fù)發(fā)、腦外轉(zhuǎn)移等導(dǎo)致治療失敗的其他原因,因多模式的治療方法可獲得更好控制,但腦轉(zhuǎn)移治療方法較少,一旦出現(xiàn)神經(jīng)系統(tǒng)受累,中位生存期僅3~4.5個(gè)月,預(yù)后差,且嚴(yán)重影響患者生活質(zhì)量[5,13]。目前,對于完全緩解期小細(xì)胞肺癌,推薦行預(yù)防性顱腦照射(prophylactic cranial irradiation,PCI)[14]。因常規(guī)化療藥物藥物難以有效的進(jìn)入腦組織,腦成為腫瘤細(xì)胞潛在的庇護(hù)所,因此PCI并非起預(yù)防作用,而是消滅尚未被發(fā)現(xiàn)的潛在轉(zhuǎn)移灶,但消滅亞臨床轉(zhuǎn)移灶所需放射劑量遠(yuǎn)低于消滅肉眼可見腫瘤所需劑量,而后者則可能已超出正常腦組織的耐受范圍,可導(dǎo)致晚期神經(jīng)性后遺癥[15]。因此,不推薦在PS評分較差(3~4分)或有神經(jīng)功能認(rèn)知障礙的患者行PCI,年齡較大(>60歲)也與慢性神經(jīng)毒性有關(guān)聯(lián),應(yīng)用PCI時(shí)需臨床醫(yī)生評估[16-17]。PCI作為預(yù)防性治療,雖可降低患者腦轉(zhuǎn)移發(fā)生率,但仍有近1/3的患者出現(xiàn)腦部疾病進(jìn)展,該部分患者再次腦照射有效率<50%,預(yù)計(jì)生存期4~6個(gè)月[18]。
福莫司汀為亞硝基脲類抗腫瘤藥,易于穿透細(xì)胞和通過血腦屏障,主要毒副反應(yīng)為骨髓抑制,表現(xiàn)為血小板減少和白細(xì)胞減少,發(fā)生時(shí)間較晚,常見Ⅰ、Ⅱ度骨髓抑制,次要毒副反應(yīng)為中度惡心、嘔吐,多出現(xiàn)在注射后2 h內(nèi),給予預(yù)防性藥物應(yīng)用,可避免胃腸反應(yīng)發(fā)生,通過臨床觀察,福莫司汀相關(guān)毒副反應(yīng)未影響治療進(jìn)程,未明顯降低患者生活質(zhì)量。目前雖無應(yīng)用福莫司汀預(yù)防小細(xì)胞腦轉(zhuǎn)移相關(guān)文獻(xiàn)報(bào)道,但其在治療腦膠質(zhì)瘤和肺癌腦轉(zhuǎn)移瘤方面,已取得一定成果。本研究中治療組腦轉(zhuǎn)移發(fā)生率低于對照組,無疾病進(jìn)展生存期高于對照組,可認(rèn)為福莫司汀對完全緩解小細(xì)胞肺癌腦轉(zhuǎn)移有預(yù)防作用,并可提高患者無疾病進(jìn)展生存期,治療組與對照組1 a生存率差異無統(tǒng)計(jì)學(xué)意義,可能與樣本量少有關(guān)。福莫司汀常見骨髓抑制、胃腸道反應(yīng),未見潛在神經(jīng)系統(tǒng)毒性,且上述毒副反應(yīng)均可在短時(shí)間內(nèi)恢復(fù),對于應(yīng)用福莫司汀后腦轉(zhuǎn)移患者,可給予全腦放療,且對全腦放療有效率無影響,為預(yù)防性腦轉(zhuǎn)移治療后期復(fù)發(fā)提供更多有效治療途徑。該研究為不能行PCI的患者提供了另一種可行的臨床治療方法,為緩解期小細(xì)胞肺癌預(yù)防腦轉(zhuǎn)移提供新的臨床思路。但由于本研究入組病例有限,若要進(jìn)一步明確福莫司汀在預(yù)防完全緩解期小細(xì)胞肺癌腦轉(zhuǎn)移的相關(guān)作用,還需大樣本、多中心的臨床研究。
參考文獻(xiàn):
[1]Siegel R,Naishadham D,Jemal A.Cancer statistics,2013[J].CA Cancer J Clin,2013,63(1):11-30.
[2]Jackman DM,Johnson BE.Small-cell lung cancer[J].Lancet,2005,366(9494):1385-1396.
[3]Greenspoon JN,Evans WK,Cai W,et al.Selecting patients with extensive-stage small cell lung cancer for prophylactic cranial irradiation by predicting brain metastases[J].J Thorac Oncol,2011,6(4):808-812.
[4]Manapov F.Central nervous system relapse continues to be a therapeutic challenge in extensive disease small-cell lung cancer patients with initial symptomatic brain metastases and good response to chemoradiotherapy[J].J Neurooncol,2010,98(3):349-355.
[5]Manapov F,Kl?cking S,Niyazi M,et al.Primary tumor response to chemoradiotherapy in limited-disease small-cell lung cancer correlates with duration of brain-metastasis free survival[J].J Neurooncol,2012,109(2):309-314.
[6]Bremnes RM,Sundstrom S,Aaseb? U,et al.The value of prognostic factors in small cell lung cancer: results from a randomised multicenter study with minimum 5 year follow-up[J].Lung Cancer,2003,39(3):303-313.
[7]賈春祎,張立新,張曉凱,等.福莫斯汀治療非小細(xì)胞肺癌腦轉(zhuǎn)移的臨床觀察[J].癌癥進(jìn)展,2014,12(1):89-92.
[8]Travis WD.Advances in neuroendocrine lung tumors[J].Ann Oncol,2010,21 Suppl 7:vii65- vii71.
[9]Zakowski MF.Pathology of small cell carcinoma of the lung[J].Semin Oncol,2003,30(1):3-8.
[10]van Meerbeeck JP,Fennell DA,De Ruysscher DK.Small-cell lung cancer[J].Lancet,2011,378(9804):1741-1755.
[11]Chen G,Huynh M,Chen A,et al.Chemotherapy for brain metastases in small-cell lung cancer[J].Clin Lung Cancer,2008,9(1):35-38.
[12]任成波,趙麗霞.甘露醇在預(yù)防小細(xì)胞肺癌腦轉(zhuǎn)移中的作用[J].現(xiàn)代腫瘤醫(yī)學(xué),2012,20(4):744-745.
[13]Paumier A,Cuenca X,Le Péchoux C.Prophylactic cranial irradiation in lung cancer[J].Cancer Treat Rev,2011,37(4):261-265.
[14]Alberts WM,American College of Chest Physicians.Diagnosis and management of lung cancer executive summary: ACCP evidence-based clinical practice guidelines (2nd Edition)[J].Chest,2007,132(3 Suppl):1S-19S.
[15]胡曉,陳明.局限期小細(xì)胞肺癌預(yù)防性全腦照射:爭議與研究進(jìn)展[J].中國肺癌雜志,2013,16(7):373-377.
[16]Slotman BJ,Mauer ME,Bottomley A,et al.Prophylactic cranial irradiation in extensive disease small-cell lung cancer: short-term health-related quality of life and patient reported symptoms: results of an international Phase Ⅲ randomized controlled trial by the EORTC Radiation Oncology and Lung Cancer Groups[J].J Clin Oncol,2009,27(1):78-84.
[17]Wolfson AH,Bae K,Komaki R,et al.Primary analysis of a phase Ⅱ randomized trial Radiation Therapy Oncology Group (RTOG) 0212: impact of different total doses and schedules of prophylactic cranial irradiation on chronic neurotoxicity and quality of life for patients with limited-disease small-cell lung cancer[J].Int J Radiat Oncol Biol Phys,2011,81(1):77-84.
[18]Castrucci WA,Knisely JP.An update on the treatment of CNS metastases in small cell lung cancer[J].Cancer J,2008,14(3):138-146.
Prevention Efficacy of Fotemustine for Brain Metastasis of Small Cell Lung Cancer in Complete Remission
Huang Kun1,Kuang Xiankui2,Han Wei1,Zhao Xiangtong1,Yan Yan1,Dong Wenjie1,Wang Liping1
(1.DepartmentofOncology,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China;2.DepartmentofOncology,thePeople’sHospitalofXiangchengCity,Zhoukou466200,China)
[Abstract]ObjectiveTo assess the prevention efficacy of fotemustine for brain metastasis of small cell lung cancer in complete remission.MethodsSixty-eight patients with small cell lung cancer in complete remission were randomly divided into two groups.The 31 patients in the fotemustine treatment group received fotemustine (100 mg·m-2,ivgtt,d1,8),21 days was a chemotherapy cycle,2 cycles of chemotherapy were given; the other 37 patients in the control group were given regular review.The 15 month brain metastases rate,progression-free survival and 1-year survival rate were compared between the two groups.ResultsThe 15 month brain metastases rate of the fotemustine treatment group was lower than that of the control group,the progression-free survival was longer than that of the control group (P<0.05); there was no statistical difference in the 1-year survival rate between the two groups (P>0.05).ConclusionEarly application of fotemustine can reduce incidence of brain metastasis of small cell lung cancer in complete remission,and lengthen the progress free survival.
[Key words]small cell lung cancer; fotemustine; prevention; complete remission; brain metastasis
(收稿日期:2015-10-10)
[中圖分類號(hào)]R734.2;R730.6
[文獻(xiàn)標(biāo)識(shí)碼]A
[文章編號(hào)]1673-5412(2016)01-0064-04
DOI:10.3969/j.issn.1673-5412.2016.01.020
作者簡介:黃堃(1991-),女,碩士在讀,主要從事肺癌的診斷和綜合治療工作。E-mail:13939093211@163.com通信作者:王麗萍(1963-),博士,教授,主任醫(yī)師,碩士生導(dǎo)師,主要從事肺癌的診斷和綜合治療工作。E-mail: wlp@zzu.edu.cn
基金項(xiàng)目:河南省衛(wèi)生廳科技攻關(guān)項(xiàng)目(編號(hào):201303038)

