基于證據(jù)推理解答電化學(xué)試題
摘要:結(jié)合實(shí)例,介紹基于證據(jù)推理的解題思維模型,認(rèn)為應(yīng)在試題情境和設(shè)問中確定認(rèn)識對象和認(rèn)識角度,收集進(jìn)行推理判斷的證據(jù);建立問題、證據(jù)和結(jié)果之間的邏輯關(guān)系是基于證據(jù)推理的關(guān)鍵。應(yīng)用這種思維模型解答化學(xué)試題,可以幫助學(xué)生突破原有的認(rèn)識誤區(qū),減少或避免錯(cuò)誤。
關(guān)鍵詞:證據(jù)推理;電化學(xué);電解質(zhì)溶液;化學(xué)試題
文章編號:1005–6629(2017)11–0080–04 中圖分類號:G633.8 文獻(xiàn)標(biāo)識碼:B
科學(xué)必須實(shí)事求是,需要讓結(jié)論建立在證據(jù)基礎(chǔ)上,需要可以重復(fù)驗(yàn)證;科學(xué)探究是提出假說,再加以驗(yàn)證,最后得出結(jié)論的過程[1]。學(xué)生在學(xué)習(xí)化學(xué)過程中,限于知識的階段性或不連貫等原因,總會(huì)產(chǎn)生一些認(rèn)識誤區(qū)(包括知識理解不到位、認(rèn)識角度不明確、認(rèn)識思路有偏差等等),而且所產(chǎn)生的認(rèn)識誤區(qū)往往會(huì)影響學(xué)生解決問題的思考過程,誘使他們犯錯(cuò)誤。所以,在化學(xué)教學(xué)中必須要讓學(xué)生明白,在解化學(xué)試題時(shí)不能完全憑借已學(xué)知識去推理判斷。教師必須通過各種手段了解學(xué)生學(xué)習(xí)過程中認(rèn)識誤區(qū)形成的原因,了解認(rèn)識誤區(qū)可能給學(xué)生解決問題時(shí)所帶來的負(fù)面影響,尋找?guī)椭鷮W(xué)生突破認(rèn)識誤區(qū)的方法。實(shí)踐中發(fā)現(xiàn),引導(dǎo)學(xué)生基于證據(jù)推理解答化學(xué)試題,有利于學(xué)生對科學(xué)本質(zhì)的認(rèn)識,有助于促進(jìn)學(xué)生形成和發(fā)展證據(jù)推理的素養(yǎng)。另外,倡導(dǎo)基于證據(jù)推理解決問題的思路,也是培養(yǎng)和提升學(xué)生化學(xué)學(xué)科思維能力的有效途徑。
1 基于證據(jù)推理解題的基本步驟
證據(jù)推理是化學(xué)學(xué)科核心素養(yǎng)之一,其內(nèi)涵是:“能初步學(xué)會(huì)收集各種證據(jù),對物質(zhì)的性質(zhì)及其變化提出可能的假設(shè);基于證據(jù)進(jìn)行分析推理,證實(shí)或證偽假設(shè);能解釋證據(jù)與結(jié)論之間的關(guān)系,確定形成科學(xué)結(jié)論所需要的證據(jù)和尋找證據(jù)的途徑;能認(rèn)識化學(xué)現(xiàn)象與模型之間的聯(lián)系,運(yùn)用多種模型來描述和解釋化學(xué)現(xiàn)象,預(yù)測物質(zhì)及其變化的可能結(jié)果;能依據(jù)物質(zhì)及其變化的信息建構(gòu)模型,建立解決復(fù)雜化學(xué)問題的思維框架;具有證據(jù)意識,能基于證據(jù)對物質(zhì)組成、結(jié)構(gòu)及其變化提出可能的假設(shè),通過分析推理加以證實(shí)或證偽;建立觀點(diǎn)、結(jié)論和證據(jù)之間的邏輯關(guān)系;知道可以通過分析、推理等方法認(rèn)識研究對象的本質(zhì)特征、構(gòu)成要素及其相互關(guān)系,建立模型;能運(yùn)用模型解釋化學(xué)現(xiàn)象,揭示現(xiàn)象的本質(zhì)和規(guī)律。[2]”
聯(lián)系到化學(xué)試題,立意、情境、設(shè)問是試題的三要素,立意必定體現(xiàn)在試題情境和設(shè)問中,設(shè)問是建立在試題情境的基礎(chǔ)上的[3]。所以,我們從試題的情境、設(shè)問開始,構(gòu)建以下解題的思維模型(如圖1):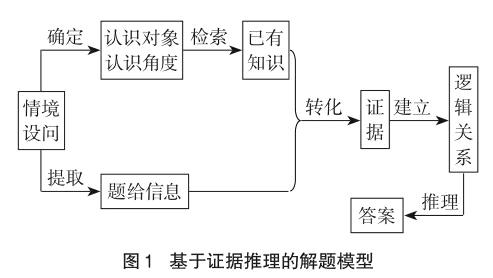
從上述解題思維模型中可看出,在試題情境和設(shè)問中確定相關(guān)認(rèn)識對象、認(rèn)識角度和給出了哪些新的信息都是為了獲得推理判斷的證據(jù),建立問題、證據(jù)和結(jié)果之間的邏輯關(guān)系是基于推理判斷的關(guān)鍵。根據(jù)這種思維模型解答化學(xué)試題,可以突破一些認(rèn)識誤區(qū),減少和避免犯錯(cuò)誤。下面以電解相關(guān)的試題為例加以具體說明。
2 基于證據(jù)推理突破認(rèn)識誤區(qū)
由于有較多學(xué)生對電解原理存在認(rèn)識誤區(qū),影響學(xué)生解題的思考角度、思維路徑和認(rèn)識深度,導(dǎo)致產(chǎn)生錯(cuò)誤。要幫助學(xué)生突破認(rèn)識誤區(qū)正確解題,可以用上述解題思維模型,讓學(xué)生基于證據(jù)(而不是基于記憶、基于所謂的“規(guī)律”)作出推理判斷。
2.1 破除關(guān)于“離子移動(dòng)”的認(rèn)識誤區(qū)
電解池工作時(shí),由于受電場影響電解質(zhì)溶液中陰離子要向陽極作定向移動(dòng)、陽離子要向陰極作定向移動(dòng),這是電解過程中電解質(zhì)溶液導(dǎo)電微觀原理。但有一些學(xué)生會(huì)認(rèn)為這是電解時(shí)影響電解質(zhì)溶液中離子移動(dòng)方向的唯一因素,就是一種“以偏概全”的認(rèn)識誤區(qū)。實(shí)際上,在電解池(原電池也一樣)的電解質(zhì)溶液中,影響離子移動(dòng)的因素有多項(xiàng),主要有:

2.2 破除關(guān)于“放電順序”的認(rèn)識誤區(qū)
雖然在教材中沒有給出電解放電順序,但很多課外輔導(dǎo)書給出了“陽極上陰離子放電順序”“陰極上陽離子放電順序”,有學(xué)生將這些“規(guī)律”當(dāng)作解決電解問題的基本思路,這是一種認(rèn)識誤區(qū)。實(shí)際上,電解是很復(fù)雜的過程,電解產(chǎn)物的判斷既涉及微粒本身的性質(zhì),也不能脫離所處的環(huán)境(如溫度、濃度、電解質(zhì)的性質(zhì)、電極材料、電流密度等)。雖然中學(xué)階段不要求學(xué)生了解這些情況,但千萬不能將在一定條件的事實(shí)變成絕對化的“規(guī)律”。如在工業(yè)電解飽和食鹽水的條件下,陽極上是Cl-比OH-優(yōu)先放電生成Cl2,并不能由此推斷放電能力Cl-比OH-強(qiáng),絕不能認(rèn)為所有條件下電解食鹽水陽極上一定是Cl-放電生成Cl2,因?yàn)镃l-、OH-在陽極上的放電受多種因素影響,有時(shí)也可以是OH-優(yōu)先放電,有些情況下還可以是兩種離子同時(shí)放電。其他離子之間也有類似情況,當(dāng)然中學(xué)階段還不對這些內(nèi)容作要求。
例2 某同學(xué)為了探究Cl-、OH-的失電子能力,用如圖3實(shí)驗(yàn)裝置進(jìn)行電解實(shí)驗(yàn)(用鉛筆芯作電極),3min后將濕潤的淀粉-KI試紙靠近陽極處不變藍(lán),用帶火星木條靠近陽極,木條復(fù)燃。寫出陽極的電極反應(yīng)式。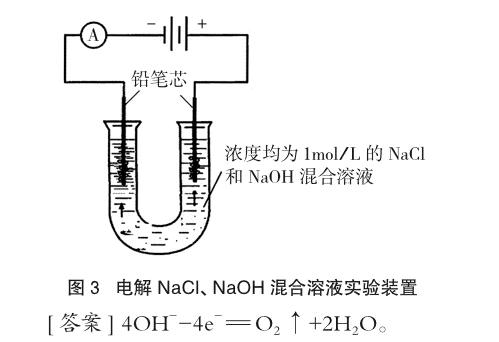
有學(xué)生會(huì)根據(jù)所謂的“放電順序規(guī)律”,不加分析就判斷是Cl-在陽極上被氧化生成Cl2,導(dǎo)致本可避免的錯(cuò)誤。題中給出的“陽極生成氣體不能使淀粉-KI試紙變藍(lán),能使帶火星木條復(fù)燃”是重要信息,可轉(zhuǎn)化為關(guān)鍵證據(jù)判斷出陽極生成的氣體是氧氣,所以該實(shí)驗(yàn)條件下是OH-離子在陽極上優(yōu)先放電。
初步學(xué)會(huì)收集各種證據(jù),對物質(zhì)的性質(zhì)及其變化提出可能的假設(shè),并能基于證據(jù)進(jìn)行分析推理、證實(shí)或證偽假設(shè)。“實(shí)驗(yàn)探究與創(chuàng)新意識”指發(fā)現(xiàn)和提出有探究價(jià)值的化學(xué)問題,能依據(jù)探究目的設(shè)計(jì)并優(yōu)化實(shí)驗(yàn)方案,完成實(shí)驗(yàn)操作并能尊重事實(shí)和證據(jù),具有獨(dú)立思考、敢于質(zhì)疑和批判的創(chuàng)新精神[4]。endprint
例3 水銀法電解食鹽水曾是氯堿工業(yè)發(fā)展進(jìn)程中的重要里程碑,以制得堿液純度高、質(zhì)量好著稱,其生產(chǎn)原理如圖4所示: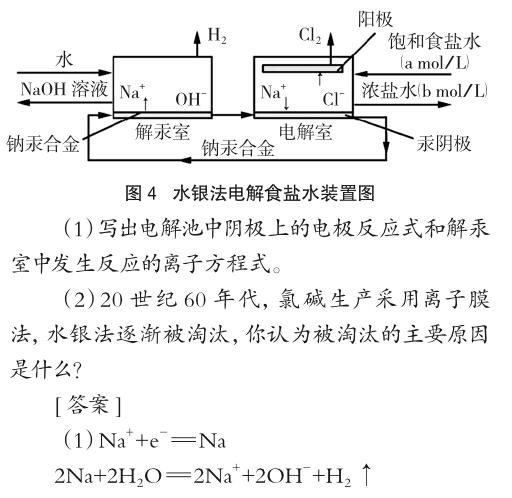
(2)因?yàn)楣拘詮?qiáng),易造成污染。
遇到這樣的試題,有很多學(xué)生總是不重視從試題中尋找信息,死板地用所謂的“陽離子放電順序”來判斷,認(rèn)為H+比Na+更容易在陰極上放電,導(dǎo)致錯(cuò)誤答案。事實(shí)上,只要觀察題給示意圖,就能找到三條重要信息:“電解室中陰極上是Na+放電”、“鈉汞合金從電解室流到解汞室”、“解汞室里是Na→Na+”,根據(jù)其中任何一條都可判斷出該生產(chǎn)條件下電解室中陰極上是Na+比H+優(yōu)先放電。從中可以看出平時(shí)學(xué)習(xí)形成的“認(rèn)識誤區(qū)”是那么頑固,要克服其影響是何等難!
中學(xué)化學(xué)中,考慮到學(xué)生的知識和認(rèn)識基礎(chǔ),對某些問題作簡單化處理是合理的,對一些共性的東西進(jìn)行歸納也是必需的,但絕不能將簡化的內(nèi)容擴(kuò)大化,將總結(jié)的經(jīng)驗(yàn)泛規(guī)律化,要防止所謂的“規(guī)律”束縛學(xué)生的認(rèn)識。
2.3 破除關(guān)于“陰極、陽極放電離子種類”的認(rèn)識誤區(qū)
學(xué)習(xí)電解原理時(shí),有較多學(xué)生會(huì)有“電解時(shí)陽極上一定是陰離子放電(或者陽離子不會(huì)在陽極上放電)、陰極上一定是陽離子放電(或者陰離子不會(huì)在陰極上放電)”的錯(cuò)誤認(rèn)識,帶著這種錯(cuò)誤認(rèn)識去解決有關(guān)電解問題,在思考過程中會(huì)走很多彎路,甚至引來不可避免的錯(cuò)誤。實(shí)際上,電解過程中,陰極上有電子流入(外電源負(fù)極上電子流向陰極),此時(shí)陰極相當(dāng)于極強(qiáng)的還原劑,多種微粒會(huì)被還原(絕不僅僅是陽離子才可以在陰極上被還原!);相應(yīng)地,陽極要流出電子(這些電子流向外電源正極),此時(shí)陽極相當(dāng)于極強(qiáng)的氧化劑,多種微粒會(huì)被氧化(絕不僅僅是陰離子才可能在陽極上被氧化!)。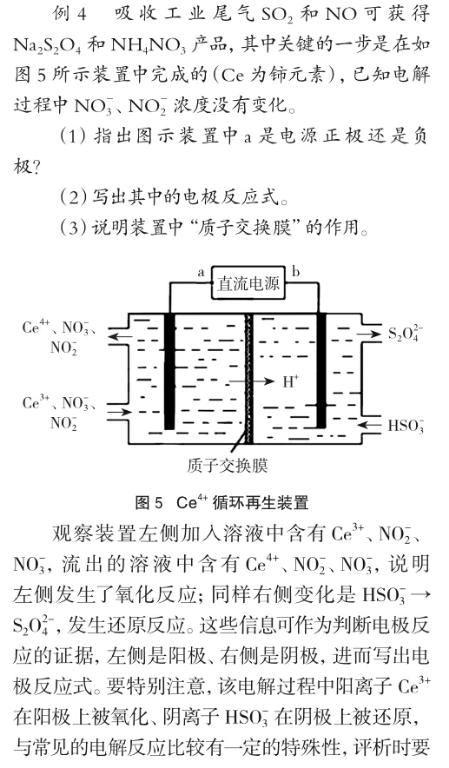

以上列舉的都是關(guān)于電化學(xué)的試題,實(shí)際上在解答其他內(nèi)容的化學(xué)試題時(shí),也應(yīng)該倡導(dǎo)學(xué)生基于證據(jù)推理的思路方法。總之,基于證據(jù)推理是突破認(rèn)識誤區(qū)的一種有效方法,其基本的步驟為“提取題給信息→轉(zhuǎn)換成證據(jù)→根據(jù)證據(jù)等建立邏輯關(guān)系→推理判斷→獲得解決。
當(dāng)然,由于試題情境和設(shè)問的不同,收集關(guān)鍵證據(jù)并作出推理判斷也有不同的層次要求,常見試題中的證據(jù)推理要求大致可分成以下四種。
第一種,能從物質(zhì)及其變化的事實(shí)中提取證據(jù),依據(jù)證據(jù)證實(shí)或證偽。
第二種,能從宏觀與微觀結(jié)合上收集證據(jù),依據(jù)證據(jù)從不同角度分析,再推出合理結(jié)論。
第三種,能從定性與定量結(jié)合上收集證據(jù),能通過定性分析和定量計(jì)算,推出合理結(jié)論。
第四種,能從各個(gè)角度發(fā)現(xiàn)不同特征,找出充分的證據(jù),推出合理結(jié)論,并能解釋證據(jù)和結(jié)論之間的關(guān)系。
教學(xué)中要根據(jù)學(xué)生知識基礎(chǔ)和認(rèn)識發(fā)展水平,選用或編制能力要求不同的試題讓學(xué)生練習(xí),以幫助學(xué)生突破認(rèn)識誤區(qū),提高基于證據(jù)推理解答化學(xué)試題的能力。
參考文獻(xiàn):
[1]吳俊明,張磊.科學(xué)本質(zhì)觀及其養(yǎng)育[J].化學(xué)教學(xué),2016,(3):4~8.
[2]普通高中課程標(biāo)準(zhǔn)修訂組.普通高中化學(xué)課程標(biāo)準(zhǔn)(征求意見稿)[S]. 2016:3~5.
[3]陳進(jìn)前.關(guān)于試題情境的研究[J].化學(xué)教學(xué),2017,(1):80~85.
[4]霍華德·加德納.多元智能新視野[M].北京:中國人民大學(xué)出版社,2008.endprint

