化學平衡狀態的判斷
■河南省鄲城縣第一高級中學 李永彬
【基本概念辨析】
1.可逆反應。
(1)概念:在相同條件下,既能向正反應方向進行,又能向逆反應方向進行的化學反應。
(2)特點——“二同一不能”。
①“二同”:同一條件下,正、逆反應同時進行。
②“一不能”:反應物和生成物同時存在,任意物質不能全轉化為生成物,即反應物的轉化率小于100%。
2.化學平衡狀態。
(1)建立過程:一定條件下的可逆反應隨著反應的進行,正反應速率與逆反應速率相等,反應體系中所有參加反應的物質的濃度保持不變的狀態(如圖1)。
(2)特點:①逆:化學平衡研究的對象是可逆反應。②等:達到平衡時正反應速率和逆反應速率相等。③定:達到平衡時反應體系中各組分的濃度保持恒定。④動:化學平衡是一種動態平衡。⑤變:當外界條件發生變化時,平衡可能發生移動。
【考點誤區警示】
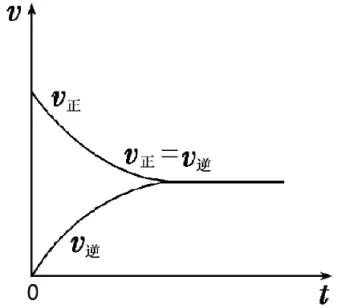
圖1
(1)對于在不同條件下進行的反應物和生成物相反的反應不能認為是可逆反應。如不是可逆反應。(2)對于可逆反應,無論什么條件下,反應物都不可能完全轉化為生成物。如H2+I2?2HI的反應體系中,加入1mol H2與1molI2充分反應后,生成HI的量一定小于2mol。(3)可逆反應達到化學平衡狀態時,化學反應速率不等于零。(4)對于有特征現象的化學反應,可以通過觀察現象來判斷反應是否達到平衡,如Fe3++3SCN-?Fe(SCN)3的反應,當反應體系的顏色不再改變時,反應達到平衡。(5)外界條件發生變化,化學平衡狀態不一定發生移動,如使用催化劑。
【平衡狀態判據】
化學平衡狀態的判斷問題是常見的考題,要求考生正確理解化學平衡狀態的本質(即正、逆反應速率相等)、化學平衡狀態的表現(如各組分濃度和百分含量、反應物的轉化率保持不變),以及從化學平衡狀態的概念中延伸出平衡體系中氣體的相對分子質量、密度等。
常用到的判斷標志為:
1.直接判斷依據。
v正(A)=v逆(A)>0
各物質濃度保持不變}?達到平衡狀態
2.間接判斷依據:反應達到平衡狀態時,正、逆反應速率相等,平衡時各種物質的物質的量、濃度、含量等不再發生變化,以及由此衍生的其他量不變,并由此進行判斷。注意理解化學平衡狀態的判斷,選擇的物理量應隨反應進行發生變化,該物理量由變化到不變,說明到達平衡。具體方法如下:
(1)速率法:①同一物質的v正=v逆≠0,對于不同物質的速率要通過化學計量數轉化為同一物質的速率;②同一物質化學鍵斷裂速率與化學鍵生成速率相等。用速率描述時,一定要注意一“正”、一“逆”,且相等。
(2)壓強法:對于反應前后氣體計量數不等的可逆反應,在未達到平衡之前,等容密閉容器中氣體的總的物質的量始終在改變,氣體的壓強也會隨著改變,因此,體系內的總壓強不變時說明達到平衡狀態。對于等容條件下反應前后氣體計量數相等的可逆反應,體系內的總壓強始終是不變的,體系內的總壓強不變不能作為判定是否達到平衡狀態的依據。壓強對平衡的影響實質是濃度的影響,因此要注意充入無關氣體時的兩種情況:恒容時,雖然總壓增大,但有關氣體的濃度不變,故平衡不移動;恒壓時,雖然總壓不變,但有關氣體的濃度減小,平衡向著氣體體積增大的方向移動。
(3)體積法:對于反應前后氣體計量數不等的可逆反應,在未達到平衡之前,等壓密閉容器中氣體的總的物質的量始終在改變,氣體體積也會隨之改變,因此,體系內的總體積不變時說明達到平衡狀態。對于等壓條件下反應前后氣體計量數相等的可逆反應,體系內的總體積始終是不變的,體系內的總體積不變不能作為判定是否達到平衡狀態的依據。
(6)顏色法:有顏色物質參加或生成的可逆反應,體系的顏色不隨時間的改變而改變時,可判斷該可逆反應達到化學平衡狀態;常見的有色氣體有 NO2、Br2、I2。
(7)化學平衡常數法:一定溫度下的可逆反應,如果生成物濃度的冪之積與反應物濃度的冪之積的比值(即濃度商),與該溫度的化學平衡常數相等,可判斷該反應處于化學平衡狀態。濃度商大于Kc時,平衡向逆反應方向移動;濃度商等于Kc時,平衡不移動;濃度商小于Kc時,平衡向正反應方向移動。
(8)轉化率法:可逆反應達到化學平衡狀態,反應混合物各物質的含量保持不變,反應物的轉化率不變。
恒容時改變反應物的用量對轉化率(α)的影響:
①若反應物只有一種,如aA(g)?bB(g)+cC(g),增加A的量,若a=b+c,則α(A)不變;若a>b+c,則α(A)增大;若a<b+c,則α(A)減小。a≠b+c時,增大或減小反應物的濃度,平衡按加壓或減壓處理。
②若反應物不止一種,如mA(g)+nB(g)?pC(g)+qD(g),若只增加A的量,則平衡向正反應方向移動,α(A)減小而α(B)增大;若同倍數地同時增大或減小各反應物的濃度,平衡也按加壓或減壓處理。
【典型例題剖析】
例1反應N2(g)+3H2(g)?2NH3(g)ΔH<0,若在恒壓絕熱容器中發生,下列選項表明反應一定已達平衡狀態的是( )。
A.容器內的溫度不再變化
B.容器內的壓強不再變化
C.相同時間內,斷開 H-H 鍵的數目和生成N-H鍵的數目相等
D.容器內氣體的濃度c(N2)∶c(H2)∶c(NH3)=1∶3∶2
解析:該反應在絕熱容器中發生,正反應是放熱反應,容器內的溫度不再變化,反應一定達到平衡狀態,A項正確;該反應在恒壓容器中發生,壓強始終相等,容器內的壓強不能作為化學平衡狀態的判據,B項錯誤;根據反應方程式可得,斷開H—H鍵和生成N—H鍵的反應進行的方向相同,不能作為化學平衡狀態的判據,C項錯誤;容器內氣體的濃度c(N2)∶c(H2)∶c(NH3)=1∶3∶2,不能作為化學平衡狀態的判據,D項錯誤。
答案:A
例2合成氨所需的氫氣可用煤和水作原料經過多步反應制得,其中的一步反應為:
ΔH<0。反應達到平衡后,為提高CO的轉化率,下列措施中正確的是( )。
A.增加壓強 B.降低溫度
C.增大CO的濃度 D.更換催化劑
解析:A項,增加壓強平衡不移動,CO的轉化率不變,錯誤;B項,降低溫度平衡正向移動,正確;C項,增大CO的濃度,CO的轉化率降低,錯誤;D項,催化劑對平衡無影響,錯誤。
答案:B
例3一定條件下,將NO2與SO2以體積比1∶2置于密閉容器中發生反應NO2(g)+SO2(g)?SO3(g)+NO(g),下列能說明反應達到平衡狀態的是( )。
A.體系壓強保持不變
B.混合氣體顏色保持不變
C.SO3和NO的體積比保持不變
D.每消耗1molSO3的同時生成1molNO2
解析:反應前后氣體分子數不變,故體系的壓強始終不變,不能確定是否平衡;隨著反應的進行,NO2的濃度減小,顏色變淺,不變則達平衡;SO3和NO都是生成物,比例保持1∶1,不能確定是否平衡;D中所述的兩個速率都是逆反應速率,不能確定是否平衡。
答案:B
例4在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)?2NO2(g),隨溫度升高,混合氣體的顏色變深。
回答下列問題:
(1)反應的 ΔH____0(填“大于”或“小于”);100℃時,體系中各物質濃度隨時間變化如圖2所示。在0~60s時段,反應速率v(N2O4)為____mol·L-1·s-1,反應的平衡常數K1為____。
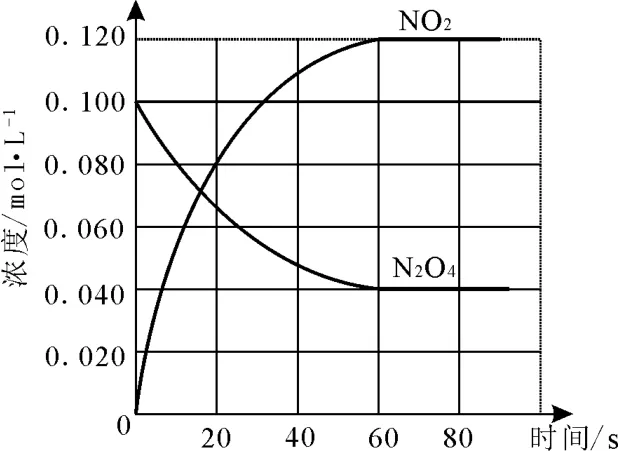
圖2
(2)100℃時達到平衡后,改變反應溫度為T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,經10s又達到平衡。
①T____100℃(填“大于”或“小于”),判斷理由是____。
②列式計算溫度T時反應的平衡常數K2:___。
(3)溫度T時反應達平衡后,將反應容器的容積減少一半,平衡向____(填“正反應”或“逆反應”)方向移動,判斷理由是____。
解析:(1)溫度升高,體系的顏色加深,化學平衡正向移動,反應吸熱,ΔH>0;v(N2O4)=
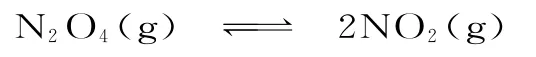
起始:0.1mol·L-10
轉化:0.06mol·L-10.12mol·L-1
平衡:0.04mol·L-10.12mol·L-1
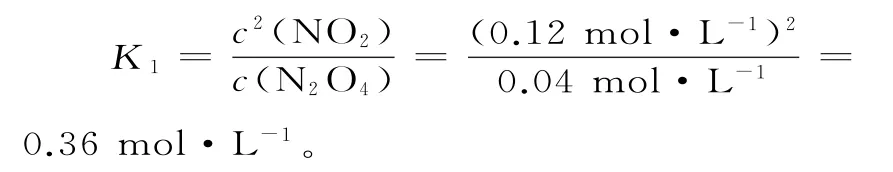
(2)①升高溫度,化學平衡正向移動,T大于100℃。
②c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,經10s又達到平衡,依據溫度越高,反應速率越快,可列三段式:

起始:0.04mol·L-10.12mol·L-1
轉化:0.02mol·L-10.04mol·L-1
平衡:0.02mol·L-10.16mol·L-1
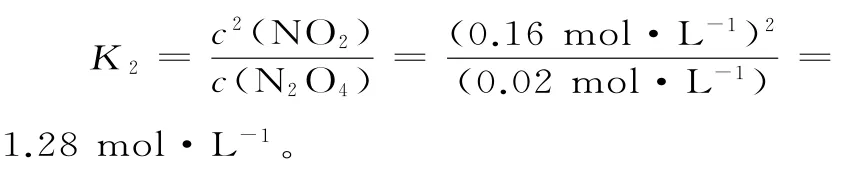
(3)該反應正向是氣體體積增大的反應,容器體積減小,壓強增大,平衡向逆反應方向移動。
答案:(1)大于 0.001 0.36mol·L-1
(2)①大于 反應正方向吸熱,反應向吸熱方向進行,故溫度升高
(3)逆反應 對氣體分子數增大的反應,增大壓強平衡向逆反應方向移動

