勇于直面問題敢于解決問題
葉蘭峰
摘要:“酸雨與二氧化硫”采用任務驅動教學模式可將高中學科核心素養較好地滲透課堂教學,正面引導學生,讓學生勇于直面“酸雨”問題,敢于解決“酸雨”問題,培養當代中國學生的社會擔當及責任意識。
關鍵詞:核心素養;任務驅動;酸雨與二氧化硫
文章編號:1008-0546(2019)10-0069-06 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2019.10.019
一、概念認知
高中化學核心素養包括“宏觀辨識與微觀探析”“變化觀念與平衡思想”“證據推理與模型認知”“實驗探究與創新意識”“科學態度與社會責任”,這是高中化學課程的重要目標,也是衡量高中化學教學教學的重要標準。任務驅動化學教學模式是建立在建構主義理論基礎上的一種教學模式,要求圍繞化學學習任務展開教學。隨著新課程改革的實施和不斷推進,任務驅動化學教學模式可理解為將高中化學核心素養組織在一個或幾個真實的、科學的、開放的典型任務之中,讓學生在任務的驅動下主動地進行探究學習,不斷地獲得成就感,進一步激發求知欲望。在完成任務的過程中,學生不僅建構了化學學科的知識結構,更為重要的是逐步掌握了化學學科的學習方法,逐步提高了運用化學知識分析、解決實際問題的能力,逐步形成了獨立思考、合作探索的科學創新品質。
二、問題提出
蘇教版《化學1》對于二氧化硫的性質和作用,是以酸雨的形成、危害、治理為明線,以二氧化硫的性質為暗線編寫的,且暗線穿插于明線之中,充分體現了化學源于生活、服務于生活。有些專家指出以酸雨引入二氧化硫的教學,可能會給學習者帶來對于化學認識的負面性,如化學是有污染、是有危害的,不建議選用教材中的酸雨作為學習二氧化硫的載體,而另選載體,因此也設計了一些優秀的課例,體現了用教材教而不是教教材。課堂教學需要“百花齊放各爭鳴”,而筆者有些不成熟的思考,希望能與同行們進行交流。筆者認為教材以酸雨的形成、危害、治理為明線,正體現了當前核心素養所提倡的培養中國學生的社會擔當及責任意識。“酸雨與二氧化硫”采用任務驅動教學模式可將高中學科核心素養較好地滲透課堂教學,正面引導學生,讓學生勇于直面“酸雨”問題,敢于解決“酸雨”問題。
三、設計意圖
“酸雨與二氧化硫”以“酸雨如何形成?”“酸雨如何防治?”“二氧化硫如何定量檢測?”作為課堂教學的三個任務線索,建構、完善、運用、再認知sO2的性質模型為知識線索,并結合演示實驗、探究實驗、交流討論、繪制流程圖、關注社會熱點等多種活動方式促使高中學科核心素養充分滲透進入課堂教學。
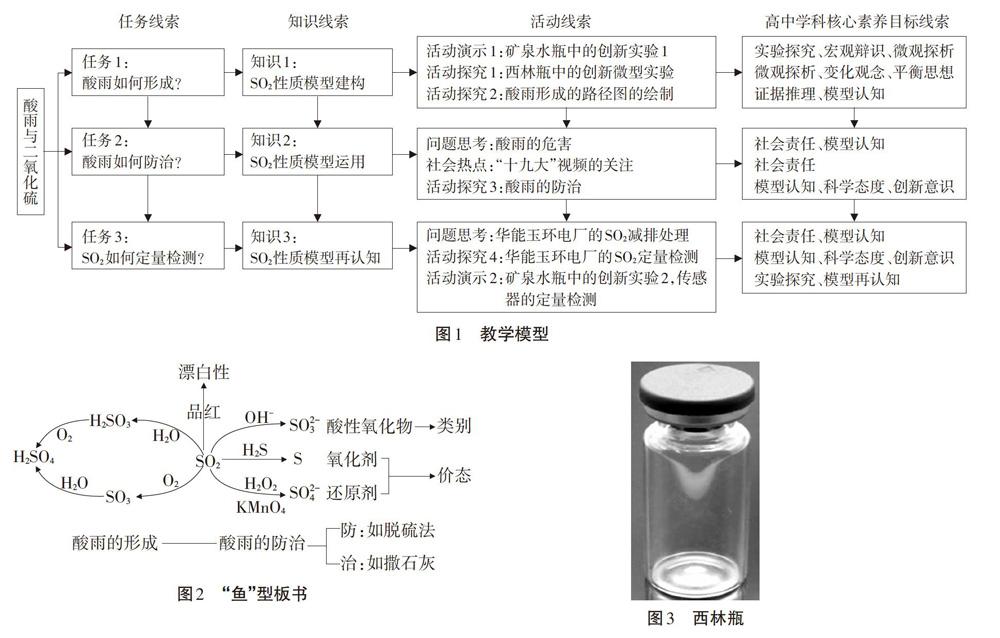
1.教學模型
如圖1所示。
2.綠色實驗
本文實驗共涉及三組,分別以帶瓶蓋的礦泉水瓶、帶瓶塞的西林瓶、帶氣球的試管作為實驗容器,均為安全密封裝置,因此教學過程中不會受SO:的刺激性氣味所干擾,從而提高教學高效性,并達成了化學實驗的綠色化。
第一組實驗是本課時的實驗主線,發揮了三個重要作用,分別是[活動演示1]引課暖場去除師生陌生度并激發學生求知欲(用注射器向裝有二氧化硫的礦泉水瓶中注入紫色石蕊試液)、[實驗論證]sO2水溶液與氯水的漂白性的不同原理([活動演示1]的混合溶液始終呈現紅色)、[活動演示2]突破了傳統的定量檢測方法,開闊了學生的視野,提升了學生的創新意識(打開[活動演示1]的礦泉水瓶的瓶塞,將實驗室手持sO2傳感器的感應頭靠近礦泉水瓶的瓶口)。第二組是學生對SO2性質開展的活動探究實驗,西林瓶小巧精致,選用少量化學試劑便能清晰地觀察到明顯的實驗現象,大大節省了試劑原料并有效防止SO2散發。第三組實驗是在試管口套一個氣球,這一簡單處理不僅能夠有效防止SO2氣體散發,同時在實驗操作加熱后恢復到室溫,氣球中的SO2氣體重新溶解于水使品紅溶液再次褪色。
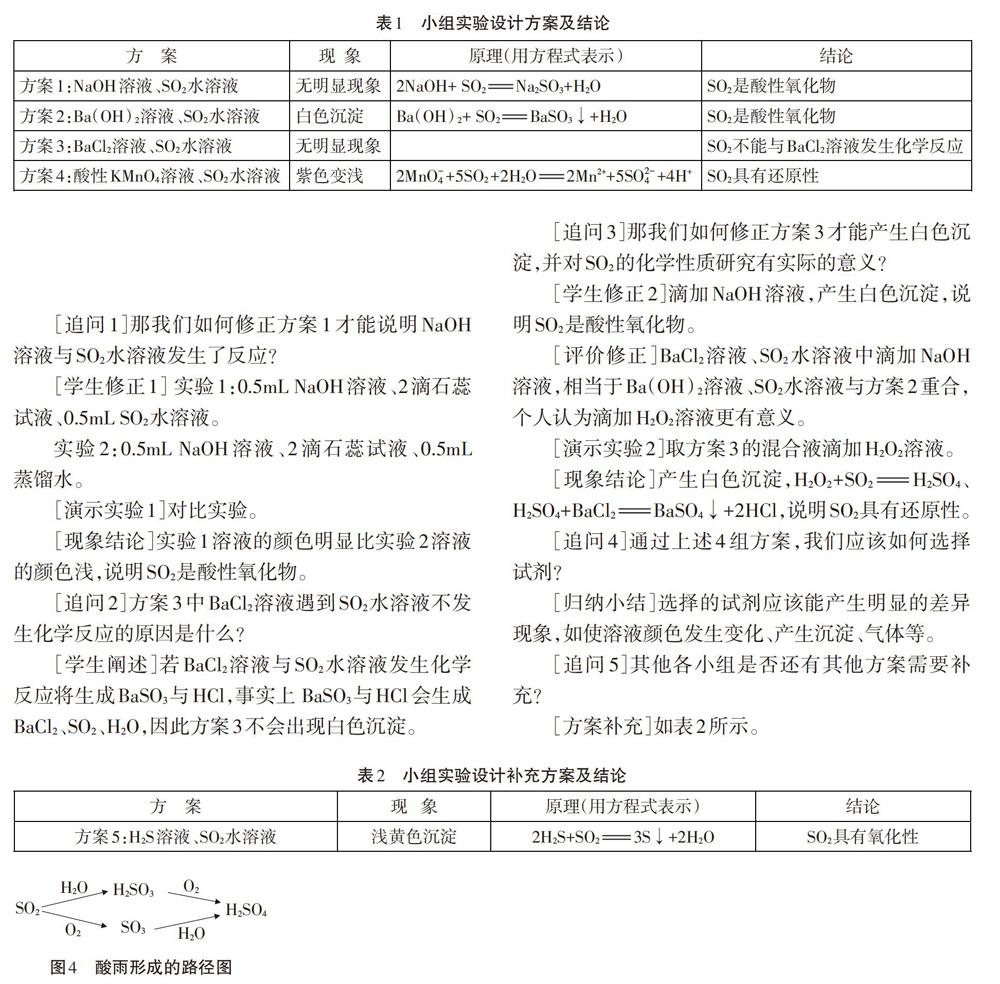
3.“魚”型板書
“魚”型板書,如圖2所示,是一種化學美,是一種藝術美,更是一種生活美,蘊含了人與自然的和諧可持續發展。
四、課堂實錄
1.直面酸雨形成,建構SO2性質模型
任務1:酸雨如何形成?——SO2的性質
[實物展示]一瓶裝有二氧化硫的礦泉水瓶。
[問題思考1]人們一談到二氧化硫就與酸雨聯系在了一起,你們知道其中的原因嗎?
[學生搶答]二氧化硫溶于水顯酸性。
[活動演示1]創新實驗:用注射器向裝有二氧化硫的礦泉水瓶中注入少量紫色石蕊試液。
[匯報總結]礦泉水瓶癟了,溶液變為紅色,說明二氧化硫溶于水,并且與水反應生成了亞硫酸,二氧化硫是一種酸性氧化物。
設計意圖:實驗是化學課堂教學最能博人眼球的教學手段,宏觀表象礦泉水瓶的癟、溶液顏色的變化,可以引發對微觀世界的探析,深入思考微粒之間發生怎樣的變化,二氧化硫還可能具備哪些化學性質。
[教學過渡]二氧化硫除了能與水反應,其他的化學性質就交給大家進行探究。接下來,四人一小組,根據提供的藥品,設計實驗方案、挑選合理試劑、開展實驗探究,并完成表格的填寫。
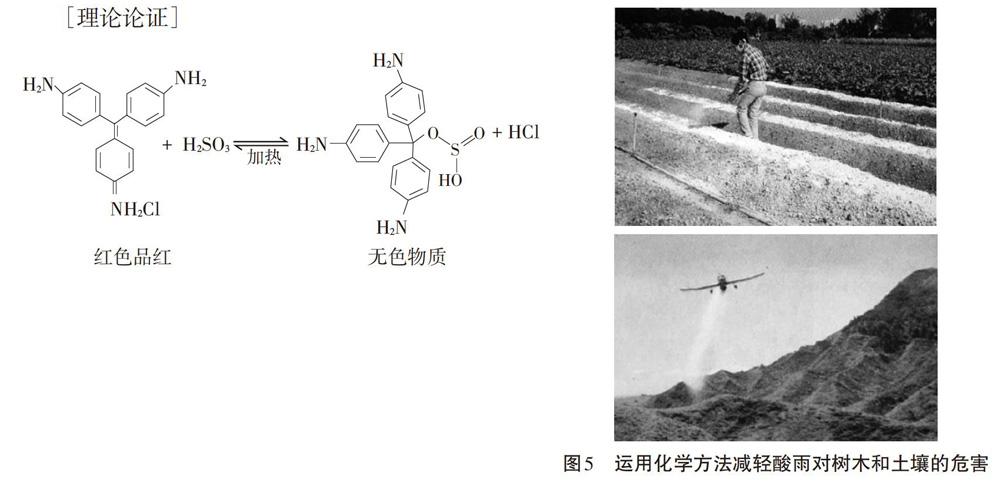
[儀器及藥品展示]西林瓶(密封小試劑瓶)如圖3所示、裝有S02水溶液的注射器、BaCI2溶液、鹽酸、H2O2溶液、酸性KMnO4溶液、Ba(OH)2溶液、NaOH溶液、H2S溶液、H2SO4溶液。
[活動探究1](1)打開西林瓶橡皮塞,將0.5mL左右(半吸管)的所選試劑加入西林瓶中,蓋上瓶塞。
(2)將0.5mL左右SO2水溶液注射到西林瓶中,振蕩。
[成果分享]學生闡述實驗方案及設計方案的理由,并通過微型實物投影分享小組實驗的成果,如表1所示。
[問題思考2]上述小組的4組實驗方案,大家看看是否都合理?
[學生質疑]方案1沒有明顯現象不能說明NaOH溶液與SO2水溶液發生了化學反應;方案3的設計對SO2的化學性質研究好像沒有什么特別的意義,可以去除。
[歸納總結]上述方案實際上體現了兩條線:化合價沒有發生變化的反應體現了SO2具有酸性氧化物的性質;化合價發生變化的反應,如化合價升高體現了sO2具有還原性,如化合價降低體現了SO2具有氧化性。
設計意圖:探究實驗是化學課堂教學最能激發學生學習興趣從而積極主動參與課堂、真正體現課堂主體作用的教學方法。學生通過親自參與設計實驗方案、討論實驗方案、完善實驗方案、開展實驗探究、觀察現象變化、感知微粒變化,運用守恒思想,從而得出科學合理的實驗結論。學生探究實驗在西林瓶(裝有橡膠塞)中開展微型實驗,使整個教室感受不到任何刺激性氣味,保護了每個人的嗅覺器官,充分體現了化學的綠色化,也體現了實驗教學的創新性。
2.繪制酸雨路徑圖,完善SO2性質模型
任務1:酸雨如何形成?——路線圖
[活動探究2]酸雨是怎么形成的,請各小組成員合作繪制酸雨形成的路徑圖。
[成果分享]路徑圖,如圖4所示。
[問題思考3]硫酸型酸雨存在亞硫酸嗎?如何檢驗?
[演示實驗3]向裝有一定量sO2水溶液的試管中加入2滴品紅溶液。
[現象結論]品紅溶液褪色,說明SO2水溶液具有漂白性。
[追問6]sO2水溶液的漂白原理與氯水的漂白原理是否相同呢?
[學生闡述]不相同。氯水中含有強氧化性的HC10能夠漂白有機色素、指示劑等,而SO2水溶液不能漂白石蕊溶液。
[實驗論證][活動演示1]的混合溶液始終呈現紅色。
[理論論證]
[演示實驗4]向[演示實驗3]的試管口套上氣球,加熱,再恢復室溫。
[現象結論]加熱后,溶液恢復紅色且氣球鼓起來,說明SO2水溶液與品紅生成的新物質穩定性不強且受熱分解后有氣體產生;恢復至室溫,氣球癟了且溶液顏色再次褪去,說明鼓起來的氣體有SO2且再次體現了sO2水溶液具有漂白性。
設計意圖:繪制路徑圖是構建知識網絡的常見方法,先通過學生自主繪制酸雨路徑圖逐步完善二氧化硫的性質模型,接著通過[演示實驗3]說明了SO2水溶液具有漂白性,再通過[活動演示1]的實驗現象說明了SO2水溶液與氯水的漂白原理不同,最后通過[理論論證]和[演示實驗4]清晰地展現了SO2水溶液的漂白原理,從而進一步完善了二氧化硫的性質模型。
3.運用SO2性質模型,防治酸雨危害
任務2:酸雨如何防治?
[問題思考4]酸雨已經形成,那會帶來哪些危害呢?
[學生闡述]酸雨進入江河湖泊,會導致魚類難以生存,影響水生生物的繁殖;酸雨進入土壤,會使鈣、鎂、磷等營養元素溶出并流失,導致土壤肥力下降,并被逐漸酸化,使農作物和樹木的生長遭到破壞;酸雨會使橋梁、雕塑等建筑物的腐蝕加快,許多文物古跡遭到嚴重破壞。
[社會熱點]酸雨的危害帶來了巨大的環境問題,成為了社會關注的焦點并引起了我國政府的高度重視,下面我們看一則最新“十九大”關于酸雨的新聞報道。
[問題思考5]“十九大”新聞報道中你獲取哪些信息?
[學生闡述]我國酸雨區的面積、污染的程度都呈現明顯下降的趨勢,這是一件值得點贊的事情。
[活動探究3]大家認為我國可能采取了哪些有效措施對酸雨進行防治?
[成果分享]用太陽能、氫能等代替含硫的傳統能源;使用含硫的傳統能源前先把硫元素除去,使之轉化為工業需要的硫酸、硫酸鈣等;在受酸雨危害的地方撒石灰等。運用化學方法減輕酸雨對樹木和土壤的危害,如圖5所示。
[歸納總結]上述措施可歸納為兩個字“防”和“治”:①抓源頭,開發新能源、脫硫法進行“防”;②滅產物,利用撒石灰等進行“治”。防治結合,以防為主。
設計意圖:學生通過認識酸雨的危害,進而認識到需要采取措施防治酸雨,再通過對“十九大”熱點的關注,進一步喚醒學生的社會責任意識,并運用S02性質模型提出有效防治酸雨的具體措施,且總結出防治結合、以防為主的新型科學理念。防治酸雨的其中一項有效措施是將硫元素轉化為硫酸,該轉化方式為后續工業制備硫酸的知識學習作了有效鋪墊。
4.再認知SO2性質模型,定量檢測防治酸雨
任務3:二氧化硫如何定量檢測?
[問題思考6]華能玉環電廠是一座大型的火力發電廠,如圖6所示,為減少二氧化硫的排放,在燃煤的過程中往往添加一定量的石灰石,你知道其中的原因嗎?
[案例分析]碳酸鈣在高溫下分解生成二氧化碳和氧化鈣,氧化鈣與二氧化硫生成亞硫酸鈣,亞硫酸鈣被空氣中的氧氣氧化成硫酸鈣。
[歸納總結]華能玉環電廠選用碳酸鈣作為原料得到硫酸鈣產品,這就是應用最為廣泛的石灰石一石膏法,這種脫硫法“變廢為寶”“綠色化學”,實現了可持續性發展。
[活動探究4]華能玉環電廠二氧化硫的排放是否符合國家標準(表3)?你能設計定量的檢測方案嗎?
[方案分享]
方案1:取一定量樣品氣體,通入到足量的Ba(OH)2溶液,過濾,洗滌,干燥,稱量固體BaSO3的質量,根據元素守恒換算得到SO2的體積。
方案2:取一定量樣品氣體,通入到足量的H202溶液,滴加BaCI2溶液至沉淀完全,過濾,洗滌,干燥,稱量固體BaSO4的質量,根據元素守恒換算得到SO2的體積。
方案3:取一定量樣品氣體,通入到足量的H2S溶液,過濾,洗滌,干燥,稱量固體s的質量,根據元素守恒換算得到sO2的體積。
[方案評價]方案2相對比較完整,而方案1、方案3都有所欠缺。方案1只考慮SO2是酸性氧化物,與Ba(OH)2反應生成BaSO3沉淀,而樣品氣體中肯定含有O2,在水溶液中O2容易將亞硫酸根氧化生成硫酸根,如果部分被氧化,那得到的固體成分是BaSO3和BaSO4的混合物;如果完全被氧化,那得到的固體成分是BaSO4,所以不能準確換算出S02的體積。方案3利用SO2的氧化性,與H2S反應生成s沉淀,而樣品氣體中含有O2同樣會將H2S氧化生成s,因此不能準確換算出SO2的體積。
[教學過渡]方案2利用SO2的還原性,與H2O2溶液發生氧化還原反應,產物硫酸根再與BaCl2溶液生成硫酸鋇沉淀,最后根據s元素守恒,可以較為準確換算出SO2的含量。隨著科技的發展,SO2傳感器技術的出現可以更為便捷地判斷華能玉環電廠二氧化硫的排放是否符合國家標準。
[傳感器展示]實驗室手持SO2傳感器,如圖7所示;生活中監測用的SO2傳感器,如圖8所示。
[活動演示2]創新實驗:打開[活動演示1]的礦泉水瓶的瓶塞,將實驗室手持S02傳感器的感應頭靠近礦泉水瓶的瓶口。
[現象結論]傳感器顯示靈敏,說明SO2傳感器能快速準確的測定空氣中的SO2含量。
設計意圖:[問題思考6]讓sO2性質模型得以落地,石灰石一石膏法提升了學生“變廢為寶”“綠色化學”、可持續發展的社會責任意識,真正體現了“化學從生活中來,化學回生活中去”的教學理念。學生通過[活動探究4]對SO2的性質研究從定性走向定量,更為深刻地理解了SO2性質模型即模型的再認知,揭示了污染需從源頭抓起,以防為主。[活動演示2]不僅突破了傳統的定量檢測方法,而且開闊了學生的視野,更提升了學生的創新意識(創新是一門學科、一個國家得以發展的生長點)。
[課堂小結]通過“酸雨與二氧化硫”的學習,我們理解了酸雨的形成過程,了解了酸雨的危害,懂得了如何防治酸雨,如何定量測定空氣中二氧化硫的含量做好酸雨的提前防范,其核心就是二氧化硫的性質和作用。勇于直面酸雨問題,合理利用所學知識并敢于靈活運用于生活中解決酸雨問題,可實現變廢為寶、可持續性綠色化發展。通過學生實驗活動探究的學習,我們從物質類別的角度來看二氧化硫是一種酸性氧化物,從化合價升降的角度來看二氧化硫具有還原性也具有氧化性,二氧化硫更側重于它的還原性。在以后的元素及其化合物的學習中,我們就可以從物質的類別角度和氧化還原的角度進行分析。

