秀麗隱桿線蟲模型在阿爾茨海默病研究中的應用
唐曉麗,楊 依,劉 悅,方 芳
(北京中醫藥大學中藥學院中藥藥理系,北京 102488)
阿爾茨海默病(Alzheimer's disease,AD)是一種與衰老相關的神經退行性疾病。隨著人口老齡化,AD已被認為是65歲以上老人的健康殺手。流行病學顯示,2001年全球老年癡呆癥的患者高達2 430萬人,預計到2040年增加到8 110 萬人[1],AD則是老年癡呆癥的主要構成因素。AD的主要病理學特征為細胞外β-淀粉樣蛋白沉積,細胞內神經纖維纏結和選擇性神經元死亡。AD病人臨床表現為記憶力減退,認知障礙以及人格改變。在AD病人的腦中均存在富含β-淀粉樣蛋白的老年斑和微管相關蛋白Tau高度磷酸化形成的神經元纖維纏結,β-淀粉樣蛋白寡聚體和高度磷酸化的Tau蛋白均有神經毒性,可能參與AD的發病機制。科學家們經過不斷的探索,依然未能找到逆轉AD確有療效的藥物,主要原因是AD為一種由多因素導致的疾病,其確切的病理機制還未闡明。穩定的病理模型有利于闡明AD的病因、分子機制及治療藥物評價。近年來,秀麗隱桿線蟲因神經系統結構簡單、遺傳信息清晰、生命周期短等優點作為一種模型生物,在神經退行性疾病、肌肉萎縮癥[2]、抗感染[3]等領域的藥物研究中得到廣泛的應用。本文結合AD的主要病理特征,對近幾年秀麗隱桿線蟲在AD研究中的應用作簡要總結。
1 秀麗隱桿線蟲簡介
1.1 生物學特征秀麗隱桿線蟲(Caenorhabditiselegans,C.elegans)屬于動物界、線形動物門、小桿亞綱(Rhabditia)、小桿目(Rhabditidia)、小桿總科(Rhabditoidea),它以細菌為食,在土壤中營自由生活,成蟲體長為1.0~1.5 mm,體直徑約為70.0 μm。有雌雄同體蟲和雄蟲兩種蟲體(Fig 1),自然界中大多為雌雄同體蟲。雌雄同體蟲一生可產卵約300個,卵發育成成蟲后的雌雄同體蟲體細胞有959個,雄蟲有1 031個。線蟲從卵發育至成蟲大約為3 d,一生經歷卵、幼蟲期(L1-L4期)和成蟲期3個時期。在幼蟲時期出現食物短缺或比較擁擠的情況時,線蟲便進入生長停滯狀態(Dauer時期),該時期的線蟲有如特異的冀膜等獨特的形態學特征,運動減少且壽命延長[4]。
1.2 秀麗隱桿線蟲作為模式生物的優勢首先,線蟲具有簡單的神經系統結構,只有1~2個不分叉的突起,形成或接受突觸連接,但其基本功能與哺乳動物相似,具有主要的神經遞質(乙酰膽堿、五羥色胺、多巴胺、谷氨酰胺等),并且線蟲的神經系統含有高等動物神經系統的大多數分子成分,可利用全基因組序列提供的信息和同源克隆等方法,分離高等動物神經系統基因[5]。這些都為研究神經系統相關功能及神經環路提供了條件。其次,線蟲身體透明,在顯微鏡下易于觀察。用不同的探針染色時在激發光下激發能產生相應的熒光,便于進行定性分析,如將綠色熒光蛋白定向導入線蟲體內可觀測某個基因表達量的變化。第三,遺傳信息清晰。線蟲基因組大小為9.7×107個堿基,大約是人類的1/30,其中基因組序列40%與人類同源,與人類疾病相關的基因同源的基因有533個,在已發現的信號通路中與人類同源的有12條[6]。利用線蟲基因組與人類基因的保守性,RNAi技術也被廣泛應用,從而為觀察單個基因在線蟲中的作用研究提供可靠的條件。第四,生命周期短,后代數目多。線蟲發育至成蟲期即開始產卵,產卵周期約為3 d,在短期內可獲得大量可用的模型線蟲。這些優點使得線蟲作為模型生物用于研究衰老相關的各種疾病(包括AD等神經退行性疾病)的病理機制和候選藥物篩選成為可能。
2 AD相關的秀麗隱桿線蟲模型
2.1 Aβ轉基因線蟲模型Aβ是一段由38或40個氨基酸組成的肽,由一種跨膜蛋白——淀粉樣前體蛋白(amyloid precursor protein,APP)經β-分泌酶和γ-分泌酶剪切而形成,具有自聚集的傾向。Aβ寡聚體異常沉積不但會阻止神經遞質從突觸前到突觸后的傳遞,從而導致突觸功能障礙和神經元丟失,而且還會在AD病人的腦中異常堆積形成老年斑,對神經系統造成嚴重的傷害。在線蟲中存在與哺乳動物APP同源的基因apl-1,其過表達對壽命呈現組織特異性影響。apl-1在神經元中過表達會導致壽命減少,但是在皮下組織中過表達則能通過抑制異時轉錄因子LIN-14的功能,以及通過DAF-16、HSF-1和DAF-12發出信號來延長壽命[7]。線蟲中雖然存在APP同源的基因apl-1,但因缺少β-分泌酶而無法產生Aβ,因此轉基因線蟲AD模型主要通過轉入人源Aβ基因,使其在特定神經元或肌肉細胞中表達,這些轉基因線蟲主要表達Aβ1-40或Aβ1-42基因,從而來模擬Aβ對AD病人造成的神經損傷。Link等[8]在1995年首先建成第一個轉入Aβ1-42的線蟲模型CL2006,在該模型中檢測到了Aβ在線蟲體壁肌細胞中的細胞毒性,通過肌肉特異性啟動子unc-54在線蟲肌肉中漸進性地表達Aβ基因,使線蟲呈現漸近性癱瘓的表型。Aβ導致的癱瘓效應與年齡有關且依賴胰島素信號途徑,將Aβ表達在特定神經元如谷氨酸神經元中,線蟲出現年齡依賴性的谷氨酸神經元退化變性[9]。這些Aβ轉基因線蟲體內的基因、蛋白分子及信號通路變化與AD病人腦內的變化有很多相似之處,對于藥物篩選特別是有關Aβ解聚作用的藥物研究具有重要的意義。Tab 1是秀麗隱桿線蟲的Aβ 轉基因模型[10]。
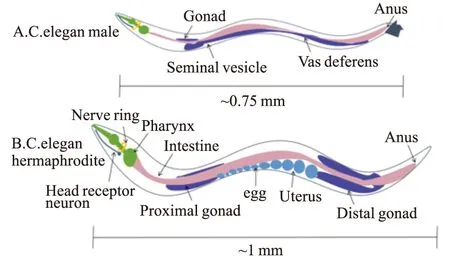
Fig 1 C.elegans pattern
2.2 Tau轉基因線蟲模型Tau蛋白過度磷酸化是AD的主要發病機制之一,Tau蛋白是一種微管結合蛋白,其過度磷酸化會降低與微管之間的親和力,過度磷酸化的Tau蛋白聚集會引起神經元纖維纏結(AD主要病理學特征之一),最終導致細胞骨架的降解[11]。研究Tau蛋白的聚集、高度磷酸化及轉錄后調控是近年來AD研究的熱點之一。Tau轉基因線蟲模型著重于tau基因的表達變化,通過其在線蟲體內特異性表達來模擬AD病人由Tau異常所造成的神經損傷。在線蟲中存在一種ptl-1的基因來負責維持細胞結構穩定性,這種基因雖與tau基因具有直向同源性,但只在一小部分神經元中表達,Tau轉基因線蟲模型用表達人Tau蛋白突變體的線蟲,可以避免內源性Tau的干擾。Kraemer等[12]在線蟲中建立了Tau轉基因模型P301L和V337M,這兩種模型能夠在觸覺神經元細胞中分別特異性地過表達人的野生型和突變型tau基因,并且都會出現運動不協調的表型,當模型線蟲中的觸覺神經元失去其功能時,由于tau基因的過表達使得神經炎癥增強,后期微管損失加重,大部分退化神經元在細胞體和神經元中產生Tau積累。Miyasaka1等[13]利用RNAi技術開發出在泛神經元中以不同水平表達人類Tau的轉基因線蟲,這種線蟲以Tau蛋白表達依賴的方式表現出行為異常,用這些模型進一步實驗發現,微管蛋白特異性伴侶或微管蛋白子集的敲低導致Tau毒性增強,即使在表達無異常行為的低表達Tau轉基因線蟲中也是如此。Tab 2是秀麗隱桿線蟲的Tau轉基因模型[14]。
2.3 Aβ和Tau雙轉基因線蟲模型Wang等[15]將轉Aβ1-42基因的線蟲CL2355和Tau轉基因線蟲BR5270通過遺傳雜交技術建立了雙轉基因的線蟲模型UM001,與單轉基因(Aβ1-42/Tau)線蟲比較,能明顯縮短線蟲壽命,與野生型線蟲N2比較,UM001后代的存活率下降以及產卵數目減少。五羥色胺作為中樞神經系統的神經遞質能夠調節多種生理功能,其含量及功能異常與AD等多種神經系統疾病的發病有關。通過遺傳雜交獲得的雙轉基因線蟲神經系統功能減弱,趨化性聯想學習記憶能力降低,五羥色胺能受到損傷,同時多巴胺能信號降低,進而丟失多巴胺能神經元。雙轉基因線蟲中的Aβ1-42影響五羥色胺能神經功能,而Tau影響五羥色胺能和多巴胺能神經功能。此外,在基因異常表達方面,對雙轉基因線蟲進行基因測序分析,有8個基因(ptch1、tbc1d16、wdfy3、arfgef2、ebf1、dao、grm1、p4ha2)與AD病人腦中的基因表達變化重合,這進一步表明雙轉基因線蟲模型更接近AD病人神經病變的生物學特征,體現Aβ1-42和Tau呈現相互促進作用,加重毒性。
3 藥物通過不同途徑保護AD模型線蟲
3.1 減少Aβ轉基因線蟲體內氧化應激水平氧化應激是指生物體細胞產生活性氧(reactive oxygen species,ROS)的不平衡,以及生物體在面對某些內源性或外源性刺激時抵消ROS這種不平衡的能力。Aβ誘導的氧化應激和毒性則是AD的主要危險因素,目前已研究出很多藥物以抗氧化劑的形式減少Aβ誘導的氧化應激。如紅曲素(monascin,MS)是一種來源于食用菌的次生代謝產物,是具有抗氧化作用的新型化合物。研究顯示,MS能使CL2006和CL4176線蟲的Aβ聚集量和癱瘓水平下降,在胡桃醌(250 μmol·L-1)誘導的氧化應激條件下,MS增加了線蟲的存活率,減弱了線蟲內源性ROS水平[16]。進一步用實時熒光定量PCR檢測到MS增加了CL4176線蟲中daf-16基因和抗氧化基因sod-1,sod-2,sod-3,hsp16.2的mRNA水平。在CL2006和CL4176線蟲中進行daf-16 RNAi,發現MS未能使癱瘓水平降低,說明MS可能依賴DAF-16而發揮降低氧化應激和Aβ毒性的作用。
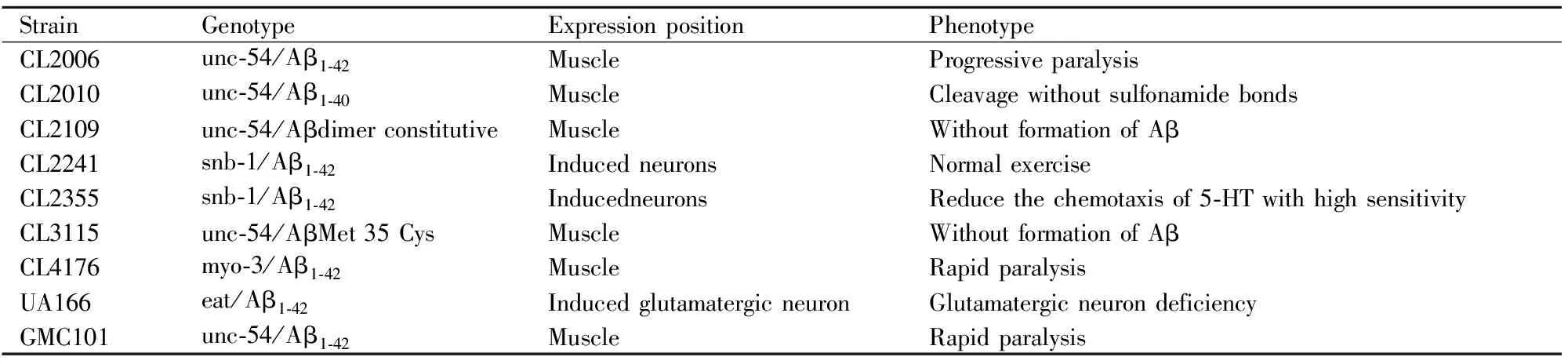
Tab 1 Aβ transgenic model of C.elegans
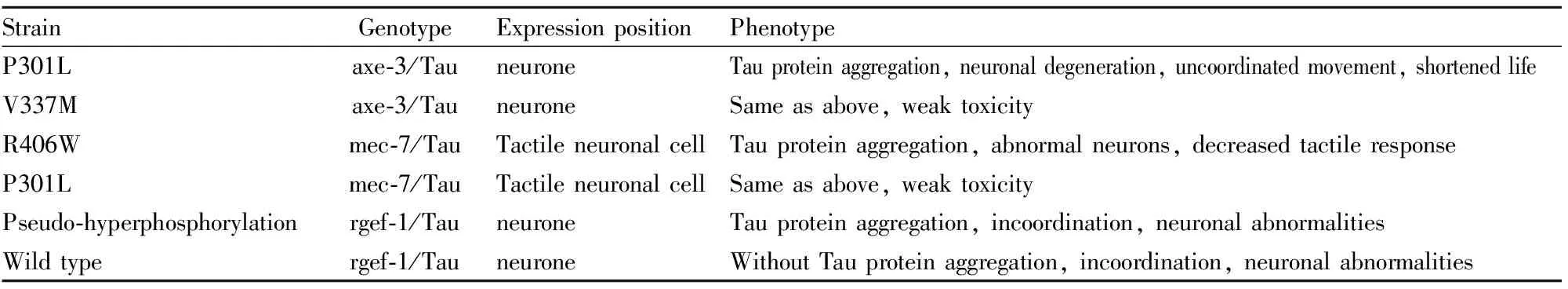
Tab 2 Tau transgenic model of C.elegans
三基數旱地菊水醇提取物(carqueja hydroalcoholic extract,CHE)和氧代異丙腎上腺素生物堿衍生物8-1也能增強氧化壓力抗性,在氧化應激狀態下通過不同的方式對線蟲起到保護的作用。CHE既在氧化應激條件下通過提高野生型線蟲的存活率并降低ROS水平來改善氧化壓力抗性,而這種作用不依賴于轉錄因子(SKN-1和DAF-16)以及應激相關的信號通路(p38, JNK和ERK)。CHE還能增加蛋白酶體活性和兩種熱休克蛋白基因hsp-16.2、hsp-4的表達,進而提高CL4176線蟲對Aβ毒性的防御能力[17]。氧代異丙腎上腺素生物堿衍生物8-1能夠延遲GMC101線蟲的麻痹表型,在H2O2誘導的急性氧化應激和百草枯誘導的慢性氧化應激條件下均可提高GMC101線蟲的存活率,同時還能增強GMC101線蟲中自噬起始基因bec-1的表達水平[18]。
3.2 抑制Aβ轉基因線蟲體內Aβ聚集從而降低毒性Aβ轉基因線蟲模型的主要特征是在線蟲的特定神經元或肌肉細胞中存在Aβ基因的漸近性表達,使線蟲表現出漸近性地癱瘓。一些天然產物和藥物成分能夠抑制CL4176、GMC101等模型線蟲中的Aβ聚集,從而來降低Aβ誘導的毒性損傷。有研究顯示,一種新型卟啉肽DhHP-6具有微過氧化物酶活性和細胞滲透性,能夠有效抑制Aβ聚集并降低Aβ的β-折疊率[19]。DhHP-6 100 μmol·L-1能顯著延長CL4176線蟲的壽命,降低癱瘓表型,抑制Aβ 斑塊形成從而降低Aβ誘導的神經毒性。此外,8-羥基喹啉(8-hydroxyquinolines,8-HQ)能以1~10 μmol·L-1的親和力結合Aβ并抑制大寡聚體(>30 kDa)的形成,通過穩定小二聚體無毒Aβ構象異構體來中和具有神經毒性的Aβ寡聚體形成,用8-HQ處理也降低了GMC101線蟲體內可溶性Aβ寡聚體的水平[20]。
3.3 維持蛋白質穩態改善Aβ轉基因線蟲的病理變化泛素-蛋白酶體系統(ubiquitin-proteasome system,UPS)負責控制細胞內許多關鍵過程相關蛋白質的降解,包括細胞周期和轉錄,以及蛋白質質量控制。蛋白酶體是UPS的重要組成成分之一,也是細胞蛋白水解網絡的組成部分,通過對正常和異常蛋白的蛋白水解作用的調節來維持蛋白質穩態[21]。基于蛋白酶體在維持蛋白質穩態中的重要作用,科學家們從蛋白酶體出發進行了一系列的研究。
不同藥物或活性成分能通過增加蛋白酶體活化特性或以DAF-16依賴的方式等多種途徑來改善蛋白質穩態。研究顯示,18α-甘草次酸(18a-glycyrrhetinic acid,18α-GA)具有蛋白酶體活化特性,可作為多細胞生物體中延長壽命和抗凝聚的因子[21]。18α-GA喂養線蟲導致蛋白酶體活性增加,隨著蛋白酶體活性的升高對Aβ模型線蟲產生了一定的影響,如CL4176和CL2006的癱瘓率降低,CL2331和CL4176中的Aβ聚集減少等。線蟲中的skn-1基因與人類Nrf基因具有同源性,能夠維持UPS的表達和活性。當蛋白酶體基因表達和活性被阻斷時,SKN-1能夠發揮激活多類蛋白酶體亞基基因的作用,在一定條件下SKN-1會參與線蟲中的蛋白酶體活化[22],18α-GA還能以SKN-1和蛋白酶體活化依賴性的方式延長線蟲的壽命。有研究表明,飲食干預可以促進健康并有助于預防AD,蜂王漿及酶處理的蜂王漿補充劑均能延緩CL2006線蟲的麻痹,發揮作用依賴于DAF-16和胰島素/胰島素樣生長因子信號通路而不需要HSF-1和SKN-1[23]。蛋白質溶解度是蛋白質穩態的標志,蜂王漿及酶處理的蜂王漿補充劑以DAF-16依賴的方式改善了蛋白質穩態。
3.4 對抗Tau過度磷酸化減輕Tau轉基因線蟲的病理變化能量代謝受損是AD發病進展的重要標志,抑制能量代謝有關的線粒體酶——二氫硫辛酰胺脫氫酶(dihydrolipoamide dehydrogenase,DLD),可導致Tau轉基因線蟲VH255全身葡萄糖水平升高以及Tau磷酸化增加。此過程通過RNAi技術抑制dld-1基因或直接用抑制劑2-甲氧基吲哚-2-羧酸抑制DLD酶,最終誘導了線蟲的高血糖和Tau磷酸化。鈣離子載體A23187可以減少由DLD的化學或遺傳抑制誘導的Tau磷酸化起到對線蟲的保護作用,但它不能減少由高血糖誘導的Tau磷酸化[24]。
Tau模型線蟲V337M表現出壽命縮短,運動不協調和磷酸化不溶性Tau積累的特征。Gamir-Morralla等[25]研究具有蛋白質抗聚集性的硫磺素T(thioflavin T,Th T)和一種具有高選擇性的糖原合酶激酶-3抑制劑NP103對V337M線蟲的影響,分別從壽命和運動表型方面進行檢測。結果顯示,Th T的不同濃度10、25、50 μmol·L-1均延長了V337M線蟲的壽命,NP103濃度為100 μmol·L-1時改善了V337M線蟲的麻痹表型,但對壽命沒有顯著影響。
4 結語
AD是一種嚴重威脅人類健康的疾病,目前尚無確切的治療方法,使用一種經濟高效的動物模型對AD的藥物研究及篩選至關重要。線蟲作為模型生物具備神經系統簡單、正向遺傳、容易進行RNAi、構建轉基因體系等優點,與大鼠、小鼠等模型相比用藥方便,飼養簡單,成為能夠研究AD等神經退行性疾病的重要手段。通過不同的技術手段建立的Aβ轉基因及Tau轉基因線蟲模型較多,目前應用Tau轉基因線蟲研究Tau蛋白的損傷機制及AD藥物的篩選與利用Aβ轉基因線蟲進行的研究相比較少,利用Tau模型線蟲還有著很大的研究空間。因此,利用線蟲進行抗AD等神經退行性疾病藥物的毒性評價及藥物篩選具有廣闊的應用前景。