基于思維發(fā)展的高三化學(xué)復(fù)習(xí)教學(xué)實踐
林立豪

[摘要]酸堿滴定曲線的圖像形式多變,考查內(nèi)容多樣,而借助解題模型的構(gòu)建培養(yǎng)學(xué)生思維的整體性、靈活性和深刻性,可有效突破酸堿滴定圖像學(xué)習(xí)的難點,促進學(xué)生思維發(fā)展,優(yōu)化復(fù)習(xí)效果,提升復(fù)習(xí)效率。
[關(guān)鍵詞]思維發(fā)展,解題模型,二元酸,滴定曲線
[中圖分類號]G633.8[文獻標識碼]A [文章編號]1674-6058(2020)11-0068-02
高三化學(xué)復(fù)習(xí)教學(xué),不應(yīng)只是讓學(xué)生對原有知識進行回顧和記憶,而是要讓學(xué)生在理解的基礎(chǔ)上靈活運用,深化鞏固,促進思維的發(fā)展,提升思維的品質(zhì)。在實際的教學(xué)實踐中,學(xué)生常會出現(xiàn)僵化的生搬硬套學(xué)習(xí)模式,無法將所學(xué)知識與實際情境建立聯(lián)系,使復(fù)習(xí)效果大打折扣。結(jié)合教學(xué)實踐分析發(fā)現(xiàn),產(chǎn)生這些問題的主要原因是教學(xué)過程缺乏對學(xué)生思維發(fā)展的引導(dǎo),使學(xué)生對知識的理解和應(yīng)用能力不足,思維得不到有效的提升和發(fā)展。
針對教學(xué)過程中所出現(xiàn)的問題,圍繞“知識一)思考→思維”的發(fā)展主線展開教學(xué),使學(xué)生更好地理解知識,并運用所學(xué)知識建立科學(xué)的分析方法,形成系統(tǒng)的思維方式,減少對知識的機械記憶和生搬硬套,實現(xiàn)有效的深度學(xué)習(xí),提升學(xué)生的學(xué)科核心素養(yǎng)和思維品質(zhì)。本文以“二元酸的滴定曲線”復(fù)習(xí)課為例,簡要闡述以思維發(fā)展為核心的高三化學(xué)復(fù)習(xí)教學(xué)實踐。
一、問題導(dǎo)學(xué),培養(yǎng)思維的整體性
思維的整體性是指思考問題時不能局限于問題的局部特征,更應(yīng)關(guān)注問題的整體結(jié)構(gòu),運用宏觀與微觀、定性與定量思想相結(jié)合的方式提取有效信息,全面分析問題,挖掘問題的關(guān)鍵和本質(zhì),構(gòu)建解題的知識系統(tǒng),從而快速、有效地解決問題。酸堿滴定曲線是利用數(shù)學(xué)工具來表示化學(xué)反應(yīng)的過程,相比于文字描述,其優(yōu)點是能夠?qū)⒎磻?yīng)過程直觀、清晰地表示出來。利用圖像將化學(xué)反應(yīng)過程轉(zhuǎn)化為數(shù)學(xué)函數(shù),考查學(xué)生提取信息、分析數(shù)據(jù)進而解決問題的能力。
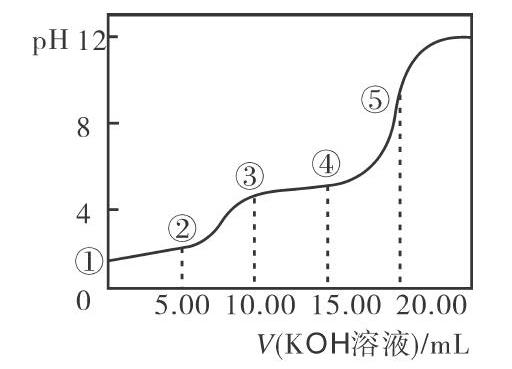
[例1]常溫下,用0.10mol·L-1KOH溶液滴定10.00mL 0.10mol·L-1H2C2O4(二元弱酸)溶液,所得滴定曲線如圖1所示(混合溶液的體積可看成混合前溶液的體積之和)。請結(jié)合圖像分析、思考以下幾個問題:
(1)②點時溶液中的溶質(zhì)是什么?
(2)②點時溶液中存在哪些平衡?(用離子方程式表示)
(3)②點溶液中K+、H2C2O4、HC2O4-、H+、OH-的微 粒濃度大小關(guān)系如何?
(4)②點時溶液中c(K+)=____mol·L-1。
(5)寫出②點溶液中存在的守恒關(guān)系(電荷守恒、物料守恒)。
以問題為導(dǎo)向,指導(dǎo)學(xué)生觀察圖像的橫縱坐標和曲線的變化趨勢,認識滴定反應(yīng)的過程,接著著眼于圖像上的某一特殊點,從宏觀反應(yīng)到微觀粒子,從定性認識到定量分析,先找出這個特殊點的溶液中的溶質(zhì)并確定各溶質(zhì)間的比例關(guān)系,再分析微粒在水溶液中存在的電離和水解平衡及電離和水解能力的強弱關(guān)系,進而得出微粒濃度間的大小關(guān)系。通過討論、分析及知識的整合,全面認識某一特殊點所涉及的問題,形成全面、完整的解題思維,構(gòu)建滴定曲線的解題模型;再運用解題模型分析圖像上其他的特殊點,實現(xiàn)知識的遷移和應(yīng)用,在實踐的基礎(chǔ)上更好地理解和應(yīng)用解題模型,促進思維發(fā)展。
二、對比分析,培養(yǎng)思維的靈活性
思維的靈活性是指善于抓住事物變化的本質(zhì)特征,根據(jù)實際情況及時調(diào)整思路和方法,進而獲得解決問題的最佳方案。酸堿滴定曲線通過變換條件形成新的滴定變化曲線,學(xué)生在原有解題模型的基礎(chǔ)上進行對比分析,找出新曲線發(fā)生的本質(zhì)變化,選擇合適的角度和方向探索解決問題的新思路,驗證新方法,并及時總結(jié)和改進,完善解題模型,增強思維能力。
在分析圖像的過程中抓住滴定反應(yīng)的特點和曲線變化的特征,可提高學(xué)生對反應(yīng)本質(zhì)的認識和理解;再結(jié)合原有的解題模型,即可突破圖像上各點溶質(zhì)的判斷和相應(yīng)微粒電離、水解能力的大小判斷以及微粒濃度大小關(guān)系的比較等難點。通過知識的類比、遷移和有效分析,實現(xiàn)對解題模型的理解和應(yīng)用,培養(yǎng)思維的靈活性。
三、自主探究,培養(yǎng)思維的深刻性
思維的深刻性是指善于透過現(xiàn)象發(fā)現(xiàn)事物發(fā)展的本質(zhì)和規(guī)律,深入思考并有效解決問題。要培養(yǎng)思維的深刻性,應(yīng)根據(jù)知識間的內(nèi)在聯(lián)系,由淺入深、由表及里、由易到難、逐步深入,加深對知識的梳理和理解,實現(xiàn)對知識的深度學(xué)習(xí)和靈活運用。
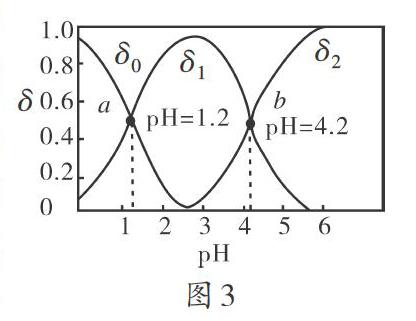
[例3]常溫下,用0.10mol·L-1的NaOH溶液滴定10.00mL 0.10mol·L-1的二元弱酸(H2A)溶液,所得溶液中各種含A的微粒的物質(zhì)的量分數(shù)(δ)與pH的變化曲線如圖3所示。
通過前面例題的演練和講解,學(xué)生對于二元酸的滴定曲線已經(jīng)有了較為深入的認識。可以讓學(xué)生結(jié)合前面的知識進行小組討論和探究,看例3可以設(shè)置哪些方面的問題進行相關(guān)知識的考查。教師收集學(xué)生的討論結(jié)果,整理出以下問題:
(1)δ0、δ1、δ2分別表示什么微粒的物質(zhì)的量分數(shù)?
(2)分別列出pH=1.2、pH=4.2時溶液中微粒間的守恒關(guān)系。
(3)分別計算常溫下的Ka1(H2A)、Ka2(H2A)。
(4)比較常溫下NaHA溶液中c(OH-)與c(H+)的大小關(guān)系。
(5)pH=1.2時,滴入的NaOH的體積5.0mL(填大于、等于或小于,下同);pH=4.2時,c(Na+)____3c(A2-)。
學(xué)生通過自主討論并設(shè)置相關(guān)問題,更好地鞏固和理解了滴定圖像分析的基本思路,在問題的討論和解析過程中培養(yǎng)了思維的靈活性。如問題(4)的實質(zhì)是比較HA-的電離和水解能力的大小,可以應(yīng)用Ka1(H2A)、Ka2(H2A)的數(shù)據(jù)進行分析,也可利用δ1的最高點溶質(zhì)主要為NaHA,此時溶液的pH<7推知HA-的電離強于水解。在學(xué)生自主探究的過程中引領(lǐng)學(xué)生重視利用數(shù)據(jù)進行推理,建立定量的認知模型,對化學(xué)學(xué)科形成深刻理解,培養(yǎng)學(xué)生深度思考的習(xí)慣,促進學(xué)生思維的發(fā)展。
總之,基于思維發(fā)展的二元酸滴定曲線復(fù)習(xí)教學(xué),應(yīng)立足于學(xué)科核心素養(yǎng)的培養(yǎng),關(guān)注教學(xué)過程的整體性和層次性,把握問題解決的主線,構(gòu)建有效的思維模型,促進學(xué)生思維的發(fā)展,使高三復(fù)習(xí)擺脫題海戰(zhàn)術(shù)的束縛,優(yōu)化復(fù)習(xí)效果,提升復(fù)習(xí)效率。

