棘白菌素類(lèi)抗真菌藥物預(yù)防侵襲性念珠菌血癥有效性與安全性的Meta分析
李莎 戴立波 姚海濤 孔旭東


摘 要目的:系統(tǒng)評(píng)價(jià)棘白菌素類(lèi)抗真菌藥物預(yù)防侵襲性念珠菌血癥的有效性及安全性,為臨床治療提供循證參考。方法:計(jì)算機(jī)檢索PubMed、Embase、Medline、Cochrane圖書(shū)館、中國(guó)期刊全文數(shù)據(jù)庫(kù)、中文科技期刊數(shù)據(jù)庫(kù)、萬(wàn)方數(shù)據(jù),檢索時(shí)限為建庫(kù)起至2019年7月,收集棘白菌素類(lèi)藥物(試驗(yàn)組)對(duì)比常規(guī)抗真菌藥物(兩性霉素B及三唑類(lèi)抗真菌藥,對(duì)照組)預(yù)防侵襲性念珠菌血癥有效性和安全性的隨機(jī)對(duì)照試驗(yàn)(RCT),對(duì)符合納入標(biāo)準(zhǔn)的臨床研究進(jìn)行資料提取并采用Cochrane系統(tǒng)評(píng)價(jià)員手冊(cè)5.0.2進(jìn)行質(zhì)量評(píng)價(jià)后,采用Rev Man 5.2 統(tǒng)計(jì)軟件對(duì)突破性侵襲性真菌感染率、真菌感染死亡率、全因死亡率及因不良反應(yīng)停藥的發(fā)生率進(jìn)行Meta 分析。結(jié)果:共納入7項(xiàng)RCT,合計(jì)3 219例患者。Meta 分析結(jié)果顯示,試驗(yàn)組患者突破性侵襲性真菌感染發(fā)生率[OR=0.58,95%CI(0.40,0.85),P=0.004]、真菌感染死亡率[OR=0.68,95%CI(0.51,0.92),P=0.01]和因不良反應(yīng)停藥的發(fā)生率[OR=0.52,95%CI(0.40,0.67),P<0.001]均顯著低于對(duì)照組,差異均有統(tǒng)計(jì)學(xué)意義;兩組患者全因死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.84,95%CI(0.67,1.05),P=0.13]。結(jié)論:與兩性霉素B及三唑類(lèi)抗真菌藥比較,棘白菌素類(lèi)藥物用于預(yù)防侵襲性念珠菌血癥可降低突破性侵襲性真菌感染發(fā)生率、真菌感染死亡率和因不良反應(yīng)停藥的發(fā)生率。
關(guān)鍵詞 棘白菌素;預(yù)防;侵襲性念珠菌血癥;隨機(jī)對(duì)照試驗(yàn);有效性;安全性;Meta分析
中圖分類(lèi)號(hào) R978.5 文獻(xiàn)標(biāo)志碼 A 文章編號(hào) 1001-0408(2020)01-0104-06
DOI 10.6039/j.issn.1001-0408.2020.01.18
ABSTRACT OBJECTIVE: To systematically evaluate the efficacy and safety of echinococcins in the prevention of invasive candidiasis, and to provide evidence-based reference for clinical treatment. METHODS: Retrieved from PubMed, Embase, Medline, Cochrane library, CJFD, VIP and Wanfang database, randomized controlled trials (RCTs) about the effectiveness and safety of echinococcins (trial group) versus conventional fungal drugs (amphotericin B and triazole antifungal agents, control group) in the prevention of invasive candidiasis were collected during database establishment to Jul. 2019. After data extraction of clinical studies met inclusion criteria and quality evaluation with Cochrane system evaluator manual 5.0.2, Meta-analysis was performed for breakthrough invasive fungal infection rate, fungal infection mortality rate, all-cause mortality rate and the incidence of drug withdrawal due to adverse reactions by using Rev Man 5.2 statistical software. RESULTS: Totally 7 RCTs were included, involving 3 219 patients. Results of Meta-analyses indicated that the incidence of breakthrough invasive fungal infection [OR=0.58,95%CI (0.40,0.85),P=0.004], fungal infection mortality rate[OR=0.68,95%CI (0.51,0.92),P=0.01] and the incidence of drug withdrawal due to adverse reactions [OR=0.52,95%CI (0.40,0.67),P<0.001] in trial groups were significantly lower than control group, with statistical significance. There was no statistical significance in the all-cause mortality rate [OR=0.84,95%CI (0.67,1.05),P=0.13]. CONCLUSIONS: Compared with amphotericin B and triazole antifungal agents, echinococcins used for the prevention of invasive candidiasis can reduce the incidence of breakthrough invasive fungal infection, fungal infection mortality rate and the incidence of drug withdrawal due to adverse reactions.
KEYWORDS Echinococcins; Prevention; Invasive candi- diasis; Randomized controlled trials; Efficacy; Safety; Meta- analysis
免疫功能受損患者發(fā)生侵襲性念珠菌菌血癥的風(fēng)險(xiǎn)極高,高危人群包括血液系統(tǒng)惡性腫瘤患者、實(shí)體器官移植或造血干細(xì)胞移植(Hematopoietic stem cell transplantation,HSCT)受者及使用過(guò)化療藥物的患者,尤其是使用過(guò)廣泛損害胃腸道黏膜藥物的患者,感染早期診斷存在困難,延遲啟動(dòng)治療會(huì)造成不良結(jié)局,因此,需早期預(yù)防真菌感染[1-2]。Cornely OA等[3]調(diào)查了13個(gè)歐洲癌癥中心267例侵襲性念珠菌菌血癥患者,結(jié)果顯示白色念珠菌和非白色念珠菌導(dǎo)致的菌血癥比例相等,非白色念珠菌中最常見(jiàn)的是熱帶念珠菌、光滑念珠菌和近平滑念珠菌;在實(shí)體腫瘤患者中,光滑念珠菌分離株的比例最高,而熱帶念珠菌和克柔念珠菌分別是血液系統(tǒng)惡性腫瘤或接受過(guò)造血干細(xì)胞移植的患者中分離出的最常見(jiàn)病原菌。根據(jù)美國(guó)感染病學(xué)會(huì)(IDSA)2016年發(fā)布的《念珠菌病臨床實(shí)踐指南》[4],對(duì)于中性粒細(xì)胞正常或減少的患者,當(dāng)不太可能存在氟康唑耐藥菌感染(如光滑念珠菌或克柔念珠菌)的非危重患者,初始預(yù)防可選用氟康唑,考慮到克柔念珠菌一律對(duì)氟康唑耐藥,光滑念珠菌分離株很可能會(huì)對(duì)氟康唑和伏立康唑交叉耐藥,可選擇棘白菌素類(lèi)藥物,如果患者對(duì)其他抗真菌藥不耐受、利用度有限或耐藥,則可選擇兩性霉素B脂質(zhì)制劑。但臨床實(shí)踐中,存在唑類(lèi)藥物預(yù)防效果不滿意、兩性霉素B的最低抑菌濃度值較高,增加劑量的同時(shí)也會(huì)引發(fā)嚴(yán)重的腎損傷等限制[5],發(fā)生侵襲性念珠菌菌血癥的高危人群最佳的預(yù)防用藥方案目前仍存在爭(zhēng)議,因此,本研究對(duì)棘白菌素類(lèi)藥物預(yù)防侵襲性念珠菌血癥的隨機(jī)對(duì)照試驗(yàn)(Randomized controlled trial,RCT)進(jìn)行系統(tǒng)評(píng)價(jià),以為臨床提供循證參考。
1 資料與方法
1.1 納入與排除標(biāo)準(zhǔn)
1.1.1 研究類(lèi)型 國(guó)內(nèi)外公開(kāi)發(fā)表的RCT,無(wú)論是否采取盲法,語(yǔ)種限制為中、英文。
1.1.2 研究對(duì)象 納入研究的患者均為侵襲性念珠菌血癥的高風(fēng)險(xiǎn)人群,包括HSCT術(shù)后、實(shí)體器官移植術(shù)后及粒缺伴發(fā)熱的患者[3,6-7],且年齡≥16歲。患者性別、國(guó)籍不限,入組前均未確診侵襲性念珠菌血癥。
1.1.3 干預(yù)措施 對(duì)照組采用常規(guī)抗真菌藥物治療,包括兩性霉素B(脂質(zhì)體、脂質(zhì)復(fù)合物)及三唑類(lèi)抗真菌藥物(氟康唑、伏立康唑、泊沙康唑);試驗(yàn)組接受棘白菌素類(lèi)抗真菌藥物(米卡芬凈、卡泊芬凈、阿尼芬凈)治療。
1.1.4 結(jié)局指標(biāo) 結(jié)局指標(biāo)分為主要指標(biāo)及次要指標(biāo),以有效性指標(biāo)作為主要指標(biāo),包括:①突破性侵襲性真菌感染率(Breakthrough invasive fungal infection, bIFI),突破性侵襲性真菌感染定義為預(yù)防用藥期間發(fā)生了確定(Proven)、可能(Probable) 和可疑(Possible) 的系統(tǒng)性真菌感染;②真菌感染死亡率;③全因死亡率;以安全性指標(biāo)作為次要指標(biāo):④因不良反應(yīng)停藥的發(fā)生率。
1.1.5 排除標(biāo)準(zhǔn) ①非預(yù)防性應(yīng)用抗真菌感染藥物;②患者年齡<16歲;③重復(fù)發(fā)表及數(shù)據(jù)不全的文獻(xiàn)。
1.2 檢索策略
計(jì)算機(jī)檢索PubMed、Embase、Medline、Cochrane圖書(shū)館、中國(guó)期刊全文數(shù)據(jù)庫(kù)、中文科技期刊數(shù)據(jù)庫(kù)、萬(wàn)方數(shù)據(jù),檢索時(shí)限均為建庫(kù)起至2019 年7 月,并追溯納入研究中的參考文獻(xiàn)。已完成臨床試驗(yàn)但未發(fā)表的文章結(jié)果通過(guò) Clinical Trials. gov 進(jìn)行檢索。中文檢索詞包括:“棘白菌素”“米卡芬凈”“卡泊芬凈”“阿尼芬凈”“真菌感染”“隨機(jī)對(duì)照試驗(yàn)”;英文檢索詞包括:“Echinocandin”“Micafungin”“Caspofungin”“Anidulafungin”“Fungin infection”“Ramdon controlled trial”。運(yùn)用通配符、邏輯符、范圍算符等制訂檢索式。
1.3 資料提取和質(zhì)量評(píng)價(jià)
1.3.1 資料提取 制訂文獻(xiàn)信息登記表采集信息。兩名評(píng)價(jià)者經(jīng)按統(tǒng)一規(guī)范的評(píng)價(jià)方法對(duì)納入文獻(xiàn)的全文進(jìn)行獨(dú)立評(píng)價(jià),逐篇閱讀初步納入文獻(xiàn),填寫(xiě)單個(gè)文獻(xiàn)信息采集表。提取的文獻(xiàn)信息包括原文題目、發(fā)表年份、作者、研究對(duì)象、研究方法、干預(yù)措施、結(jié)局測(cè)量與評(píng)價(jià)、是否采用盲法、有無(wú)失訪等。
1.3.2 質(zhì)量評(píng)價(jià) 采用Cochrane 系統(tǒng)評(píng)價(jià)員手冊(cè)5.0.2版推薦的工具評(píng)價(jià)納入RCT 的偏倚風(fēng)險(xiǎn),包括:① 隨機(jī)方法;②分配隱藏;③盲法:對(duì)研究對(duì)象、治療方案實(shí)施者、研究結(jié)果測(cè)量者采用盲法;④退出或失訪:包括干預(yù)前基線水平測(cè)量值和干預(yù)后效應(yīng)參數(shù)值、失訪/退出情況以及是否對(duì)失訪原因加以說(shuō)明;⑤意向治療分析(ITT):對(duì)于安全性問(wèn)題、陰性結(jié)果是否進(jìn)行報(bào)道;⑥其他偏倚來(lái)源:包括試驗(yàn)早停、基線不平衡等。針對(duì)每篇納入文獻(xiàn),對(duì)上述6 項(xiàng)作出“是”(低度偏倚)、“否”(高度偏倚)和“不清楚”(缺乏相關(guān)信息或偏倚情況不確定)的判斷。由兩位評(píng)價(jià)者獨(dú)立進(jìn)行方法學(xué)質(zhì)量評(píng)價(jià),如有分歧,由第三方協(xié)助解決。
1.4 統(tǒng)計(jì)學(xué)方法
采用Rev Man 5.2統(tǒng)計(jì)軟件進(jìn)行統(tǒng)計(jì)分析,計(jì)數(shù)資料采用比值比(Odds ratio,OR)及其95%置信區(qū)間(CI)表示,并對(duì)納入的研究結(jié)果進(jìn)行異質(zhì)性檢驗(yàn)。當(dāng)各RCT間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P≥0.1,I 2<50%)時(shí),采用固定效應(yīng)模型合并效應(yīng)量;反之,則分析異質(zhì)性來(lái)源,對(duì)可能產(chǎn)生異質(zhì)性的因素進(jìn)行亞組分析;若研究間存在統(tǒng)計(jì)學(xué)異質(zhì)性而無(wú)臨床異質(zhì)性或差異無(wú)統(tǒng)計(jì)學(xué)意義時(shí),可采用隨機(jī)效應(yīng)模型合并效應(yīng)量;如果兩組間異質(zhì)性過(guò)大或無(wú)法找尋數(shù)據(jù)來(lái)源時(shí),采用描述性分析。本研究采用失安全系數(shù)法進(jìn)行發(fā)表偏倚分析。本研究采用失安全系數(shù)(Nfs)法對(duì)各項(xiàng)指標(biāo)進(jìn)行發(fā)表偏倚分析。Nfs分析是指當(dāng)Meta分析的結(jié)果有統(tǒng)計(jì)學(xué)意義時(shí),為排除發(fā)表存在的偏倚,計(jì)算最少需要多少個(gè)未發(fā)表的研究報(bào)告(特別是陰性結(jié)果報(bào)告)才能逆轉(zhuǎn)該Meta分析的結(jié)論。Nfs越大說(shuō)明發(fā)表偏倚越小,結(jié)論被推翻的可能性越小,Meta分析結(jié)果越穩(wěn)定。P=0.05或者P=0.01時(shí),Nfs可用Nfs 0.05及Nfs 0.01表示。
2 結(jié)果
2.1 文獻(xiàn)篩選結(jié)果
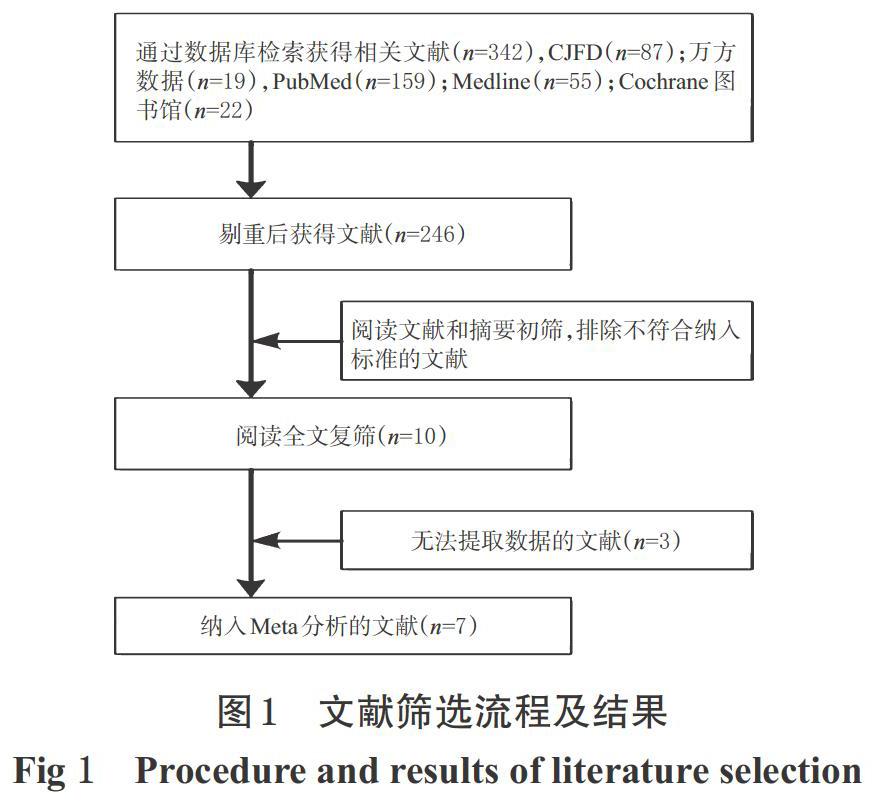
初步檢索相關(guān)文獻(xiàn)342篇,按照納入與排除標(biāo)準(zhǔn)逐層篩選后,最終納入7篇(項(xiàng))RCT[8-14] ,合計(jì)3 219例患者。文獻(xiàn)篩選流程及結(jié)果見(jiàn)圖1。
2.2 納入研究基本信息與質(zhì)量評(píng)價(jià)結(jié)果
納入的7項(xiàng)RCT均對(duì)患者的基線情況進(jìn)行了報(bào)道,均在文中提及了“隨機(jī)”,4項(xiàng)RCT[8-9,12-13]提及具體的隨機(jī)方案,1項(xiàng)RCT[11]提及是否實(shí)行分配隱藏,4 項(xiàng)RCT[8-9,11,14]實(shí)施盲法,7項(xiàng)RCT[8-14]均對(duì)缺失結(jié)果數(shù)據(jù)或缺失原因進(jìn)行描述。納入研究的基本信息與質(zhì)量評(píng)價(jià)結(jié)果詳見(jiàn)表1、表2。
2.3 Meta分析結(jié)果
2.3.1 bIFI發(fā)生率 7項(xiàng)研究(3 219例患者)[8-14]報(bào)道了bIFI發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.72,? ?I 2=0),采用固定效應(yīng)模型計(jì)算合并效應(yīng)量,Meta分析結(jié)果顯示,試驗(yàn)組患者bIFI發(fā)生率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.58, 95%CI(0.40,0.85),P=0.004]。將7項(xiàng)研究分為米卡芬凈組及其他棘白菌素類(lèi)藥物組進(jìn)行亞組分析。在米卡芬凈組,5項(xiàng)研究(1 924例患者)[9-13]報(bào)道了bIFI發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.79,I 2=0),采用固定效應(yīng)模型計(jì)算合并效應(yīng)量,Meta分析結(jié)果顯示,試驗(yàn)組患者bIFI發(fā)生率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.47,95%CI(0.28,0.80),P=0.005];在其他棘白菌素類(lèi)藥物組,2項(xiàng)研究(1 295例患者)[8,14]報(bào)道了bIFI發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.42,I 2=0),采用固定效應(yīng)模型計(jì)算合并效應(yīng)量,Meta分析結(jié)果顯示,兩組患者bIFI發(fā)生率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.73, 95%CI(0.43,1.24),P=0.24]。bIFI發(fā)生率的Meta分析森林圖見(jiàn)圖2。
2.3.2 真菌感染死亡率 5項(xiàng)研究(3 052例患者)[8-11,14]報(bào)道了真菌感染死亡率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=1.00,I 2=0) ,采用固定效應(yīng)模型計(jì)算合并效應(yīng)量, Meta分析結(jié)果顯示,試驗(yàn)組患者真菌感染死亡率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.68,95%CI(0.51,0.92),P=0.01]。將5項(xiàng)研究分為米卡芬凈組及其他棘白菌素類(lèi)藥物組進(jìn)行亞組分析。在米卡芬凈組,3項(xiàng)研究(1 757例患者)[9-11]報(bào)道了真菌感染死亡率,采用固定效應(yīng)模型計(jì)算合并效應(yīng)量, 各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.97,I 2=0),Meta分析結(jié)果顯示,兩組患者真菌感染死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.70,95%CI(0.45,1.10),P=0.13];在其他棘白菌素類(lèi)藥物組,2項(xiàng)研究(1 295例患者)[8,14]報(bào)道了真菌感染死亡率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.88,I 2=0),采用固定效應(yīng)模型計(jì)算合并效應(yīng)量, Meta分析結(jié)果顯示,兩組患者真菌感染死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.67,95%CI(0.44,1.00),P=0.05],但P值已接近有統(tǒng)計(jì)學(xué)意義的點(diǎn)。真菌感染死亡率的Meta分析森林圖見(jiàn)圖3。
2.3.3 全因死亡率 7項(xiàng)研究(3 219例患者)[8-14]報(bào)道了全因死亡率,各研究間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.90,I 2=0),采用固定效應(yīng)模型計(jì)算合并效應(yīng)量, Meta分析結(jié)果顯示,兩組患者全因死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.84,95%CI(0.67,1.05),P=0.13]。將7項(xiàng)研究分為米卡芬凈組及其他棘白菌素類(lèi)藥物組進(jìn)行亞組分析。在米卡芬凈組,5項(xiàng)研究(1 924例患者)[9-13]報(bào)道了全因死亡率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.79,? I 2=0),Meta分析結(jié)果顯示,兩組患者全因死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.89,95%CI(0.66,1.20),P=0.44];在其他棘白菌素類(lèi)藥物組,2項(xiàng)研究(1 295例患者)[8,14]報(bào)道了全因死亡率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.65,I 2=0),Meta分析結(jié)果顯示,兩組患者全因死亡率比較,差異無(wú)統(tǒng)計(jì)學(xué)意義[OR=0.79,95%CI (0.57,1.09),P=0.16]。全因死亡率的Meta分析森林圖見(jiàn)圖4。
2.3.4 因不良反應(yīng)停藥發(fā)生率 7項(xiàng)研究(3 219例患者)[8-14]報(bào)道了因不良反應(yīng)停藥發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.17,I 2=34%),采用固定效應(yīng)模型合并效應(yīng)量,Meta分析結(jié)果顯示,試驗(yàn)組患者因不良反應(yīng)停藥發(fā)生率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.52,95%CI([0.40,0.67),P<0.001]。將7項(xiàng)研究分為米卡芬凈組及其他棘白菌素類(lèi)藥物組進(jìn)行亞組分析。在米卡芬凈組,5項(xiàng)研究(1 924例患者)[9-13]報(bào)道了因不良反應(yīng)停藥發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.19,I 2=34%),采用固定效應(yīng)模型合并效應(yīng)量,Meta分析結(jié)果顯示,試驗(yàn)組患者因不良反應(yīng)停藥發(fā)生率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.44,95%CI(0.31,0.62),P=0.19];在其他棘白菌素類(lèi)藥物組,2項(xiàng)研究(1 295例患者)[8,14]報(bào)道了因不良反應(yīng)停藥發(fā)生率,各研究結(jié)果間無(wú)統(tǒng)計(jì)學(xué)異質(zhì)性(P=0.30,I 2=5%),采用固定效應(yīng)模型合并效應(yīng)量,Meta分析結(jié)果顯示,試驗(yàn)組患者因不良反應(yīng)停藥發(fā)生率顯著低于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義[OR=0.66,95%CI(0.44,1.00),P=0.05]。因不良反應(yīng)停藥發(fā)生率的Meta分析森林圖見(jiàn)圖5。
2.4 發(fā)表偏倚分析
本研究中bIFI發(fā)生率的Nfs 0.05=138.46,Nfs 0.01=61.25,真菌感染死亡率的Nfs 0.05=99.28,Nfs 0.01=45.36,因不良反應(yīng)停藥發(fā)生率的Nfs 0.05=432.05,Nfs 0.01=199.51。提示本研究所得的bIFI發(fā)生率、真菌感染死亡率和因不良反應(yīng)停藥發(fā)生率的結(jié)論發(fā)表偏倚較小。
2.5 敏感性分析
對(duì)于bIFI發(fā)生率、真菌感染死亡率、全因死亡率和因不良反應(yīng)停藥發(fā)生率的結(jié)局指標(biāo),將排除某一項(xiàng)研究再次進(jìn)行Meta分析的結(jié)果與現(xiàn)有結(jié)果比較,結(jié)果均未發(fā)生翻轉(zhuǎn),說(shuō)明本次Meta分析結(jié)果較為可靠。
3 討論
在移植物植入前期,受者發(fā)生侵襲性念珠菌病的風(fēng)險(xiǎn)最高,念珠菌菌血癥是侵襲性念珠菌病最常見(jiàn)的臨床表現(xiàn)。在常規(guī)應(yīng)用抗真菌預(yù)防治療之前,侵襲性念珠菌感染的發(fā)生率為16%~18%。雖然約一半的侵襲性念珠菌感染由白色念珠菌導(dǎo)致,但與其他患者相比,移植物受者發(fā)生非白色念珠菌屬如光滑念珠菌、熱帶念珠菌感染的風(fēng)險(xiǎn)也增加[15]。一項(xiàng)前瞻性隊(duì)列研究顯示,棘白菌素類(lèi)藥物作為一種預(yù)防侵襲性念珠菌感染的經(jīng)驗(yàn)性抗真菌藥物,米卡芬凈、卡泊芬凈和阿尼芬凈之間的有效性和安全性沒(méi)有顯著性差異[16],棘白菌素類(lèi)抗真菌藥物主要優(yōu)勢(shì)在于對(duì)念珠菌屬的殺菌活性,包括耐氟康唑的光滑念珠菌和克柔念珠菌,并且其引起腎毒性或嚴(yán)重藥物相互作用的可能性相對(duì)較低。本次納入的7項(xiàng)RCT結(jié)果表明,棘白菌素組bIFI發(fā)生率、真菌感染死亡率及因不良反應(yīng)停藥的發(fā)生率均較其他標(biāo)準(zhǔn)治療組顯著降低,為侵襲性念珠菌血癥高風(fēng)險(xiǎn)患者預(yù)防用藥提供了支持。
兩性霉素B脂質(zhì)體及三唑類(lèi)抗真菌藥物(氟康唑、伏立康唑)是目前指南推薦的用于肝移植及HSCT受者抗真菌預(yù)防的藥物,但念珠菌種類(lèi)如光滑念珠菌和克柔念珠菌對(duì)這些制劑的敏感性較低,甚至對(duì)氟康唑天然耐藥[17],對(duì)于移植術(shù)后、脊髓發(fā)育不良以及長(zhǎng)期中性粒細(xì)胞減少的患者,氟康唑不足以預(yù)防侵襲性霉菌感染(如曲霉菌病)[18]。移植患者常規(guī)使用免疫抑制劑如環(huán)孢霉素、他克莫司和西羅莫司,而氟康唑、伏立康唑與以上藥物的相互作用使給藥復(fù)雜化,在接受連續(xù)腎臟替代療法的患者中,氟康唑會(huì)被顯著清除,需要調(diào)整給藥劑量[19]。雖然兩性霉素B脂質(zhì)體與兩性霉素B去氧膽酸鹽相比降低了腎毒性風(fēng)險(xiǎn),但在腎功能不全的受者中,仍存在因腎功能而減少給藥劑量的問(wèn)題,導(dǎo)致其使用受到限制。因此,在肝移植或HSCT患者中,尤其在侵襲性念珠菌病的患病率很高(>5%)的重癥監(jiān)護(hù)病房?jī)?nèi),高風(fēng)險(xiǎn)患者可以接受棘白菌素類(lèi)藥物進(jìn)行預(yù)防[4]。
Ziakas PD等[20]報(bào)道,造血干細(xì)胞移植受體中,全身預(yù)防性抗真菌治療可以降低中性粒細(xì)胞減少患者bIFI的發(fā)生風(fēng)險(xiǎn),但總體死亡率沒(méi)有改變。本研究結(jié)果顯示,棘白菌素組與其他預(yù)防真菌感染藥物組對(duì)比,全因死亡率無(wú)顯著性差異。移植患者死亡的主要原因?yàn)楦腥拘孕菘撕喜⒍嗥鞴偎ソ吆?或基礎(chǔ)疾病惡化[19],預(yù)防性使用抗真菌藥物可在一定程度上降低bIFI及真菌感染的發(fā)生率,但對(duì)最終導(dǎo)致患者死亡的原因無(wú)顯著改善[21]。
棘白菌素類(lèi)藥物作用于真菌細(xì)胞壁的環(huán)脂肽,抑制 β-(1,3)-D-葡聚糖的合成,而人類(lèi)及哺乳動(dòng)物的細(xì)胞無(wú)細(xì)胞壁結(jié)構(gòu),因此這類(lèi)藥物對(duì)宿主的不良反應(yīng)明顯降低,但仍不能忽視其對(duì)肝功能的損害。本研究納入的7項(xiàng)RCT的分析結(jié)果顯示棘白菌素組因不良反應(yīng)而停藥的發(fā)生率低于對(duì)照組,但文中均提及棘白菌素類(lèi)藥物的不良反應(yīng),包括胃腸道反應(yīng)、過(guò)敏反應(yīng)、心臟毒性及實(shí)驗(yàn)室檢查異常,包括:丙氨酸轉(zhuǎn)氨酶(ALT)、天冬氨酸轉(zhuǎn)氨酶(AST)、嗜酸性粒細(xì)胞、血小板水平升高,膽紅素血癥、黃疸等,其中肝損傷為棘白菌素類(lèi)藥物的主要不良反應(yīng),臨床應(yīng)用時(shí)應(yīng)密切監(jiān)測(cè)。
本研究的局限性包括:(1)現(xiàn)有關(guān)于棘白菌素類(lèi)藥物預(yù)防侵襲性念珠菌血癥的RCT較少,能夠納入評(píng)價(jià)分析的數(shù)量較少;(2)各RCT評(píng)價(jià)指標(biāo)間存在差異;(3)本文未納入符合標(biāo)準(zhǔn)的中文研究,可能導(dǎo)致研究結(jié)果中種族或人群的差異;(4)因陰性結(jié)果不易發(fā)表,可能導(dǎo)致結(jié)論的可靠性降低。同時(shí),建議再次開(kāi)展棘白菌素類(lèi)藥物預(yù)防侵襲性念珠菌血癥臨床課題研究時(shí),注意以下幾個(gè)方面:(1)課題設(shè)計(jì)更加嚴(yán)謹(jǐn),盡可能描述隨機(jī)方法、實(shí)施盲法、分配隱藏的具體方案;(2)報(bào)道時(shí)應(yīng)詳細(xì)描述各項(xiàng)結(jié)局指標(biāo),并報(bào)道觀察病例有無(wú)失訪等,以提高研究質(zhì)量,為臨床提供更可靠、有價(jià)值的參考。
綜上所述,與兩性霉素B及三唑類(lèi)抗真菌藥比較,棘白菌素類(lèi)藥物用于預(yù)防侵襲性念珠菌血癥可降低突破性侵襲性真菌感染發(fā)生率、真菌感染死亡率和因不良反應(yīng)停藥的發(fā)生率。受納入研究質(zhì)量和方法學(xué)限制,該結(jié)論有待大樣本、高質(zhì)量研究證實(shí)。
參考文獻(xiàn)
[ 1 ] GARBATI MA,ALASMARI FA,Al-TANNIR MA,et al. The role of combination antifungal therapy in the treatment of invasive aspergillosis: a systematic review[J]. Int J Infect Dis,2012,16(2):e76-81.
[ 2 ] KUBIAK DW, BRYAR JM, MCDONNELL AM, et al. Evaluation of caspofungin or micafungin as empiricantifungal therapy in adult patients with persistent febrile neutropenia: a retrospective, observational, sequential cohort analysis[J]. Clin Ther,2010,32(4):637-648.
[ 3 ] CORNELY OA, GACHOT B, AKAN H, et al. Epidemiology and outcome of fungemia in a cancer cohort of the infectious diseases group (IDG) of the european organization for research and treatment of cancer[J]. Clin Infect Dis,2015,61(3):324-331.
[ 4 ] PAPPAS PG, KAUFFMAN CA, ANDES DR, et al. Clinical practice guideline for the management of candidiasis: 2016 update by the infectious diseases society of America[J]. Clin Infect Dis,2016,62(4):e1-50.
[ 5 ] 魏曉晨,朱立勤,王春革.抗真菌藥物預(yù)防肝移植術(shù)后侵襲性真菌感染的療效與安全性的Meta分析[J].中國(guó)藥房,2014,25(24):2238-2241.
[ 6 ] HUSAIN S,TOLLEMAR J,DOMINGUEZ EA,et al. Ch- anges in the spectrum and risk factors for invasive candidiasis in liver transplant recipients: prospective, multicenter, case-controlled study[J]. Transplantation,2003,75(12):2023-2029.
[7] TOMBLYN M, CHILLER T, EINSELE H, et al. Guidelines for preventing infectious complications among hematopoietic cell transplantation recipients: a global perspective[J]. Biol Blood Marrow Transplant,2009,15(10):1143-1238.
[ 8 ] WINSTON DJ, LIMAYE AP, PELLETIER S, et al. Randomized, double-blind trial of anidulafungin versus fluconazole for prophylaxis of invasive fungal infections in high-risk liver transplant recipients[J]. Am J Transplant,2014,14(12):2758-2764.
[ 9 ] KUSE ER,CHETCHOTISDKD P,DA CUNHA CA,et al. Micafungin versus liposomal amphotericin B for candidaemia and invasive candidosis: a phase Ⅲ randomized double-blind trial[J]. Lancet,2007,369(9572):1519-1527.
[10] SALIBA F, PASCHER A, COINTAULT O,et al. Randomized trial of micafungin for the prevention of invasive fungal infection in high-risk liver transplant cecipients[J]. Clin Infect Dis,2015,60(7):997-1006.
[11] VAN BURIK JA, RATANATHARATHOM V, STEPAN DE,et al. Micafungin versus fluconazole for prophylaxis against invasive fungal infections during neutropenia in patients undergoing hematopoietic stem cell transplantation[J]. Clin Infect Dis,2004,39(10):1407-1416.
[12] HANSON KE, PFEIFFER CD, LEASE ED, et al. β-D- glucan surveillance with preemptive anidulafungin for invasive candidiasis in intensive care unit patients: a randomized pilot study[J]. PLoS one,2012,7(8):e42282.
[13] OYAKE T, KOWATA S, MURAI K, et al. Comparison of micafungin and voriconazole as empirical antifungal therapies in febrile neutropenic patients with hematological disorders: a randomized controlled trial[J]. Eur J Haematol,2016,96(6):602-609.
[14] WALSH TJ, TEPPLER H, DONOWITZ GR, et al. Caspofungin versus liposomal amphotericin B for empirical antifungal therapy in patients with persistent fever and neutropenia[J]. N Engl J Med, 2004,351(14):1391- 1402.
[15] TAPLITZ RA, KENNEDY EB, BOW EJ, et al. Antimicrobial prophylaxis for adult patients with cancer-related immunosuppression:ASCO and IDSA clinical practice guideline update[J]. J Clin Oncol, 2018, 36(30):3043- 3054.
[16] KUBIAK DW, BRYAR JM, MCDONNELL AM, et al. Evaluation of caspofungin or micafungin as empiric antifungal therapy in adult patients with persistent febrile neutropenia: a retrospective, observational, sequential cohort analysis[J]. Clinical Therapeutics,2010,4(32):637- 648.
[17] WINGARD JR, CARTER SL, WALSH TJ, et al. Randomized, double-blind trial of fluconazole versus voriconazole for prevention of invasive fungal infection after allogeneic hematopoietic cell transplantation[J]. Blood,2010,116(24):5111-5118.
[18] PAPPAS PG, ALEXANDER BD, ANDES DR, et al. Invasive fungal infections among organ transplant recipients: results of the transplant-associated infection surveillance network[J]. Clin Infect Dis,2010,50(8):1101- 1011.
[19] WANG J, ZHAN P, ZHOU R, et al. Prophylaxis with itraconazole is more effective than prophylaxis with fluconazole in neutropenic patients with hematological malignancies: a meta-analysis of randomized-controlled trials[J]. Med Oncol,2010,27(4):1082-1088.
[20] ZIAKAS PD, KOURBTI IS, VOULGARELIS M, et al. Effectiveness of systemic antifungal prophylaxis in patients with neutropenia after chemotherapy: a meta-analysis of randomized controlled trials[J]. Clin Ther,2010,32(14):2316-2336.
[21] VEKEMAN F, WEISS L, ARAM J, et al. Retrospective cohort study comparing the risk of severe hepatotoxicity in hospitalized patients treated with echinocandins forinvasive candidiasis in the presence of confounding by indication[J]. BMC Infect Dis,2018,18(1):438.
(收稿日期:2019-08-16 修回日期:2019-10-08)
(編輯:劉明偉)

