內(nèi)鏡下黏膜切除術治療老年胃腸道息肉的臨床效果及對血清炎癥因子與預后的影響
魏 晟,董麗鳳,胡艷婕,蔣大健,臧 杰,謝 俏
胃腸道息肉為胃腸道內(nèi)出現(xiàn)的隆起病變,發(fā)病早期常無明顯癥狀,若未接受治療,后期容易導致消化道出血,甚至會發(fā)生癌變[1]。臨床上治療本病常應用內(nèi)鏡下電凝切除術,但是因為切除深度把握存在難度,常導致患者消化道穿孔或病灶切除不完全等,所以采用此種術式治療胃腸道息肉效果與術者手術經(jīng)驗、技術關系密切[2-3]。老年患者因為身體器官功能退化,免疫力下降,圍術期容易出現(xiàn)各種并發(fā)癥,所以尋找一種治療效果優(yōu)異且安全性高的術式對于提高老年胃腸道息肉患者治療效果意義重大。現(xiàn)內(nèi)鏡下黏膜切除術逐漸大量應用于胃腸道息肉治療中,其將電凝切除與黏膜注射兩種方式有機結(jié)合,具有微創(chuàng)、安全、易于開展等優(yōu)勢[4-5]。本研究比較老年胃腸道息肉患者行普通內(nèi)鏡電凝切除術與內(nèi)鏡下黏膜切除術治療的效果,以明確內(nèi)鏡下黏膜切除術在老年胃腸道息肉治療上的優(yōu)劣,為臨床應用提供參考。
1 資料與方法
1.1一般資料 選取2016年6月—2019年6月我院收治160例老年胃腸道息肉患者。納入標準:①內(nèi)鏡確診為胃腸道息肉;②具有普通內(nèi)鏡電凝切除術或內(nèi)鏡下黏膜切除術手術指征;③息肉直徑5~22 mm;④患者同意參與本研究,并簽署知情同意書。排除標準:①已接受過內(nèi)鏡下黏膜切除術治療者;②內(nèi)鏡檢查顯示患者黏膜存在顯著浸潤;③存在內(nèi)鏡檢查禁忌證者;④凝血功能異常者;⑤采用其他方式治療者。依據(jù)手術方式的不同將160例患者均分為研究組和對照組。兩組一般資料比較差異無統(tǒng)計學意義(P>0.05),具有可比性,見表1。本研究獲得醫(yī)院倫理委員會批準同意進行。

表1 不同術式治療的老年胃腸道息肉兩組一般資料比較
1.2治療方法 ①對照組采用普通內(nèi)鏡電凝切除術治療,將GIF-XQ230-2型胃鏡(日本奧林巴斯公司生產(chǎn))或VME-1300型電子結(jié)腸鏡(上海涵飛醫(yī)療器械有限公司生產(chǎn))置入后探查息肉,探查到息肉后在距離息肉邊界2 mm處采用高頻電刀進行切除操作,切除時注意達到黏膜上層但不要傷及肌層,后進行止血操作。②研究組采用內(nèi)鏡下黏膜切除術治療,采用PCF-Q240Z型內(nèi)鏡(日本奧林巴斯公司生產(chǎn))進行息肉探查與對照組相同,在息肉基底選擇1~4個位點,將比例為1/10 000的腎上腺素/0.9%氯化鈉注射液沿位點注入,待注射完成息肉基底完全隆起、肌層與黏膜分離后,將息肉基底采用套圈器套牢,選擇高頻電流切除息肉組織,較大息肉可行多次充分切除。手術完成后觀察創(chuàng)面2 min,有出血情況發(fā)生及時止血,若出血輕微可用0.8%去甲腎上腺素溶液沖洗。
1.3觀察指標 ①息肉切除情況:包括整塊切除率與完整切除率。整塊切除:鏡下觀察病變被整塊切除,獲得一個標本;完整切除:內(nèi)鏡觀察息肉完全被切除,病理檢查示切除樣本基底及外側(cè)邊界未受到病變累及。②圍術期指標:包括息肉切除時間、手術時間、出血量、術后開始進流食時間及住院時間,其中息肉切除時間為黏膜注射針插入后或高頻電刀開始切除至息肉切除結(jié)束時間。③炎癥因子:手術前與手術結(jié)束后收集兩組晨起空腹靜脈血離心后血清,采用酶聯(lián)免疫吸附法測定降鈣素原(PCT)、白細胞介素-6(IL-6)、C反應蛋白(CRP)、白細胞介素-17(IL-17)水平。④并發(fā)癥:包括術后出血、感染、切口過深,其中切口過深為切口達基底黏膜肌層。⑤預后情況:兩組患者術后均接受隨訪,隨訪終點為2019年12月31日,記錄兩組患者隨訪期間息肉復發(fā)情況。
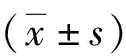
2 結(jié)果
2.1兩組息肉切除情況比較 研究組息肉整塊切除率與完整切除率均高于對照組,差異有統(tǒng)計學意義(P<0.05或P<0.01),見表2。

表2 不同術式治療的老年胃腸道息肉兩組息肉切除情況比較[例(%)]
2.2兩組圍術期相關指標比較 研究組息肉切除時間、手術時間、手術后開始進流食時間均短于對照組,出血量少于對照組,差異均有統(tǒng)計學意義(P<0.01),兩組住院時間比較差異無統(tǒng)計學意義(P>0.05),見表3。
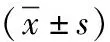
表3 不同術式治療的老年胃腸道息肉兩組圍術期相關指標比較
2.3兩組手術前后炎癥因子水平比較 兩組術前PCT、IL-6、CRP及IL-17水平比較差異無統(tǒng)計學意義(P>0.05)。術后兩組PCT、IL-6、CRP及IL-17水平均顯著上升,且研究組上述指標升高程度小于對照組,差異均有統(tǒng)計學意義(P<0.01)。見表4。
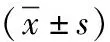
表4 不同術式治療的老年胃腸道息肉兩組手術前后炎癥因子水平比較
2.4兩組術后并發(fā)癥比較 研究組術后并發(fā)癥發(fā)生率為7.50%低于對照組術后并發(fā)癥發(fā)生率22.50%,差異有統(tǒng)計學意義(χ2=7.059,P=0.008),見表5。

表5 不同術式治療的老年胃腸道息肉兩組術后并發(fā)癥比較[例(%)]
2.5兩組息肉復發(fā)情況比較 研究組隨訪期間息肉復發(fā)率為3.75%(3/80),對照組隨訪期間息肉復發(fā)率為0,兩組隨訪期間息肉復發(fā)率比較差異無統(tǒng)計學意義(χ2=1.359,P=0.244)。
3 討論
胃腸道息肉采用普通內(nèi)鏡電凝切除術治療,雖然手術步驟簡單,容易掌握,但是切除深度一直是該術式難點,切除過深會出現(xiàn)穿孔并發(fā)癥,而切除過淺則易導致復發(fā)[6-8]。中老年群體胃腸道息肉發(fā)病率逐漸升高,由于老年患者身體機能下降,術后較易出現(xiàn)各種并發(fā)癥,常導致患者手術治療效果不佳[9-10]。
內(nèi)鏡下黏膜切除術為新型微創(chuàng)術式,其在黏膜下注射藥物使息肉與正常組織分離,隨后采用圈套器將其套好并切除,治療效果優(yōu)于普通內(nèi)鏡電凝切除術[11-13]。本研究組采用內(nèi)鏡下黏膜切除術治療,患者息肉整塊切除率與完整切除率均顯著高于采用普通內(nèi)鏡電凝切除術治療的對照組。內(nèi)鏡下黏膜切除術先采用黏膜下注射使病灶膨起,有效分離病灶黏膜及固有肌層,有利于圈套器圈套,便于其后息肉病灶切除[14-16]。本文發(fā)現(xiàn),研究組息肉切除時間、手術時間、手術后開始進流食時間均短于對照組,出血量少于對照組。因電凝切除手術切除深度難以掌握,切除深度不當容易出現(xiàn)出血及穿孔等并發(fā)癥,可能是造成本文對照組息肉切除時間、手術時間長及出血量多的原因之一。有研究顯示,胃腸道息肉采用內(nèi)鏡治療容易損傷胃腸道黏膜,組織內(nèi)部炎癥因子聚集,激活機體相關信號傳導通路,炎癥因子大量釋放入血,使得患者血液中相關炎癥因子水平顯著升高[17-18]。本研究結(jié)果顯示,術后兩組PCT、IL-6、CRP及IL-17水平均顯著上升,且研究組上述指標升高程度小于對照組,提示采用內(nèi)鏡下黏膜切除術治療胃腸道息肉對于胃腸道黏膜損傷較輕,故能減弱炎性反應程度。
本文研究組術后并發(fā)癥發(fā)生率為7.50%低于對照組術后并發(fā)癥發(fā)生率22.50%,差異有統(tǒng)計學意義。電凝切除術切除深度不當容易導致患者息肉殘留及出血發(fā)生,而內(nèi)鏡下黏膜切除術僅將息肉病灶黏膜切除,這可能是研究組術后出血及切口過深等并發(fā)癥少的主要原因。有研究者認為,內(nèi)鏡下黏膜切除術整個過程中視野清晰,可清楚觀察到病灶切除及出血情況并及時止血,是患者術后并發(fā)癥發(fā)生率低的主要原因[19]。電凝切除術電凝時間過長容易導致患者黏膜下血管受損,同時由此所致的灼燒傷使得細胞出現(xiàn)變性壞死,這種壞死逐漸擴大造成術后出血及傷口感染風險增加[20]。本文還顯示,兩組隨訪期間息肉復發(fā)率比較差異無統(tǒng)計學意義。雖然研究組息肉切除效果較好,理論上說患者術后復發(fā)率較低,但是對于較扁平的黏膜層息肉,無明顯蒂部結(jié)構(gòu),應適宜增加切除深度,減少殘留以避免復發(fā)[21]。李倩等[22]研究認為,內(nèi)鏡下黏膜切除術可以有效提高息肉切除率,降低復發(fā)率。
綜上,老年胃腸道息肉患者采用內(nèi)鏡下黏膜切除術治療效果顯著,患者炎性反應輕,息肉切除率高,術后并發(fā)癥少,可以作為首選術式。

