EuCAD基因不同位置片段RNAi對煙草木質素合成的調控效果
陳博雯, 肖玉菲, 李軍集, 張 燁, 覃子海, 張曉寧, 劉海龍
(廣西壯族自治區林業科學研究院 國家林業局中南速生材繁育實驗室/廣西優良用材林資源培育重點實驗室, 廣西 南寧 530002)
桉樹(Eucalyptus)是桃金娘科桉屬植物的總稱,原產地為澳大利亞[1-2]。目前,全世界有100多個國家種植桉樹,在我國熱帶、亞熱帶地區引種種植已有100多年的歷史[3-5]。由于桉樹速生豐產并且材質優良,已經成為短周期原料林的主要造林樹種,被廣泛用于制漿造紙、人造板和纖維板等,特別是在造紙木漿生產中具有重要地位[6-8]。
在傳統選育優良紙漿材品種的基礎上,利用基因工程手段改良木材品質是國際上研究的熱點[9-10]。尾葉桉GLU4無性系(Eucalyptusurophyllaclone GLU4)是廣西廣泛種植的桉樹良種,以此樹種為基礎,采用轉基因技術培育低木質素桉樹品種,具有良好的應用前景。為此,廣西林科院已經率先在尾葉桉良種GLU4的基礎上開展了木質素調控的轉基因技術研究,且經過前期研究已取得一定進展,在一系列木質素合成途徑基因中,已鎖定應用尾葉桉肉桂酰乙醇脫氫酶基因(EuCAD)轉化煙草可抑制木質素合成[11-12]。在前述對EuCAD基因研究中使用的是基因全長序列構建RNA干擾載體,序列較長,載體構建和應用均不便捷,而RNAi技術的優勢之一,就是利用較短的干擾片段進行轉錄后調控。為此,選擇模式植物煙草,采用生物信息學工具分析其EuCAD基因序列,根據編碼蛋白保守結構域的分布情況分別選擇EuCAD基因的部分序列構建RNA干擾抑制表達載體并轉化植物,利用遺傳轉化體系檢測分析不同位置選取的干擾片段對煙草CAD基因表達及木質素合成的調控效果,篩選鑒定出EuCAD中RNAi效果最佳的基因片段,以期為尾葉桉GLU4無性系肉桂酰乙醇脫氫酶基因(EuCAD)調控其木質素的合成提供技術參考。
1 材料與方法
1.1 材料
1.1.1 組培苗及菌株 煙草無菌組培苗、DH5α菌株和農桿菌LBA4404菌株,由廣西優良用材林資源培育重點實驗室保存。
1.1.2 試劑盒 RNA prep Pure多糖多酚植物總RNA提取試劑盒,天根生化科技有限公司;RNA LA PCR反轉錄試劑盒,大連寶生物工程有限公司;SG Fast qPCR Master Mix(2X),購自上海生工生物公司。
1.1.3 儀器 Nikon Eclipse80i光學顯微鏡,尼康公司;LightCycler480熒光定量PCR儀,羅氏公司。
1.2 方法
1.2.1 RNAi載體的構建 利用Blastp、ProtParam、psipred、SWISS-MODEL等對EuCAD基因序列分析其編碼蛋白的保守結構域,其分布在40~300氨基酸。根據保守結構域的分布情況,分別選擇包含NAD(P)結合位點、底物結合位點和Zn結合催化位點的S1片段;包含多個Zn結合結構位點的S2片段;包含多個NAD(P)結合位點的S3片段,以及帶有NAD(P)結合位點和二聚體結合界面序列的S4片段用于構建RNAi載體。每條選定片段利用Vector NTI分析篩選出40 bp左右片段,序列信息為S1-gaatttgccacagtgacattcaccagatcaagaatgatcttggcgc,S2-tggttgggtgccgcagaagctgtggcccttgcaattcggaccagctg,S3-atgtgcgctggtgtgaccgtgtacagtcctctggtgcgctttgg,S4-ccatggttatgcttgggaggaagtcaatcactgggagtttcata。利用序列設計成反向重復序列,在每條序列兩端附加XhoI酶切位點后,交由上海生工生物公司合成序列,得到攜帶目標片段的克隆載體pUC57-S1、pUC57-S2、pUC57-S3和pUC57-S4。利用XhoI酶分別消化pUC57-S1、pUC57-S2、pUC57-S3和pUC57-S4,通過凝膠電泳回收得到目標序列,同時利用XhoI酶消化pCAMBIA3301載體,同樣經過凝膠電泳回收后,得到去除bar基因序列的載體骨架。分別將載體骨架與4條合成序列連接,連接產物轉化DH5α,應用載體上的測序引物3301-F(5'-CCCTTATCTGGGAACTACTCAC-3')/3301-R(5'-CGCTGAAATCACCAGTCTCTC-3')對轉化進行PCR鑒定,對可擴增得到目標長度片段的克隆進行測序,測序結果與目標序列比對,序列一致即為構建成功的RNAi載體。RNAi載體構建成功后,按常規方法導入農桿菌LBA4404中用于轉化。
1.2.2 煙草轉化植株的培育 利用RNAi載體轉化獲得的4個轉基因煙草植株,經過愈傷組織培養和芽再生培養,經抗生素篩選獲得陽性植株,移栽后置于溫室內培養,同時保留每個植株的組培繼代芽,以備后續擴繁培養轉基因植株之用。移栽60 d后,取葉片提取基因組總DNA。應用載體上的測序引物3301-F/3301-R,對轉基因植株進行PCR鑒定,同時對長度相符的PCR擴增產物測序以驗證插入的RNAi序列準確性。
1.2.3 轉基因煙草植株CAD基因的表達水平 4個轉基因煙草植株移栽培養240 d后,以野生型(WT)植株為對照,自莖尖向下第3節處取葉片,提取RNA用于CAD基因表達水平檢測。
采用煙草actin基因作為內參基因,煙草CAD(X62343.1)基因為目標檢測基因,利用Vector NTI設計引物序列如下:
actin-F:CTGGAATCCATGAGACTACTTACAA;actin-R: AACCGCCACTGAGCACAATA;CAD-F: GTATGGCACCAGAACAAGCAG;CAD-R: CCAATGCCTCTTGTCTCTTCTTAT。
植物組織樣品采用試劑盒提取并反轉錄合成cDNA。PCR檢測條件為95℃持續3 min,40次循環,95℃持續7 s,55℃持續10 s 和72℃持續15 s。每個處理設3個生物重復及3個技術重復。
1.2.4 指標測定
1) 木質部厚度測定。取溫室培育270 d的4個轉基因煙植株,以野生型(WT)植株為對照,自莖部頂端向下數,選取其莖部第4節和第6節莖部組織,按常規方法制成石蠟切片,并用番紅-固綠法染色[13]。制好的切片用Nikon光學顯微鏡進行觀察,NIS-Elements拍照并測量莖部直徑。測量時每個樣品選取1張切片,在莖部截面的各個方向分別采集60個莖部直徑數據和木質部厚度數據。
2) 木質素及纖維素含量測定。取溫室培育270 d的4個轉基因煙植株,以野生型(WT)植株為對照,選擇自頂端向下第3~10節莖部,去除葉片后65℃烘干24 h,粉碎后過40目篩,用于木質素和纖維素含量檢測。
木質素含量:參照GB/T20808-2006要求采用酸性洗滌方法測定。稱取1 g樣品,加入2%CTAB和2~3滴正辛醇后煮沸1 h。消煮液用玻璃砂漏斗抽濾后,將漏斗轉移至50 mL燒杯中,加入15℃的12.0 mol/L硫酸至半滿,將結塊打碎并攪拌呈糊狀,20℃保溫3 h,期間根據流出量不斷補充12.0 mol/L硫酸。消解后抽濾并用熱水洗滌至pH試紙檢測呈中性。取出漏斗和殘余物置于105℃烘箱中烘干至恒重。
木質素含量=烘干后木素殘渣質量/絕干樣品質量×100%
纖維素含量:采用硝酸法測定。稱取1 g樣品置于錐形瓶中,加入25 mL硝酸-乙醇(4∶1)混合液,裝上回流冷凝器,沸水浴1 h,期間隨時震蕩燒瓶。靜置至殘渣沉積后小心倒出上清液至恒重的玻璃濾器中,用真空泵吸干濾液并將流入濾器中的殘渣移回錐形瓶中。量取25 mL硝酸-乙醇混合液分數次將濾器及錐形瓶口附著的殘渣移入瓶內。再次裝上回流冷凝器,沸水浴1 h。3次重復后,將錐形瓶內容物全部移入濾器,用10 mL硝酸-乙醇混合液洗滌殘渣,再用熱水洗滌至洗液中性,最后用乙醇洗滌2次,吸干濾液,濾器置于105℃烘箱中烘干至恒重。
纖維素含量=烘干后纖維素殘渣質量/絕干樣品質量×100%
1.3 數據處理
采用SPSS 19.0進行統計與分析。
2 結果與分析
2.1 RNAi載體的構建
從圖1看出,pCAMBIA3301載體上的測序引物3301-F/3301-R分別位于XhoI酶切位點旁側約50 bp處,XhoI酶切位點之間的bar基因序列分別被替換為S1~S4的目標序列,PCR產物長度從650 bp左右縮短至約200 bp。每個載體都檢測得到擴增出目標特異性條帶的陽性克隆,對陽性克隆提取質粒測序結果顯示,插入序列與預期序列一致,RNAi載體構建成功,分別命名為pCAMBIA3301-S1、pCAMBIA3301-S2、pCAMBIA3301-S3和pCAMBIA3301-S4。
2.2 煙草轉化植株的培育
從圖2可見,RNAi載體轉化獲得的4個轉基因煙草植株基因組上插入RNAi載體的轉基因植株中可檢測到長度200 bp的特異性片段,而未整合RNAi載體的植株則未擴增到目標條帶。陽性植株經進一步PCR擴增產物測序結果顯示,其序列與目標RNAi序列一致,獲得的轉基因煙草植株分別命名為pS1、pS2、pS3和pS4。
2.3 轉基因煙草植株CAD基因的表達水平
從圖3看出,pS1、pS2、pS3和pS44個轉基因煙草植株的CAD基因表達水平與野生型(WT)相比,均呈顯著下降趨勢,pS1與pS2間差異不顯著,pS1和pS2顯著低于pS3和pS4,pS3顯著低于pS4。其中,pS1和pS2降幅最大,分別為87.48%和87.30%;pS3降幅其次,為67.93%;pS4降幅最小,為49.70%。從基因表達調控效果看,RNAi片段S1和S2的調控效果最好。
2.4 轉基因煙草植株莖部直徑及木質部的厚度
從表1可知,野生型和4個轉基因煙草植株莖部直徑及木質部厚度的變化。直徑:第4節和第6節分別為6 194.57~6 634.29 μm和8 293.15~8 576.63 μm,依次分別為WT>pS2>pS4>pS1>pS3和WT>pS4>pS1>pS2>pS3,不同植株間差異均不顯著。木質部厚度:第4節為283.21~320.91 μm,依次為WT>pS4>pS3>pS2>pS1,WT與pS3和pS4差異不顯著,但顯著厚于pS1和pS2;pS1、pS2、pS3和pS4間差異不顯著。第6節為384.53~427.53 μm,依次為WT>pS3>pS4>pS2>pS1,WT顯著厚于pS1,與其余3個植株間差異不顯著;pS1、pS2、pS3和pS4間差異不顯著。
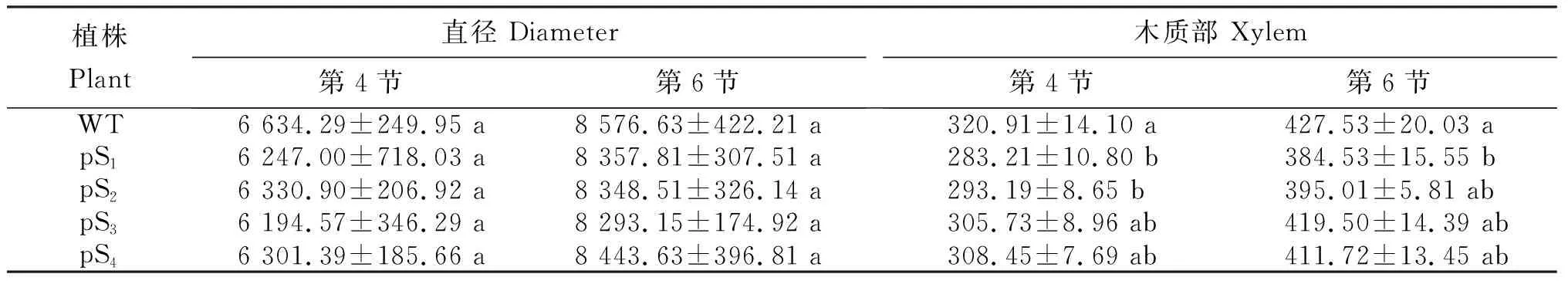
表1 轉化植株莖部直徑及木質部的厚度Table 1 Diameter and xylem thickness in the stem of transformed plants μm
2.5 轉基因煙草植株莖部木質素及纖維素的含量
從表2可知,野生型和4個轉基因煙草植株木質素及纖維素含量的變化。木質素:WT最高,為13.37%;pS4其次,為12.36%;pS1最低,為11.33%;WT顯著高于其余植株,pS1顯著低于其余植株,其余植株間差異顯著。pS1、pS2、pS3和pS4分別較WT降低15.26%、11.44%、10.62%和7.55%。纖維素:pS3最高,為36.08%;WT其次,為35.16%;pS1最低,為31.43%;pS3顯著高于其余植株,pS1顯著低于其余植株,其余植株間差異顯著。pS1、pS2和pS4較WT分別降低10.61%、5.03%和3.10%,pS3較WT提高2.62%。

表2 轉基因煙草植株的木質素及纖維素含量Table 2 Lignin and cellulose content in transgenic tobacco %
3 結論與討論
由于調控靶序列的特異性和高效性,RNAi已成為轉錄后調控的首選方法[14]。在對目標基因序列不清楚時,RNAi常采用基因全長序列構建RNAi載體,這種常規研究策略在許多植物中取得了較好的效果。但也有研究者指出,干擾片段過長,會使自身復制過程中堿基錯配幾率增大,同時較長的序列更容易與其他非目標基因序列匹配,脫靶風險更高[15]。若選擇目標基因的部分片段用于RNAi,所選擇的位置至關重要。HOLEN等[16]根據目標基因的不同位置設計4條21~23 bp的RNAi片段研究發現一種可能的位置效應,調控效果最佳的RNAi片段hTF167i和hTF372i能夠抑制85%~90%的基因活性,而 hTF562i片段只表現出一種中間效應,hTF478i的活性則很低;且進一步深入研究發現,針對靶點hTF167設計的干擾片段hTF158i和 hTF161i與hTF167i序列僅相差幾個堿基,幾乎完全喪失調控效果。張斌等[17]對OsPUT1基因的RNA干擾研究也提出類似的位置效應,基因中段序列的干擾效果優于首尾片段。由此推斷,針對目標基因選擇RNA干擾片段時,既應考慮片段在基因CDS中的位置,也應考慮片段包含的特異性位點。
鑒于CAD蛋白在木質素合成中的重要功能,在許多植物中都對其展開了研究,目前為止,NCBI已收錄2 428條陸生植物CAD蛋白序列,不同植物中的CAD具有高度的同源性。對CAD蛋白序列比對分析發現,幾乎所有CAD都具有三類典型的保守的結構域。第一類是輔酶和底物結合結構域,包括NAD(P)結合位點和底物結合位點。第二類是酶活性中心結構域,包括Zn結合催化位點和Zn結合結構位點。第三類是二聚體結合結構域。對CAD蛋白三級結構分析表明,該蛋白以二聚體形式存在,涉及到二聚體結合界面的結構域對二聚體的形成與穩定具有極其重要的作用[18]。
研究分別選擇包含NAD(P)結合位點、底物結合位點和Zn結合催化位點的S1片段,包含多個Zn結合結構位點的S2片段,包含多個NAD(P)結合位點的S3片段,以及帶有NAD(P)結合位點和二聚體結合界面序列的S4片段用于構建RNAi載體。在將4條RNAi片段分別轉化煙草后發現,S3和S4片段的調控效果不理想,多項表型檢測結果與野生型相比降幅較小或無差異。S1和S2片段對木質素的調控效果則最為明顯,從基因表達水平到木質素含量和木質部厚度均較野生型降低。
從序列編碼蛋白的結構域看,S1片段編碼蛋白兼具輔酶、底物結合結構域和酶催化結構域,生物學功能重要;S2片段編碼蛋白則幾乎涵蓋CAD中所有預測的Zn結合結構位點,缺失前述任一段蛋白片段勢必極大地影響酶學活性。從基因序列位置分析,S1片段近于轉錄翻譯的起始端,S2片段也位于基因序列的前1/3處,若RNA干擾在S1或S2片段發生,CAD酶幾乎無法轉錄或翻譯,對酶活性的抑制將更明顯。前述分析結果與試驗結果相一致,說明S1和S2片段是較為理想的RNAi片段。
S3和S4片段在設計時涵蓋了大多數的預測NAD(P)結合位點和二聚體結合界面的結構域,但S3和S4片段的調控效果卻甚微,可能是由于S3和S4片段引發RNA干擾時,由于片段位于基因中后部,大部分序列仍可翻譯為殘損的CAD蛋白,殘損蛋白雖缺失上述片段編碼的結構域,但蛋白的其他NAD(P)結合位點和二聚體結合界面的結構域位點可能仍具有活性,所以殘損蛋白仍具有生物學活性。此外,研究中選取的片段長度為44 bp,在后續研究中應進一步優化縮短干擾片段,有望獲得高效RNAi片段。
研究結果表明,植物莖部結構特點是從上到下木質化程度逐漸提高,而在pS1和pS2植株中,隨著木質化程度的提高,通過抑制CAD基因表達調控木質素合成的效果逐漸弱化。造成此變化的原因可能是CAD對木質素合成的調控主要發生在木質化初期,在木質化中后期,其調控效果被其他代謝通路中的基因應答作用所掩蓋。同時,pS1和pS2植株中木質部厚度的降幅均在10%左右,降幅較低,較小的降幅可能在木質化過程中被逐漸積累的木質部厚度稀釋,造成降幅差異逐漸減小。對此,在后續研究中,可嘗試使用底物標記等手段,分階段解讀木質化過程,有望深入揭示抑制CAD基因調控木質素合成的生理生化機制。

