鋁酸三鈣氧化鋁溶出行為研究
劉吉龍,潘曉林,程 濤,武莎莎,于海燕
(1.東北大學多金屬共生礦生態化冶金教育部重點實驗室,遼寧 沈陽 110819;2.東北大學 冶金學院,遼寧 沈陽 110819;3.廣西華昇新材料有限公司,廣西 防城港 538000)
近年來,我國氧化鋁和電解鋁工業發展迅猛,對優質鋁土礦資源需求日益增加。我國自有鋁土礦平均品位持續走低,鋁土礦的對外依存度高達56%,鋁土礦資源成為制約我國鋁工業發展的瓶頸[1]。為解決鋁資源短缺的問題,很多學者對從粘土、頁巖、霞石或粉煤灰等非鋁土礦資源提取氧化鋁做了大量研究[2]。而鋁酸三鈣(3CaO·Al2O3·6H2O,TCA)作為拜爾法生產氧化鋁過程中的中間脫硅產物[3-4],含有豐富的氧化鋁資源,但對其氧化鋁溶出行為的研究卻鮮有報道。
TCA在氧化鋁生產中起著重要作用,廣泛用作助濾劑和脫硅劑[5-7]。作者在前期研究中提出了一種以鈣鐵榴石(3CaO·Fe2O3·nSiO2·(6-2n)H2O)為有效脫硅產物,添加石灰和活性鐵礦物處理低品位鋁土礦的鈣鐵榴石一步堿熱法,工藝中所用鋁酸鈉溶液的苛堿濃度與常規拜耳法相近,較水熱法有大幅的降低。處理后殘渣的Al2O3/SiO2質量比和Na2O含量可分別降至0.3~0.5和1%以下[8]。此工藝為了在溶出過程中提高氧化鋁的溶出率,采用了較高苛性比的鋁酸鈉溶液進行高壓溶出反應,反應后溶出液的苛性比為2~5。在高壓溶出后,通過TCA的合成工序,可得到分子比較高的循環母液,以保證堿液的循環和氧化鋁產品的提取。此過程產生了大量的TCA廢渣,其中含有大量的氧化鋁,其堆棄造成了資源的極大浪費。通過TCA的溶出工藝,可回收氧化鋁,實現資源綜合利用[9]。
1 實 驗
1.1 原料與設備
實驗選用的鈣質原料采用山西玉竹地區的工業石灰,對石灰活性進行測定,其活性CaO為94.92%。所用藥品為鋁酸鈉、氫氧化鈉、碳酸鈉(分析純,天津市科密歐化學試劑有限公司)。實驗用水為去離子水,由實驗室自制。
DZKW-S-4型恒溫水浴鍋(北京永光明醫療儀器有限公司),PW3040-60X型X射線衍射儀(XRD,日本島津(SHIMADZU)公司),GSL-IOIB型激光顆粒分布測量儀(遼寧儀表研究有限責任公司),DY8型低壓群釜反應器(長沙特種硬質合金工業公司),JSM-6360LV型掃描電子顯微鏡(SEM,日本JEOL公司)。
1.2 實驗方法
采用鋁酸鈉溶液和工業石灰為原料制備TCA,所用的鋁酸鈉溶液由鋁酸鈉和氫氧化鈉配制而成。在三口瓶內進行TCA的制備。設定反應條件為:C/A=1.4,鋁酸鈉溶液苛性堿濃度(以Na2O計)ρNK=250 g/L、分子比αK=5,T=80 ℃,t=2 h。在反應結束后進行固液分離,合成產物烘干待用。
TCA的溶出試驗在以硅油為加熱介質的高壓反應釜內進行。溶出時采用的鋁酸鈉溶液為一步堿熱法碳分后的母液,其苛堿濃度約為15 g/L,分子比約為2。取配置好的鋁酸鈉溶液100 mL裝入鋼彈,加入制備好的TCA以及分析純碳酸鈉,密封。在苛堿濃度ρNK=15 g/L、液固比L/S=5的條件下研究碳堿濃度、分子比、時間、溫度、液固比對TCA溶出性能的影響規律。碳堿濃度(ρNC,以Na2O計)分別為130 g/L、145 g/L、160 g/L,分子比分別為1.98,2.22,2.53,溶出溫度分別為160 ℃、180 ℃、200 ℃,反應時間分別為30 min、60 min、120 min。反應結束后進行固液分離,將溶出產物洗凈后烘干,經化學分析測量Al2O3和CaO的含量,由公式(1)計算氧化鋁溶出率:
(1)
式中:η——TCA的氧化鋁溶出率,%;
(A/C)1——TCA與氧化鈣的質量分數之比;
(A/C)2——溶出產物中氧化鋁與氧化鈣的質量分數之比。
官廳水庫黑土洼濕地系統2016年水質監測評價分析……………………………………… 楊壘,吳玉欣,王彥芹(3-137)
對溶出固相進行XRD(Philips X`Pert PW3040-60X)檢測,分析物相組成。儀器參數采用Cu Kα輻射,管電壓40 kV,管電流40 mA,掃描速度為15°/min,掃描范圍5°~90°。使用激光顆粒分布測量儀(PSD,Malvern Hydro 3000)測量了溶出固相的粒度,以蒸餾水作為分散介質。使用掃描電鏡(SEM,SHIMADZUSSX-550)分析溶出固相的微觀結構與形貌,設備操作電壓為15 kV,進行掃描電鏡觀察前,少量粉體首先進行鑲樣,然后于4 Pa真空下進行兩次60 s的噴金處理。
2 結果與討論
2.1 合成的TCA的表征
對合成的TCA進行XRD檢測,結果如圖1所示。由圖1可知,合成產物的主要物相主為TCA,除此之外還含有少量的CaCO3與Ca(OH)2。其中CaCO3是由于溶解在鋁酸鈉溶液中的CO2與Ca(OH)2反應生成的。合成產物的SEM分析結果如圖2所示。由圖2的SEM結果可知,氧化鈣與鋁酸鈉溶液反應后的產物晶粒生長相對完整,呈正方體,且存在粒子團聚現象。TCA是具有羥基的水化物,羥基的存在使分子間作用力增強,顆粒間容易聚集成團[13],所以在TCA制備過程中有明顯團聚現象的發生[14-15]。

圖1 合成產物的XRD圖

圖2 合成產物的SEM圖
2.2 溶液成分對溶出的影響
在T=180 ℃,αK=2.22,t=1 h的條件下,考察了碳堿濃度在130~160 g/L范圍內TCA的氧化鋁溶出性能。通過計算得到TCA的氧化鋁溶出率,如圖3所示。從圖3可以看出,氧化鋁的溶出率隨碳堿濃度的升高而增大。碳堿濃度由130 g/L增加到145 g/L時溶出率的增漲幅度較大,繼續增大碳堿濃度對提高TCA的溶出率影響有限。這是因為在碳堿濃度較低時,碳堿濃度是限制反應速率的主要因素。提高碳堿濃度增大了單位時間、單位體積內參與反應的分子的數量,可以明顯增大反應率,但當濃度提高到可以消除濃度對反應速率的限制時,再提高濃度就不能有效增加參與反應的分子數量,溶出率的增速變慢。因此,碳堿濃度選擇145 g/L為宜。

圖3 不同碳堿濃度下TCA的Al2O3溶出率
在ρNC=145 g/L,T=180 ℃,t=1 h的條件下研究了分子比對TCA溶出性能的影響,氧化鋁溶出率如圖4所示。由圖4可以看出,當分子比從2.22增加到2.53時,TCA的氧化鋁溶出率變化不大,增長幅度較小。這表明在αK=2.22時,溶出率已基本不在改變,繼續增加分子比并不能顯著提高氧化鋁溶出率。因此選擇分子比為2.22.。

圖4 不同分子比條件下TCA的Al2O3溶出率
2.3 工藝參數對溶出的影響
在ρNC=145 g/L,αK=2.22,t=1 h,考察了不同溶出溫度(T=160 ℃、180 ℃、200 ℃)對TCA溶出性能的影響,結果如圖5所示。由圖5可知,溫度對TCA溶出過程影響較大,提高溫度能有效提高TCA的氧化鋁溶出率。這是由于溫度升高可以使反應物分子能量增加,反應容易沖破反應能量壁壘,反應速率提高。當溫度為160 ℃時,溶出率為89.1%;溫度升高到180 ℃時,溶出率達到91.64%,繼續增加溫度溶出率上升趨勢變緩。為了降低溶出能耗,最佳溶出溫度應選擇180 ℃。

圖5 不同溫度條件下TCA的Al2O3溶出率
在ρNC=145 g/L,αK=2.22,T=180 ℃時考察了不同反應時間對TCA溶出性能的影響,結果如圖6所示。由圖6可以看出,在30~60 min的時間內,溶出率有很大幅度的增長,在60 min時溶出率已達到91.64%。繼續增加反應時間,Al2O3的溶出率提升幅度很小。說明反應在60 min時就已經達到平衡,因此應控制溶出時間為60 min。

圖6 不同時間條件下TCA的Al2O3溶出率
2.4 TCA溶出機理研究
綜合2.2與2.3節的研究發現,TCA溶出過程的最佳條件為:碳堿濃度為145 g/L,溶液分子比為2.22,溶出溫度為180 ℃,時間為60 min,此時氧化鋁溶出率達到92%左右。
TCA在碳堿溶液中的反應方程式為:
3Ca·Al2O3·6H2O+3Na2CO3
=3CaCO3↓+2NaAl(OH)4+4NaOH
(2)
對ρNC=145 g/L,αK=2.22,T=180 ℃,t=60 min條件下的溶出產物進行XRD檢測,結果如圖7所示。從圖7可以看出,溶出產物含有TCA和碳酸鈣,大部分是碳酸鈣,TCA的含量很少。碳酸鈣的特征峰主要集中在2θ=30°~50°之間,形狀尖銳,說明其結晶良好。
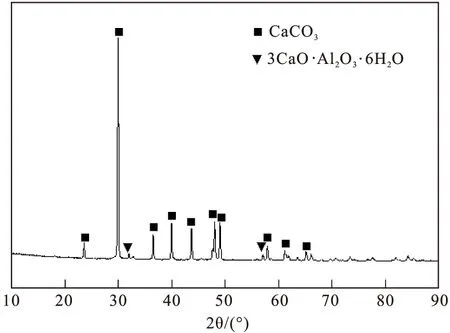
圖7 溶出產物的XRD圖
將同樣條件下的溶出產物進行SEM分析,結果如圖8所示。由圖8可以看出,碳酸鈣顆粒分散較好,單個顆粒晶型較完整,形貌主要為立方體,基本上均勻分布,部分發生團聚。溶出產物中出現團聚,可能是因為產物中含有部分未轉變TCA,其相互之間通過分子間作用力發生了團聚。

圖8 溶出產物的微觀形貌
使用馬爾文3000激光粒度測試儀,分析了不同反應條件下溶出產物的粒度,結果如圖9所示。從圖9(a)可以看出,碳堿濃度變化對產物粒度影響很大。當碳堿濃度為130 g/L時,產物的粒度較大,其分布呈多峰形態,這是由于碳堿濃度較低時,存在較多的TCA顆粒之間團聚現象嚴重。當濃度升高到145 g/L時,粒度分布變窄,多峰分布變為雙峰分布,產物越來越均勻;碳堿濃度繼續升高到160 g/L時,粒度分布曲線整體趨勢與之前相同,有向單峰分布的趨勢。這是由于碳堿濃度升高,碳酸鈣含量增多,顆粒之間比較分散,粒度變小。由圖9(b)可知,分子比對產物粒度影響不大,粒度分布曲線、平均粒徑基本不隨分子比的改變發生變化。由圖9(c)可知,時間對產物粒度影響較大,隨著反應時間的增加,粒度減小,其分布由多峰分布變為雙峰分布。這是由于隨著反應時間的增加,水TCA逐漸分解,生成了粒徑小的碳酸鈣。由圖9(d)可知,溶出溫度變大時,粒度分布曲線有左移趨勢,粒徑變小,說明升高溫度有利于反應的進行,容易生成粒徑較小的碳酸鈣。

圖9 不同條件下溶出產物粒度分析
TCA經溶出后其固相產物為碳酸鈣,溶出液為低分子比(αK=2.8)的鋁酸鈉溶液。低分子比鋁酸鈉溶液可直接通入二氧化碳生成氫氧化鋁。碳酸鈣經過焙燒分解為石灰和二氧化碳,產生的氧化鈣可用于TCA制備的過程。
3 結 論
為實現TCA中氧化鋁的回收利用,研究了TCA中氧化鋁的溶出行為,獲得了氧化鋁溶出的最佳工藝,結論如下:
(1) TCA的氧化鋁溶出率隨碳堿濃度、溶出溫度、溶出時間的提高而增加,溶出產物的平均粒徑隨之減小;溶液分子比對TCA的溶出率和平均粒徑影響較小;溶出時間超過60 min后氧化鋁溶出率變化較小,此時溶出反應基本達到平衡。
(2) TCA的最佳溶出條件為:碳堿濃度為145 g/L,溶液分子比為2.22,溶出溫度為180 ℃,時間為60 min,此時氧化鋁溶出率達到92%左右。
(3)溶出產物主要為結晶良好的碳酸鈣和少量未反應的TCA。碳酸鈣經焙燒后產生的氧化鈣可用于TCA的制備,實現了物料的循環利用。

