基于網絡藥理學研究桃仁-紅花治療高脂血癥的作用機制*
崔金鵬,李淑洲,王佐梅,李雪瑩,姚欣卉,苗金雪,肖洪彬
黑龍江中醫藥大學,黑龍江 哈爾濱 150040
桃仁是薔薇科植物桃Prunuspersica(L.)Batsch或山桃Prunusdavidiana(Carr.)Franch的干燥成熟種子,其味甘、苦,性平,行血活血之藥也,而其活血之性緩。《神農本草經》云:“主瘀血”,《名醫別錄》曰“破癥瘕”。紅花是菊科植物紅花CarthamustinctoriusL.的干燥花,其味辛性溫,入心肝二經,可逐腹中惡血而補血虛。血瘀證是由于血液循環障礙而造成的全身或局部組織器官供血供氧不足,引起組織的炎癥、增生、壞死、血栓、出血等。中醫學認為肝主疏泄、肝藏血。肝通過疏泄功能調暢氣機,氣機逆亂,則清濁混淆,津血敗壞為痰濁瘀血,痰濁瘀血壅塞于脈絡之間,影響津血的正常運行,致使血液發生濃、黏、凝、聚的異常變化,誘發非酒精性脂肪肝[1]、腦梗死[2]、冠狀動脈粥樣硬化性心臟病[3]和心肌梗死[4]等,以上是高脂血癥形成的原因之一。王微[5]、馬貴萍[6]、曾定倫[7]、王臬[8]等醫家都對高脂血癥痰濁血瘀型進行過論述。高脂血癥是體內脂質代謝紊亂引起的血脂水平增高的一種全身性疾病,嚴重威脅著人類健康。高脂血癥屬于西醫病名,其論述散見于胸痹、中風、痰濕、濁阻等病中,現代中醫將其歸屬于傳統中醫學的痰濁、血瘀范疇[9]。痰濁和血瘀的高脂血癥的主要病理產物,痰瘀互結證也是高脂血癥的常見證型[10]。由于中藥多成分、多靶點、多途徑協同作用,使中藥作用機制難以明確。近年來通過對疾病基因網絡和藥物作用網絡的分析研究發現,藥物不僅作用于多個靶點,同時靶點也作用于多種疾病,因此就形成了復雜的藥物-靶點-疾病的復雜網絡。網絡藥理學是將系統科學、網絡科學、生物信息學、計算機科學和數學等多學科融合,通過數據收集、靶點預測、網絡分析與可視化、多組分相互作用和信號通路預測,使多靶點藥物分子設計更為精確,從而提高應用基礎研究的成功率。網絡藥理學的發展與應用,將會對疾病特別是復雜疾病發病機制的全面了解,以及治療藥物的發現和研究做出貢獻。所以本研究通過網絡藥理學方法分析桃仁-紅花治療高脂血癥的作用,為中西醫結合治療高脂血癥提供新的研究思路,同時為活血化瘀降脂藥的研究提供參考依據。
1 方法
1.1 高脂血癥相關作用靶點收集在Drugbank疾病靶點數據庫和TTD(therapetutic target datebase)疾病靶點數據庫輸入疾病名稱“Hyperlipidemia”“Hyperlipemia”檢索高脂血癥的作用靶點,運用Uniprot數據庫獲得人源Uniprot ID,以供后續分析。
1.2 桃仁-紅花活性成分的收集及靶點預測運用中藥系統藥理學分析平臺(TCMSP)數據庫檢索桃仁、紅花化學成分,共獲得化學成分255個,其中桃仁66個、紅花189個,考慮中藥在體內吸收、分布、代謝、排泄后作用靶點器官及數據量,設置口服藥物利用度(drug-like,OB)≥30%、類藥性(oral bioavailability,DL)≥0.18、化合物的半衰期(half-life,HL)≥4。運用TCMSP數據庫獲得活性成分預測靶點,應用Uniprot數據庫獲得人源Uniprot ID。
1.3 構建桃仁-紅花活性成分-潛在靶點網絡將藥物預測的靶點與高脂血癥作用靶點運用VENNY 2.1數據庫篩選共同靶點,運用Cytoscape3.7.1軟件繪制桃仁-紅花活性成分-潛在靶點網絡。
1.4 潛在靶點生物學過程及通路分析使用Cytoscape插件ClueGO對16個潛在靶點基因進行GO(gene ontology)生物學過程富集分析和KEGG(kyoto encylopedia of genes and genomes)通路富集分析,選取具有顯著性差異的生物學過程和通路。
2 結果
2.1 高脂血癥靶點收集基于TTD、Drugbank數據庫挖掘并刪除重復靶點,將靶點信息導入Uniprot數據庫獲取人源基因,得到高脂血癥47個作用靶點(表1)。
2.2 桃仁-紅花活性成分及預測靶點經TCMSP數據庫檢索并設置OB≥30%、DL≥0.18、HL≥4,獲得桃仁活性成分23個,紅花活性成分16個,去除無明確作用靶點及靶點無人源基因的活性成分后,獲得32個活性成分(包含1個共有成分)(表2)。對篩選后的化合物成分進行分析,桃仁化合物成分主要有黃酮及其苷類、甾體和萜類、酚酸類等,且《中國藥典》將苦杏仁苷作為控制桃仁藥材的指標性成分。
2.3 桃仁-紅花活性成分-潛在靶點網絡構建與分析應用TCMSP數據庫獲得活性成分預測靶點564個,其中桃仁133個、紅花431個。運用VENNY 2.1數據庫篩選桃仁-紅花預測靶點和高脂血癥作用靶點,獲得16個靶點,即ESR1、PPARG、CASP3、CYP3A4、ALB、SLC6A4、TNF、SLC6A2、INSR、AKR1C3、SLC6A3、MAOB、MAOA、ABCG2、PPARA、PPARD。推測桃仁-紅花活性成分主要通過對16個潛在靶點的作用治療高脂血癥。應用Cytoscape3.7.1構建桃仁-紅花活性成分-潛在靶點網絡(圖1)。其網絡中共包括29個節點(13個活性成分節和16個潛在靶點節點),組成41條活性成分-潛在靶點聯系,充分體現了中藥多成分、多靶點相互作用的復雜網絡關系,驗證了桃仁-紅花對高脂血癥治療是通過多途徑、多靶點、整體協同方式發揮作用的。經過Network Analyzer對網絡中節點進行分析,桃仁-紅花活性成分-潛在靶點網絡中靶點平均節點度為2.6,共有7個靶點蛋白Degree≥3,分別是半胱氨酸天冬氨酸蛋白酶3(CASP3)、過氧化物酶體增殖物激活受體-γ(PPARG)、鈉依賴去甲腎上腺素轉運體(SLC6A2)、鈉依賴5-羥色胺轉運體(SLC6A4)、細胞色素P450(CYP3A4)、腫瘤壞死因子(TNF)、胰島素受體(INSR),即以上靶蛋白是桃仁-紅花活性成分發揮治療高脂血癥的關鍵靶點。
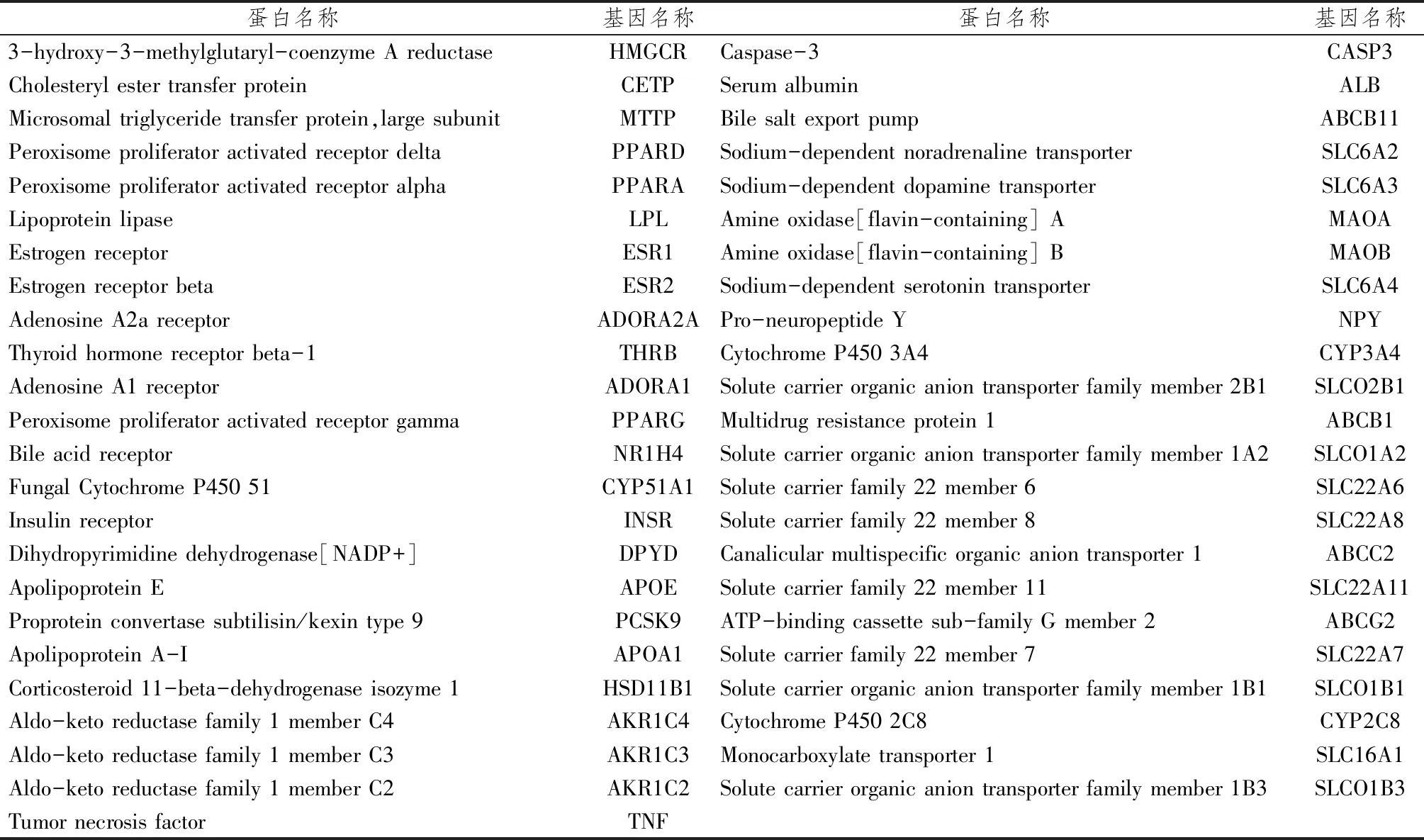
表1 桃仁-紅花47個與高脂血癥相關靶點
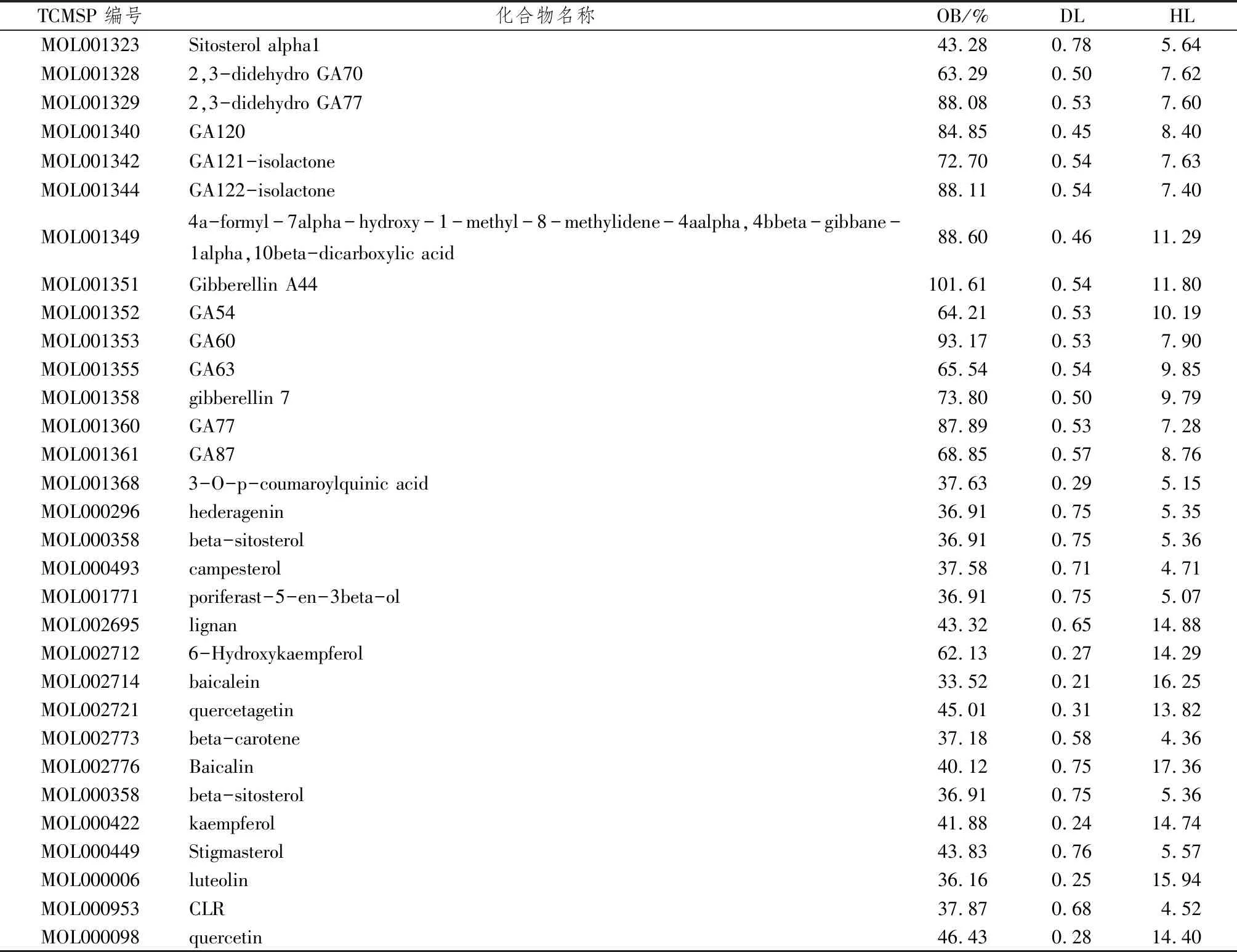
表2 桃仁-紅花活性成分基本信息
2.4 桃仁-紅花治療高脂血癥的潛在靶點GO基因功能富集分析富集分析共得到22條P≤0.05的生物過程,結果分為3部分,富集分析網絡圖、富集分析餅狀圖、柱狀圖。依據P值越小可靠性越高,排名前10位的生物學過程依次為dopamine catabolic process(多巴胺的分解過程)、catechol-containing compound catabolic process(含兒茶酚的化合物分解代謝過程)、catecholamine catabolic process(兒茶酚胺分解過程)、phenol-containing compound catabolic process(含酚化合物分解代謝過程)、response to nicotine(對尼古丁反應)、sequestering of triglyceride(甘油三酸酯隔絕)、organic hydroxy compound catabolic process(有機羥基化合物分解代謝過程)、dopamine uptake(多巴胺吸收)、monoamine transport(單胺運輸)、catecholamine uptake(兒茶酚胺吸收)。這些生物學過程表明高脂血癥相關靶點偏于通過調節靶基因轉錄、蛋白水解、神經遞質轉運的方式,從而促進高脂血癥的發生和發展。
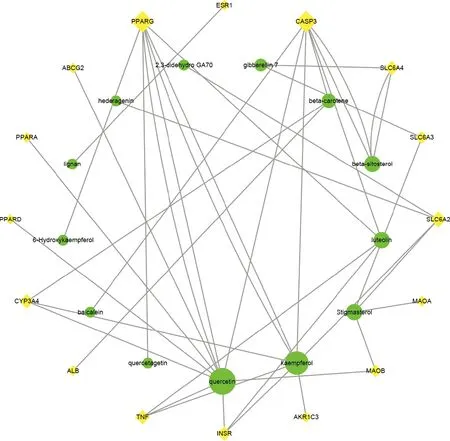
圖1 桃仁-紅花活性成分-潛在靶點網絡
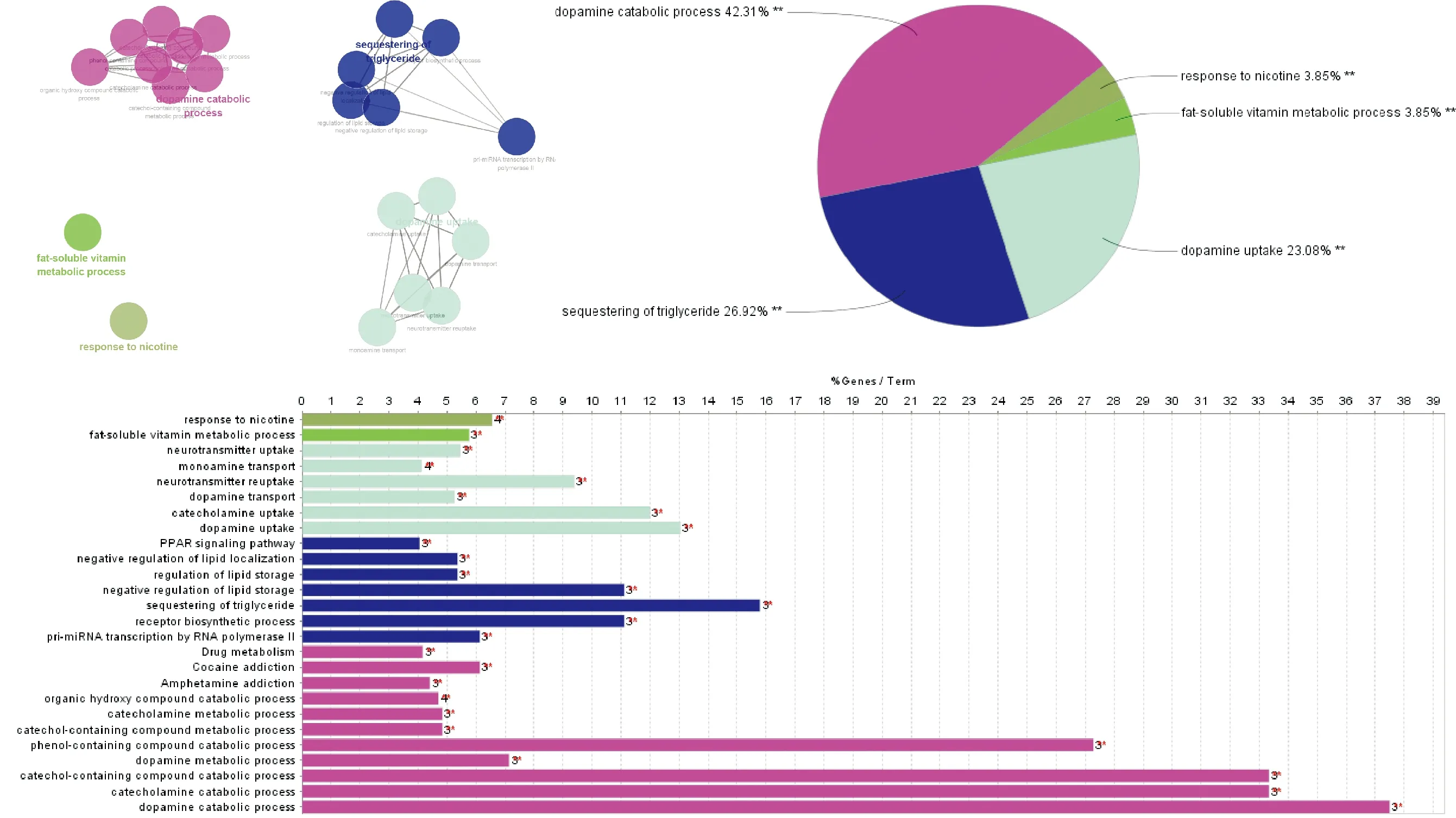
圖2 桃仁-紅花治療高脂血癥的潛在靶點GO基因功能富集分析

表3 桃仁-紅花治療高脂血癥潛在靶點生物學過程的GO分析
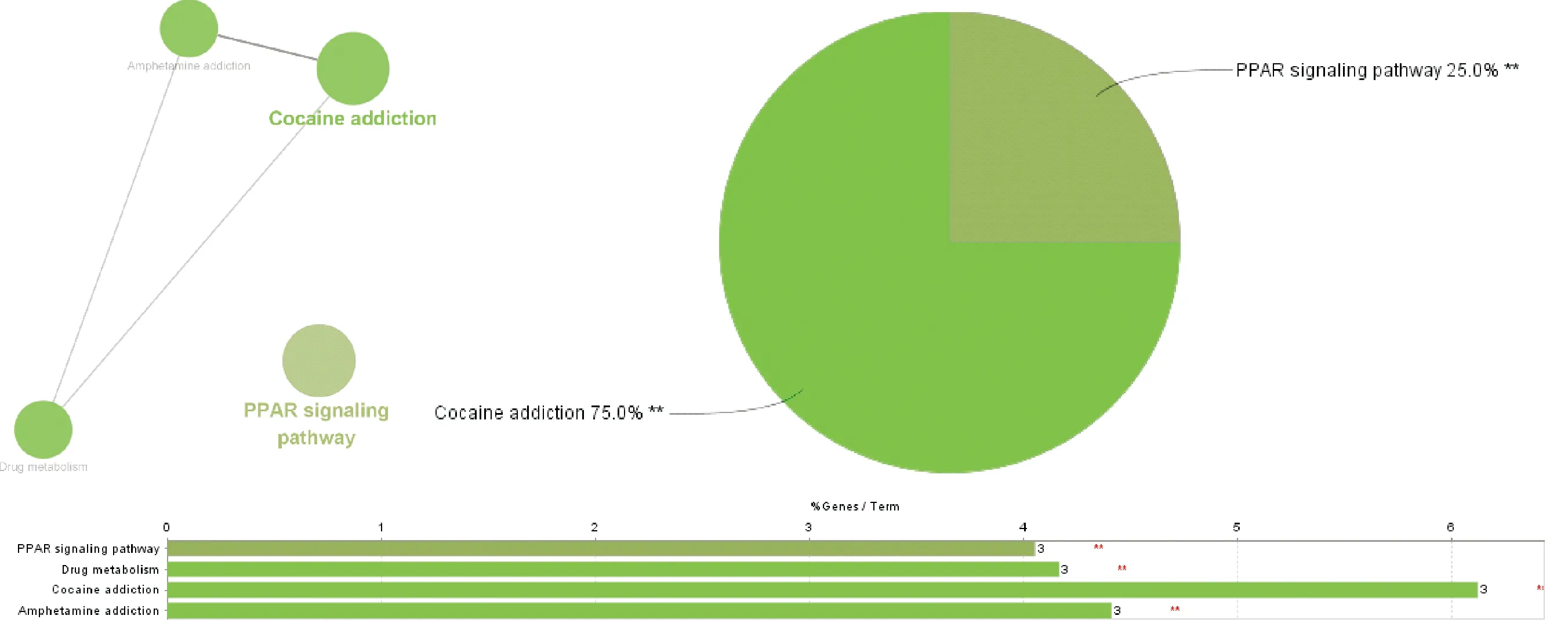
圖3 桃仁-紅花治療高脂血癥的潛在靶點KEGG通路富集分析
2.5 桃仁-紅花治療高脂血癥的潛在靶點KEGG通路富集分析共得到4條P≤0.05的通路,PPAR信號通路(PPAR signaling pathway)、藥物代謝(drug metabolism)、可卡因成癮(cocaine addiction)、安非他明成癮(amphetamine addiction)。

表4 桃仁-紅花治療高脂血癥的潛在靶點通路
3 討論
高脂血癥是體內脂質代謝紊亂引起的血脂水平增高而產生的一種全身性疾病,易誘發多種疾病及并發癥。研究表明,高脂血癥與腦血栓、心肌梗死、心臟猝死、糖尿病、高血壓、脂肪肝等有密切的關系,是形成冠狀動脈粥樣硬化性心臟病的主要危險因素之一。隨著生活水平的提高及飲食習慣的改變,高脂血癥的潛在人群不斷增加,已逐漸成為威脅人類健康的重要因素之一。高脂血癥受多種因素的共同影響,多信號分子參與其發生發展,使得對高脂血癥的細胞內信號的轉輸做出正確的預測。本研究通過網絡藥理學方法,篩選桃仁-紅花中的活性成分及預測靶點,獲取高脂血癥治療靶點,映射出桃仁-紅花治療高脂血癥的網絡圖,從系統上研究藥物對人體之間的相互作用及規律,并且確定分子層面的靶點、生物學過程、通路等,闡釋桃仁-紅花治療高脂血癥的效應機制。通過對高脂血癥治療靶點與桃仁-紅花活性成分的預測靶點對比,獲得16個對高脂血癥有明確治療意義的靶點,其中半胱氨酸天冬氨酸蛋白酶3、過氧化物酶體增殖物激活受體-γ、鈉依賴去甲腎上腺素轉運體鈉依賴5-羥色胺轉運體、細胞色素P450、腫瘤壞死因子、胰島素受體被視為桃仁-紅花治療高脂血癥的重要靶點。過氧化物酶體增殖物激活受體-γ控制著脂肪酸的過氧化物酶體β氧化途徑是脂肪細胞分化的關鍵調節因子。降低 PPAR-γ 的表達能夠抑制脂肪肝的發生[11]、脂肪細胞分化[12]、脂肪細胞分泌的Adiponectin、Leptin,有效地抑制BMMSCs向脂肪細胞的過度分化[13]、非酒精性脂肪肝病中脂代謝[14]。鈉依賴去甲腎上腺素轉運體是單胺轉運體。去甲腎上腺素通過其高親和力的鈉依賴性再攝取到突觸前終末而終止其作用[15]。伍菲凡[16]研究發現,高脂飲食小鼠的五羥色胺濃度會顯著降低。胰島素受體是介導胰島素多向作用的受體酪氨酸激酶,胰島素結合可導致多種細胞內底物磷酸化。增加胰島素受體底物的基因表達,可能是治療肥胖的作用機制之一,增強胰島素受體底物活性可改善非酒精性脂肪肝大鼠胰島素抵抗[17]。相關實驗表明[18-19],非酒精性脂肪性肝病血清腫瘤壞死因子-α明顯上升,給予藥物后患者血清脂質指標改善同時,腫瘤壞死因子-α水平顯著降低。對半胱氨酸天冬氨酸蛋白酶3靶點對治療高脂血癥研究相對較少,可做深入研究。通過對潛在靶點的GO和KEGG富集分析結果說明,高脂血癥主要與藥物代謝、PPAR信號通路最為相關。歐麗娜等[19]通過研究發現,具有雌激素樣作用的補腎陽藥可調節脂代謝,膽固醇逆向轉運關鍵蛋白介導藥物可調控脂代謝[20]。PPAR信號通路已經通過關鍵靶點過氧化物酶體增殖物激活受體-γ在通路中起到的作用驗證了通路的可靠性。
本研究應用網絡藥理學方法對桃仁-紅花治療高脂血癥的活性成分、作用靶點和作用機制進行了初步探索,為進一步研究活血化瘀降脂藥提供參考和依據。

