選擇性COX-2抑制劑在手屈肌腱損傷圍手術期的應用
張國磊 張哲敏 段文旭 王豐羽
隨著我國社會和工業的發展,手部損傷患者逐年增多,屈肌腱損傷是手外傷中一種較常見的損傷。國內統計,手部損傷中單純的肌腱損傷或合并有肌腱損傷的病例高達30%[1]。一項美國的回顧性分析數據顯示,手或手腕肌腱損傷的發生率為33.2/10萬人年[2]。肌腱損傷患者經手術治療后約40%可發生不同程度肌腱粘連,導致肢(指)體活動受限,甚至終生殘疾[3]。許多學者通過改進手術技術、藥物、生物材料防粘連膜、康復鍛煉、物理療法與基因治療等方法預防肌腱粘連[4,5]。其中早期活動仍是預防術后粘連的基礎和關鍵[6]。疼痛是限制患者術后早期康復訓練的重要原因,因此選擇合適的鎮痛藥物對于減輕患者術后疼痛、促進患者早期康復具有重要意義。有動物實驗證明非甾體類抗炎藥(NSAIDs)能夠減少肌腱的粘連[7],同時NSAIDs類藥物也是目前臨床上常用的鎮痛藥物。昔布類藥物是選擇性抑制環氧化酶-2(COX-2)的NSAIDs類藥物,具有安全性好和不良反應少的特點[8]。本研究擬采用選擇性COX-2抑制劑(帕瑞昔布、塞來昔布)和中樞性鎮痛藥(曲馬多)進行對比,探討其用于手部屈指肌腱損傷術后的鎮痛效果、不良反應以及手功能恢復等情況。
1 資料與方法
1.1 一般資料 選擇2016年11月至2019年11月我科收治的銳器傷致手屈肌腱Ⅱ、Ⅲ、Ⅳ區損傷且年齡18~60歲的成年患者32例。排除標準:(1)非甾體類藥物、磺胺類及阿片類藥物過敏者;(2)既往肝腎功能不全、消化道潰瘍、胃腸道出血、冠心病史者;(3)有酒精依賴史或藥物成癮史的患者;(4)長期因其他疾病使用止疼藥物者。將患者隨機分為COX-2抑制劑組和曲馬多組,每組16例。2組患者在性別比、年齡、損傷分區等方面的差異均無統計學意義(P>0.05),具有可比性。本研究已通過本院倫理委員會批準,并與患者或家屬簽署知情同意書。見表1。

表1 2組患者的性別、年齡、損傷分區比較 n=16
1.2 手術方法 患者手術均由經過專業培訓的手外科醫師完成,手術在臂叢神經阻滯麻醉及上臂止血帶下進行,使用3-0 TICRON聚酯縫線[9],肌腱縫合技術均采用ZM法[10]。術后給予腕關節中立位,掌指關節屈曲60°,指間關節伸直位石膏固定。
1.3 鎮痛方案 COX-2抑制劑組治療方案:于入院后給予注射用帕瑞昔布納(Pharmacia & Upjohn Company LLC)40 mg肌內注射,1次/12 h,持續72 h,后改為塞來昔布膠囊(輝瑞制藥有限公司)200 mg口服,1次/12 h,至術后2周。曲馬多組治療方案:于入院后給予鹽酸曲馬多注射液(德國格蘭泰有限公司)100 mg肌內注射,1次/12 h,持續72 h,后改為鹽酸曲馬多膠囊(德國格蘭泰有限公司)100 mg口服,1次/12 h,至術后2周。當2組患者中出現VAS(視覺模擬評分法)[11]疼痛評分≥7分時,給予鹽酸哌替叮注射液(東北制藥集團沈陽第一制藥有限公司)50 mg肌內注射。
1.4 康復方案 2組均在住院期間每天由同一醫師指導進行相同的康復訓練。去除繃帶對手指的固定,保留石膏托,只固定腕關節和掌指關節。每組被動屈指主動伸指5次,主動屈伸手指3次,3組/d。被動屈指要充分,主動屈指要緩慢,至指尖觸及掌面或患者感覺明顯遇到阻力為止。3周后去除石膏,每組主被動屈伸手指各10次,3組/d。
1.5 評價方法 定時分別記錄2組患者術后1、2、3、7、14 d鍛煉時的VAS疼痛評分;記錄2組患者不良反應的發生情況;術后1周、2周、4周、8周采用TAM系統評定法[12]對2組患者進行手功能評價。

2 結果
2.1 2組鎮痛效果比較 在術后1、2、3、7、14 d時選擇性COX-2抑制劑組患者鍛煉時的VAS評分更低,差異有統計學意義(P<0.05)。見表2。
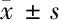
表2 2組患者各時間點鍛煉時VAS評分比較 n=16,分,
2.2 2組不良反應比較 2組患者均獲得完整的隨訪,未出現肌腱斷裂。COX-2抑制劑組在給藥后發生惡心嘔吐的不良反應數少于曲馬多組,差異有統計學意義(P<0.05);COX-2抑制劑組在給藥后發生頭痛頭暈、乏力嗜睡的不良反應數也少于曲馬多組,但差異無統計學意義(P>0.05)。見表3。

表3 2組患者用藥后不良反應情況比較 n=16,例
2.3 2組手功能恢復比較 2組手功能恢復情況比較,COX-2抑制劑組患者的術后1周、2周、4周、8周手功能TAM評定更優,差異有統計學意義(P<0.05)。見表4。
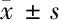
表4 2組患者的TAM比較 n=16,分,
3 討論
3.1 鎮痛與藥物 止痛藥按其藥理作用及作用機制可以分為兩大類:一是作用于中樞神經系統而產生鎮痛作用的中樞性鎮痛藥;二是具有解熱、鎮痛、抗炎作用的非甾體抗炎藥。曲馬多是一種強效中樞性鎮痛藥,通過激動阿片受體、單胺能機制及協同作用機制共同發揮鎮痛作用,其鎮痛療效與哌替啶相當,約為嗎啡的十分之一[13],其常見的不良反應為:惡心嘔吐、頭痛頭暈、乏力嗜睡[14]等。昔布類藥物是一種高選擇性COX-2抑制劑的非甾體抗炎藥,通過阻斷前列腺素類的合成和釋放,從而發揮鎮痛、抗炎作用,因對COX-1無抑制作用,故胃腸道不良反應較少[8]。選擇性COX-2抑制劑能夠在外周組織損傷周圍消除導致疼痛的炎癥因子,發揮外周消炎鎮痛作用,同時抑制中樞(脊髓背角和大腦)的COX-2表達上調,抑制中樞痛覺超敏,從而使患者對疼痛的感受減少[15]。《成人手術后疼痛處理專家共識》推薦使用選擇性COX-2抑制劑用于圍手術期鎮痛,可發揮抗炎、抑制外周和中樞敏化作用[16]。
圍術期鎮痛是骨科醫生最常面臨的最主要臨床問題之一。術后疼痛可以造成交感神經系統興奮、心臟負荷增加、呼吸功能下降、胃腸功能減弱、尿潴留、高凝狀態、影響睡眠等一系列的影響[16],處理不當會嚴重影響患者的康復。持續的疼痛刺激可引起中樞神經系統發生病理性重構,有可能發展為難以控制的慢性疼痛(chronic post-surgical pain,CPSP)[17],引起心理、精神和性格的改變。
3.2 肌腱的愈合及粘連 手屈肌腱損傷后功能的恢復主要為預防和控制肌腱的粘連。肌腱粘連與肌腱愈合密切相關。手術修復后肌腱愈合經歷3個重疊階段:炎癥(第1~7天),增殖(第3~14天)和重構(第10天起),各時期持續時間的長短與肌腱損傷程度相關[18]。目前對肌腱愈合機制基本達成共識,即肌腱愈合分為內源性愈合[19]和外源性愈合[20]。內源性愈合是由肌腱表面及內部的肌腱細胞經周圍滑液及細胞因子營養刺激自身增殖和遷移完成,這種愈合有利于提高愈合后肌腱的機械強度,降低肌腱粘連的嚴重程度[21]。外源性愈合主要為肌腱周圍的成纖維細胞增殖,長入肌腱斷端,最終形成瘢痕組織,因此外源性愈合難免會引起肌腱周圍粘連組織形成。
在肌腱粘連形成相關的信號轉導通路的研究中人們發現環氧化酶(COX)-2/前列腺素E(PGE)/前列腺素4型受體(EP4)信號轉導通路在肌腱粘連形成中具有重要作用。研究發現,在肌腱愈合過程中,COX-2含量增加,其可以催化花生四烯酸(AA)分解為PGE,后者可作用于靶細胞膜上的EP4,從而啟動COX-2/PGE/EP4信號轉導通路[22]。Ackerman等[23]進行實驗驗證了小鼠S100a4細胞中PGE2受體EP4缺失會減少粘連形成的假設。
肌腱愈合的炎癥期有大量炎癥因子釋放,其介導的過度炎癥反應是導致肌腱粘連形成的重要原因[24]。因此,許多學者使用非甾體抗炎藥藥物抑制與粘連發生相關的炎性細胞和因子,希望通過減輕炎癥反應來防治肌腱粘連[25]。Tan等[7]通過兔子的動物實驗證明非甾體類抗炎藥能夠減少肌腱的粘連。Wang等[25]的研究發現,大劑量非甾體抗炎藥可以通過線粒體/caspase-3途徑誘導大鼠肌腱干細胞形態學凋亡,不利于肌腱愈合。
傳統的觀點認為屈肌腱修復術后應制動3周,但很容易造成嚴重的肌腱粘連,影響功能,常需要二期行肌腱松解術。眾多研究表明屈肌腱修復術后早期的主被動功能鍛煉可減輕肌腱粘連、促進肌腱愈合和塑形、增加肌腱強度、改善手功能[26,27]。但早期的康復訓練可能引起肌腱的斷裂,因此良好的縫合技術十分重要。我們的既往研究認為結合TICRON聚酯縫線的ZM肌腱縫合技術可以為早期主被動活動提供足夠的強度[9,10,28]。
3.3 研究結果分析 本研究表明帕瑞昔布聯合塞來昔布在手屈肌腱損傷修復后術后功能鍛煉時的鎮痛效果強于曲馬多,其可能的原因是:(1)COX-2抑制劑本身可抑制肌腱粘連的形成[7],減少鍛煉的阻力,從而緩解疼痛;(2)盡早使用COX-2抑制劑可抑制中樞和外周的疼痛敏化作用,從而發揮外周和中樞的雙重鎮痛[15,16];(3)COX-2抑制劑能在分子水平上抑制炎性細胞反應及炎性介質的釋放,減少組織愈合期間的腫脹及出血[29],從而減輕疼痛;(4)中樞性鎮痛藥物對靜止時的疼痛效果好,對運動性疼痛療效有限,而高選擇性COX-2抑制劑對運動性疼痛效果較好[30]。
COX-2抑制劑組患者的手功能TAM評定更優,其原因可能是:(1)COX-2抑制劑本身可抑制肌腱粘連的形成,有利于功能恢復[7,27,29];(2)鎮痛效果更好,有助于早期康復訓練;(3)選擇性COX-2抑制劑能抑制炎性反應,減輕術后組織腫脹,更有利于早期功能鍛煉[31]。
綜上,治療劑量的昔布類藥物其良好的鎮痛效果和抑制肌腱粘連的作用相互促進,且不影響肌腱的順利愈合。應用選擇性COX-2抑制劑用于手部屈肌腱損傷后的圍手術期治療,較傳統的中樞性鎮痛藥物具有優勢,鎮痛效果確切,不良反應少,術后手功能恢復滿意。

