心房顫動射頻消融術后左房容積及收縮功能改變對心房顫動復發的影響分析
陳小麗 施林生 林 剛 趙東生 邰晨輝
(南通市第一人民醫院,江蘇南通226001)
房顫即心房顫動,是臨床常見的一種心律失常,其發生率僅次于冠心病、高血壓,且其發生率隨年齡增長呈上升趨勢,若不積極治療,致死率、致殘率均較高,臨床治療主要通過恢復正常竇性心律并長期維持治療以改善患者心功能[1-2]。以往臨床實踐中大多予以抗心律失常藥物以緩解癥狀,但效果并不理想,且治療期間部分藥物反而增加了患者心律失常風險。隨著射頻消融技術的逐漸普及,房顫治愈率明顯提高,但其對于患者左房結構及左心房功能的影響仍未確切闡明,為此,本研究特選取經本院確診的房顫患者,以分析射頻消融術治療房顫患者對其左心房容積結構及收縮功能的影響,報道如下。
1 資料與方法
1.1 一般資料
選取2018 年1 月至2019 年12 月期間經本院確診的房顫患者83 例作為觀察對象,納入標準:(1)經心電圖、動態心電圖及心臟超聲等檢查確診;(2)經一種或幾種抗心律失常藥物治療無效;(3)向患者說明手術目的及存在的潛在危險,遵循患者及其家屬意愿,簽署相關協議書。排除標準:(1)合并擴張型心肌病、瓣膜性心臟病或左心功能嚴重障礙者;(2)既往心臟手術史;(3)合并甲狀腺功能亢進;(4)其他原因(如酒精)導致的心房顫動;(5)合并肝腎功能不全者;(6)存在嚴重精神疾病者;(7)同期參與其他臨床試驗者;(8)病例資料不完整者。研究經相關醫學倫理委員會審批。
1.2 方 法
1.2.1 研究方法 均施以射頻消融術治療,術后隨訪6 個月,若疾病復發則視為射頻消融治療失敗(失敗組),未復發則視為射頻消融治療成功(成功組)。
1.2.2 治療方法 均采用射頻消融治療。待患者入院后進行詳細的實驗室檢查、影像學檢查已明確病情;術前給與華法林(商品名:華法林鈉片、生產廠家:芬蘭奧立安藥廠,批準文號:H20171095,規格:3mg×100 片)抗凝治療至術前3d 停止給藥,同時予以低分子肝素(商品名:注射用低分子量肝素鈣、生產廠家:兆科藥業 (合肥) 有限公司,批準文號:H10980166、規格:5000 抗 Xa 因子國際單位×12 支)皮下注射治療。射頻消融術操作:常規消毒鋪巾后,穿刺部位選取左鎖骨下靜脈、股靜脈,經過左鎖骨下靜脈放置冠狀靜脈竇電極,并經股靜脈送入Swartz鞘,通過鞘管向體內注入肝素溶液,在Carto 系統指導下進行環肺靜脈消融術。治療部位位于肺靜脈開口外0.5-1.0cm 設置功率30-40W,溫度設定在43℃為宜,射頻消融治療期間以17mL/min 實物流速靜脈滴注0.9%氯化鈉溶液(商品名:氯化鈉注射液(0.9%)、生產廠家:四川科倫藥業股份有限公司,批準文號:H51021157,規格:250mL:2.25g×1 瓶),作用間歇期流速調至2mL/min,消融點放電時間>30min,射頻消融結束后將Lasso 電極置于肺靜脈口外5mm處,并詳細記錄殘存肺靜脈電位,并在最早的電位處再次進行消融治療,使肺靜脈處于完全隔離狀態。術后48h 內持續監測患者各項生命體征,同時予以華法林口服治療及低分子肝素皮下注射治療。術后隨訪6 個月,若患者在隨訪期間無房性心律失常情況則停止華法林治療,予以常規抗心律失常藥物,定期復查。
1.2.3 治療效果評估標準 術后隨訪期間若再次出現房顫、房撲、房速等情況,且每次持續時間在30s以上則視為疾病復發[3]。
1.3 觀察指標
(1)左心房容積結構:通過美國GE 公司生產的Vicid 7 型彩色多普勒超聲診斷儀,探頭頻率2.0-3.5MHz,測定術前及術后6 個月左心房內徑(LAD)、左房最大面積(LAAmax)及左房最大容積(LAVmax)。(2)左心房收縮功能:同(1)中相同的方法測定術前、術后1d 及及術后6 個月二尖瓣血流頻譜A 峰值流速(VA)、左房射血力(LAF)及舒張期心肌組織運動峰速(Va)。
1.4 統計學分析
2 結 果
2.1 兩組患者一般資料比較
兩組患者一般資料比較,差異無統計學意義(P<0.05)。詳見表 1。
表1 兩組患者一般資料比較()
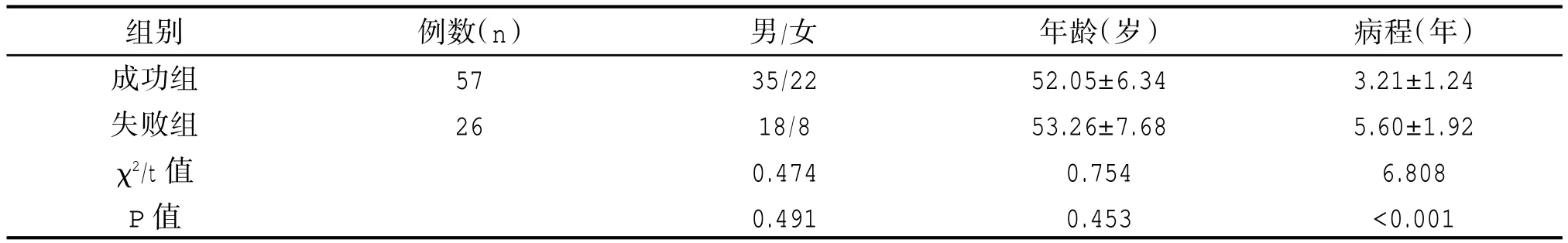
表1 兩組患者一般資料比較()
組別成功組失敗組χ2/t 值P 值例數(n)57 26男/女35/22 18/8 0.474 0.491年齡(歲)52.05±6.34 53.26±7.68 0.754 0.453病程(年)3.21±1.24 5.60±1.92 6.808<0.001
2.2 兩組治療結果評估
83 例患者均完成射頻消融術治療,且術后經6個月隨訪,其中有26 例患者出現復發,復發率31.33%,57 例治療成功,成功率68.67%。
2.3 兩組患者左心房容積結構相關指標比較
術后6 個月,治療成功組LAD、LAAmax及LAVmax均明顯較術前降低,且明顯低于失敗組,差異有統計學意義(P<0.05)。詳見表2。
表2 兩組患者左心房容積結構相關指標比較()
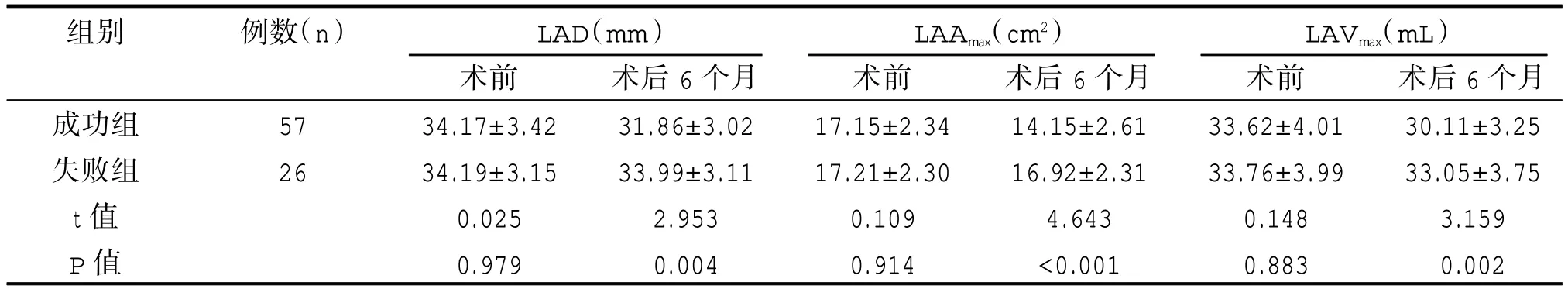
表2 兩組患者左心房容積結構相關指標比較()
組別例數(n)LAD(mm)LAAmax(cm2)LAVmax(mL)成功組失敗組t 值P 值57 26術前34.17±3.42 34.19±3.15 0.025 0.979術后6 個月31.86±3.02 33.99±3.11 2.953 0.004術前17.15±2.34 17.21±2.30 0.109 0.914術后6 個月14.15±2.61 16.92±2.31 4.643<0.001術前33.62±4.01 33.76±3.99 0.148 0.883術后6 個月30.11±3.25 33.05±3.75 3.159 0.002
2.4 兩組患者左心房收縮功能相關指標比較
兩組患者射頻消融術后1d VA、LAF 及Va 值均較術前下降,差異有統計學意義(P<0.05),且術后6個月成功組上述指標明顯高于對照組,差異有統計學意義(P<0.05);失敗組術后6 個月上述指標未見升高,明顯低于術前,差異有統計學意義(P<0.05),而成功組術后6 個月上述指標與術前差異無統計學意義(P>0.05)。詳見表3
表3 兩組患者左心房收縮功能相關指標比較()
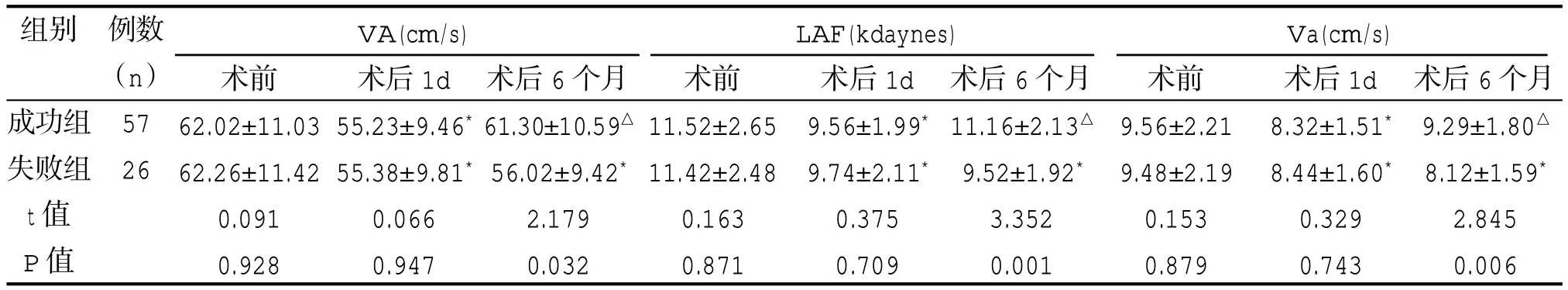
表3 兩組患者左心房收縮功能相關指標比較()
注:表示和術前比較,*P<0.05;△表示和術前比較,P>0.05。
組別VA(cm/s) LAF(kdaynes) Va(cm/s)成功組失敗組t 值P 值例數(n)57 26術前62.02±11.03 62.26±11.42 0.091 0.928術后1d 55.23±9.46*55.38±9.81*0.066 0.947術后6 個月61.30±10.59△56.02±9.42*2.179 0.032術前11.52±2.65 11.42±2.48 0.163 0.871術后1d 9.56±1.99*9.74±2.11*0.375 0.709術后6 個月11.16±2.13△9.52±1.92*3.352 0.001術前9.56±2.21 9.48±2.19 0.153 0.879術后1d 8.32±1.51*8.44±1.60*0.329 0.743術后6 個月9.29±1.80△8.12±1.59*2.845 0.006
3 討 論
研究發現,相較健康人群而言,房顫患者存在明顯的左心房體積增加,故存在左心房重構,且隨著疾病惡性發展,或者疾病發作的次數增加或發作時間延長,左心房容積呈進行性增大[4]。相關研究指出,如若能夠轉復竇性心律并長期維持,將可逆轉左心房重構現象。射頻消融術作為一種微創手段,術后早期射頻消融能量直接作用于肺靜脈周圍心房心肌細胞,進一步產生熱損傷,致使心肌細胞脫水、干燥、凝固、壞死,以致心房肌細胞數量減少;且隨時間推移,炎癥反應的參與以及術后瘢痕組織的收縮等均促使左心房縮小[5]。結合本次研究結果,所有患者均完成射頻消融術治療,且術后經6 個月隨訪成功率高達68.67%,且術后6 個月,消融治療成功組LAD、LAAmax及LAVmax均明顯較術前降低,且明顯低于消融失敗組。
LAF 是左心房處于收縮期時驅使血液經過二尖瓣向左心室流入時的力量,其可反映左心房機械收縮功能及左心室舒張特性,故該指標可較為準確地反映左心房收縮功能;VA 及Va 值是左心房功能的重要評估指標,其可反應左心房收縮功能。本研究中,房顫患者經治療后,術后1d 出現左心房收縮功能相關指標(LAF、VA 及 Va 值)下降情況,這可能由于射頻消融術后引起的廣泛心房損傷,繼而影響左心房收縮功能,即射頻消融術后即刻或短暫性的心肌頓抑現象;再者,術后左心房心肌細胞仍處于抑制狀態,繼而影響電-機械偶聯過程;此外,術后瘢痕組織的形成也可能是導致術后短期內左心房收縮功能降低的重要原因之一。但治療成功組患者術后6個月VA、LAF 及Va 值明顯恢復至術前相當的水平,該結果與既往文獻[6]基本吻合,進一步說明,射頻消融術用于治療房顫雖然術后早期會出現左心房收縮功能下降情況,但這種影響是短暫的。
綜上所述,射頻消融術用于房顫患者治療具有較高的成功率,主要通過對患者左心房結構重塑的逆轉以達治療目的,雖射頻治療術后早期可能導致患者左心房收縮功能下降,但不會對其左心房收縮功能造成長期損傷,可供臨床參考。

