新生兒氣管插管后聲門下狹窄1例
高祎 馬曉路
患兒男,出生16 h余,因“生后呼吸困難16 h余”于2019年7月29日入院。患兒系孕1產1,孕40+6周因“相對頭盆不稱”剖宮產娩出,出生體重3 880 g,羊水Ⅲ度污染,羊水量200 ml,胎盤、臍帶情況無殊,出生時Apgar評分1 min 9分,5 min 10分,10 min 10分。患兒生后即出現(xiàn)氣促,哭聲低弱,在當?shù)蒯t(yī)院接受氣管插管輔助呼吸治療16 h無好轉后轉入浙江大學醫(yī)學院附屬兒童醫(yī)院NICU。入院查體:體溫35.1℃,脈搏152次/min,呼吸64次/min,血壓85/53 mmHg,反應欠佳,前囟平,4.0號氣管插管下常頻機械通氣,呼吸急促,吸氣性三凹征陽性,雙肺未聞及啰音,心律齊,心音中,未聞及明顯雜音,腹平軟,肝脾肋下未及,四肢肌張力適中,生理反射欠完善,肢端溫。輔助檢查:血氣分析pH 7.247,PaCO254.8 mmHg,PaO229.7 mmHg,乳酸 5.5 mmol/L,HCO3-23.0 mmol/L,實際堿剩余-4.7 mmol/L;血WBC 20.60×109/L,中性粒細胞 86.3%,Hb 150 g/L,PLT 157×109/L,超敏CRP 27.13 mg/L。胸部X線片提示兩肺紋理增多、模糊,呈磨玻璃樣改變。患兒父親30歲,母親26歲,孕期無特殊用藥史,未訴特殊家族史。
患兒入院后診斷為“新生兒胎糞吸入綜合征”,存在呼吸困難,血氣分析提示CO2潴留,繼續(xù)機械通氣,入院第5天呼吸情況好轉,予撤機改鼻導管吸氧。患兒撤機1 h后出現(xiàn)呼吸費力,經皮氧飽和度下降,遂再次予氣管插管(3.5號)。入院第9天第2次拔除氣管插管改無創(chuàng)呼吸機NIPPV模式輔助通氣,撤機2 h后又出現(xiàn)呼吸困難,經皮氧飽和度下降,再次予氣管插管(3.5號)。入院第12天第3次撤機后仍有呼吸急促,伴喉部喘鳴音,予地塞米松靜脈應用及霧化吸入減輕上呼吸道水腫,無創(chuàng)呼吸機輔助通氣等治療,呼吸困難進行性加重。入院第29天再次行氣管插管術,發(fā)現(xiàn)插管困難(2.5號),考慮存在上氣道梗阻。請耳鼻咽喉科會診發(fā)現(xiàn)患兒存在重度聲門下狹窄(subglottic stenosis,SGS),僅留有直徑約 1.5 mm 孔隙(圖1),予無創(chuàng)高頻通氣支持,患兒家長考慮后拒絕氣管切開,于入院第43天全麻下行內鏡下球囊擴張術,用7 mm×17 mm的鼻竇球囊導入狹窄處,用3、6、10個標準大氣壓(atm)依次擴張3次,每次約30 s,充分止血后用CO2低溫冷凍探頭于12、3、6、9點方向分別冷凍,每次持續(xù)1 min。術后患兒鼻導管吸氧下呼吸困難顯著緩解,偶爾聞及喘鳴音,經皮血氧飽和度穩(wěn)定,分別于入院第46、50天再次全麻下行內鏡下球囊擴張術。患兒入院第59天大氣壓下呼吸平穩(wěn),經皮血氧飽和度穩(wěn)定,喂養(yǎng)可,復查喉鏡見聲門下擴張部位氣道狹窄不明顯,氣道通暢(圖2),予出院后耳鼻咽喉科門診隨訪。

圖1 喉鏡檢查提示聲門下狹窄
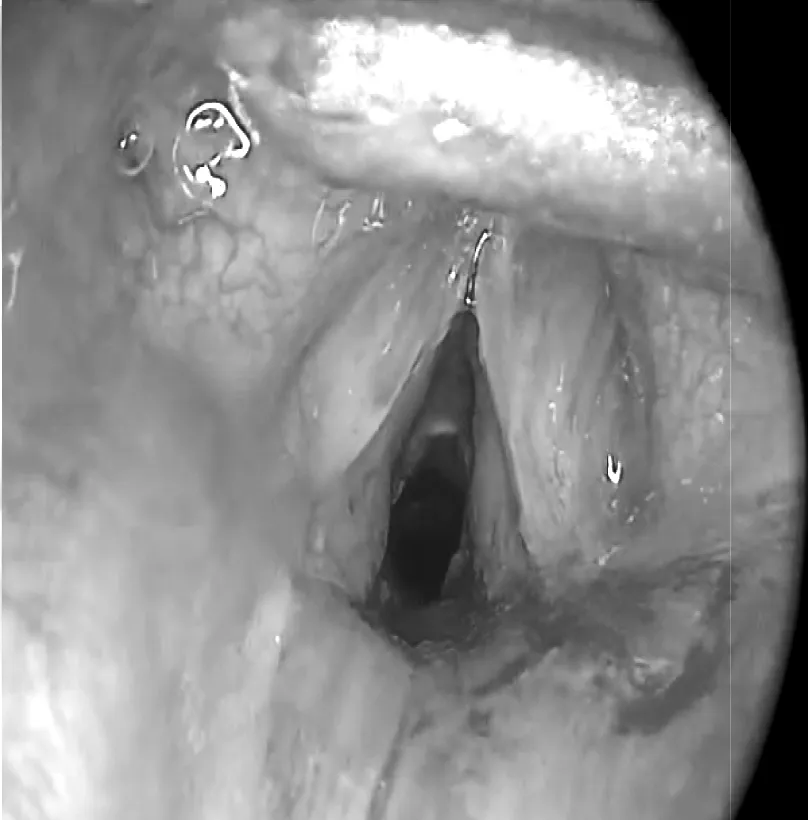
圖2 氣管狹窄球囊擴張術后
討論SGS是新生兒喉氣管狹窄中最常見的疾病,在足月新生兒中,SGS定義為環(huán)狀軟骨水平氣道直徑<4 mm,在早產兒中則定義為<3 mm[1]。SGS的臨床特點是出現(xiàn)不同程度的呼吸困難和喘鳴[2]。引起SGS的病因分為獲得性及先天性兩類,獲得性最為常見,約占90%,其中大多數(shù)患兒繼發(fā)于氣管插管[3-4]。研究發(fā)現(xiàn)插管次數(shù)增加、有創(chuàng)機械通氣時間延長、創(chuàng)傷性氣管插管、過大管徑的氣管插管等將增加新生兒SGS的發(fā)生率[5]。通常應用Myer-Cotton分級來評估SGS嚴重程度,Ⅰ度:喉氣管阻塞面積/呼吸道橫截面積比值≤50%,Ⅱ度:比值為51%~70%,Ⅲ度:比值為71%~99%,Ⅳ度:喉氣管完全阻塞[6]。
本例患兒由外院轉入,體重3 880 g,首次插管由外院醫(yī)生完成,選用4.0號氣管插管,管徑相對偏大。入院后考慮患兒胸部X線片提示胎糞吸入并不嚴重,對呼吸機的要求不高,近期撤機可能性大,因此未及時更換成3.5號氣管插管。氣管插管管徑過大,對氣管黏膜產生壓迫后導致血供減少,引起局部潰瘍,同時引發(fā)炎癥級聯(lián)反應,激活成纖維細胞,促進瘢痕形成,可能是該患兒發(fā)生SGS的重要原因。如圖1喉鏡檢查結果顯示,根據(jù)Myer-Cotton分級進行評估,本例患兒SGS為Ⅲ度,屬于重度氣管狹窄,因此導致反復的撤機困難。
SGS的治療以外科手術為主,包括開放性喉氣管重建術、環(huán)氣管切除-端端吻合術、氣管切開術等。盡管開放性外科手術是既往經典的治療方式,可以立即解決呼吸困難的問題,但術后的切口護理以及長期的造口護理給醫(yī)院、家庭帶來沉重的負擔,給護理人員和患兒造成極大的痛苦。同時,開放性外科手術本身會給氣道帶來其他并發(fā)癥,如氣管塌陷、持續(xù)的氣管肉芽組織形成和氣管狹窄、出血、感染、黏液阻塞等[7-8]。
過去幾十年,兒童SGS的微創(chuàng)外科手術已經取得重大進展,其具有縮短手術及住院時間、避免外部切口、避免發(fā)聲障礙、降低感染風險等潛在優(yōu)勢,成為治療SGS的新興手段[9]。治療SGS的微創(chuàng)方法有多種,包括內鏡下氣管擴張術、內鏡下肉芽組織激光切除術、內鏡下支架植入術等。同時,類固醇注射、CO2冷凍術、質子泵抑制劑等作為輔助手段,可以有效抑制炎癥反應,減輕肉芽組織的增生,避免氣管內瘢痕收縮,提高微創(chuàng)手術的成功率[9-10]。
英國國家健康和臨床研究所于2011年發(fā)布了關于使用內鏡下球囊擴張術治療聲門下或氣管狹窄的介入指南,指南肯定了微創(chuàng)手術治療的安全性及有效性,但未提供關于球囊尺寸、充氣壓力及充氣時間、擴張次數(shù)的明確建議。因此,外科醫(yī)生通常利用自己的經驗來指導相關治療過程。但過大的球囊尺寸、過高的充氣壓力、過長的充氣時間會損壞氣管甚至導致氣管破裂,反之又會降低手術效率并導致需要更多次數(shù)的手術。有研究分析了166例接受內鏡下球囊擴張術患兒的相關情況,結果表明喉和聲門下使用的氣囊直徑等于適合年齡的氣管導管外徑+1 mm,氣管為適合年齡的氣管導管外徑+2 mm[11]。
內鏡下球囊擴張術治療有效的定義包括患兒癥狀的好轉,內鏡或影像學檢查發(fā)現(xiàn)解剖學改善,肺活量或肺功能檢查的提高,避免進行開放性氣道手術[9]。有學者對英國59例氣道狹窄患兒的球囊擴張療效進行評估,結果顯示約有一半患兒術后Myer-Cotton分級的狹窄程度立即降低[12]。
與開放性手術相比,內鏡下球囊擴張術創(chuàng)傷小,并發(fā)癥少,但仍存在少量出血、發(fā)聲障礙、氣管再狹窄、氣管裂傷、吞咽困難、胃食管反流、肺水腫等可能。導致死亡很罕見,一般是由先天性心臟病、肺炎等基礎疾病所致[7,13]。
內鏡下球囊擴張術治療SGS的有效性受多種因素的影響,包括先天性狹窄、合并其他綜合征、多級氣道疾病、早產、年齡等。有文獻回顧分析了接受外科治療的SGS患兒的相關資料,發(fā)現(xiàn)球囊擴張失敗的患兒中Myer-Cotton分級為Ⅲ~Ⅳ度的比例更高,嚴重狹窄的存在是影響球囊擴張治療效果唯一具有統(tǒng)計學意義的變量[14]。
本例患兒接受內鏡下球囊擴張術聯(lián)合CO2冷凍術的治療,術中逐漸增加球囊充氣壓力,持續(xù)時間約30 s,以降低損傷氣道的可能,并應用CO2低溫探頭對氣管四周行冷凍術,從而減少瘢痕形成,防止氣管再狹窄。本例患兒共行3次內鏡下氣管成形術,術后患兒呼吸困難明顯好轉,對氧氣的依賴逐漸降低,復查喉鏡見聲門下擴張部位氣道狹窄不明顯,氣道通暢,提示治療效果理想。且手術過程未發(fā)生相關并發(fā)癥,其有效性及安全性得到了驗證。
綜上所述,新生兒獲得性SGS多由氣管插管引起。內鏡下球囊擴張術因創(chuàng)傷小、并發(fā)癥少、管理方便等優(yōu)點,將越來越多地取代開放性手術。

