影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后情況的相關因素
繆桂華,梁 達,李一帆
(昆山市第一人民醫院神經內科,江蘇 蘇州 215316)
腦梗死是指由于腦部局部血液供應障礙,引起腦組織缺血、缺氧,進而造成腦組織壞死與相應腦功能缺損,其屬于神經內科臨床常見的疾病之一。急性大動脈閉塞性腦梗死是一種因腦血管驟然閉塞,側支循環代償性差而造成的腦組織損害疾病,其致死、致殘率較高,已成為危害患者健康的主要原因之一[1]。有報道指出,在接受靜脈溶栓治療后,急性大動脈閉塞性腦梗死患者的血管再通率不足10%,不僅治療模式單一,且預后欠佳[2]。多模式血管再通屬于綜合性治療手段,包括靜脈溶栓橋接支架取栓、動脈溶栓、抽吸取栓、單純支架取栓、球囊擴張、支架置入等,其中可回收支架取栓被認為是治療急性大動脈閉塞性腦梗死的首選治療方案。但單純支架取栓血管再通率較低,需要球囊擴張、支架置入等補救措施,導致患者預后效果不佳[3]。基于此,本研究旨在探討影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后情況的相關因素,為臨床提供更有價值的預防措施依據,現報道如下。
1 資料與方法
1.1 一般資料 回顧性分析2018年1月至2021年1月昆山市第一人民醫院收治的98例急性大閉塞性腦梗死患者的臨床資料,分別接受了靜脈溶栓橋接支架取栓、動脈溶栓、抽吸取栓、單純支架取栓、球囊擴張、支架置入等多模式血管再通治療,均于治療后3個月采用改良Rankin量表(mRS)評分[4]對患者預后進行評估。根據mRS評分將98例患者分為預后良好組(65例,mRS ≤?2分)與預后不良組(33例, mRS ≥?3分)。診斷標準:參照《中國急性缺血性腦卒中診治指南2014》[5]中關于急性大動脈閉塞性腦梗死的診斷標準。納入標準:符合上述診斷標準,且經影像學診斷確診者;于發病前循環8 h內或后循環24 h內治療者;美國國立衛生研究院卒中量表(NIHSS)評分[6]≥?6分者等。排除標準:出血性腦卒中者;合并其他惡性腫瘤者;嚴重營養不良者等。本研究經昆山市第一人民醫院醫學倫理委員會審核并批準。
1.2 方法 兩組患者均接受頭部影像學[(CT+CT血管成像(CTA)+CT灌注(CTP))]檢查,觀察患者血管成像、頸動脈顱外段、顱內段及基底動脈閉塞情況,根據影像學檢查結果,局部麻醉或全身麻醉后,采用Seldinger技術穿刺患者的股動脈,同時行全腦血管減影造影,對責任血管進行觀察并分析側枝代償情況。顱內遠端中小血管閉塞且發病6 h內者動脈內推注注射用重組人TNK組織型纖溶酶原激活劑(廣州銘康生物工程有限公司,國藥準字S20150001,規格:1.0×10E7IU/16mg/支)5 mg動脈溶栓,超6 h者動脈內推注注射用鹽酸替羅非班(沈陽新馬藥業有限公司,國藥準字H20153204,規格:5 mg/支)0.5 mg動脈抗栓;大血管閉塞患者則置入導引導管和(或)中間導管,微導絲攜帶微導管至閉塞的責任動脈遠端,造影證實在真腔,在責任動脈的閉塞段中置入取栓支架,釋放后靜置5 min,隨后將支架、微導管及(或)中間導管撤回,結合患者血流情況,決定取栓次數。取栓后,利用造影對血管再通情況進行觀察,若患者血管狹窄率超過70%,予以其球囊擴張治療;若患者狹窄段回縮明顯或有夾層出現,予以其支架置入治療。釋放支架后,患者若出現急性血栓或血管壁影像學特征為毛糙,可通過微導管將替羅非班注入責任動脈;若經造影檢查,閉塞動脈顯示暢通,則結束手術治療。此外,若手術超過3 h,卻仍未有效開通血管,同樣結束手術。患者均于術后即刻及24 h復查CT,根據CT結果給予藥物治療,如抗血小板聚集、調脂、脫水降顱內壓、活血化瘀、清除自由基、改善循環、營養腦細胞等。
1.3 觀察指標 ①對兩組患者的臨床資料進行單因素分析,包括性別、年齡、術前與術后24 h NIHSS評分(NIHSS評分總分42分,分值越高表示神經缺損程度越嚴重)、發病~穿刺時間、穿刺~開通時間、是否合并高血壓、是否合并糖尿病、是否合并心房顫動、是否行局部麻醉、血管再通改良腦梗死溶栓(mTICI)分級[7](其中mTICI 0 ~ Ⅱ a級為未通,Ⅱ b ~ Ⅲ級為血管開通成功)、取栓次數、是否取出栓子、是否接受支架置入、是否接受動脈溶栓、是否接受球囊擴張、是否使用替羅非班等。②將單因素分析中差異有統計學意義的變量納入多因素Logistic回歸分析模型,篩選影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后不良的危險因素。
1.4 統計學方法 應用SPSS 22.0統計軟件分析數據,計數資料以[ 例(%)]表示,行χ2檢驗;計量資料以(±s)表示,行t檢驗;采用多因素Logistic回歸分析篩選影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后不良的危險因素。以P<0.05為差異有統計學意義。
2 結果
2.1 單因素分析 單因素分析結果顯示,預后不良組患者為男性、合并糖尿病、血管再通mTICI分級為0 ~ Ⅱ a級的患者占比及術后24 h NIHSS評分均顯著高于預后良好組,差異均有統計學意義(均P<0.05),見表1。
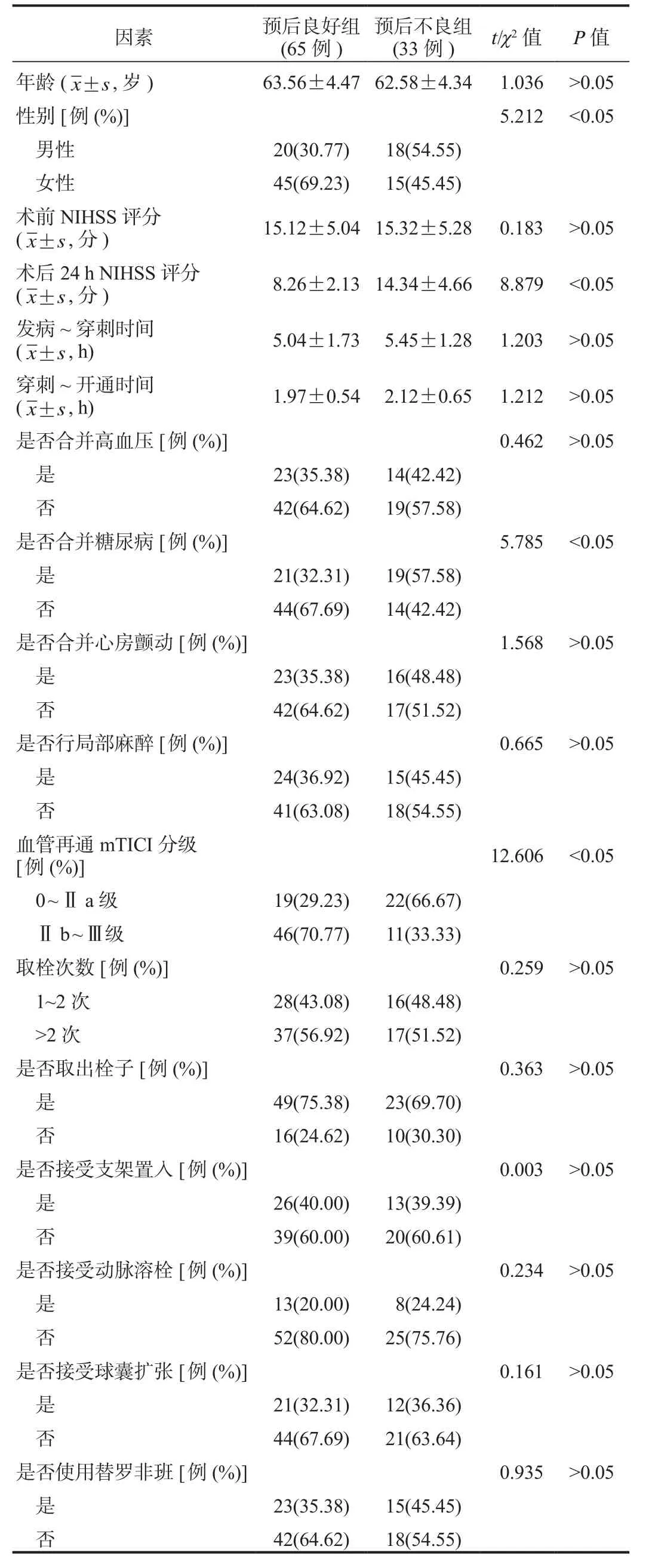
表1 影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后不良的單因素分析
2.2 多因素Logistic回歸分析 以急性大動脈閉塞性腦梗死患者行多模式血管再通治療后預后情況作為因變量,將單因素分析中差異有統計學意義的因素作為自變量,進行多因素Logistic回歸分析,結果顯示,合并糖尿病、血管再通mTICI分級為0 ~ Ⅱ a級均為影響急性大動脈閉塞性腦梗死患者預后不良的獨立危險因素(OR=5.836、1.192,均P<0.05),見表 2。
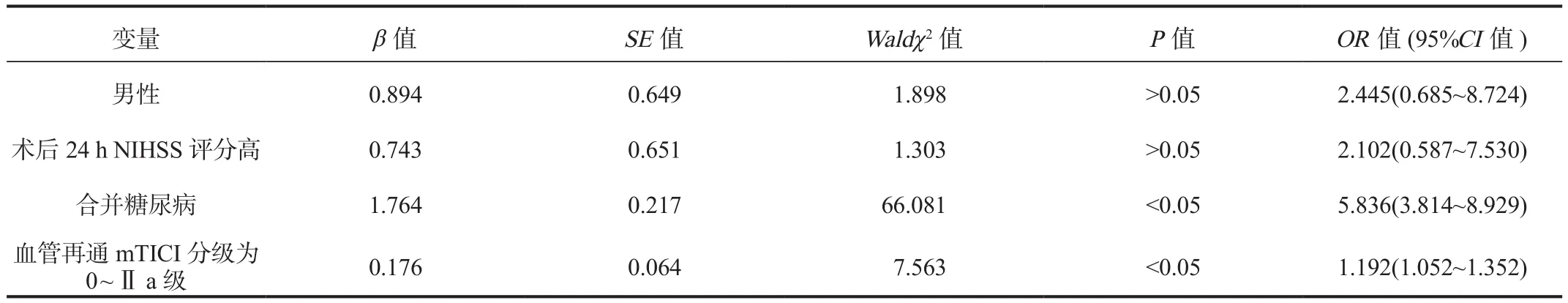
表2 影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后不良的多因素Logistic回歸分析
3 討論
急性大動脈閉塞性腦梗死是腦梗死的重要類型,也是血管內機械再通治療的目標人群。急性大動脈閉塞性腦梗死的病因復雜,有研究表明,合并動脈粥樣硬化性疾病患者接受可回收支架取栓治療的效果不理想,需要聯合其他補救措施[8]。隨著醫療技術的發展,多模式血管再通治療在臨床中的應用逐漸廣泛,急性大動脈閉塞性腦梗死病死率大幅下降,有效改善了以往單一治療效果欠佳的不足,但由于患者病情進展差異較大,部分患者應用該治療手段后難以改善癥狀,預后不佳,由此引起的疾病致殘率較高,不僅嚴重影響患者的生活質量,也給患者家庭與社會各界造成沉重的經濟壓力和精神壓力。因此,篩選急性大動脈閉塞性腦梗死患者行多模式血管再通治療后預后不良的相關危險因素,有助于完善之后的治療方案,改善患者預后。
本研究結果顯示,合并糖尿病、血管再通mTICI分級為0 ~ Ⅱ a級均為影響行多模式血管再通治療急性大動脈閉塞性腦梗死患者預后不良的危險因素,分析原因可能為,患者機體長期處于高血糖狀態,可使血管膠原蛋白和結構蛋白出現非酶性糖基化,血管脆弱性增加,造成內皮細胞功能障礙,出血性轉化的風險升高[9]。此外,血糖濃度升高后,可對一氧化氮生物利用度造成限制,進而抑制一氧化碳介導的血管舒張;長期高血糖還可引起纖溶功能和凝血功能異常,不僅使血液黏度增加、乳酸水平升高、紅細胞功能被破壞,還可加重腦細胞水腫現象,不利于預后,因此臨床中針對合并糖尿病的患者,應幫助其制定合理健康的飲食計劃、清淡飲食,加強身體鍛煉,保持健康的生活方式,少攝入多消耗,同時嚴格控制糖分攝取,進而控制血糖水平,還應加強術前觀察,結合患者糖尿病病情進展,制定合理的治療方案。血管再通mTICI分級在一定程度上可反映患者的顱內支循環恢復情況,分級越低提示血管再通性越差,而血管再通是恢復腦血流再灌注的基礎。既往研究表明,良好的側支循環是缺血半暗帶延遲轉化為核心梗死區的保護因素,若缺血半暗帶無法得到有效的再灌注,其核心梗死區將快速擴張,增加腦水腫風險,加速神經功能惡化,影響預后[10];因此臨床中可充分利用經顱多普勒超聲檢查評估患者mTICI分級、血管再通情況的變化,并據此通過完善手術方案,提高閉塞血管完全再通率,為患者預后良好提供基礎。
綜上,合并糖尿病、血管再通mTICI分級為0 ~ Ⅱ a級均為影響急性大動脈閉塞性腦梗死患者行多模式血管再通治療后預后不良的危險因素,臨床上可通過加強對以上因素的篩查與干預,調整治療方案,提高治療效果,改善預后。此外,臨床可增加樣本量對急性大動脈閉塞性腦梗死患者行多模式血管再通治療后預后不良與以上各項指標的關系進行進一步深入研究。

