高效液相色譜法測定番茄醬中乙二胺四乙酸二鈉
◎ 烏吉木
(巴彥淖爾市產品質量計量檢測中心,內蒙古 巴彥淖爾 015000)
乙二胺四乙酸二鈉,也可稱作EDTA-2Na,是一種重要的絡合劑,能絡合亞鐵離子。它不僅能作為真空采血管中的血液抗凝劑,還可以用在食品添加劑方面,控制聚合反應快慢,通常作為螯合劑、防腐劑和抗氧化劑等來使用。EDTA-2Na不僅能阻止食品由于金屬離子作用而出現的腐敗、變質,還能有效地遏制維生素C被氧化,減少營養物質的損失,同時還能夠阻止油脂的過氧化值升高、口感變差。
但是過量乙二胺四乙酸二鈉對人體有害,其每日允許最大攝入量為0.205 mg·kg-1。美國對乙二胺四乙酸二鈉有嚴格的限量要求,如液體狀多種維生素制劑不得超過150 mg·kg-1(與鐵離子一起作為液體狀多種維生素制劑中維生素B12的穩定劑)、罐裝黑斑豆不得超過145 mg·kg-1(護色)、罐裝菜豆不得超過165 mg·kg-1(護色)。《食品安全國家標準 食品添加劑使用標準》(GB 2760—2014)規定醬菜和罐頭不得超過0.25 g·kg-1[1]。在不同介質中乙二胺四乙酸二鈉的測定方法有比色法、滴定法、高效液相色譜法以及離子色譜法等[2-5]。比色法和滴定法無法定性只能定量,高效液相色譜法既能定性又能定量,因此本文通過高效液相色譜法對乙二胺四乙酸二鈉-Fe標準物質外標法定性定量,根據方程計算出乙二胺四乙酸二鈉-Fe絡合物的含量,也就是乙二胺四乙酸二鈉的含量[6-13]。
1 材料與方法
1.1 材料與試劑
甲醇,色譜級;乙酸,色譜級;鹽酸,分析純;四丁基溴化銨,分析純;乙酸鈉,分析純;三氯甲烷,分析純;三氯化鐵,分析純;水,去離子水。
乙二胺四乙酸二鈉標準品,中國計量科學研究院,編號GBW(E)060025d,批號1504,規格40 g,純度99.95%
1.2 儀器與設備
Agilent 1260高效液相色譜儀(配有二極管陣列檢測器);電子天平,感量為0.1 mg和0.01 g;離心機,轉速≥7 500 r·min-1;渦旋振蕩器;超聲波清洗機;微孔濾膜(0.45 μm)。
1.3 儀器條件
色譜柱:Agilent XDB-C18,柱長250 mm,內徑4.6 mm,粒徑5.0 μm;流動相比例:A-四丁基溴化銨-乙酸鈉混合溶液90%,B-甲醇10%;流速:1.0 mL·min-1;進樣量:10~20 μL;柱溫:35 ℃,檢測波長:254 nm。
1.4 實驗方法
1.4.1 試劑配制
(1)三氯化鐵溶液。將0.54 g三氯化鐵,溶于90 mL去離子水中,加入0.1 mL鹽酸,100 mL容量瓶定容充分搖勻。
(2)四丁基溴化銨-乙酸鈉混合溶液。稱取6.45 g四丁基溴化銨、2.46 g乙酸鈉加20 mL乙酸,用水定容至1 000 mL。
1.4.2 標準溶液配制
(1)標準液的制備。乙二胺四乙酸二鈉標準儲備液(1 000 μg·mL-1):精確稱取 0.1 g(精確至0.000 1 g)乙二胺四乙酸二鈉標準品,放入100 mL容量瓶,用去離子水溶解并定容。
(2)標準工作液。分別吸取乙二胺四乙酸二鈉標準儲備液0.05 mL、0.02 mL、0.05 mL、0.10 mL、0.50 mL及1.00 mL,分別用水定容至100 mL、10 mL、10 mL、10 mL、10 mL 及 10 mL,配制成 0.5 μg·mL-1、2.0 μg·mL-1、5.0 μg·mL-1、10.0 μg·mL-1、50.0 μg·mL-1及100.0 μg·mL-1濃度的乙二胺四乙酸二鈉標準系列溶液(配制系列需加FeCl3溶液1 mL,再用水定容)。
1.4.3 樣品處理
(1)樣品提取。準確稱取5 g(精確至0.01 g)試樣于50 mL離心管中,加入15 mL水,渦旋混合提取10 min,然后加三氯甲烷20 mL溶液,渦旋混合提取10 min,4 000 r·min-1離心 10 min,將上清液轉移至50 mL玻璃具塞比色管(容量瓶)中,再用15 mL水重復提取2次,合并提取液于50 mL具塞玻璃比色管中[14]。
(2)樣品衍生化。向上述樣品提取液中加1mL FeCl3溶液渦旋混合、超聲20 min,用水定容至刻度。
(3)樣品凈化。準確移取10 mL上述衍生化樣品溶液于50 mL具塞玻璃離心管中,加入5 mL三氯甲烷,在渦旋混合器上混合10 min,4 000 r·min-1離心5 min。上清液用0.45 μm濾膜過濾,濾液供液相色譜測定。
2 結果與分析
2.1 線性關系
如圖1所示,在上述方法條件下,標準系列在0.5~100.0 μg·mL-1呈線性關系,通過計算峰面積(y)與濃度(x,μg·mL-1)得線性方程公式為y=14.698 36x+0.395 69,相關系數r=0.999 992,實驗結果表明線性范圍良好。
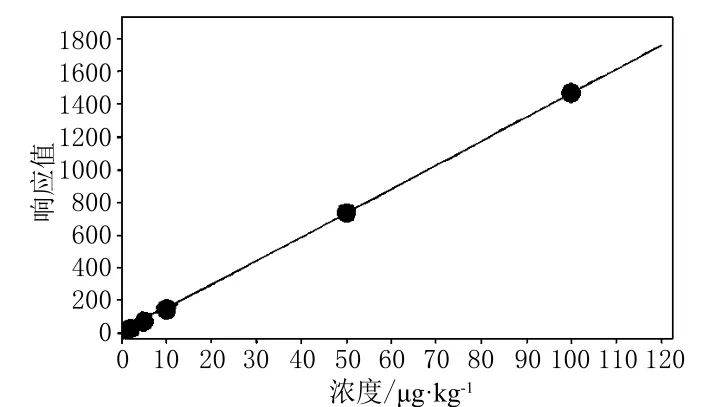
圖1 標液線性關系圖
2.2 空白及乙二胺四乙酸標準品色譜圖
實驗結果如圖2、圖3所示,在上述試驗儀器條件下,試劑空白圖無雜峰出現,標液出峰良好,理論塔板高。

圖2 乙二胺四乙酸二鈉空白色譜圖

圖3 乙二胺四乙酸二鈉標液出峰色譜圖
2.3 精密度及回收率
空白番茄醬樣品中加入濃度為1 000 μg·mL-1的乙二胺四乙酸二鈉標準儲備液0.15 mL和1.00 mL,進行2個水平的加標回收試驗,測定含量分別為0.03 g·kg-1和0.20 g·kg-1。每個濃度試樣水平平行測定8次,計算回收率和相對標準偏差(RSD),見表1。當加標濃度為 0.03 g·kg-1時,8 次測量平均值為 0.024 90 g·kg-1,回收率平均值為82.93%;當加標濃度為0.20 g·kg-1時,8次測量平均值為0.183 0 g·kg-1,回收率平均值為91.48%。

表1 番茄醬加標回收數據統計表
2.4 檢出限的測定
以儀器的S/N=3計算,測得該方法乙二胺四乙酸二鈉的最低檢出限,結果如表2所示。用外延法計算該實驗室本檢驗方法檢出限。用番茄醬加標0.01 g·kg-1進行檢出限測定,乙二胺四乙酸二鈉方法檢出限是0.002 g·kg-1。
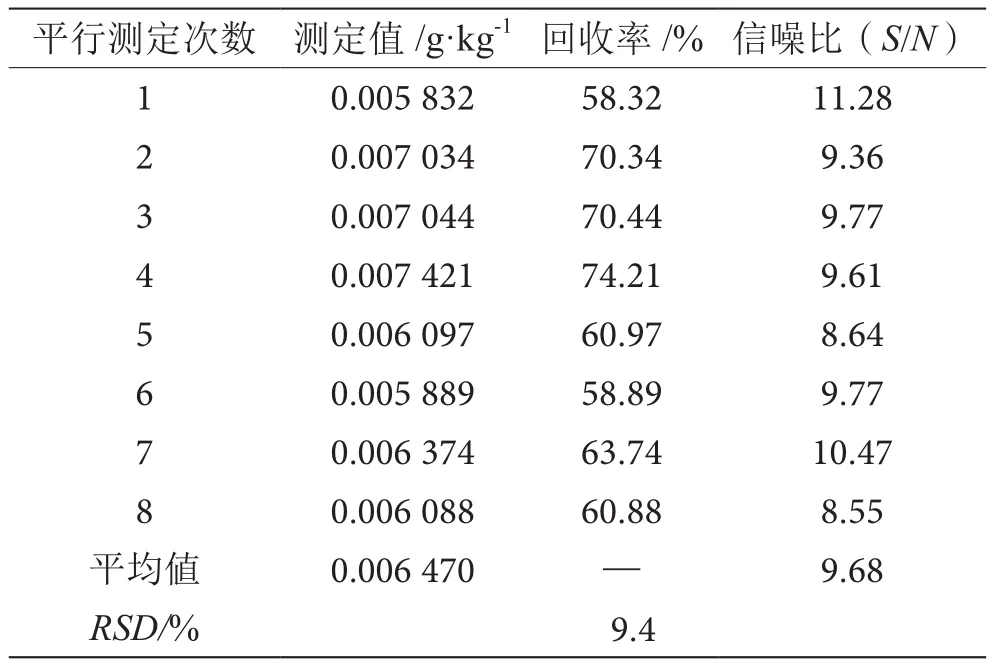
表2 最低檢出限測定數據統計表
2.5 樣品處理方法的選擇
根據《食品安全國家標準 食品中乙二胺四乙酸鹽的測定》(GB 5009.278—2016)的前處理方法,樣品加入水提取之后絡合,經混合陰離子固相萃取柱凈化時樣品中的雜質與乙二胺四乙酸二鈉競爭吸附柱易導致回收不理想。因為乙二胺四乙酸二鈉絡合物易溶于水,所以用水來提取效果好,成本也低。由于番茄醬基質復雜,影響實驗結果,不容易分離,還有可能堵塞儀器,故提取液中加入一定量的三氯甲烷,乙二胺四乙酸二鈉不易溶于有機溶劑,三氯甲烷可以與水分層,溶解樣品中的雜質,起到非常好的凈化效果,且提取液中加入還原劑使乙二胺四乙酸二鈉與三氯化鐵形成絡合物,經過再次凈化去除雜質測定時能夠達到很好的回收率和分離效果,見圖4、圖5。

圖4 番茄醬中無乙二胺四乙酸二鈉出峰色譜圖
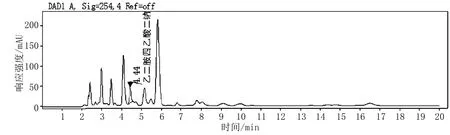
圖5 番茄醬中加乙二胺四乙酸二鈉出峰色譜圖
2.6 儀器條件的選擇
根據《食品安全國家標準 食品中乙二胺四乙酸鹽的測定》(GB 5009.278—2016)規定的色譜條件,乙二胺四乙酸二鈉-Fe需要在較低的pH環境下測定,本實驗探索了3種流動相條件,分別加入磷酸調節四丁基溴化銨-乙酸鈉混合溶液的pH=4.0、pH=2.5,加入20 mL乙酸調節四丁基溴化銨-乙酸鈉混合溶液進行試驗,試驗表明加入20 mL乙酸沒有測定pH的混合溶液對乙二胺四乙酸二鈉-Fe分離效果最好,見圖2、圖3。
2.7 色譜條件選擇
WatersSunFire-C18、Tnature-C18、Phenomenex-C18和Agilent XDB-C18作為液相色譜柱和A-四丁基溴化銨-乙酸鈉混合溶液、B-甲醇(A∶B=90∶10)作為流動相進行試驗。結果表明,Agilent XDB-C18對乙二胺四乙酸二鈉-Fe和干擾物能夠達到很好的分離效果,通過調整流速和流動相比例對EDTA的出峰時間進行調整。
本試驗中標液用A-四丁基溴化銨-乙酸鈉混合溶液,B-甲醇(A∶B=85∶15)作為流動相,流速0.8 mL·min-1出峰良好,試驗中采用以上條件對未添加乙二胺四乙酸二鈉的番茄原醬進行檢測,譜圖中雜質峰與標液EDTA峰重合,容易造成誤判。A-四丁基溴化銨-乙酸鈉混合溶液,B-甲醇(A∶B=90∶10)作為流動相,流速1.0 mL·min-1可以達到很好的分離效果。
3 結論
本實驗優化了高效液相色譜法測定番茄醬中添加劑乙二胺四乙酸二鈉的前處理方法和高效液相色譜檢測方法,通過對樣品前處理條件的調整,使樣品只要進行溶液渦旋液液萃取加以衍生,即可對乙二胺四乙酸二鈉的含量進行測定,流動相采用乙酸不需要調節pH值,且不易造成色譜柱堵塞。本方法簡單、快速、重復性和回收率較好,具有較高的準確度和精密度,能實現檢測番茄醬中乙二胺四乙酸二鈉的需要,可為食品中檢測乙二胺四乙酸二鈉提供實際操作和技術參考。

