微創(chuàng)旋切手術(shù)在乳腺良性腫瘤治療中的臨床應(yīng)用價(jià)值*
鄒寶山,陳元文,劉 磊
1.重慶市第五人民醫(yī)院甲乳外科,重慶 400062;2.重慶市南岸區(qū)人民醫(yī)院外科,重慶 400060
乳腺癌已躍居成為全球女性新發(fā)第一大惡性腫瘤,同時(shí)也是導(dǎo)致女性死亡的首要因素[1]。隨著對(duì)乳腺疾病重視度的逐漸增強(qiáng),越來(lái)越多的女性積極自查或行超聲檢查,進(jìn)而更多的乳腺良性腫瘤被檢查出。傳統(tǒng)開(kāi)放手術(shù)能夠有效去除乳房腫塊,但該手術(shù)方式存在手術(shù)時(shí)間長(zhǎng)、術(shù)后恢復(fù)慢、乳房變形、手術(shù)疤痕明顯等缺點(diǎn)[2]。隨著微創(chuàng)外科理念和技術(shù)的進(jìn)步,乳腺疾病的手術(shù)治療也逐漸向減少損傷和微創(chuàng)方向發(fā)展。微創(chuàng)旋切手術(shù)作為一種新型的乳腺良性腫瘤手術(shù)方式,備受醫(yī)生與患者的青睞[3]。為明確微創(chuàng)旋切手術(shù)與傳統(tǒng)開(kāi)放手術(shù)在乳腺良性腫瘤治療中的臨床效果及安全性,本研究對(duì)實(shí)施兩種手術(shù)方式的患者進(jìn)行對(duì)照分析。
1 資料與方法
1.1一般資料 回顧性分析2019年1月至2021年7月于重慶市第五人民醫(yī)院就診的208例單側(cè)乳腺良性腫瘤患者的臨床資料。納入標(biāo)準(zhǔn):(1)均接受手術(shù)治療,術(shù)后病理結(jié)果明確為良性腫瘤;(2)單側(cè)乳腺良性腫瘤;(3)單側(cè)乳房病灶≤2個(gè),病灶最大徑≤3 cm;(4)臨床資料完整。排除標(biāo)準(zhǔn):(1)有出血傾向、凝血機(jī)制障礙等;(2)合并嚴(yán)重心、肺基礎(chǔ)疾病,不能耐受手術(shù);(3)哺乳期、妊娠期及有急性感染性疾病;(4)臨床資料不完整。根據(jù)手術(shù)方式分為微創(chuàng)旋切手術(shù)組(128例)與傳統(tǒng)開(kāi)放手術(shù)組(80例),比較分析兩組的一般資料(年齡、病灶最大徑),術(shù)前相關(guān)指標(biāo)(白細(xì)胞計(jì)數(shù)、中性粒細(xì)胞絕對(duì)值、C反應(yīng)蛋白及血糖),圍術(shù)期指標(biāo)(手術(shù)時(shí)間、術(shù)中出血量、傷口長(zhǎng)度、傷口愈合時(shí)間)及術(shù)后并發(fā)癥(局部血腫、傷口感染、乳房外觀改變、病灶殘留及總發(fā)生率)發(fā)生情況。
1.2方法
1.2.1超聲引導(dǎo)下行微創(chuàng)旋切手術(shù) 患者取仰臥位,常規(guī)消毒鋪巾,超聲定位乳房病灶,確定最佳進(jìn)針位置。病灶周圍浸潤(rùn)麻醉及注射麻醉藥至乳腺與胸大肌之間的間隙,進(jìn)針點(diǎn)切開(kāi)皮膚0.3~0.5 cm,在超聲引導(dǎo)下穿刺插入旋切刀并達(dá)到病灶下方,超聲實(shí)時(shí)監(jiān)測(cè)下反復(fù)切割病灶,直至病灶消失。抽吸殘腔積血后拔出旋切刀,加壓包扎[4]。設(shè)備選用美國(guó)巴德安珂乳腺旋切主機(jī)與一次性乳腺旋切刀套裝。
1.2.2傳統(tǒng)開(kāi)放手術(shù) 患者取仰臥位,常規(guī)消毒鋪巾,病灶周圍浸潤(rùn)麻醉,根據(jù)超聲定位標(biāo)記病灶位置,做放射狀或乳暈切口,分離皮膚與皮下組織,尋找病灶并完整切除,創(chuàng)面電凝止血,逐層縫合關(guān)閉殘腔,可吸收線皮內(nèi)縫合切口,加壓包扎。
1.2.3評(píng)價(jià)指標(biāo) (1)比較兩組一般資料,包括年齡、病灶最大徑。(2)比較術(shù)前相關(guān)指標(biāo),包括白細(xì)胞計(jì)數(shù)、中性粒細(xì)胞絕對(duì)值、C反應(yīng)蛋白及血糖。(3)比較兩組圍術(shù)期指標(biāo),包括手術(shù)時(shí)間、術(shù)中出血量、傷口長(zhǎng)度、傷口愈合時(shí)間,術(shù)中出血量采用估測(cè)法,1張紗布計(jì)5 mL。(4)比較兩組術(shù)后并發(fā)癥,包括局部血腫、傷口感染、乳房外觀改變、病灶殘留等,病灶殘留采用術(shù)后1個(gè)月復(fù)查彩超評(píng)估;同時(shí)比較兩組術(shù)后并發(fā)癥總發(fā)生率。
2 結(jié) 果
2.1兩組年齡、病灶最大徑比較 兩組年齡、病灶最大徑比較,差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),具有可比性,見(jiàn)表1。
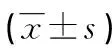
表1 兩組年齡、病灶最大徑比較
2.2兩組術(shù)前相關(guān)指標(biāo)比較 兩組術(shù)前白細(xì)胞計(jì)數(shù)、中性粒細(xì)胞絕對(duì)值、C反應(yīng)蛋白及血糖比較,差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),見(jiàn)表2。
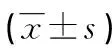
表2 兩組患者術(shù)前相關(guān)指標(biāo)比較
2.3兩組圍術(shù)期指標(biāo)比較 與傳統(tǒng)開(kāi)放手術(shù)組比較,微創(chuàng)旋切手術(shù)組手術(shù)時(shí)間、傷口長(zhǎng)度、傷口愈合時(shí)間均縮短,術(shù)中出血量減少,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見(jiàn)表3。
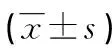
表3 兩組圍術(shù)期指標(biāo)比較
2.4兩組術(shù)后并發(fā)癥比較 兩組局部血腫、病灶殘留發(fā)生率比較,差異均無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);兩組傷口感染、乳房外觀改變及術(shù)后并發(fā)癥總發(fā)生率比較,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見(jiàn)表4。

表4 兩組術(shù)后并發(fā)癥比較[n(%)]
3 討 論
乳腺疾病可對(duì)廣大女性身心健康造成巨大的困擾。常見(jiàn)的乳腺良性疾病有乳腺增生、乳腺纖維腺瘤、非哺乳期乳腺炎及導(dǎo)管內(nèi)乳頭狀瘤[5]。乳腺增生是乳腺正常發(fā)育和退化過(guò)程失常導(dǎo)致的,主要有3種預(yù)防方法:密切隨訪、藥物干預(yù)和手術(shù)干預(yù),該病本身無(wú)手術(shù)治療指征,外科干預(yù)的主要目的是為了避免漏診、誤診乳腺癌或切除可疑病灶[6]。非哺乳期乳腺炎包括乳腺導(dǎo)管擴(kuò)張癥、導(dǎo)管周圍乳腺炎、肉芽腫性小葉乳腺炎,治療以傳統(tǒng)開(kāi)放手術(shù)為主,必須完整充分切除病灶,徹底切除所有肉眼可見(jiàn)的病變組織,盡可能保證陰性切緣,否則容易復(fù)發(fā)[7]。導(dǎo)管內(nèi)乳頭狀瘤是良性病變,手術(shù)是唯一的治療方法,半數(shù)以上的專家建議行傳統(tǒng)開(kāi)放手術(shù)切除,在有設(shè)備條件的醫(yī)院,也可在超聲引導(dǎo)下使用微創(chuàng)旋切手術(shù)進(jìn)行完整切除[8]。乳腺纖維腺瘤是最常見(jiàn)的乳腺良性腫瘤,可以發(fā)生于青春期后任何年齡段的女性,臨床多明確診斷后即選擇手術(shù)切除,傳統(tǒng)開(kāi)放手術(shù)適用于較大的纖維腺瘤,腫瘤最大徑≤3 cm的患者選擇微創(chuàng)旋切手術(shù),其具有創(chuàng)傷小,外形美觀的特點(diǎn)[9]。
回顧性分析重慶市第五人民醫(yī)院收治的208例單側(cè)乳腺良性腫瘤患者,根據(jù)手術(shù)方式進(jìn)行分組比較。兩組患者年齡、病灶最大徑比較,差異均無(wú)統(tǒng)計(jì)學(xué)意義(P<0.05),具有可比性。兩組患者白細(xì)胞計(jì)數(shù)、中性粒細(xì)胞絕對(duì)值、C反應(yīng)蛋白及血糖水平比較,差異均無(wú)統(tǒng)計(jì)學(xué)意義(P<0.05),提示兩組患者基線水平差異不大;但微創(chuàng)旋切手術(shù)組的術(shù)后并發(fā)癥總發(fā)生率低,微創(chuàng)旋切手術(shù)更具有減少術(shù)后并發(fā)癥的優(yōu)勢(shì)。雖然結(jié)果提示微創(chuàng)旋切手術(shù)組術(shù)后血腫與病灶殘留的發(fā)生率較高,但差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。術(shù)后血腫是微創(chuàng)旋切手術(shù)最常見(jiàn)的并發(fā)癥,多為術(shù)后處理不佳,包括按壓時(shí)間不夠,繃帶松解或移位等,大部分血腫可以自行吸收,也可通過(guò)負(fù)壓抽吸、加壓包扎等措施降低風(fēng)險(xiǎn)。追溯病灶殘留患者提示單側(cè)乳房2個(gè)病灶,最大徑分別為2.8 cm與3.0 cm。與相關(guān)研究認(rèn)為病灶殘留多與腫瘤初始大小及數(shù)目相關(guān)的結(jié)果一致,即腫瘤越多、越大,術(shù)后病灶殘留風(fēng)險(xiǎn)越大[10]。
隨著現(xiàn)代醫(yī)療技術(shù)的進(jìn)步,提出了“內(nèi)科外科化、外科微創(chuàng)化”的醫(yī)學(xué)發(fā)展觀念。超聲引導(dǎo)下的微創(chuàng)旋切手術(shù)在乳腺疾病治療中也越來(lái)越普遍。微創(chuàng)旋切手術(shù)不僅用于診斷乳腺腫瘤良惡性,而且也被用于完全切除乳腺良性腫瘤,尤其是纖維腺瘤。雖然目前認(rèn)為微創(chuàng)旋切手術(shù)不能用于切除乳腺癌,但隨著科技設(shè)備的提升,期待未來(lái)能將該技術(shù)應(yīng)用范圍擴(kuò)大到乳腺惡性腫瘤的治療上[11]。超聲引導(dǎo)下乳腺良性腫瘤微創(chuàng)旋切手術(shù)可以清晰觀察乳腺病灶的大小、數(shù)量及周圍組織關(guān)系,精準(zhǔn)定位乳房觸診陰性的病灶,提高了病灶完整切除成功率[12-13]。微創(chuàng)旋切手術(shù)安全可靠且復(fù)發(fā)風(fēng)險(xiǎn)低;更重要的是微創(chuàng)旋切手術(shù)收集到的完整連續(xù)的腫瘤標(biāo)本,與傳統(tǒng)開(kāi)放手術(shù)獲得的標(biāo)本得到的病理和免疫學(xué)結(jié)果一致,可為早期原發(fā)性乳腺癌的微創(chuàng)治療提供準(zhǔn)確的診斷基礎(chǔ),從而避免擴(kuò)大手術(shù)范圍,最大化保留乳房形狀和外觀美容度[14]。
綜上所述,乳腺良性腫瘤選擇微創(chuàng)旋切手術(shù)治療可縮短手術(shù)時(shí)間,減少術(shù)中出血與術(shù)后并發(fā)癥的發(fā)生,具有術(shù)后恢復(fù)快、保持乳房美觀度的優(yōu)勢(shì)。微創(chuàng)旋切手術(shù)有較高的臨床治療效果和較好的安全性,值得臨床推廣應(yīng)用。
- 檢驗(yàn)醫(yī)學(xué)與臨床的其它文章
- 探討老年2型糖尿病患者血尿酸水平與骨代謝標(biāo)志物、骨密度、骨質(zhì)疏松的相關(guān)性
- 咪達(dá)唑侖聯(lián)合氟馬西尼用于懸雍垂腭咽成形術(shù)麻醉蘇醒期的有效性與安全性觀察
- 以自我效能為核心的護(hù)理路徑對(duì)胃腸腫瘤術(shù)后腸造口患者生活質(zhì)量的影響
- 制霉菌素與克霉唑陰道片對(duì)外陰陰道假絲酵母菌病患者臨床療效及免疫功能的影響研究
- 心理及行為干預(yù)聯(lián)合家庭式無(wú)痛分娩對(duì)產(chǎn)后抑郁及分娩過(guò)程的影響分析*
- 肝硬化失代償期患者并發(fā)社區(qū)獲得性血流感染的臨床特征分析*

