比較2種途徑注入生大黃對重癥急性胰腺炎伴腹內高壓患者的影響
樊凰玉,何朝珠,彭 園,徐 琴,熊 丹
(南昌大學a.第一附屬醫院急診科; b.護理學院; c.第一附屬醫院消化科; d.第一附屬醫院心血管科,南昌 330006)
重癥急性胰腺炎(SAP)是一種臨床較為常見的急腹癥,其發病急、病情重、進展快、并發癥多、病死率高,可達20%[1]。SAP因炎癥因子刺激使腸道麻痹,腸功能減弱,大量腹腔液滲出,導致腹內高壓(IAH),當壓力持續升高達20 mmHg(2.66 kPa)以上且合并器官功能障礙或衰竭時即可診斷為腹腔間隔室綜合征(ACS)[2],IAH和ACS的發生嚴重影響SAP患者的預后[3]。
生大黃具有瀉下、通便、利膽等作用,在SAP治療中療效得到肯定。臨床可經口服、胃管、空腸管及保留灌腸等途徑給藥,既往研究[4-5]顯示,不同給藥途徑療效存在一定差異。本研究在常規綜合治療基礎上,比較經胃管和經空腸管兩種途徑注入生大黃對SAP伴IAH患者的療效,將結果報告如下。
1 資料與方法
1.1 一般資料
選擇南昌大學第一附屬醫院消化內科2019年3—12月收治的38例SAP伴IAH患者作為研究對象。患者均符合SAP的診斷標準[6]且腹內壓>12 mmHg(1.596 kPa),排除精神疾病或大黃藥物過敏者。本研究經本院倫理委員會批準,患者均知情同意且簽署知情同意書。按生大黃液的不同給藥途徑分為鼻胃管組和鼻空腸管組,每組19例。2組年齡、性別、BMI、急性生理與慢性健康(APACHE Ⅱ)評分、床旁急性胰腺炎嚴重度(BISAP)評分、全身炎癥反應綜合征(SIRS)評分等比較差異無統計學意義(P>0.05),具有可比性。見表1。
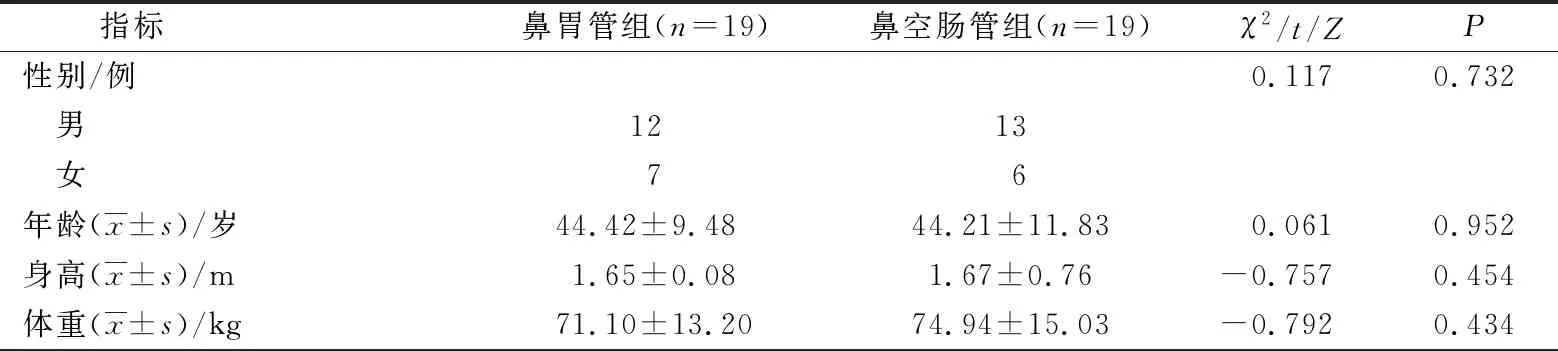
表1 2組基線資料比較
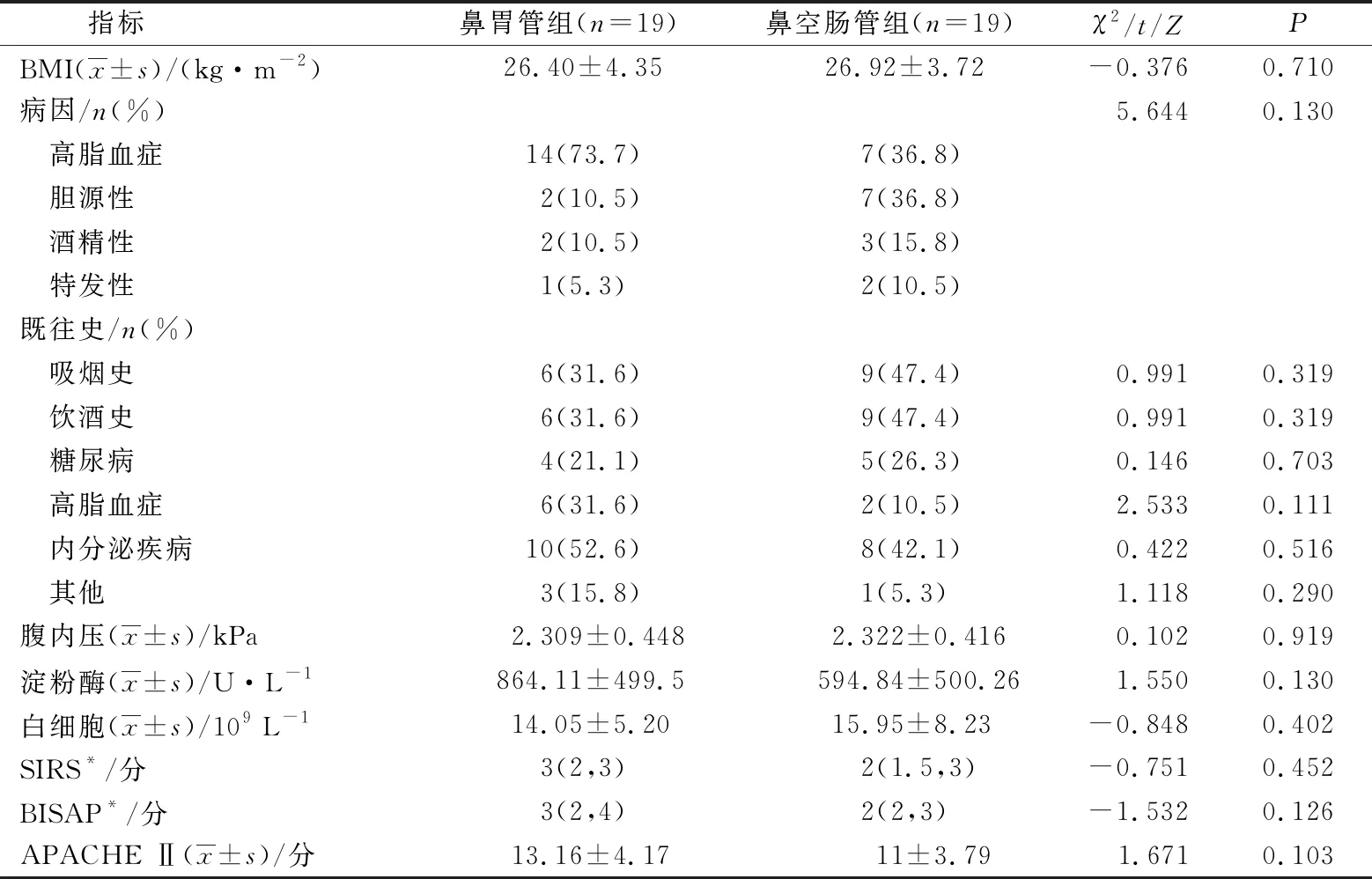
表1(續)
1.2 方法
1.2.1 常規治療
2組患者均予重癥監護、禁食禁飲、胃腸減壓、抑酸抑酶、擴容補液、抗休克、抗感染、糾正水電解質和酸堿平衡紊亂、全腹皮硝外敷、營養支持等綜合治療。
1.2.2 生大黃泡制
取生大黃片50 g加入120 mL開水浸泡10 min后去渣提取出生大黃液100 mL,待冷卻至37 ℃,備用。
1.2.3 生大黃液的使用
在常規治療的基礎上,2組入院當天注入生大黃液。鼻胃管組經胃管注入生大黃液,每天3次,每次100 mL。鼻空腸管組采用床邊盲插法將復爾凱螺旋鼻胃腸管置入105 cm以上,置管后行床邊腹部平片或腹部立位片確定導管尖端達空腸后,經空腸管注入生大黃液,每天3次,每次100 mL。
1.2.4 腹內壓測量
腹內壓測量采用膀胱內壓力間接測量法[7]。測量前排空膀胱,患者取平臥位,然后向膀胱內注入25 mL生理鹽水,通過醫用三通連接導尿管和測壓器,以腋中線為零點,校零后于呼吸末壓力為膀胱內壓力,每4 h測量1次,當日腹內壓取當日所有數值平均值,單位為kPa。
1.2.5 療效標準
治愈:各項癥狀完全消失,各臟器功能恢復正常。血清淀粉酶及脂肪酶恢復正常,無異常體征,假性囊腫等并發癥得到控制,CT或B超檢查胰腺完全恢復正常;好轉:急性胰腺炎癥狀消失,臟器功能部分恢復,但合并并發癥如腹腔炎癥、感染未完全恢復,假性囊腫未完全消失;無效:各項癥狀和臟器功能無改善甚至加重,各項指標均到不到好轉標準。
1.2.6 觀察指標
觀察用藥前及用藥后第3、5、7天腹內壓;第0、7天的APACHE Ⅱ評分、BISAP評分、SIRS評分、監護室住院時間、總住院時間、出院好轉、ACS發生率及病死率。
1.2.7 統計學方法
采用SPSS 25.0對數據進行處理。計數資料用率表示,采用χ2檢驗。計量資料如符合正態分布,以均數±標準差表示,2組組間比較采用t檢驗;2組不同時間點的比較采用兩因素重復測量方差分析。如不符合正態分布以中位數(M)和四分位距(P25,P75)表示,采用非參數檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 腹內壓的比較
2組隨著時間的變化對患者腹內壓值及腹內壓下降率的影響見表2。由表2可見,時間因素對腹內壓值及腹內壓下降率差異有統計學意義(P<0.05),腹內壓值組別×時間的交互作用差異無統計學意義(P>0.05);腹內壓下降率組別×時間的交互作用有統計學意義(P<0.05)。2組用藥后第0、3、5、7天腹內壓值的變化見表2。由表2可見,用藥后第0、7天2組間腹內壓值差異無統計學意義(P>0.05),用藥后第3、5天腹內壓值鼻空腸管組較鼻胃管組低(P<0.05);腹內壓下降率第0、3、5、7天鼻空腸管組腹內壓下降率較鼻胃管組高(P<0.05)。
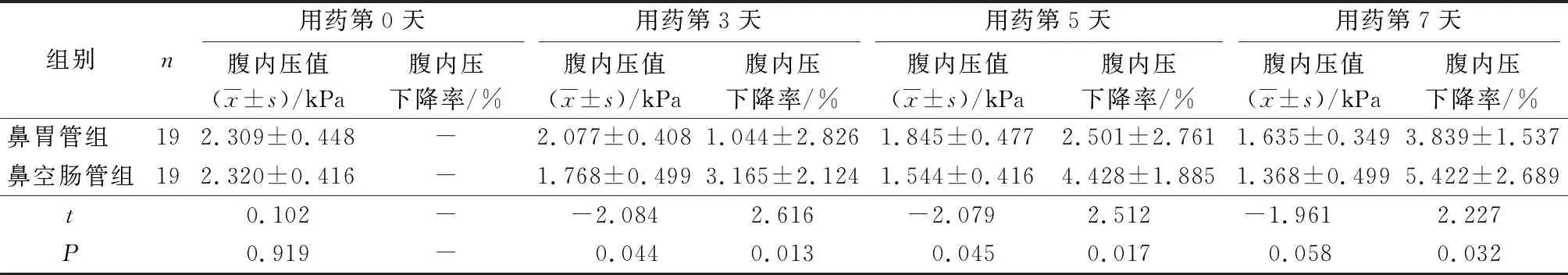
表2 2組患者不同時間點腹內壓值和腹內壓下降率的比較
腹內壓比較:F時間=35.855,P時間<0.001;F時間×組間=1.605,P時間×組間=0.196。腹內壓下降率比較:F時間=51.414,P時間<0.001;F時間×組間=2.800,P時間×組間=0.036。
2.2 APACHE Ⅱ、BISAP、SIRS評分比較
用藥第0天、7天時,2組APACHE Ⅱ、BISAP、SIRS評分比較,差異無統計學意義(P>0.05),見表3。
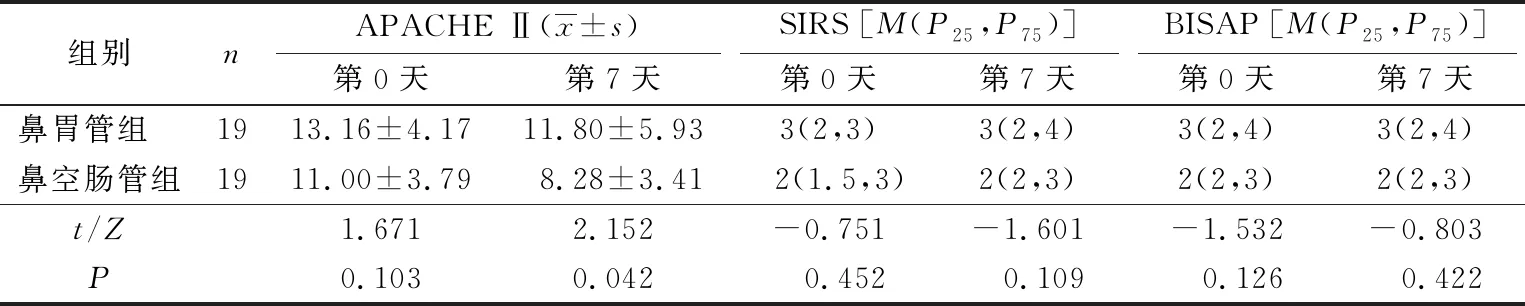
表3 2組APACHE Ⅱ、BISAP、SIRS評分比較 分
2.3 預后及住院時間比較
鼻空腸管組患者ACS發生率較鼻胃管低、監護室住院時間較鼻胃管組低,2組比較差異有統計學意義(P<0.05),但患者出院好轉、總住院時間及病死率比較差異無統計學意義(P>0.05),見表4。
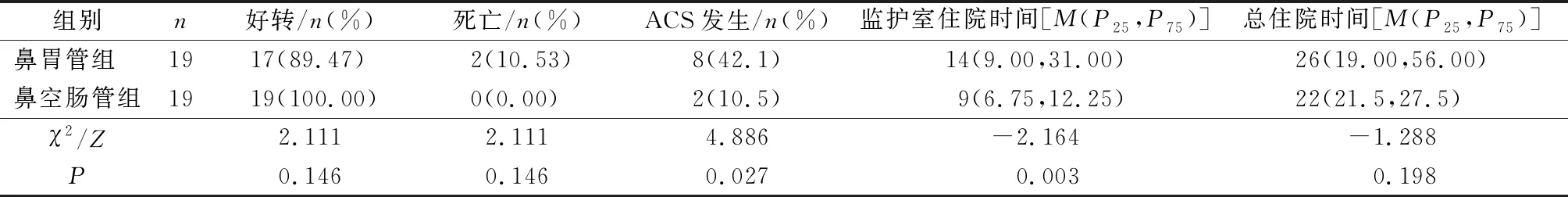
表4 2組預后及住院時間比較
3 討論
SAP因大量炎癥因子釋放入血,腸道黏膜屏障功能受損、通透性增加,菌群及內毒素移位,導致多器官功能障礙綜合征(MODS)或全身炎癥反應綜合征(SIRS)的發生[8],而腸道屏障功能減弱及菌群變化會加重急性胰腺炎病情[9]。因此,阻斷炎性反應,預防腸功能障礙,防止MODS的發生是治療SAP的重點[10]。
大黃具有瀉下通便、利膽的作用,在腸道屏障功能和結構的維持和修復中具有多靶點多層次聯合效應[11],可促進腸道黏膜修復,加快細菌、內毒素的外排,限制炎癥反應進一步擴散等作用,是SAP的重要治療手段之一。
本研究通過經空腸管與胃管不同途徑注入生大黃液用于SAP合并IAH患者,結果顯示空腸管組用藥第7天腹內壓下降率較胃管組更高,且第3天和第5天腹內壓值較胃管組低。其原因可能為經鼻空腸管注入生大黃液時,藥物可直接作用于腸道而發揮藥效,而經胃管注入時因SAP患者腸蠕動減弱,胃排空延遲,藥物在胃內潴留未及時排入腸道,從而延緩了藥物作用時間。同時因SAP合并IAH患者部分會出現嘔吐現象,且多數患者需行胃腸減壓,注入藥物未及時排空而被吸出或嘔出,從而導致進入腸道內的有效藥物劑量減少而影響藥物療效。
據研究[12-15]顯示,APACHE Ⅱ、BISAP、SIRS評分在評估急性胰腺炎患者的嚴重程度和判斷其預后具有一定的臨床指導意義。本研究結果顯示,用藥第7天2組APACHE Ⅱ、BISAP、SIRS評分無明顯差異,可能與觀察時間較短、自然病程有關。另外,較鼻胃管組,鼻空腸管組ACS發生率更低,監護室住院時間更短,其原因可能為鼻空腸管組藥物直接作用于腸道,早期促進腸蠕動,防止菌群移位和腸源性感染,保護腸黏膜屏障,恢復腸功能,預防ACS發生,減少監護室住院時間。但2組患者總住院時間和預后轉歸無差異,可能與治療時間延遲、患者自然病程轉歸和常規積極治療有關。
總之,在重癥急性胰腺炎伴腹內高壓患者中早期經鼻空腸管注入生大黃液較鼻胃管注入生大黃液對腹內壓降低影響更明顯,但該研究存在因樣本量少而導致統計結果存在一定偏差,其結果尚需更多更大樣本的臨床研究進一步驗證。

