《原子結構》第一課時課堂實錄
王麗
第一階段:引入。
教師:漂亮的彩虹、精彩的煙火,科學家通過探索原子的結構問題揭示了五顏六色的色彩秘密。正是因為電子在運動過程中有能量的變化,我們才看到了這些絢麗的色彩。在電子運動過程中產生的這些光線,我們稱之為光譜。我們在學習中還知道很多金屬元素在火焰上灼燒時,會顯示出具有它們特征的焰色。為什么每一種金屬會顯示出各自不同的焰色呢?除了金屬以外,其他元素是否也能產生類似的光譜呢?今天,我們就從最簡單的元素——氫元素的光譜開始了解光譜、了解電子運動的狀態。
第二階段:認識氫原子光譜,學習從宏觀現象推理微觀世界的一種方法。
(多媒體展示氫原子的光譜圖以及氫原子的微觀示意圖。)
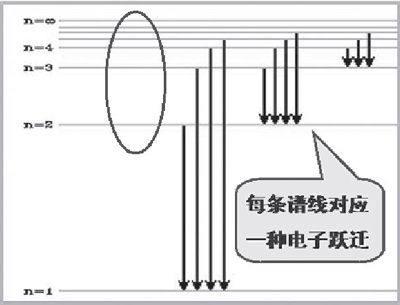
教師:在光譜圖中,我們可以看出它對應有四條譜線,這四條譜線說明氫原子核外電子在運動過程中會向外輻射能量。它的能量是從哪兒來的?是什么樣的過程輻射出能量?它的能量為什么又是以一條條一定波長的光來體現的?我們看一下模擬演示過程。
電子在它固定的軌道上運動的時候,是不會向外輻射能量的。請大家注意觀察:當我們給電子提供一定的能量時,電子就會跳到更高能量的電子層上,這一過程稱之為躍遷。圖示的躍遷過程中,電子吸收了能量,所以躍遷后能量升高了。可是,電子在高能量的狀態時不穩定,還會躍遷到低能量狀態。我們看到的譜線,就是電子在高能量狀態躍遷回低能量狀態時釋放出的能量。這個能量對應一定波長的光,所以一種躍遷就對應了一條譜線。那么,同學們可能又會產生一個疑問:氫原子核外只有一個電子,它為什么能產生多條譜線呢?而且我們截取的僅僅是氫原子在可見光區的譜線就有四條。請結合圖示分析原因。(提示:圖示中標示了n=1、n=2、n=3……,其中n代表什么?)
李磊:n代表電子層。
教師:每條譜線對應一種電子躍遷,此處標出的四種電子躍遷就對應上圖中的四條譜線。通過這個分析,你是否能看出它產生四條譜線的原因?
李磊:跳躍的電子層數不一樣,第一條是從第三層躍遷到第二層,第二條是從第四層躍遷到第二層,以此類推。
教師:雖然氫原子核外只有一個電子,但是被激發以后,不同的電子可以跳到不同的電子能層上,而不同電子能層的電子在往回躍遷的時候就輻射出了不同能量的光。科學家玻爾也正是依據以上實驗事實和分析,最早給出了原子核外電子是分層排布的說法。(出示:描述電子能量大小的主量子數n取值不同時,表示不同的能層,即電子層。)這就是我們要說的原子結構量子化模型的最初說法。
第三階段:應用科學思想,發揮思維能力和想象能力,深入學習。
教師:當了解了氫原子光譜以后,我們再選擇一種大家熟悉的鈉元素,大家發揮想象,鈉元素的光譜圖會是怎樣的?
學生想象一分鐘后,教師出示氫元素和鈉元素的光譜圖。
教師:觀察鈉元素光譜圖,與你想象的一樣嗎?
學生:不一樣(不太一樣)。
教師:現在大家對比兩種元素的光譜,看看有哪些異同,你有哪些疑問。
學生以小組為單位,相互討論。
教師:無論是疑問,還是你們討論的結果,都記錄在學案上。討論后,我們將以小組為單位匯報,要求每個組匯報的內容不同。
學生匯報:
1組:鈉的譜線比氫的譜線多,相同頻率對應位置有相同的譜線,鈉的譜線比較集中,而氫的譜線是單一的。
2組:同一顏色的譜線粗細不同。
3組:氫的空白處鈉卻有譜線,鈉比氫多了黃線。
……
教師:同學們發現的信息都是很有價值的:鈉譜線比氫譜線多了,鈉譜線中包含了氫譜線,在鈉的譜線中有波長非常接近的一組譜線挨著,但氫中都是一條譜線,還有的同學說鈉比氫多了黃線。接下來,請大家討論一下,為什么兩種元素的譜線會有這些差異?
學生以小組為單位討論,時間約2分鐘。
教師:這個環節我們稱為“猜想”環節。點到名字的同學說說你的猜想或看法,不怕說錯。
王宇航:在相同的區域中,鈉的光譜與氫的光譜顏色一樣。
教師:為什么會一樣?
王宇航及其他學生:鈉的光譜中包含了氫的光譜,是因為鈉的核外電子躍遷包含了與氫相似的電子躍遷。
姚易飛:鈉的核外電子多,所以它的電子躍遷有多種可能。
教師:電子多了,電子層多了嗎?躍遷的電子層多了嗎?
姚易飛:電子層多了,躍遷的電子層沒有變化。
教師:對,剛才我們看到氫原子核外雖然只有一個電子,但它可以從第六層或者第五層發生躍遷,鈉元素核外的電子也是在這些電子層間躍遷,但是電子多了,情況確實變得復雜了。
張藝丹:離核越遠能量越高,應該是與能量有關系吧。
教師:是的,躍遷過程就是吸收或釋放能量。不同的躍遷輻射出的光譜不同,現在電子多了,譜線復雜了,為什么會這樣?
張藝丹:電子多了,能量變化就多了。
曲一帆:能量變化的狀態多了,所以譜線多了。
……
教師:好的,通過本輪猜想,我們再次明確氫原子核外只有一個電子,但是它只有一個電子層嗎?
學生:不是!
教師:每個原子核外無論有幾個電子,它都有若干個電子層,電子層之間的差異就是能量不同。請大家思考:觀察鈉的光譜圖中的一組紅色譜線,它們的波長相近,能量略有差異,可是氫光譜中看到層與層之間躍遷的能量差異很大,于是我預測:對于氫原子,相鄰能層的躍遷只形成一條譜線,但是多電子原子在相鄰能層間的躍遷產生了多條譜線,那么在一層里又分出了多個小層,這些小層之間能量有差異,由于它們都處于同一電子層中,所以能量差異不大。當這些電子從這些小層躍遷到同一能層時,就形成了波長相差不多的多條譜線。我的預測合理嗎?
學生:合理。
教師:通過大量的實驗和計算,科學家也幫我證實了這種預測,即在一個能層中又分為若干層,并為它取名為角量子數,用l表示,當l不同時,再結合主量子數,表示為ns、np、nd等,s、p、d也稱為能級,它們之間也有能量差,但是能量差比層與層之間的能量差小多了。所以,描述一個電子在原子核外的能量狀態有了兩個量子數,分別是主量子數和角量子數。
第四階段:更多猜想,深化科學思維方法。
教師:有些科學家做了這樣一些光譜實驗:我們在同一能層中的s和p能級之間,如果電子從p能級向s能級躍遷的時候應該會產生一條譜線,但如果實驗是在外加磁場的環境中進行,發現一種躍遷居然出現了三條或多條譜線,根據這種現象,我沿用同學們和科學家給我的啟發,再次預測:能級還可以再分裂,但只在有外加磁場的時候能量變得不同。我查閱資料發現,科學家對此也早有說明,相同的能級在外加磁場的作用下能量會變得不同,用磁量子數,符號m,來描述這種差異。
教師:電子的運動狀態確實是非常復雜的問題,目前科學家建立的原子電子云模型中描述電子狀態的量子數有四個,除了我們已經認識的三個量子數以外,第四個是自旋量子數,請大家利用網絡資料繼續自主學習自旋量子。
借助一些實驗以及科學家給我們的啟發和經驗,我們初步建立了原子的量子力學模型。接下來大家可以利用網頁回顧今天的學習過程,也可以選擇你喜歡的其他欄目加以關注,或者查閱我們的若干猜想在科學家的研究中是否能夠找到依據。
第五階段:網絡學習了解更多原子結構的信息,并發表感想。
教師:請同學們說說看了什么欄目,有什么想法?
劉宇哲等:1.對科學實驗感覺到神奇;2.看玻爾原子模型,感嘆科學家的聰明和嚴謹;3.喜歡宇宙大爆炸等相關資料。
注:本課獲得“全國中小學信息技術創新與實踐活動”一等獎。
(作者單位:北京第十二中學)

