評析2014、2015年的“江南十校”兩道化學選擇題
榮娜娜
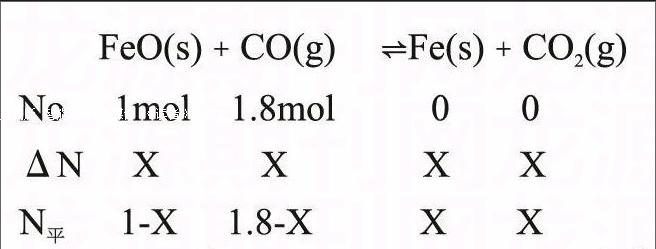
【內容摘要】針對2015年安徽省江南十校聯考化學選擇題10,本文分析認為這道題基本考查了影響化學平衡的因素,更重要的是這些因素在選項中的設置比較新型,體現了新課標的教學要求,也體現了江南十校考題一貫的風格 ——活。
【關鍵詞】江南十校 化學平衡 化學反應速率 轉化率 問題情境
2015年安徽省“江南十校”聯考選擇題10:已知t℃時,1L恒容密閉容器中發生如下反應:FeO(s)+CO(g)?Fe(s)+CO2(g),該反應的平衡常數K=0.5,下列說法正確的是( )
A.加入炭粉對該平衡無影響
B.將FeO(s)粉碎,不能縮短達平衡所需的時間
C.t℃時,反應達到平衡后再充入CO,達新平衡后n(CO):n(CO2)比值增大
D.若向該容器中加入1molFeO(s),并通入1.8molCO,t℃時反應達到平衡,此時FeO(s)轉化率為60%
一、命題意圖分析
該題考查影響化學平衡的因素:溫度、壓強、濃度、反應接觸面積等,轉化率的計算等等,命題思路清晰,問題情境的設置比較巧妙,體現了新課標的教學要求,是一道比較靈活的化學選擇題。因為有些知識點在選項中設置得比較巧妙,干擾性比較大,從而體現了江南十校的題目風格——活,也體現了高考理綜化學選擇題的趨勢:“穩”“變”“新”,問題情境設置越來越新穎。
二、試題解析
解這道題的關鍵是要熟悉影響化學平衡的因素:溫度、壓強、濃度、反應接觸面積、催化劑等。現分析如下:該反應為可逆反應,在某一條件下存在化學平衡,反應的特點是:(1)有固體參加;(2)等體積的反應。A選項中加入炭粉,乍一看炭粉不參加反應,又是固體,學生一旦思維定勢,認為對平衡似乎沒影響,就很容易誤選。可仔細分析來,炭粉是還原劑,會和CO2(g)反應。CO2(g)減少,CO(g)增加,會使平衡向正反應方向移動,故加入炭粉對該平衡有影響。B選項有同學認為將FeO(s)粉碎,FeO(s)是固體,對壓強沒影響。故不能縮短達到平衡所需要的時間。可FeO(s)是反應物,將其粉碎可以增大反應接觸面積,進而加快化學反應速率,可以縮短達到平衡所需要的時間。考查了反應物接觸面積對化學反應速率、化學平衡的影響。C溫度不變,達到平衡后K不變,又因為該反應為等體積的反應,1/K也是不變,即n(CO):n(CO2)比值不變。D選項通過三段式求法考查了學生的計算能力。
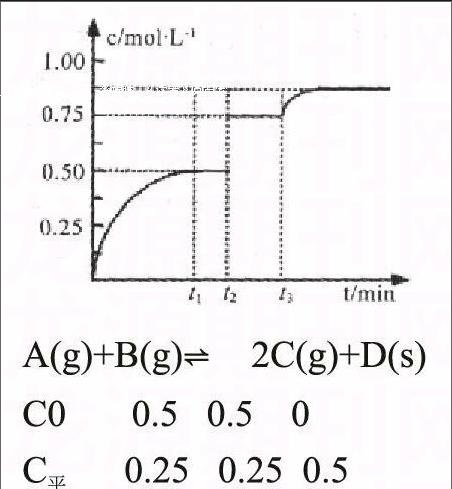
2014年安徽省江南十校聯考選擇題:一定溫度下,將1molA和1molB氣體充入2L恒容密閉容器,發生反應A(g)+B(g) ?xC(g)+D(s),t1時達到平衡。在t2、t3時刻分別改變反應的一個條件,測得容器中氣體C的濃度隨時間變化如圖所示。下列說法正確是( )
A.反應方程式中的x=l
B.t2時刻改變的條件是使用催化劑
C.t3時刻改變的條件是移去少量物質D
D.t1~t3間該反應的平衡常數均為4
現在做一下比較:二者考查的都是化學平衡,2014年結合c-t圖形分析改變化學平衡的條件,t1時刻該反應達到化學平衡,t2時刻改變反應條件,氣體C的濃度增大,但平衡沒發生移動,說明改變的條件不是催化劑,而是增大壓強。所以B選項錯。又因為平衡不移動,所以該反應是一個反應前后體積保持不變的反應。在這里應該特別注意的是反應物D的狀態是固體,故方程式中的C物質的系數x=2。所以A選項錯。t3時刻氣體C的濃度增大,因為D是固體,移去少量的D對化學平衡沒有影響,所以t3時刻改變的條件是通入氣體C。故選項C也是錯的。D選項t1時刻到t3時刻溫度沒有改變,所以K值不變。根據x=2和t1時刻的數據由三段式求得,由圖像可知,平衡時氣體C的濃度為0.5mol/L。
三、高考復習啟示
在第一輪復習時一定注重基礎知識梳理,幫助學生構建知識框架,做到知識的整理歸納和融會貫通,培養學生分析問題和解決問題的能力,強調解題規范性,加強計算能力的培養。在講題目過程中注意解題思路和解題方法的培養,建議同學們在理清知識框架的基礎上細化知識點,強化主干知識,在做題中查漏補缺及時修正知識框架,做到點面結合。指導學生熟悉當今有關化學發展前沿的熱點話題,應對以“化學、社會、生活及邊緣交叉學科”為情景的試題,建議學生注意總結萬能答題術語,有關實驗操作的語言描述,不斷強化考試基本技能和方法,以不變應萬變,即以“穩”來應對“變”和“新”。
【參考文獻】
[1] 劉孝元. 2013年全國新課標理綜卷Ⅰ化學試題“穩”“變”“新”[J]. 中學化學教學參考,2013(7):54-56.
(作者單位:安徽省界首中學)

