脛骨高位截骨術治療膝內翻骨關節炎的研究進展
張杭,何森
近年來,脛骨高位截骨術(High tibial osteotomy,HTO)已廣泛用于治療有癥狀的膝內翻骨關節炎患者。1958年Jackson 等報道了HTO 作為治療內翻膝關節單間室骨關節炎的一種選擇,后經過Coventry等人的不斷努力,使用HTO治療因下肢力線不良引起的關節炎的觀念逐漸深入人心。HTO的治療原理是通過截骨矯形把下肢力線從發生炎癥和磨損的膝關節內側間室轉移到相對正常的外側間室,以減輕內側間室負荷、使已磨損的軟骨和受損傷的半月板有條件得以自我修復,進而達到緩解疼痛、延緩膝關節置換時間以及恢復患者高水平的活動[1]。HTO的手術方式包括內側開放楔形截骨術(Medial opening wedge high tibial osteotomy,MOWHTO)、外側閉合楔形截骨術(Lateral closing wedge high tibial osteotomy,LCWHTO)以及圓頂弧形截骨術。研究表明HTO 具有理想的短期和中期療效,但同時具有一定的局限性[2];常見并發癥包括神經血管損傷、筋膜間室綜合征、脛骨外側皮質斷裂、延遲愈合或不愈合、矯正不足、過度矯正或畸形復發等。同當前的單髁關節置換(Unicompartmental knee arthroplasty,UKA)和全膝關節置換(Total knee arthroplasty,TKA)相比,HTO的病例選擇更加嚴格。HTO獲得成功的關鍵首先是嚴格地選擇患者、全面的病史和體格檢查、精確的術前計劃,同時需要有熟練的手術技術作為保障。
1 HTO的適應證和禁忌證
HTO 的適應證包括:年齡<65歲(女性<60歲);膝關節活動度基本正常;屈曲畸形<10°;脛骨內翻畸形>5°;內側脛骨近端角(Medial proximal tibial angle,MPTA)<85°;外側軟骨和半月板功能正常[3]。該手術的其他適應證包括:在關節保留手術中使用HTO,以減輕軟骨修復部位負荷,即微骨折、軟骨細胞移植(Autologous chondrocyte implantation,ACI),骨軟骨自體移植或同種異體移植,并通過改變矢狀面斜度解決交叉韌帶功能不全的問題。
HTO 的禁忌證包括:內側間室嚴重骨關節炎(Osteoarthritis,OA)(Ahlback Ⅲ級或更高)、重度髕股關節或外側間室關節炎、三間室關節炎、炎癥性關節炎(如類風濕性關節炎)、年齡>65歲和運動受限(膝關節活動度<120°,屈曲攣縮>5°)的顯著癥狀性軟骨損傷、大面積脛骨和股骨關節面裸露(>15 mm×15 mm)以及長期吸煙者[4]。年齡方面禁忌證并非絕對,如果患者年齡>65歲應綜合評估其膝關節炎程度以及功能障礙程度。
Hinterwimmer[4]及Bonasia 等[5]認為術前脛骨內翻角(Tibial bone varus angle,TBVA)>5°(圖1)、術后脛股關節線傾斜度接近0°、術后5 周外翻≥8°、年齡<50歲、術前膝關節評分良好、內側關節炎(Ahlback 0級)均是預后良好因素。
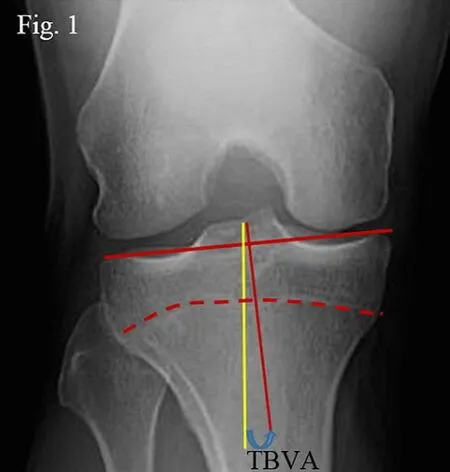
Fig.1 Standard anteroposterior view of knee joint圖1 膝關節正位像
2 病史及體格檢查
術前應詳細地評估患者既往史和現病史。既往史包括是否有膝關節創傷性損傷和內側關節炎隱襲發作病史,是否合并術區切口瘢痕狀態。現病史包括評估患者當前的活動水平、期望值和身體健康狀況,充分考慮疼痛的位置和特點;任何懷疑患有膝關節內翻的患者均應進行雙下肢負重X線片來客觀評估冠狀位力線;術者應檢查同側的髖關節功能是否良好,如髖關節合并病變需行手術治療,為消除髖關節疾病引起的膝關節反射性疼痛,髖關節手術應先于HTO。
通過步態分析可以測量行走過程中膝關節受力的分布,內收力矩的峰值預示著內側間室承受負荷的大小。Lee 等[6]認為下肢檢查應先確認是否存在下肢力線不良,并對側向負荷作出評價、分析術前步態內收力矩。如患者存在高內收力矩,即在步態周期中存在明顯的側向負荷,則預示術后效果較差,這些患者應過度矯正下肢力線。術者根據患者行走時的內收力矩情況來決定術中矯正的程度,還可以幫助患者術后進行步態訓練。
術前的影像學檢查是進行精確術前計劃的基礎,包括雙下肢負重全長X線片、膝關節負重正側位X線片、髕骨軸位X線片、屈膝30°Tunnel位X線片和屈膝45°Rosenburg位X線片。內側間室關節炎的嚴重程度和磨損情況可以通過正側位X線片評估,髕骨高度可以在側位片測量Insall-Salvati、Blackbume-Peel 或Caton-Desehamps 指數進行評估[7],而雙下肢負重全長X線片可以評估下肢力線和肢體長度。磁共振成像(MRI)可以評估軟組織病理學,如韌帶損傷、半月板撕裂、骨軟骨缺損或軟骨下骨水腫。
3 術前計劃
術者在下肢全長像上測量機械軸(從股骨頭中心至踝關節中心的線)、解剖軸(從梨狀窩至膝關節中心的線和穿過脛骨長軸的線)和負重軸線(從股骨頭中心至踝關節中心的線),確定矯正截骨的位置、方向和嚴重程度,但是應注意軟組織的張力、關節線的傾斜以及上肢軀干的偏移均會影響運動中股脛關節面的應力分布。測量冠狀面上的畸形程度有助于明確截骨的位置并判斷是否需要使用特殊器械。
根據承重軸線測量法,將脛骨平臺由內到外從0~100%進行等分以確定機械軸與膝關節相交的適宜位點,股骨頭中心和距骨頂中心與此點連線的夾角即截骨所需矯正的角度[8]。在計算截骨角度時應特別注意關節內骨缺損的問題。對于由側副韌帶松弛引起的成角畸形和股脛關節分離的距離應在截骨時減去,每毫米減1°,防止過度矯正。當內側副韌帶松弛合并內側間室過度負重時,在X 線片上難以發現,一旦術后負重移向對側間室會出現下肢力線矯枉過正。有些脛骨近端內翻畸形的患者可能同時合并有股骨遠端關節面外翻畸形,股骨遠端關節面傾斜會影響截骨矯形的角度。MOWHTO 的合頁頂點位于脛骨近端干骺端外側皮質上脛腓關節近側緣水平,大約在外側平臺軟骨下硬化區下方1.5 cm左右。術者將患肢的機械軸調整到膝關節脛骨平臺外側62%~66%的區域,通過截骨的角度來確定最終的截骨量。如HTO術后力線通過最佳區域,軟骨破壞則不再進展。Dugdale 等[8]認為截骨術后力線通過冠狀面上脛骨平臺外側62%~66%的區域即Fujisawa點(圖2),該點通常對應脛骨平臺外側嵴的外側斜坡以及3°~5°的股骨脛骨機械外翻角。
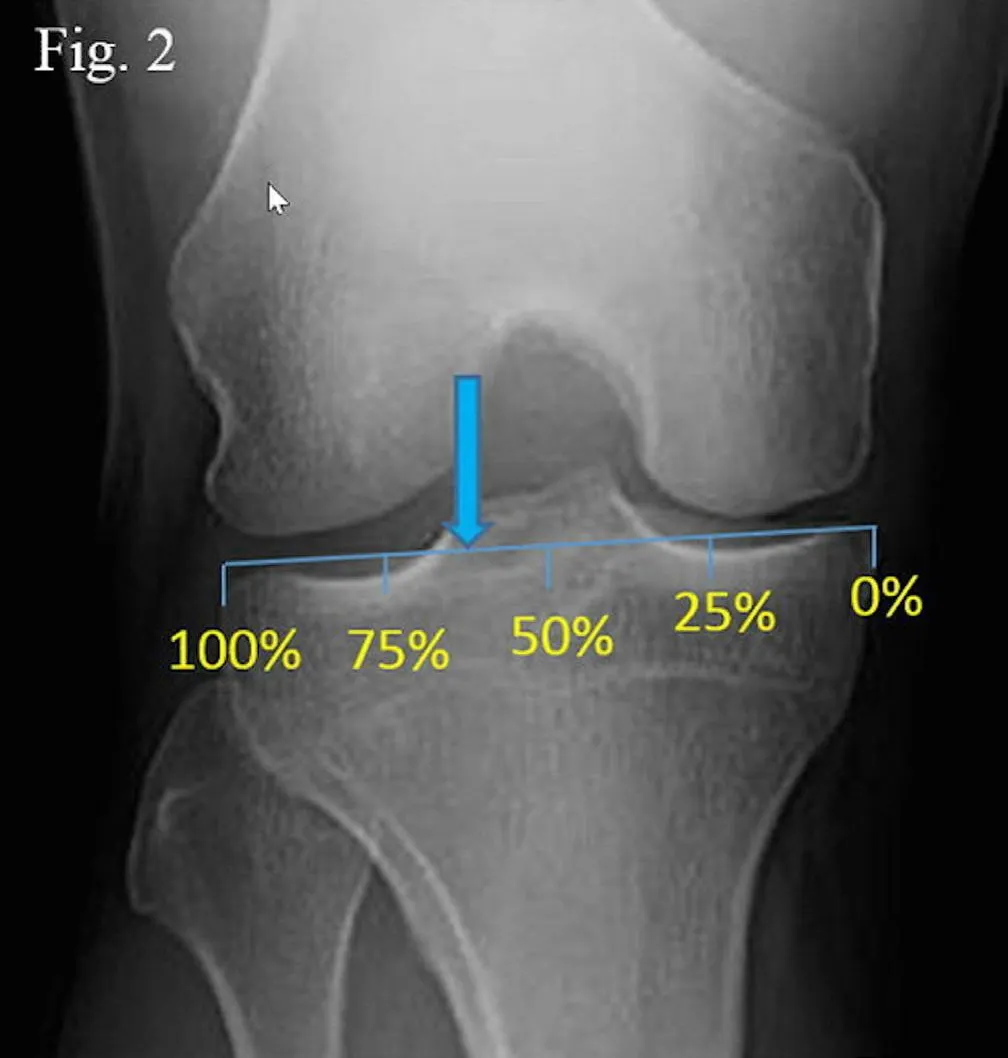
Fig.2 Standard anteroposterior view of knee joint圖2 膝關節正位像
4 手術技術
4.1 外側閉合楔形截骨術 Coventry 在上世紀60年代幫助推廣了LCWHTO[9],其優點是矯正的程度大、初始穩定性較好、允許立即承重、較低的畸形愈合和不愈合率、脛骨后傾角度(Posterior tibial angle,PTA)增加和發生髕骨低位的風險較低[9]。缺點是LCWHTO 需要同時進行腓骨截骨或上脛腓關節分離、截骨后解剖結構的改變,如矯形角度大時可能使得以后的TKA 變得復雜,另外發生腓總神經損傷的風險較高(發生率為3.3%~11.9%)。
手術采用沿脛骨結節外側邊緣的垂直線和平行于膝關節遠側1 cm的水平線形成倒置的前外側“L”形切口。術者將腓總神經自近端腓骨莖突至遠端2~2.5 cm 處解剖,穿過腓骨頸并保護。LCWHTO 需要首先解決腓骨的限制。通常采用的方法有3 種,包括內側1/3腓骨頭切除、游離上脛腓關節和腓骨遠端10 cm腓骨干截骨。術者截骨最好自關節線下方15 mm 脛骨結節上方處開始,從脛骨近端骨膜下剝離脛前肌顯露脛骨上端。如截骨線距關節面較近可能導致脛骨平臺骨折。術者行LCWHTO 時截骨方向應指向脛骨內側并且需要平行于膝關節線,同時保持脛骨內側皮質和骨膜作為鉸鏈。Rossi 等[10]建議去除比術前計劃小2~3 mm的楔形骨塊,以避免因近端與遠端骨節段重疊而導致過度矯正。
4.2 內側開放楔形截骨術 近年來,由于鋼板材料和固定技術的創新,骨移植物選擇更廣泛以及手術易于暴露操作,MOWHTO變得更為流行。對于膝關節單間室關節炎,通過MOWHTO能很好地矯正下肢不良力線[11]。優點是能夠校正兩個平面(冠狀和矢狀)的力線、不需要行腓骨截骨、不損傷脛腓骨關節面、腓總神經損傷的風險小、沒有縮短下肢、單個切口而不需要分離肌肉、沒有骨缺損、更容易轉換為TKA,并且手術過程中能夠調整矯正角度。缺點是可能需要植骨、有延遲愈合或骨不連的風險,以及MOWHTO之后內側側副韌帶變得稍微緊張。此外,還可能出現PTA 增加、髕骨高度(Tibial height,PH)降低和髕股關節腔壓力增高的情況。McNamara等[12]提出,為了避免髕骨低位、髕股關節間室壓力增加以及未來TKA 復雜化,如需要超過12.5 mm 的矯正,宜同時進行脛骨結節截骨術。髕骨低位的病因可歸因于PTA 的變化和隨后的脛骨平移,表現為髕韌帶的相對縮短或脛股關節線相對于靜態髕骨位置的增高。Han 等[13]研究了18例新鮮冷凍人尸體膝關節,發現一個可以避免脛骨外側皮質斷裂的安全區域,該區域位于腓骨頭頂端至腓骨頭圓周線之間。因此截骨時必須注意保留脛骨外側皮質作為鉸鏈,同時切開內側和后內側皮質的2/3,使用薄骨鑿逐漸打開截骨處,最后使用校準的骨鑿實現所需的矯正。
PTA 過度增加會導致冠狀面矯正失敗,為了使PTA和PH保持在正常范圍內,術中可通過調整骨鑿的楔入方向來控制,避免醫源性PTA 增加。Reising等[14]認為導航系統的使用不能提高內翻性OA 患者MOWHTO 的精確度,但其有助于避免矯正過度或不足。
4.3 圓頂弧形截骨術 當所需的矯正角度超過20°時,可能需要圓頂弧形截骨。通常在脛骨結節水平附近進行倒“U”形截骨。優點是保持了髕骨的高度、允許脛骨結節向前平移、減小了髕股關節的壓力,即使截骨角度大時也不會增加關節面的傾斜。理論上,圓頂弧形截骨的力線矯正角度是不受限的,而LCWHTO的矯正角度則受到骨量的限制。此外,該術式在矯正力線的同時增加了內側副韌帶的張力,且保持脛骨結節與關節面之間的相對關系不變。其主要缺點是一部分患者難以接受需要使用外固定架,而且經皮克氏針可能會損傷腓總神經或其分支。Chiang等[15]認為圓頂弧形截骨術雖然可以避免髕骨低位,但將來行TKA 翻修術會增加術中困難以及術后感染率。
5 固定方法
5.1 Puddu 鋼板及TomoFix 鋼板 帶間隙墊塊的固定鋼板,即Puddu板和Aescula 板是小而薄型的植入物,軟組織損傷較小并且固定方便。然而,這些鋼板剛性大、生物力學強度差、不能提供足夠的穩定性、促進成骨作用差且截骨間隙較大需植骨。采用Puddu 鋼板和Aescula 鋼板固定可能會出現延遲愈合、骨不愈合、固定不良和PTA 增加,術后需要較長時間(至少6周)持續非負重[16]。
鎖定加壓截骨板固定器,即TomoFix 鋼板是基于鎖定加壓板(LCP)的概念,具有牢固固定的優點,允許患者術后早期膝關節功能鍛煉,維持了髕股關節正常的生物力學環境。8個鎖定螺栓是用于剛性固定的所需最小數量的螺釘,其中4 個位于截骨位置近端,另4 個位于截骨位置的遠端。術者首先固定近端骨段,然后將拉力螺釘插入截骨處下方的第一個遠側孔中,通過側向鉸鏈處加壓來增加固定穩定性。在剩下的3個螺栓中插入單皮質螺釘。鑒于TomoFix鎖定鋼板的原理,不需要鋼板與脛骨完全貼敷、不需要彎板,簡化了手術操作步驟。其近排螺釘位于Gerdy 結節水平,離關節面較遠,這樣避免了螺釘穿入關節,同時保留了髂脛束等關節囊周圍軟組織的完整性。
TomoFix 鋼板在固定牢固性和允許早期負重方面優于帶間隙墊塊的固定鋼板。Kim 等[17]研究了Puddu鋼板和TomoFix鋼板的構造剛度和固定強度,發現兩者均能夠在超過2 500 N的載荷下保持矯正,并且均能提供足夠的穩定性,以便在單肢姿勢或行走期間保持成人膝關節的軸向壓縮負荷;然而,當脛骨外側皮質骨折時,TomoFix鋼板在抗壓縮和抗扭轉方面較Puddu鋼板具有更好的穩定性。
5.2 HTO 后植骨與骨愈合 LCWHTO 由于截骨處去除楔形骨塊后截骨兩斷端閉合,無骨缺損、不需要植骨以及骨不愈合率低(約0~5.7%)。MOWHTO由于內側截骨撐開后存在楔形骨缺損,并且隨著撐開角度越大、骨缺損容積越大,潛在不愈合可能性增高。目前對于截骨區域是否需要植骨存在爭議。El-Assal 等[18]認為盡管常規植骨作為MOWHTO 手術的一部分,但即使截骨間隙達到14 mm 也無需植骨,這樣可縮短手術時間并避免植骨引發的并發癥。Siboni 等[19]認為肥胖和脛骨初始外側皮質骨折是MOWHTO不穩定和矯正角度過大的危險因素,因此建議在矯正角度>10°的情況下,可以考慮進行自體骨或骨替代物移植。而Türkmen等[20]研究中發現26例膝關節截骨間隙為10~12.5 mm和8例膝關節截骨間隙為>12.5 mm 術后均愈合良好,認為骨愈合過程需要理想的生物和機械穩定環境,在保證精確截骨矯正畸形以及固定強度足夠的前提下,術中不植骨也可取得滿意預后。綜上所述,筆者建議術中矯形撐開角度較大時,為避免骨不愈合需要植骨;MOWHTO截骨處在有堅強內固定的情況下,可以采取植骨或者不植骨。但是以下情況需要考慮植骨:矯正內翻畸形過大(超過12°)或撐開距離過大(超過14 mm);存在“合頁”處骨折,特別是TakeuchiⅡ型骨折[根據骨折與近端脛腓關節(Promximal tibial fibular joint,PTFJ)的相互關系,將骨折分為三種類型:Ⅰ型為穩定型,Ⅱ、Ⅲ型為不穩定型];某些高危人群如合并肥胖、吸煙、高齡以及其他一些影響骨愈合的情況。
5.3 HTO 與植骨相關填充物 良好的骨移植填充材料從生物學活性和結構上可分為以下幾種:自體髂骨、新鮮冷凍或冷凍干燥同種異體骨、脫鈣骨、人工骨材料。人工骨材料包括珊瑚狀的羥基磷灰石(HAP)、磷酸三鈣(β-TCP)等。許多術者喜歡用自體髂骨或骨替代物填充截骨間隙以增強關節穩定性并加速其愈合。
自體髂骨骨移植被認為是存在骨不連風險的吸煙和肥胖患者的良好選擇。與同種異體骨和其他骨替代物如磷酸鈣陶瓷間隔物相比,自體髂骨的臨床結果良好、并發癥少;由于其良好的骨傳導性、骨誘導性和成骨性等優點,自體髂骨被認為是最成功的骨填充材料。然而,取髂骨會增加包括取骨區疼痛、周圍皮膚感覺異常、切口感染、骨折、增加手術創傷、增加手術時間和術中出血量等風險[21]。
同種異體骨移植材料具有骨組織的完整性結構、機械穩定性、生物學活性、骨誘導能力和低免疫性以及與宿主骨有較強的愈合能力等優點,由于其隨時可用性、取材方便而無需額外的手術切口,可以避免發生自體髂骨潛在的并發癥。缺點是具有感染病毒的風險。
脫鈣骨易于匹配骨缺損處形狀和大小,具有良好骨傳導和骨誘導的特性,但是缺乏骨支撐作用。HAP、β-TCP 等人工骨具有促進成骨特性同時又有一定的機械支撐能力、生物相容性好、可降解等特性,是較為理想的植骨材料,但有軟組織刺激和感染等缺點。Saragaglia 等[22]在MOWHTO 中應用β-TCP植骨和鋼板固定結果發現截骨處骨愈合良好,與自體髂骨植骨相比更有優勢,無并發癥、組織相容性好,便于截骨失敗后行TKA,長期隨訪優良率為74%。Rolvien 等[23]研究認為β-TCP 可以作為自體髂骨移植物的替代材料,在治療脛骨平臺凹陷性骨折方面有效、安全、具有良好的骨傳導性;組織學分析表明在β-TCP移植物周圍有新骨長入,但未觀察到β-TCP的完全再吸收。
6 并發癥
全面的病史和體格檢查、精確的患者選擇和術前計劃、使用適當的固定技術和康復治療方案有助于獲得長期的良好結果。據報道,HTO 的并發癥發生率在7%~55%[24],9%的MOWHTO 最終需要行翻修術。與任何手術一樣,均有學習曲線,術者豐富的手術經驗可以降低并發癥發生率,幾年內并發癥發生率從15%降至8%[25]。MOWHTO并發癥包括脛骨外側平臺骨折、內側副韌帶損傷、鋼板斷裂、鋼板刺激(發生率高達40%)、矯正角度丟失和骨不連;而LCWHTO 的并發癥包括腓總神經損傷、腓骨截骨處骨不連、內側脛骨皮質骨折和筋膜間室綜合征。
外側皮質斷裂被認為是MOWHTO 固定失敗的重要危險因素,特別是TakeuchiⅡ型、Ⅲ型(不穩定型)骨折可導致矯正角度的丟失、截骨處延遲愈合。由于MOWHTO 操作的失誤導致在撐開的過程中外側鉸鏈骨折,造成Ⅰ型骨折的原因是截骨線過深;導致Ⅱ型骨折的原因是截骨線過低;導致Ⅲ型骨折的原因是截骨深度不夠。Nakamura 等[26]認為安全鉸鏈位置基本位于上脛腓聯合的中間部位,此部位的骨質結構和周圍軟組織的附著決定了該部位較其他部位有較好的穩定性,不容易發生截骨過程中的骨折,避免截骨矯正角度的丟失和截骨失敗的發生。
PTA 對于維持膝關節穩定性、屈伸活動度及半月板等均有重要影響,PTA 的改變會引起膝關節穩定性和屈曲活動度改變。MOWHTO 會增大PTA、LCWHTO 會減小PTA,過度的后傾對HTO 的長期效果有害,特別是當前交叉韌帶功能不全時可能會造成脛骨向前半脫位,并且會使以后轉換TKA 時手術困難[27]。趙允等[27]研究發現,MOWHTO 聯合調整PTA治療屈曲受限型膝內翻OA,可有效改善膝關節屈曲角度,獲得良好早期療效。
HTO 對髕骨的影響是多方面的,會改變髕骨的高度、Q 角和脛骨結節的位置。由于HTO 手術方式的不同,髕骨的高度變化也不同。理論上弧形截骨和脛骨結節下截骨對脛骨結節的位置沒有影響,MOWHTO 會使脛骨結節下移,而LCWHTO 會使脛骨結節上移,此外髕韌帶的長短也會由于瘢痕形成和制動等因素發生變化。
7 HTO的生存率
良好的長期結果與正確的患者選擇、手術技術、堅強的固定及術后密切康復指導有關。已發現LCWHTO的5年生存率為95%,15年生存率為60%。MOWHTO的10年生存率優于LCWHTO[28]。好的臨床結果與一些術后因素有關,包括無屈曲攣縮、外翻解剖角度為10°以及可能伴隨的髕股關節減壓手術。Coventry 等[9]認為如果HTO 能達到至少8°外翻的過度矯正,則75%的患者行TKA 可以延遲10年。Khoshbin 等[3]對2 671例在轉換為TKA 之前接受過HTO 的患者進行了研究,發現某些因素降低了HTO生存率,包括高齡、女性、韌帶損傷和既往有半月板切除病史,該研究發現HTO 的10年生存率平均為67%。
8 HTO術后臨床療效比較
8.1 MOWHTO 與LCWHTO 總體而言,MOWHTO和LCWHTO 治療內翻畸形的臨床結果相似[28-29]。Duivenvoorden等[28]對412例荷蘭患者的長期隨訪結果顯示,MOWHTO 的10年生存率優于LCWHTO(90%vs.75%),但MOWHTO 并發癥發生率更高(包括鋼板拆除率71%),而LCWHTO 為48%;LCWHTO組腓總神經感覺麻痹率為4%;MOWHTO 組髂嵴取骨區持續疼痛發生率為9.8%。在一項隨訪6年的隨機對照試驗中,Duivenvoorden 等[29]研究未發現MOWHTO 與LCWHTO 患者在臨床結果和放射學評分方面存在顯著差異,但發現MOWHTO 容易導致PTA 增加、矯正過度和髕骨低位風險升高,而LCWHTO轉換為TKA的翻修率較高。
雖然這兩種技術均有良好的矯正準確性,但同樣存在對畸形的矯正不足問題。Nerhus等[30]的一項對比研究發現,即使規范的MOWHTO也能使PTA增加1°,而LCWHTO 將其減少了2.5°;在該研究中,MOWHTO 的下肢長度平均增加了3.1 mm,而LCWHTO的平均長度減少了5.7 mm。
8.2 HTO 與UKA 一些研究已經證實,UKA 和HTO的臨床結果具有可比性:兩者的10年生存率沒有差異,兩種手術之間的顯著差異是HTO可能適用于具有高運動要求的患者。此外,HTO 術后恢復的確要考慮到骨愈合時間,通常在術后幾周內膝關節更加疼痛。一般認為,高齡、運動功能要求較低、膝關節屈伸功能良好以及下肢力線不良能夠預期矯正的患者傾向于行UKA;而對于年輕、膝關節穩定性良好、運動功能要求較高、膝關節屈伸功能良好以及髕股關節及外側間室關節軟骨無明顯退變的患者傾向于行HTO;對于年齡55~65歲、膝關節內翻<10°、膝關節屈伸功能良好、髕股關節及外側間室關節軟骨正常或輕度退變的非肥胖患者,UKA或HTO均適合。根據患者的年齡、體質量指數、OA 等級和患者活動水平,仔細考慮每位患者的治療方案。Cao等[31]的一項薈萃分析共納入了10 項研究,發現與HTO 患者相比,UKA 患者的翻修率更低、并發癥更少、術后疼痛更少,然而HTO 患者獲得了更多的膝關節活動度,在膝關節功能評分和手術結果之間沒有觀察到顯著差異,認為UKA 為OA 提供了安全有效的替代方案。Smith 等[32]從基于年齡分層-成本效益方面將UKA與HTO比較得出,HTO在年齡<60歲的患者可能是最具成本效益的選擇,而UKA在60歲及以上的患者中更好。
8.3 HTO 及隨后的TKA 任何HTO 手術方式都會改變膝關節區域的基本解剖結構,從而可能使隨后的TKA 手術時間和手術操作步驟增加,出現術后膝關節僵硬并發癥[33]。然而,在中長期隨訪中,初次TKA 與HTO 之后行TKA 翻修術的臨床結果沒有明顯差異。Han 等[33]系統評價表明,MOWHTO 和LCWHTO后行TKA的臨床結果相似,包括翻修率在內的臨床和放射學評分結果未顯示出統計學差異;然而,LCWHTO 后行TKA 翻修較MOWHTO 組有更多的手術技術問題,包括股四頭肌重建、側方韌帶組織松解和脛骨結節截骨的發生率更高。Niinim?ki等[34]分析了一項基于注冊的1 036例HTO后行TKA的病例對照研究,研究者在Kaplan-Meier 分析中發現,HTO后行TKA患者5年生存率為95.3%、10年為91.8%、15年為88.4%;低于未接受HTO 治療的TKA患者(分別為97.2%、94.5%和90.6%)。盡管HTO后行TKA 患者翻修率略高,但是與初次TKA 相比,前者的臨床效果滿意。
總之,HTO的適應人群為年輕、具有高運動強度要求、術前膝關節屈伸功能及穩定性好、且內側間室OA 程度較輕(Ahlback 0~Ⅱ級)的患者。排除病例選擇的因素,術前膝關節狀況、術后力線角度矯正的準確程度是術后最終療效的決定因素。術前設計依靠標準的X 線片和步態分析,未來可以借助計算機輔助導航促使HTO 力線角度矯正更加準確。選擇合適的術式、使用堅強的內固定和術后早期功能鍛煉有助于獲得良好的長期結果,從而達到緩解疼痛、改善功能、延緩TKA,滿足患者高水平活動需求的目的。

