MHD患者LDL-C/HDL-C與頸動脈粥樣硬化程度的關系
楊亞寧,溫紅梅,曹啟環,楊亞慧,郭晨旭
維持性血液透析(MHD)為慢性腎衰竭(CRF)的主要治療方法,而心血管系統疾病屬于MHD患者主要伴隨疾病,且為其首位死亡原因[1]。目前認為,脂質代謝異常為動脈粥樣硬化及心腦血管疾病的主要誘因,有報道低密度脂蛋白膽固醇(LDL-C)/高密度脂蛋白膽固醇(HDL-C)比值與冠心病存在緊密聯系[2-3]。本研究以152例MHD患者為研究對象,探討其LDL-C/HDL-C比值變化,并分析其與頸動脈狹窄程度的關系。
1 對象與方法
1.1 研究對象 選取醫院2017年2月~2018年3月收治的152例行MHD治療的原發性慢性腎衰竭患者,納入標準:(1)CRF患者,接受規范性MHD治療,且 MHD 時間>6 個月;(2)年齡>18 歲;(3)臨床診治資料完整;(4)治療前1個月內未服用降脂藥物;(5)簽署研究知情同意書,并得到醫院倫理委員會批準。排除標準:(1)長期使用降脂藥;(2)有高脂血癥家族史;(3)伴隨感染、腫瘤、心力衰竭等疾病;(4)有心腦血管病史;(5)合并肝功能障礙。其中男80 例,女 72 例,年齡 18~77(54.63±6.75)歲。 另選擇同期在醫院體檢的152例體檢健康者為A組,其中男 84 例,女 68 例,年齡 18~75(55.08±6.79)歲。
1.2 檢測指標
1.2.1 頸動脈超聲 研究對照入選后,采用西門子SEQUOIA 512B彩超診斷儀,探頭置于患者頸根部,對頸總動脈主干進行縱向掃查,再逐漸上移,仔細觀察內膜面光滑情況、有無斑塊存在,直至頸總動脈膨大(頸動脈分叉)處,并于距此處10 mm部位,測量頸總動脈血管內皮厚度及血流速度;然后上移探頭,對患者頸總動脈膨大部位與距頸膨大10 mm部位的頸內動脈,采取同樣方法檢測血管內皮厚度與血流速度;然后患者頭偏另一側,采用同法檢測對側,記錄最大內膜-中膜厚度(IMT)。按照頸動脈超聲結果,將患者分為硬化組與非硬化組。頸動脈粥樣硬化判斷標準:超聲顯示頸動脈有增厚、狹窄、斑塊等。并依據頸動脈狹窄程度,將硬化組患者再分為輕度組、中度組與重度組。狹窄程度判定標準:輕度:IMT<1.0 mm;中度:1.0 mm≤IMT≤1.2 mm;重度:頸動脈粥樣硬化斑塊呈局部隆起增厚,同時向管腔內突出>1.2 mm。
1.2.2 血生化指標 于空腹12 h后MHD前,抽取患者腹靜脈血3 ml,以羅氏COBAS INTEGRA 800全自動生化分析儀進行常規生化指標檢查,包括甘油三脂(TG)、總膽固醇(TC)、血清肌酐(Scr)、尿素氮(BUN)、LDL-C、HDL-C、載脂蛋白 A1(ApoA1)、載脂蛋白B(ApoB);計算LDL-C/HDL-C比值。
1.3 方法 收集研究對象一般資料[包括性別、年齡、體質量指數(BMI)、每周透析時間、透析齡、原發病等]、頸動脈超聲和血生化指標檢查結果,進行組間比較,分析LDL-C/HDL-C比值與頸動脈狹窄程度的相關性。
1.4 統計學方法 應用SPSS19.0統計軟件分析,計數資料以頻數和百分率表示,采用χ2檢驗;計量資料以±s表示,多組間比較采用F檢驗,兩兩比較采用t檢驗;相關性分析采用Pearson檢驗法,P<0.05為差異有統計學意義。
2 結果
2.1 各組一般資料比較 根據超聲檢查結果,MHD患者中,硬化組64例,非硬化組88例,各組性別、年齡、BMI比較均無明顯差異(P>0.05);硬化組與非硬化組每周透析次數、透析齡及原發病亦無明顯差異(P> 0.05)。 見表 1。
2.2 各組血生化指標比較 各組TG、ApoA1、ApoB無明顯差異(P>0.05);硬化組與非硬化組Scr、BUN、LDL-C、HDL-C 比較無明顯差異(P> 0.05),但與A組比較,兩組Scr、BUN、LDL-C明顯升高(P<0.05),而 HDL-C 明顯降低(P< 0.05);硬化組 TC 明顯高于非硬化組與A組(P<0.05),而非硬化組與A組比較無明顯差異(P>0.05)。見表2。
2.3 各組LDL-C/HDL-C比較 根據超聲頸動脈狹窄程度檢查結果,硬化組中,輕度組20例,中度組23例,重度組21例,各組LDL-C/HDL-C比值為:A組(2.17±0.32)<非硬化組(3.54±0.46)<輕度組(4.27±0.61)<中度組(6.18±0.73)<重度組(7.25±0.84),均有顯著差異(P< 0.05)。
2.4 LDL-C/HDL-C與頸動脈狹窄程度相關性分析相關性分析顯示,LDL-C/HDL-C與頸動脈狹窄程度呈顯著正相關(r=0.968,P< 0.05)。
3 討論
目前尚未完全闡明CRF患者脂質代謝異常的發病機制,而血脂代謝異常普遍存在于MHD患者中[4]。動脈粥樣硬化產生原因與人體內分泌關系主要為:一旦人體血脂濃度升高,將引起自由基清除劑活性減弱,容易形成大量脂質過氧化物分子,影響前列環素/血栓素2平衡,提高血小板聚集率,大量釋放5-羥色胺,提高凝血活性。當該類因素互相影響,就會損傷內皮細胞,促進平滑肌細胞增生,產生泡沫細胞[5-6]。而這些泡沫細胞能夠在皮下不斷聚集形成脂紋,引起更復雜損害。有研究指出,TG、TC、LDL-C均為動脈粥樣硬化影響因素[7-8]。此外,國際與我國血脂異常防治指南均指出,LDL-C水平達標為臨床防治心血管病變發生首要目標[9]。

表1 各組一般資料比較
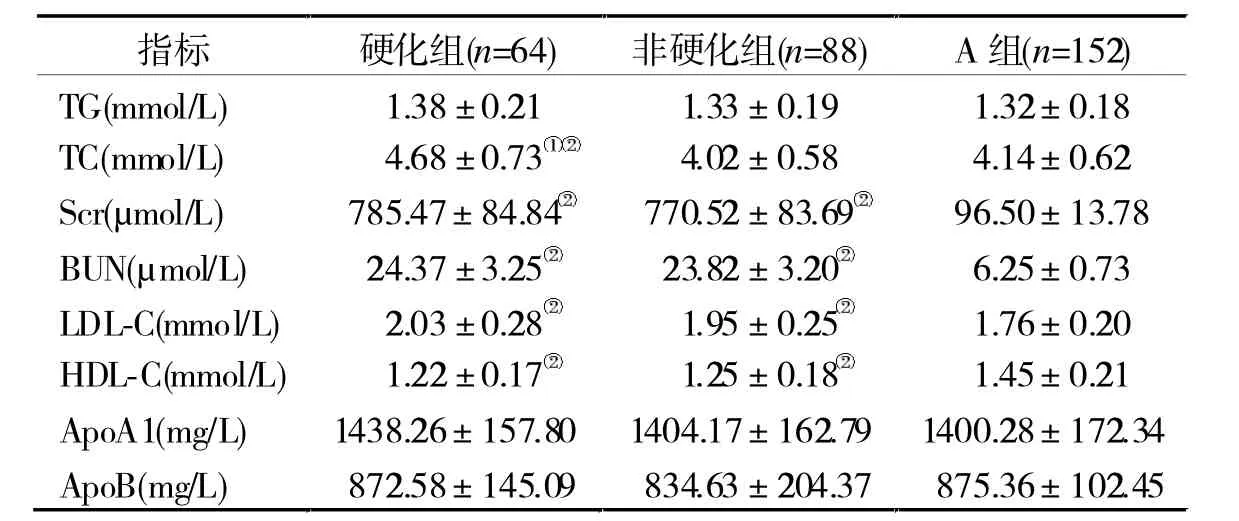
表2 各組血生化指標比較
LDL-C組成中最多的是TC,其次是膽固醇酯,其能與動脈壁上的蛋白多糖結合形成不溶性沉淀,促進纖維組織增生。同時,LDL-C亦能附著于動脈內皮上面與LDL-C受體結合,并且沉積于動脈內膜表面。血LDL-C水平已明確被證實為頸動脈粥樣硬化產生主要危險因素,降低其水平能夠減少心血管事件風險[10]。但仍有研究發現,LDL-C水平與頸動脈粥樣硬化產生無顯著相關性[11]。分析其原因,可能在于LDL-C分子被氧化修飾之后的氧化型LDL-C屬于動脈粥樣硬化形成關鍵步驟之一[12-13]。
本研究結果顯示,硬化組與非硬化組Scr、BUN、LDL-C、HDL-C水平比較無顯著差異,但與A組比較,兩組Scr、BUN、LDL-C顯著升高,而HDL-C顯著降低,與宋雪冬等[14]研究結論一致。說明MHD患者會出現血脂異常,面臨心腦血管病發生風險。結果還顯示,硬化組TC顯著高于非硬化組與A組,表明TC升高為頸動脈粥樣硬化影響因素。LDL-C/HDL-C比值為:A組<非硬化組<輕度組<中度組<重度組,且相關性分析發現LDL-C/HDL-C與頸動脈狹窄程度呈正相關,提示在評估頸動脈硬化方面,LDL-C/HDL-C可作為有效預測指標。
綜上所述,行MHD治療的原發性慢性腎衰竭患者血清LDL-C/HDL-C值會呈一定程度的升高趨勢,且與頸動脈狹窄程度呈顯著正相關。

